|
 |
- Search
| J Korean Med Assoc > Volume 58(10); 2015 > Article |
Abstract
Medical device industry has characteristics of multi-disciplinary convergence and is easy to apply with information communication technology. Such nature makes Korea medical device industry more globally competitive than the pharmaceutical industry. The foreign direct investment (FDI) of service industry in Korea continues to be at a standstill and the medical device industry is not an exception. Among this stagnant FDI situation in Korea, Covidien, a global medical device company has established the Covidien Center of Innovation as both an education and training facility for domestic and foreign healthcare professionals and a medical device research and development (R&D) center in August 2013. Along with the global attractiveness of superior clinical outcomes generated by healthcare professionals, the future medical device industry development will be fueled by continued R&D investments, researchoriented hospital R&D activities, and clinical studies, etc. It is important to provide attractive investment environments to embrace FDI similar to Covidien Center of Innovation into Korea in order to leverage healthcare professionals' competency at maximum and lead collaboration between medical device companies and healthcare professionals. It is imperative that 'innovative medical device enterprise' certification system similar to the curent 'innovative pharmaceutical enterprise certification' is created. If additional premium reimbursement prices are granted to medical devices developed and manufactured by the innovative enterprises which contribute to domestic R&D and healthcare professional education and training through FDI in Korea, it will help FDI activation in Korea to a great extent. And the reimbursement coverage for routine care costs in clinical trial will stimulate FDI in Korea.
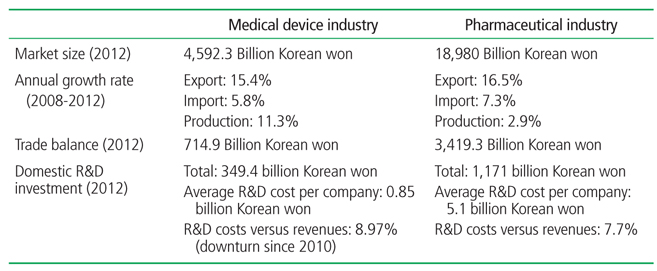
의료기기산업은 전기·전자, 생물, 화학, 금속공학 등 다학제산업의 융복합 특성을 띠고 있으며 정보통신기술 접목이 용이하다. 산업융합과 다양성을 기반으로 제약산업 대비 우리나라가 국제경쟁력을 갖추기에 유리한 산업구조이다[1]. 2012년 세계 의료기기 시장규모는 약 280조 원(3,083억 달러)이며 국내 시장규모는 약 3조7천억 원(40.8억 달러)으로 세계 13위(1.3%)를 차지하고 있다. 건강보험 진료비 지출자료 분석에 의한 행위별 수가 청구건을 4대 분류별로 구분한 진료비(2014년) 자료에 따르면, 치료재료 지출액은 2조 1,881억 원(4.31%)으로 기본진료료 14조 3,199억 원(28.20%), 진료행위료 20조 8,169억 원(41.00%), 약품비 13조 4,491억 원(26.49%)에 비해 현저하게 적으며 국내시장 규모는 그리 크지 않음을 알 수 있다[2]. 의료기기산업은 국내의 협소한 시장규모를 벗어나 전세계 시장을 겨냥한 국제경쟁력 강화를 통해 얼마든지 국제 선도산업으로 키울 수 있는 분야이다.
우리나라 정부는 국정과제인 보건산업을 미래성장산업으로 육성 발전시키기 위해 의료기기산업 중장기 발전계획을 마련하고 이를 현실화하기 위한 작업을 실행해 오고 있다. 범정부 차원(보건복지부, 기획재정부, 미래창조과학부, 산업통상자원부, 식품의약품안전처, 중소기업청, 특허청 등)에서 발표한 2020년 세계 7대 의료강국 진입을 위한 의료기기산업 중장기발전계획에 따르면, 2020년까지 수출액 13.5조 원, 시장점유율 3.8%, 고용인력 13만 명 달성을 위한 4대 전략과 70개 세부과제를 마련하였다[3,4]. 중장기 발전계획에서 밝혔듯이 의료기기산업은 지속적인 고성장이 전망되는 고부가가치 유망산업으로 세계 의료기기 시장규모는 2018년 에 510조 원, 연평균 성장률이 6.7%(2013-2018년)에 이를 것으로 전망되고 있다. 전세계적인 의료기기산업 구조는 소수의 글로벌 대기업을 제외하고는 대다수가 중소기업으로 구성되어 있어 중소기업 육성에 유망한 산업이다. 짧은 제품 생명주기와 다품종 소량생산이라는 산업적 특성에 따라 여타 제조업뿐만 아니라 제약산업과도 차별화되며 높은 고용을 창출하는데 매우 유리한 산업이다.
이와 같이 고부가가치 및 고성장이 전망되는 유망산업임에도 불구하고 국내로 유치된 외국직접투자는 극히 저조하며 최근 10년간 사례를 찾아보기 매우 어렵다. 최근 의료기기 산업에서 과거 실행된 외국직접투자와는 차별화된 형태의 '코비디엔혁신센터' 외국직접투자 사례를 살펴보고 향후 의료기기산업에서 국내 외국직접투자 유치를 촉진할 수 있는 방안을 살펴보고자 한다.
정부의 '유망서비스산업 육성 중심의 투자활성화 대책' 발표에 따르면, 7대 유망 서비스산업 육성을 위한 135개 정책과제 가운데 보건의료 분야가 포함되어 있다. 우리나라 기업들의 국내 투자는 부진한 반면 해외투자는 매우 빠른 속도로 증가하고 있는 가운데, 높은 생산비용과 불합리한 규제 등이 국내 투자환경 미흡 원인으로 지적되고 있다. 서비스 산업에서 국내 외국직접투자가 답보상태를 지속하는 가운데 의료기기산업도 예외는 아니다[5].
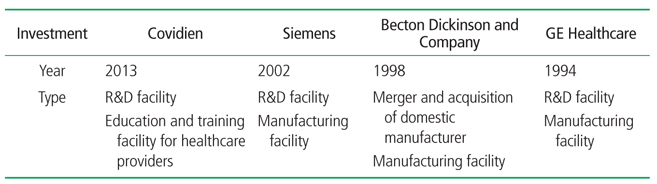
과거 의료기기산업에서 외국기업의 국내직접투자 사례로 GE 헬스케어와 지멘스를 꼽을 수 있다. 1984년 4월에 GE삼성의료기기 주식회사로 설립된 GE 헬스케어코리아는 10년 후인 1994년 6월 한국성남초음파진단기기연구개발 및 생산공장을 설립하여 경기도 성남에 공장을 준공하였고 2002년 11월에는 한국 GE 초음파(GE Ultrasound Korea)로 분리하였다. 한국GE초음파는 대규모 글로벌 초음파 연구개발 및 생산 기지로서 입지를 구축하고 있다[6]. 지멘스코리아는 2002년 경기도 성남을 비롯한 4곳에 연구개발센터인 메디컬초음파사업부를 설립하고 자체개발한 초음파를 전 세계에 수출하며 의료기기·IT융합 관련 전초기지를 구축하고 있다[7,8]. 2014년 상반기 보건상품 수출품목 통계자료를 살펴보면, 국내기업 투자 및 외국직접투자에 힘입어 '초음파 영상진단기(2.2억 달러)'는 '기초화장용 제품류(3.5억 달러)'의 뒤를 이어 2위를 차지하고 있다[9]. 위와 같은 2개 외국기업의 연구개발센터 및 제조 생산시설 설립을 통한 국내 외국직접투자 사례와 더불어 국내 의료기기 제조업체 인수를 통한 직접투자 사례가 있다. 미국계 글로벌 기업인 벡톤디킨슨(Becton Dickinson and Company)은 1985년 한국법인 설립 후 1998년에 수액세트, 일회용 주사기·주사침, 척추침, 채혈기 등을 생산하는 국내 의료기기 제조기업인 보인메디카와 신동방의료를 각각 인수 합병하였다[10]. 벡톤디킨슨은 한국을 거점으로 한 아시아지역 투자확대를 위해 보인메디카를 350억여 원에 인수하였는데 글로벌 의료기기 기업이 국내업체를 인수해 국내시장에 진출한 첫 사례였다. 그러나 2010년에 10여 년간 가동해 온 공장을 전격 철수하기로 결정하였는데, 인건비 상승과 더불어 투자 대비 수익 악화 등 경쟁력 약화로 인한 것으로 알려졌다. 당시 벡톤디킨슨의 국내 연간 생산금액이 약 424억 원으로 국내 전체 의료기기 생산 10위(1.53%) 수준이었다[11]. GE 헬스케어와 지멘스의 국내 초음파장비 연구개발센터 및 제조시설 투자 시점은 각각 1994년과 2002년으로 과거 10-20년 전에 투자된 것으로 우리나라 정보통신기술산업의 우수한 인프라와 연구개발 역량이 반영된 투자라고 볼 수 있다. 이와 달리 벡톤디킨슨의 투자는 상대적으로 열악한 상황인 치료재료(의료용품) 분야 투자였으나 큰 빛을 발하지 못하고 10년 만에 투자에서 손을 뗐다. 위의 3가지 사례 이후로는 의료기기 산업에서 제조 혹은 연구개발 분야 등에 외국기업의 국내 직접투자는 찾아보기 어렵다. 이러한 상황에서 글로벌 의료기기 기업인 코비디엔(Covidien)은 2013년 8월에 충청북도 청원군 오송첨단의료복합단지 내 기업부설 연구시설로서 국내외 의료진들을 위한 교육훈련센터뿐만 아니라 수술용 의료기기 연구개발을 목표로 약 6,300 m2 규모의 '코비디엔혁신센터(Covidien Center of Innovation)'를 설립하였다(Table 1).
코비디엔혁신센터는 '첨단의료복합단지 지정 및 지원에 관한 특별법(이하 첨복특별법)'에 따라 설립된 연구개발 및 교육시설로서 오송첨단의료복합단지에 유치된 최초의 외국직접투자이다[12]. 우리나라를 아시아 태평양지역에서 혁신연구센터로 육성하기 위한 목적으로 1) 첨단의료기기 개발을 위한 국내외 공동연구개발 및 기술교류; 2) 장비 및 시설의 공동사용과 국내외 연구개발인력의 교류; 3) 국제컨퍼런스 및 세미나, 학술대회 등 공동개최를 실행하고 있다. 의료기술 향상을 위한 연구개발 공동투자를 진행하고 이를 통해 얻은 성과물에 대해 관련 의료기술을 교환하기 위한 업무를 진행하고 있다. 코비디엔은 대한외과학회, 대한흉부심장혈관외과학회, 대한탈장학회, 대한내시경복강경외과학회 등과 코비디엔혁신센터 활용 업무협약을 맺고 각 학회 소속 전공의들을 위한 수련시설로 활용함으로써 표준화된 의무교육 커리큘럼 및 의료기기 사용에 관한 교육훈련 프로그램을 개발해 오고 있다. 의료진의 교육프로그램 개발은 국내에 머물지 않고 아시아태평양 지역의 의료진을 위해 시술과 수술에 필요한 술기를 이론과 실습을 통해 완벽하게 습득할 수 있도록 개발된 마스터클래스 프로그램 및 교육 커리큘럼 개발을 위해 관련 학회와 협력하고 있다. 현재까지 코비디엔혁신센터에서 교육받은 외국 의료진(일본, 호주, 중국, 대만, 홍콩, 싱가폴, 태국, 러시아, 미얀마, 인도, 말레이시아, 베트남, 인도네시아, 필리핀 등)은 약 300명에 이른다. 이러한 해외 의료진들의 국내 교육훈련 경험들은 각 해외국가들로 전파되고 국내 우수한 의료진들이 외국에 초청되어 외국 의료진 교육훈련에 이바지하게 되며, 궁극적으로 우리나라의 의료시스템 수출에도 기여한다. 의료진들의 교육훈련 센터로서의 기능뿐만 아니라, 궁극적으로 연구기관 및 대학과의 공동연구를 통해 신제품 개발과 연구개발 컨설팅을 제공하여 선순환의 혁신고리를 제공한다.
코비디엔은 주로 의료용품을 취급하고 있으며 국내 의료기기산업에서 국제경쟁력이 떨어지는 치료재료(의료용품) 분야에서 코비디엔혁신센터와 같은 외국직접투자는 국내 의료기기산업 발전에 의미하는 바가 크다. 2012년 '국내 의료기기 제조유통실태-수입업' 자료에 따르면, 2012년 국내 의료기기 수입업체(1,399개)의 의료기기 분야 추정 매출액은 5조 9,957억 원이다(수입제품 매출액 5조 2,150억 원[87.0%], 국내 매입제품 매출액 7,807억 원[13.0%]). 수입제품 매출액 기준 유형군별 분석자료에 따르면, 의료용품이 전체 매출의 26.5%인 1조 3,796억 원으로 가장 높았고, 방사선영상진단기기 5,442억 원(10.4%), 정형용품 4,783억 원(9.2%) 순이었다. 수입제품 취급비율이 가장 높은 유형군은 의료용품(45.6%)이며, 체외진단기기(13.0%), 정형용품(9.7%), 방사선영상진단기기(4.0%) 순이었다[13].
외국 의료진이 코비디엔혁신센터의 교육훈련 과정을 위해 우리나라를 방문 시 지출하는 비용을 감안할 때 추가적인 경제효과를 기대할 수 있다. 문화체육관광부에서 발표한 2013년 외래관광객 실태조사에 따르면, 2013년 방한 외래관광객의 1인 평균 지출경비는 1,648.2달러이며 1일 평균 지출 경비는 290달러로 나타났다[14]. 외국의 경우 의료진의 경제수준이 다른 직업군과 비교시 더 높은 수준임을 감안할 때 평균 지출경비는 이보다 높을 것으로 추정된다.
앞에서 살펴보았듯이 의료기기산업에서 우리나라에 외국직접투자를 유치하기는 쉽지 않은 상황이다. 정보통신기술 산업 분야에서 우리나라의 높은 국가 경쟁우위로 인해 관련 의료기기의 외국직접투자를 유치할 수 있을지 모르겠으나, 작은 시장규모와 더불어 원천기술이 없고 투자환경이 열악하며 대다수 수입에 의존하는 의료기기 산업에서 외국의 제조 및 연구개발 시설을 국내에 유치하기는 현실적으로 매우 어렵다. 현재 모든 글로벌 기업들이 중국에 투자를 집중하고 있는 상황에서 우리나라의 투자 매력도는 더욱 더 떨어질 수 밖에 없다. 이러한 현실에서 코비디엔혁신센터가 주는 시사점은 매우 크다. 우리나라는 치료재료 분야에서 낮은 기술력, 높은 인건비, 토지 비용, 생산비, 물류비 등으로 인해 의료기기 제조시설로서의 매력도는 매우 낮으나 우수한 국내 의료진의 강점을 극대화 할 수 있는 장점을 갖고 있다. 현재까지는 임상적 성과의 우수성이 가장 높은 매력도이나 지속적으로 추진되고 있는 연구개발 투자, 연구중심병원에서의 연구 활동, 임상연구 활동 등 노력에 힘입어 향후 의료기기산업 발전 가능성은 높다[15].
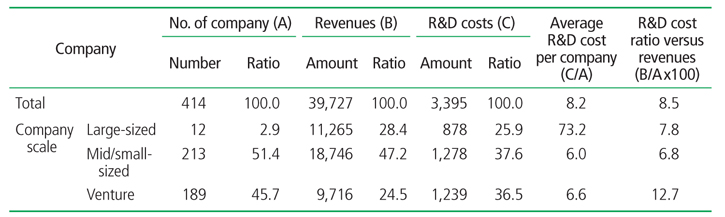
우리나라 의료기기 분야의 연구개발비 현황을 살펴보면, 2012년 의료기기 제조업체(414개) 연구개발비는 3,550억 원으로 이 가운데 실질적으로 의료기기 분야 투자 연구개발비는 3,395억 원(95.6%)이었다, 매출액 대비 연구개발비 비중은 8.5%였으나, 기업당 평균 연구개발비는 약 8억 원에 불과하다(대기업 73억 원, 중소기업 6억 원, 벤처기업 7억 원 수준)[16] (Table 2). 연구분야별 연구비 비중을 살펴보면, 진단 및 계측기기 분야가 52.5%(1,783억 원)로 전체 의료기기 연구비의 절반 이상을 차지하고 있으며 수술 및 치료기기(598억 원, 17.6%), 치과기기 및 재료(469억 원, 13.8%), 의료용품 및 치료재료(399억 원, 11.8%)에 각각 10% 이상의 연구비가 투입되고 있으며 의료기기 산업 내 분야별 높은 편차를 알 수 있다. 연구과정별 연구비 비중의 경우, 시작품 개발연구 단계 연구비 34.1%(1,158억 원), 생산공정 개발연구 25.3%(858억 원), 성능인증 및 임상연구 22.5%(764억 원), 기초연구 18.1%(615억 원) 순이었다. 아이디어를 구체화시킨 원형 개발, 성능·외형 등의 최적화를 위한 디자인 개발 등의 활동을 하는 시작품 개발연구 단계에 가장 많은 연구비를 투자한 것으로 나타났다[16]. 산출물 별로는 방사선영상진단기기에 대한 연구비가 29.6%(1,005억 원), 생체계측기기 16.4%(556억 원), 전동식 수술 및 치료기기 8.8%(299억 원), 치과재료 8.6%(293억 원), 치과용 기기·기계 6.4%(216억 원) 등이었다. 의료용품 및 정형용품의 경우 국내 큰 시장규모와 높은 수입품목 점유율에도 불구하고 연구산출물별 낮은 연구비를 보이며 의료기기산업 현실과의 부조화를 보이고 있다(Figure 1).
의료기기 개발은 주로 의료진이 제시한 아이디어로부터 필요성이 제기되어 의료기기 기업과 협력을 통해 제품이 개발 상용화되는 것이 일반화된 과정이다[17,18,19]. 코비디엔혁신센터는 연구개발된 시작품을 이용하여 인체를 대상으로 한 임상시험에 앞서 동물을 대상으로 한 전임상연구가 가능하고 의료진 등이 시작품의 안전성과 성능에 대해 평가할 수 있고 시작품에 대한 피드백을 제공하여 최적의 제품개발을 위한 기틀을 제공한다. 시작품 개발연구 단계 연구비가 가장 큰 부분을 차지하는 있는 상황을 감안할 때, 우수한 국내 의료진을 연구개발 분야에 적극 활용한다면 의료기기 분야의 산업매력도는 더욱 높아질 것으로 기대된다. 국내 의료기기 제조시설 유치를 위한 노력도 필요하겠으나 국내 의료진의 역량을 극대화하고 의료기기 기업과 콜라보레이션을 이끌어낼 수 있는 코비디엔혁신센터와 같은 연구개발 및 교육·훈련시설을 적극적으로 국내에 유치하는 것이 보다 현실적이고 효과적인 전략이다. 이러한 전략은 최근 발표된 코비디엔혁신센터와 유사한 또 다른 외국직접투자를 통해 그 효과가 입증된다. 일본계 다국적 의료기기 기업인 올림푸스는 2017년 2월까지 총 363억 원의 투자(일본 올림푸스 본사 직접투자 150억 원 포함)를 통해 인천 송도에 의료기기 교육시설 및 서비스센터를 건립하기로 발표하였다[20]. 코비디엔혁신센터 사례에 기초한 우리나라에 적합한 의료기기산업에서의 외국직접투자 유치방안은 다음과 같다.
법률 제11690호(2013년 3월 23일)로 제정된 첨복특별법의 입법 목적은 "첨단의료복합단지의 지정 및 지원을 통하여 기업, 대학, 연구기관, 의료기관 등의 상호협력에 의한 의료연구개발의 활성화 및 연구성과의 상품화를 촉진함으로써 첨단의료복합단지를 세계적인 의료연구개발의 중심지로 육성하고 국내 의료산업의 발전에 이바지"하는 것이다. 무엇보다도 입법 목적에 부합하는 지원을 지속적으로 강화하여 외국직접투자 유치 가능성을 높여야 한다. 연구개발 및 교육·훈련 시설 투자 활성화를 위해서는 투자 유치기관에 대한 보조금(국비 및 지방비) 및 세제 혜택 지원 등도 중요하겠으나 첨단의료복합단지 내 입주기관 수를 늘리고, 기관간의 상호교류와 협력강화를 위한 네트워크구축 지원에 보다 많은 관심을 기울여야 한다. 연구개발은 개방적 협력을 통해 보다 많은 성과를 도출해 낼 수 있으며 이를 위해서는 기관간 정보공유 및 협력체계 구축 지원이 매우 중요하다.
'혁신형 제약기업' 인증제도와 유사한 '혁신형 의료기기기업' 인증제도가 필요하다. '제약산업 육성 및 지원에 관한 특별법(법률 제11690호. 2013년 3월 23일 시행)'은 "제약산업의 체계적인 육성·지원과 혁신성 증진 및 국제협력 강화를 통하여 제약산업의 발전기반을 마련하고 외국 제약기업의 국내투자유치 환경을 조성하여 제약산업이 국제적인 경쟁력을 갖추도록 함으로써 국민의 건강증진과 국가경제의 발전에 이바지하는 것을 목적"으로 입법되었다. 특별법을 통해 보건복지부장관으로부터 인증되는 '혁신형 제약기업'은 신약 연구개발 등에 대통령령으로 정하는 규모 이상의 투자를 하는 제약기업이거나 국내에서 대통령령으로 정하는 규모 이상의 신약 연구개발 투자실적이 있거나 신약 연구개발을 수행하고 있는 외국계 제약기업이 포함된다[21]. 혁신형 제약기업에 대한 인센티브로서 연구개발비 우대, 세제지원, 규제완화, 정책자금융자, 인력지원, 약가 우대정책 등 다양한 제도가 마련되어 있으며 다양한 지원방안 가운데 적정성·투명성·예측 가능성을 담보하는 약가체계 개편이 가장 중요한 안건으로 지적된 바 있다[22,23]. 제약산업에서의 예와 같이 의료기기산업에서도 의료기기 보험급여 및 가격 결정에 있어서 적정성, 투명성, 예측 가능성을 가장 중요한 정책과제로 논의되고 있음을 고려할 때 '혁신형 의료기기기업' 인증이 현실화될 경우에 가장 핵심적으로 다루어야 할 사항이다.
'혁신형 의료기기기업' 인증제도를 마련할 때, 제약산업과 의료기기산업 간의 차이를 반영해야 한다. 제약산업 육성 및 지원에 관한 특별법 시행령 '제2조(연간 연구개발비의 규모 등)'에 따른 혁신형 제약기업 인증 시 자격기준을 살펴보면, (1) 연간 의약품 매출액이 1천억 원 미만인 제약기업의 경우 연간 50억 원 또는 연간 의약품 매출액의 100분 의 7, (2) 연간 의약품 매출액이 1천억 원 이상인 제약기업의 경우 연간 의약품 매출액의 100분의 5, (3) 미합중국 또는 유럽연합의 정부나 공공기관으로부터 적합판정을 받은 의약품 제조 및 품질관리기준을 보유한 제약기업의 경우 연간 의약품 매출액의 100분의 3을 요건으로 하고 있다. 앞서 기술하였듯이 외국자본의 국내 의료기기 제조시설 유치는 현실적으로 매우 어려우며 코비디엔혁신센터와 같은 유형의 투자가 보다 현실적이고 매력적이다. 따라서 인증방법 상에서 제약산업과 차이를 둘 필요가 있다. 외국계 제약기업의 경우 국내에 신약도입 시 식품의약품안전처 판매승인을 위해 허가 전 국내 임상시험이 요구되고 있고 임상시험 비용이 연구개발비로 인정이 되고 있는 반면, 의료기기의 경우 인종 간 차이가 거의 없어 외국 임상시험 자료를 통해 판매승인이 이루어지고 있기 때문에 국내 소재 외국기업의 연구개발비 부분은 크지 않다. 코비디엔혁신센터 사례에서 보듯이 연간 40억 원 이상이 의료진 교육·훈련비용으로 투자되고 있으며 회계상 이러한 비용은 연구개발비로 인정되지 못하고 있다. 또한, 제약과 의료기기산업 및 기업 규모의 차이 또한 간과할 수 없으며 의료기기산업 현실에 부합하는 기준을 마련하여 '혁신형 의료기기기업'을 인증할 필요가 있다[1] (Table 3).
'혁신형 의료기기기업' 인증 기업이 국내에 신기술을 도입할 때, 치료재료 상한금액 산정에서 가산율을 제공할 필요가 있다. 신기술 의료기기가 국내로 도입될 때 식품의약품안전처의 판매 승인, 한국보건의료연구원의 신의료기술평가 승인, 보건복지부·건강보험심사평가원의 행위 및 치료재료 급여 여부 결정 및 상대가치점수·상한금액, 보험급여 기준 등과 같은 다양한 절차를 거치게 된다. 이와 같은 절차를 거쳐 궁극적으로는 제품의 가치를 판단하는 치료재료 상한금액을 결정하는데 의료기기산업 전반적으로 신기술 제품의 시장 진입가격이 낮게 책정되어 신기술 도입에 대한 유인책이 열악하며 신기술제품이 비급여로 결정되는 경우가 빈번하여 실제적으로 신기술의 환자 접근성이 훼손되어 왔다. 최근에는 4대 중증질환 보장성 강화 등을 통해 비급여 결정을 억제하는 방향으로 선회되고 있으나 아직도 비급여 결정이 다수 이루어지고 있다. 최근 개정된 '행위 치료재료 등의 결정 및 조정 기준, 치료재료 상한금액의 산정기준'에 따라, 신청제품이 기 등재된 품목에 비하여 임상적 유용성, 비용·효과성, 기술혁신 등이 입증자료를 통해 개선된 경우에는 '가치평가기준표'의 평가 결과에 따라 기 등재된 품목의 상한금액 또는 최고가를 초과하여 최대 100%까지 가산율을 산정할 수 있게 되었다. 또한, 추가적으로 보건복지부장관이 지정한 보건의료기술진흥법 제3장 15조에 의한 연구중심병원(2013년 기준 10개 의료기관), 보건복지부장관이 지정한 의료기기임상시험센터(영남대학교, 전북대학교) 등에서 임상시험을 하고 임상문헌을 제출한 경우 추가적으로 가산율을 5% 더 산정할 수 있는 제도가 마련된 바 있다[24]. 이와 유사하게 외국직접투자를 통해 의료기기 연구개발 및 의료진 교육훈련 및 연구개발을 위해 기여한 기업이 신기술 의료기기를 보험급여로 신청 시 상한금액 결정에 일정 부분 가산율을 적용한다면 보다 외국직접투자를 활성화할 수 있다. 이러한 가산율이 적용된다 하더라도 제약과 달리 의료기기의 특성상 일개 제품의 사용량은 높지 않아 가산율 적용에 대한 추가 건강보험 재정 지출보다는 국내 직접투자로 인한 편익이 훨씬 더 크다.
코비디엔혁신센터에서 창출된 연구개발 성과가 제품 상용화라는 궁극적인 과실을 맺기 위해서는 안전성 및 유효성을 입증하기 위한 임상시험이 반드시 수반되어야 한다[25]. 이에 의료기기 임상연구에서 소요되는 통상진료비용(예를 들어, 입원료, 검사료, 수술료 등)을 보험급여로 지원할 필요가 있다. 외국의 경우에는 임상연구에 요구되는 비용의 보험급여 지원제도를 마련하고 있다[26]. 보건복지부는 영리목적이 아닌 연구 및 리서치 등 학술 목적의 연구자 임상시험의 경우, 시험군과 대조군 환자의 통상적인 요양급여 비용 전체에 대해 보험급여 적용이 가능하다고 행정해석을 내린 바 있다[27]. 최근 보건복지부의 글로벌 임상시험 유치 활성화 및 발전계획 발표에서 보듯이 임상시험은 국가 경제성장에 기여할 수 있는 분야이다. 현재 보건복지부 발표내용은 제약산업에만 국한된 것으로 보이나 향후 의료기기 산업에도 공히 적용될 것으로 예측된다. 임상시험 활성화를 위한 인프라 강화와 CRO (contract research organization) 이용비용 지원뿐만 아니라 궁극적으로 임상시험 통상진료비용의 보험급여 적용 방안을 계획하고 있는 바 향후 임상시험 분야 발전에 대한 기대가 높다[28]. 위와 같은 보건복지부 발표와는 별개로 '첨단의료단지법' 제22조(국민건강보험법에 관한 특례)는 "첨단의료복합단지 안에 있는 보건복지부장관이 지정하는 의료기관에서 의료연구개발을 위한 의약품, 의료기기 및 의료기술을 임상연구 대상자에게 사용하는 경우는 이를 요양급여로 본다"라고 규정하고 있다. 현재까지 첨단의료복합단지 내 설립된 의료기관이 없어 위의 규정에 적용된 사례는 없으나 향후 의료기관을 유치하여 임상시험이 활성화될 경우 코비디엔혁신센터 연구개발 성과물과의 연계성이 강화되어 신기술 개발이 보다 촉진될 것으로 예상된다.
의료기기산업은 산업융합과 다양성을 기반으로 제약산업 대비 우리나라가 국제경쟁력을 갖추기에 유리한 산업이다. 고부가가치 및 고성장이 전망되는 유망산업임에도 불구하고 국내로 유치된 외국직접투자는 찾아보기 매우 어렵다. 과거 3곳의 외국기업 국내 직접투자 및 코비디엔혁신센터 투자 사례로 살펴보았듯이 국내 외국기업 제조시설 투자유치 노력보다는 우리나라의 우수한 임상 분야 역량을 최대한 활용할 수 있는 교육훈련 및 연구개발 투자 유치가 보다 현실적이다. 외국직접투자를 촉진하기 위한 첨단복합단지 인프라 강화, 혁신형 의료기기기업 인증제도 신설, 치료재료 상한금액 산정 시 가산율 적용, 임상연구 통상진료비용의 보험급여 적용 등과 같은 제도적 뒷받침이 요구된다.
의료기기산업은 산업 융합과 다양성을 기반으로 제약산업 대비 우리나라가 국제경쟁력을 갖추기에 유리할 뿐만 아니라 높은 고용을 창출하는데 매우 효과적인 산업이다. 하지만 아직까지 국내시장 규모는 그리 크지 않아, 국내의 협소한 시장규모를 벗어나 전세계 시장을 겨낭한다면 의료기기산업의 국제경쟁력 강화를 통해 얼마든지 국제 선도산업으로 키울 수 있을 것이다. 본 논문은 코비디엔혁신센터가 오송단지에 설립되어 현재 수행하고 있는 역할 및 우리나라 의료기기 산업발전 측면에서의 기여 등을 기술한 글로서, 코비디엔의 사례에 기초하여 우리나라에 적합한 투자유치 방안을 제시하고 있다. 의료기기 산업분야가 우리나라 정부가 국정과제인 보건산업을 미래성장산업으로 발전시키기 위해 주목하고 있는 분야라는 점에서 의의가 있는 논문이라 판단된다.
[정리: 편집위원회]
References
1. Korea Health Industry Development Institute. Study on research and development reality of pharmaceutical products and medical devices in 2012 [Internet] Cheongju: Korea Health Industry Development Institute. 2014;cited 2015 Sep 29. Available from: http://www.khidi.or.kr/board/view?linkId=100784&menuId=MENU00085
2. Health Insurance Review and Assessment Service. National health insurance expenditures in 2014 [Internet] Seoul: Health Insurance Review and Assessment Service. 2015;cited 2015 Sep 29. Available from: http://www.hira.or.kr/dummy.do?pgmid=HIRAA020041000000&cmsurl=/cms/notice/02/1332409_24959.html&subject=
3. Ministry of Health and Welfare. Announcement of medical device industry mid-term/long-term development plan for entering the 7th global medical power country by 2020 [Internet] Sejong: Ministry of Health and Welfare. 2014;cited 2015 Sep 29. Available from: http://www.mw.go.kr/front_new/al/sal0301vw.jsp?PAR_MENU_ID=04&MENU_ID=0403&page=1&CONT_SEQ=299308&SEARCHKEY=TITLE&SEARCHVALUE=
4. Presidential Advisory Council on Science & Technology. Leading creative economy through bio and climate change responsiveness strategy [Internet] Sejong: Presidential Advisory Council on Science & Technology. 2014;cited 2015 Sep 29. Available from: http://www.msip.go.kr/cms/www/news/news/report/__icsFiles/afieldfile/2014/11/19/140717_10%EC%8B%9C%20%EC%9D%B4%ED%9B%84%20[%EB%B3%B4%EB%8F%84]%20%EC%A0%9C11%EC%B0%A8%20%EA%B5%AD%EA%B0%80%EA%B3%BC%ED%95%99%EA%B8%B0%EC%88%A0%EC%9E%90%EB%AC%B8%ED%9A%8C%EC%9D%98%20%EA%B0%9C%EC%B5%9C.pdf
5. Ministry of Strategy and Finance. Announcement for investment activation plan focusing on promising service industry development [Internet] Sejong: Ministry of Strategy and Finance. 2014;cited 2015 Sep 29. Available from: http://www.mosf.go.kr/news/news02.jsp?actionType=view&hdnTopicDate=2014-08-12&runno=4091443
6. GE Healthcare Korea. Company introduction [Internet] Seoul: GE Healthcare Korea. cited 2015 Sep 29. Available from: http://www3.gehealthcare.co.kr/ko-kr/about_us/about_gehc
7. Korea Health Industry Development Institute. Ultrasound imaging system. Medical Device Market Research Report. Vol. 4 [Internet] Cheongju: Korea Health Industry Development Institute. 2014;cited 2015 Sep 29. Available from: http://www.khidi.or.kr/board/view?linkId=138972&menuId=MENU00356
8. Siemens Korea. Company introduction [Internet] Seoul: Siemens Korea. cited 2015 Sep 29. Available from: http://www.siemens.co.kr/healthcare/
9. Korea Health Industry Development Institute. Analysis on the 1st half year healthcare industry import and export trend in 2014 [Internet] Cheongju: Korea Health Industry Development Institute. 2014;cited 2015 Sep 29. Available from: http://www.khidi.or.kr/board/view?linkId=148999&menuId=MENU00088
10. Munhwailbo. US medical device company, Becton Dickinson and Company acquired Boinmedica [Internet] Seoul: Munhwailbo. 1998;cited 2015 Sep 29. Available from: http://www.munhwa.com/news/view.html?no=1998080611001401
11. Medical Observer. Becton Dickinson and Company closes the manufacturing facility in Daegu by the end of 2010 [Internet] Seoul: Medical Observer. 2010;cited 2015 Sep 29. Available from: http://www.monews.co.kr/news/articleView.html?idxno=36848
12. American Chamber of Commerce in Korea. Healthcare as Korea's future engine of growth: AMCHAM Healthcare Innovation Seminar 2014. Session B: growth through open inno-vation and global collaboration between local and global medi-cal device manufacturers [Internet] Seoul: American Chamber of Commerce in Korea. 2014;cited 2015 Sep 29. Available from: http://www.amchamkorea.org/publications/HC%20Seminar%202014/B/5_Woon_Yong_Kim.pdf
13. Korea Health Industry Development Institute. Weekly health-care industry at a glance [Internet] Cheongju: Korea Health Industry Development Institute. 2014;cited 2015 Sep 29. Available from: http://www.khiss.go.kr/board/bbs_read.jsp?tname=MINBOARD358&bbsid=B305&cat_bbsid=&bbs_seq=107&jkey=&jword=&pg=1&htxt_code=133938779978134299384428462&wj_vcs=&reverseNum=106&forwardNum=1
14. Ministry of Culture, Sports and Tourism. International visitor survey in 2013 [Internet] Sejong: Ministry of Culture, Sports and Tourism. 2014;cited 2015 Sep 29. Available from: http://kto.visitkorea.or.kr/kor/notice/data/statis/tstatus/forstatus/board/view.kto?id=421189&rnum=2
16. Korea Health Industry Development Institute. Analysis on R&D reality of domestic medical device manufacturers in 2012 [Internet] Cheongju: Korea Health Industry Development Institute. 2014;cited 2015 Sep 29. Available from: http://www.khidi.or.kr/board/view?linkId=148955&menuId=MENU00088
17. Smith SW, Sfekas A. How much do physician-entrepreneurs contribute to new medical devices. Med Care 2013;51:461-467.


18. Chatterji AK, Fabrizio KR, Mitchell W, Schulman KA. Physi-cian-industry cooperation in the medical device industry. Health Aff (Millwood) 2008;27:1532-1543.


19. Xu S, Avorn J, Kesselheim AS. Origins of medical innovation: the case of coronary artery stents. Circ Cardiovasc Qual Outcomes 2012;5:743-749.

20. Incheon Free Economic Zone. Attraction of Olympus Korea training and education center in Songdo, Incheon [Internet] Incheon: Incheon Free Economic Zone. 2015;cited 2015 Sep 29. Available from: http://www.ifez.go.kr/frt/biz/bbs/layout02/selectBoardArticle.do?bbsId=BBSMSTR_000000000072&nttId=1697257
21. Special Act on Fostering and Support of Pharmaceutical Indu-stry. Pub. L. No. 10519. 2011. 03. 30.
22. Ministry of Health and Welfare. Announcement of innovative pharmaceutical enterprise certification and performance analy-sis result [Internet] Sejong: Ministry of Health and Welfare. 2014;cited 2015 Sep 29. Available from: http://www.mw.go.kr/front_new/al/sal0301vw.jsp?PAR_MENU_ID=04&MENU_ID=0403&CONT_SEQ=307431&page=1
23. Ministry of Health and Welfare. Pharmaceutical industry support plan: new year discussion meeting between Ministry of Health and Welfare and innovative pharmaceutical enterprises [Internet] Sejong: Ministry of Health and Welfare. 2013;cited 2015 Sep 29. Available from: http://www.mw.go.kr/front_new/al/sal0301vw.jsp?PAR_MENU_ID=04&MENU_ID=0403&CONT_SEQ=280861&page=1
24. Ministry of Health and Welfare. Criteria for the reimbursement decision and adjustment of medical procedures and medical devices, etc: pricing rule on maximum reimbursement prices of medical devices [Internet] Sejong: Ministry of Health and Welfare. 2014;cited 2015 Sep 29. Available from: http://www.mw.go.kr/front_new/jb/sjb0406vw.jsp
26. Lee SS. Medical technology development and globalization: the role of the medical device industry. J Korean Med Assoc 2014;57:919-926.

27. Ministry of Health and Welfare. Notice letter 3639 from the Division of Health Insurance Benefits: the notice about reimbursement coverage of investigator-initiated clinical trial [Internet] Sejong: Ministry of Health and Welfare. 2015;cited 2015 Sep 29. Available from: https://www.kha.or.kr/board/dept/view
28. Ministry of Health and Welfare. Clinical trial global compe-titiveness enhancement plan for global top 5 clinical trial country by 2020 [Internet] Sejong: Ministry of Health and Welfare. 2015;cited 2015 Sep 29. Available from: http://www.mw.go.kr/front_new/al/sal0301vw.jsp?PAR_MENU_ID=04&MENU_ID=0403&CONT_SEQ=325129&page=1
- TOOLS
-
METRICS

-
- 0 Crossref
- Scopus
- 2,827 View
- 19 Download
-
Related articles in
J Korean Med Assoc -
Future development of helicopter emergency medical services in Korea2020 April;63(4)