 |
 |
- Search
| J Korean Med Assoc > Volume 66(9); 2023 > Article |
|
Abstract
Background: Despite various advances in resuscitation science, the overall survival outcome remains very low in patients who sustain sudden cardiac death. Regardless of the cause of the collapse, multiple organ systems may be injured secondary to post-cardiac arrest syndrome. This column highlights the interventions that can be incorporated as a bundle of post-resuscitation care, to narrow the gap between return of spontaneous circulation (ROSC) and neurologically intact survival.
Current Concepts: The post-cardiac arrest care algorithm presents treatment strategies and therapeutic goals to be considered in the initial stabilization stage, followed by investigating the cause of cardiac arrest and intensive care strategies to reduce additional brain damage. Immediately after ROSC, multimodal interventions required for post-ROSC care are bundled into a care regimen (treatment of the reversible cause, adequate seizure management, and glycemic control). It is also essential to establish definitive airway management to maintain normocapnic ventilation, prevent hyperoxia, and optimize hemodynamic management. Targeted temperature management after ROSC confers neuroprotection and leads to improved neurological outcomes.
Discussion and Conclusion: Post-cardiac arrest care is also emphasized as a key element in the chain of survival. The interventions outlined could lead to more patients being discharged alive from the hospital, with good neurological function. In addition, continued management planning, such as secondary prevention and social rehabilitation for cardiac arrest survivors and neurological prognostication for patients who do not recover consciousness after a certain period, are included.
Current Concepts: The post-cardiac arrest care algorithm presents treatment strategies and therapeutic goals to be considered in the initial stabilization stage, followed by investigating the cause of cardiac arrest and intensive care strategies to reduce additional brain damage. Immediately after ROSC, multimodal interventions required for post-ROSC care are bundled into a care regimen (treatment of the reversible cause, adequate seizure management, and glycemic control). It is also essential to establish definitive airway management to maintain normocapnic ventilation, prevent hyperoxia, and optimize hemodynamic management. Targeted temperature management after ROSC confers neuroprotection and leads to improved neurological outcomes.
Discussion and Conclusion: Post-cardiac arrest care is also emphasized as a key element in the chain of survival. The interventions outlined could lead to more patients being discharged alive from the hospital, with good neurological function. In addition, continued management planning, such as secondary prevention and social rehabilitation for cardiac arrest survivors and neurological prognostication for patients who do not recover consciousness after a certain period, are included.
돌연사(sudden cardiac death) 혹은 급성심정지(acute cardiac arrest) 환자에서 심폐소생술 후 자발순환 회복(return of spontaneous circulation) 상태가 되면 즉시 통합적인 소생 후 치료(post-resuscitation care)에 들어간다. 현재 적용되는 전 세계 공용 가이드라인과 2020년 한국심폐소생술가이드라인 지침 또한 주요 생존사슬(chain of survivals)의 한 축으로 심정지 후 치료(post-cardiac arrest care)를 다루고 있지만, Figure 1과 같이 2010년 이전까지는 생존사슬에 전문심장구조술의 일부로 포함되어 있었으나 2015년 이후 독립적인 생존사슬로 중요성이 강조되었고, 현재에 이르고 있다[1].
심정지 후 치료의 근본적인 목표는 소생 후 증후군에서 나타나는 광범위한 장기 손상을 정상화하고, 좋은 신경학적 예후로 회복시키기 위한 통합적 치료를 제공하는 것으로 심폐소생술(cardiopulmonary resuscitation)을 심폐뇌소생술(cardiopulmonary cerebral resuscitation)로 지칭하는 이유이기도 하다. 소생 후 통합치료에는 자발순환 회복 후 기도 확보, 호흡 유지, 순환 유지를 포함하는 초기 안정화 조치와 심장정지 유발 원인에 대한 진단 및 치료, 추가적인 뇌 손상을 완화하기 위한 집중치료, 신경학적 예후 예측, 생존자를 위한 지속적인 재활 치료가 포함된다. 따라서 소생 후 통합 치료는 체계화된 프로토콜을 사용한 다학제간 협력이 필요하다[2].
주요 치료 목표로는 소생 후 통합치료가 가능한 적절한 병원이나 중환자실로 환자 이송, 심정지 유발 원인의 확인과 치료, 재발 방지, 신경학적 회복을 위한 체온조절, 급성 관상동맥증후군의 확인과 중재, 신경학적 평가 및 다발성 장기부전의 예측, 치료 및 예방, 심정지 생존자에 대한 구조화된 선별 평가와 장기 재활 치료가 해당한다.
소생술 후 자발순환이 회복된 심정지 환자에서는 심정지 동안 및 자발순환회복 직후부터 진행되는 전신 허혈 및 재관류에 따른 복잡한 병태생리적 변화가 진행되면서 여러 장기 손상이 초래될 수 있는데, 이를 심정지 후 증후군(postcardiac arrest syndrome)이라 한다[3]. 심정지 후 증후군은 크게 심정지 후 뇌 손상, 심정지 후 심근 기능부전, 전신 허혈/재관류 반응, 그리고 촉발 원인 질환으로 구성된다. 심정지 후 증후군의 중증도는 심정지 원인과 기간에 따라 다양하고 동반되는 뇌 손상, 심근 기능부전, 전신 허혈/재관류 반응의 정도에 따라 다양한 임상경과를 보일 수 있다. 따라서 심정지 후 증후군의 치료과정에서는 개별 환자에 맞추어진 적절한 집중치료가 요구된다.
심정지 후 뇌 손상은 혼수, 발작, 다양한 수준의 신경인지장애 그리고 뇌사 등의 형태로 나타날 수 있는데, 뇌 미세순환 장애, 뇌 자동조절능 손상, 저혈압, 저탄산혈증, 저산소혈증, 고열, 저혈당, 고혈당 그리고 발작 등에 의해 악화될 수 있다. 심정지 후 심근 기능부전은 심정지 후 흔히 발생하지만, 대개는 2-3일 내에 회복된다[4]. 전신 허혈/재관류 반응은 면역과 응고기전에 영향을 미쳐 다발성 장기부전을 초래하고, 감염의 위험을 증가시킬 수 있다. 또한 심정지 후 증후군은 혈관 내 용적 감소, 혈관확장, 혈관내피손상, 그리고 전신 미세순환 장애 등의 패혈증과 유사한 임상양상을 보인다[5].
최근 심정지 후 좋은 예후와 함께 성공적으로 사회에 복귀하기 위해 궁극적으로 3요소가 필수적이며[6], 이 3개 요소에는 중환자 치료, 예후평가 및 통합적 의학-사회 재활 제공이 포함된다. 소생 후 치료과정 흐름도에는 초기 안정화 단계에서 고려해야 할 치료 전략과 목표가 제시되었고, 이어 심정지 원인에 대한 진단과 가역적 원인에 대한 치료, 추가적인 뇌 손상을 줄이기 위한 집중치료 전략이 포함되었다. 또한 일정시간 경과 후에도 의식이 회복되지 않는 환자를 대상으로 한 신경학적 예후 예측과 심정지 생존자에 대한 2차 예방 및 재활 등의 지속 치료에 대한 계획이 새롭게 포함된다(Figure 2).
자발순환이 회복된 심정지 환자는 집중치료가 가능한 중환자실에서 진료하는 것이 권장된다. 적절한 환기와 산소화를 유지하기 위해 호흡기계 및 심혈관계 관리를 하고 호흡 부전 및 쇼크 등에 대해 적극적으로 대처하며 혼수상태인 경우 목표체온유지요법을 고려할 수 있다. 2020 한국심폐소생술가이드라인을 토대로 2020 소생 후 치료과정 흐름도(Figure 3)와 함께 각 치료 목표 별로 최신 지견을 적용하도록 한다[2].
목표체온유지치료(targeted temperature management)는 보통 유도저체온요법(induced hypothermia)이라고도 불리며, 환자의 심부 체온을 특정 온도로 낮추는 치료를 통칭한다. 두개내압이 상승하였을 때에는 32-36℃로 체온을 유지하여 뇌와 전신의 신진대사 및 산소 소비량을 감소시켜 뇌세포를 보호하는 치료 전략이다[7]. 이러한 목표체온유지치료는 성인 심정지 환자의 뇌 손상을 최소화하여 생존율을 높이고 신경학적 예후를 개선한다[8-11]. 특히 심정지 후 뇌손상의 원인이 되는 산화스트레스(oxidative stress)와 흥분성 아미노산의 증가 및 에너지 고갈 등은 심정지 동안이나 자발순환회복 직후부터 발생하는 것으로 알려져 있기 때문에 심정지 환자에서는 가능한 빨리 경도의 저체온 유도를 시작해야 한다.
다만 목표체온유지치료는 체온이 낮아질수록 신체 전반의 다양한 생리적인 변화들과 함께 감염 위험 증가, 전해질 불균형, 인슐린 저항성 증가, 응고 병증, 오한(shivering) 등의 합병증 발생의 위험이 증가하여 주의가 필요하다[12]. 특히 신경계 중환자에서 뇌부종 및 뇌압 관리를 위해 목표체온 유지치료를 시행할 경우 약 1-2주 이상의 치료기간이 필요한 경우들이 많지만[13], 심정지 소생 후 치료(post-cardiac arrest care)를 시행할 때에는 목표체온유지치료의 총 기간이 48시간 내외로 비교적 짧아 부작용을 최소화하면서도 효과를 극대화할 수 있는 연구가 진행 중이다. 심정지 후 소생 환자에서 목표체온유지치료 적응증에 대한 국내외 많은 연구들이 이루어져 있는데, 초기 리듬에 상관없이 자발순환 회복이 회복된 심정지 환자 중 구두지시에 의미 있는 반응을 보이지 않는 환자에게 32-36℃ 사이의 목표 체온을 일정하게 유지하는 목표체온유지치료를 시행한다(권고 등급 I에 해당).
목표체온유지치료로 체온을 낮추는 과정은 저체온 유도기(induction phase), 유지(maintenance), 및 재가온(rewarming)의 세 단계로 구분할 수 있고, 각 시기별로 저체온 유지에 따른 전신적인 합병증이 발생할 수 있다. 체온 요법을 조절하는 방법은 표면 냉각(surface cooling)과 혈관 내 냉각(endovascular cooling)으로 구분한다. 외부 표면 냉각방법(예, 냉각요, 얼음주머니)은 사용하기 쉽고 적용하기 편리한 장점이 있지만 중심체온을 떨어뜨리는 속도가 느리고 체온을 일정하게 유지하기가 어렵지만, 최근 혈관 내 도관(catheter)을 이용한 냉각장비나 정밀한 자동 되먹임 온도 조절 장치를 갖춘 체외 냉각장비들이 도입되면서 체온조절이 쉬워졌다.
첫 단계인 유도기는 환자의 중심체온 32-36℃ 사이(권고 등급 I)로 목표 온도를 설정할 것을 권고하며, 발열이 생기지 않도록 적극적으로 체온을 감시한다. 이 시기에서는 최대한 신속히 목표 체온에 도달하도록 한다. 유지 단계는 목표에 도달한 체온을 치료기간 동안 일정하게 유지하는 것이며, 이를 위해 심부 체온의 변동이 최소화되도록 한다. 유지 단계의 적정 기간은 최소 24시간 일정하게 유지하도록 한다[14]. 하지만 최근 추가된 주요 연구에서 소생된 혼수 환자에서 72시간 동안 기구나 중재술을 이용한 발열 예방법(device-based active fever prevention)을 적용하는 경우, 24시간 저체온 유지 후 48시간 추가로 발열 예방 전략을 선택했을 때 감염이나 출혈, 경련과 같은 이상반응 차이가 없었다는 근거를 통해 72시간까지 연장하는 것을 고려 중이다[15]. 재가온은 정상 체온으로 되돌리는 단계이며, 심정지 환자의 치료에서는 일반적으로 시간당 0.25-0.5℃의 속도를 적용하도록 하고, 정상 체온(36.5-37.5℃)에 도달한 후에도 지속적으로 혼수상태가 지속되는 환자는 자발순환회복 후 72시간까지는 열이 나지 않도록 예방하고 가능한 정상 체온을 유지한다[16].
자발순환회복 후 의식이 없는 경우, 심폐소생술 동안 기관 내 삽관이 실시되지 않았다면 신속하게 기관 내 삽관을 한다. 자발순환회복 후 동맥혈 산소포화도를 94-98%로 유지할 수 있도록 흡입산소농도를 조절하도록 한다. 또한, 고이산화탄소혈증은 뇌혈류와 뇌압을 증가시키는 반면, 저이산화탄소혈증은 뇌혈류와 뇌압을 감소시킨다. 현재로서는 자발순환회복 후 정상보다 높은 이산화탄소혈증을 목표로 하는 치료를 권장하거나 권장하지 않기 위한 근거가 부족하다. 성인 심정지 환자에서 자발순환회복 후 동맥혈 이산화탄소 분압을 정상 범위인 35-45 mmHg로 유지한다[17].
심정지에서 회복된 이후 지속적인 순환 장애와 쇼크가 발생하는지 심혈관계 기능에 대한 모니터링을 지속적으로 해야 한다. 저혈압은 뇌를 포함한 장기로의 관류를 저하시켜 조직으로의 산소전달을 저해한다. 이에 자발순환회복 후 저혈압(수축기혈압 90 mmHg 이하 또는 평균 동맥압 65 mmHg 이하)은 신속하게 교정하고 수축기 혈압을 90-100 mmHg 이상 유지한다[18]. 저혈압 시 수액량은 심장기능이 감소되어 있는 경우가 아니면 일차로 1-2 L의 생리식염수를 투여하여 교정하며, 이후에도 저혈압성 쇼크인 경우 에피네프린(epinephrine), 노르에피네프린(norepinephrine) 투약을 고려한다.
급성 관상동맥증후군은 심인성 심정지의 가장 흔한 원인이다. 자발순환회복 즉시 12유도 심전도검사와 심장 표지자 검사를 해서 급성 관상동맥증후군 여부를 확인해야 한다. 자발순환회복 후 심전도에서 ST 분절 상승이 있는 모든 환자는 의식 상태와 상관없이 응급 관상동맥 조영술을 시행할 것을 권고한다[19,20]. 심인성 심정지이면서 자발순환회복 후 심전도에서 ST 분절 상승이 없는 환자 중 급성 관상동맥증후군이 의심되는 모든 경우 의식 상태와 상관없이 조기에 관상동맥 조영술 시행을 권고했던 2015년 가이드라인과 달리, 2020년 가이드라인에서는 자발순환회복 후 심전도에서 ST 분절 상승이 없는 성인에서 명백한 비심장성 원인이 확인되지 않았을 때 즉시 관상동맥 조영술을 하는 것보다는 신경학적으로 회복된 후 입원 중 관상동맥 조영술을 시행하도록 한다. 다만 자발순환회복 후 심전도에서 ST 분절 상승이 없더라도 지속성 심실빈맥 혹은 심실세동을 보이는 전기적 불안정 상태인 경우나 심인성 쇼크의 경우 조기에 관상동맥 조영술을 시행하는 것이 좋다[21].
소생술의 일차 목표는 뇌기능의 유지이다. 심정지 후 혼수 상태인 성인에서 발작을 치료하는 것을 매우 중요하다(권고 등급 I). 소생 후 혼수 환자에서 발작, 비발작성 경련지속증(nonconvulsive status epilepticus), 그리고 기타 유사발작의 유병률은 약 20-30%로 추정된다[22]. 과호흡이나 과환기에 유의하며, 뇌파검사와 같은 신경생리학적 정보를 모니터링하는 것은 환자의 상태를 파악하고 예후를 예측하는 데 도움이 된다. 지속적이고 치료에 반응하지 않는 발작은 다른 질환에서는 이차적인 뇌 손상과 연관이 있는 것으로 알려져 있기 때문에 심장정지 후 발작이 발생하는 경우에도 적극적으로 치료하여 부가적인 뇌 손상이 발생치 않도록 한다[23]. 하지만 예방적 목적으로 항경련제를 사용하는 것은 이를 뒷받침할 근거가 부족하다.
고혈당은 심정지로부터 소생된 환자의 사망률과 나쁜 신경학적 예후와 연관이 있는 것으로 알려져 있어 자발순환을 회복한 환자의 고혈당을 적절히 조절해야 한다. 저혈당을 예방하기 위해 자발순환이 회복된 환자의 혈당을 144-180 mg/dL의 목표 범위로 적용할 것을 제안한다[24,25]. 180 mg/dL 이상의 고혈당은 병원별 프로토콜에 따라 인슐린 점적주사로 치료하고, 저혈당(<80 mg/dL)이 발생되지 않도록 주의하는데, 만약 저혈당이 발생되면 즉시 포도당액으로 교정한다. 특히 목표체온유지요법을 경도 저체온으로 유도하거나 재가온하는 단계에는 혈당 변화가 심하므로 자주 혈당 검사를 시행하는 것이 바람직하다.
체외심폐소생술(extracorporeal cardiopulmonary resuscitation)이란 심장정지 환자에게 심폐 우회장치를 사용하여 혈액순환을 유지하는 방법이다. 체외심폐소생술의 목적은 회복 가능한 것으로 추정되는 가역적 심정지 원인을 치료하는 동안 환자의 생명을 유지하는 것이다. 체외심폐소생술을 이용하여 심정지 원인을 치료하고 환자를 회복시키려면 체외순환장치를 시술하는 팀과 중환자 치료를 담당하는 팀의 협력이 중요하다. 통상적인 소생술을 체외순환 소생술로 전환하는 과정에서 환자상태가 악화되지 않도록 호기말 이산화탄소 평가 등과 같은 방법으로 환자 상태를 파악하기 위한 노력이 계속되어야 좋은 예후를 기대할 수 있다[28]. 체외심폐소생술을 심정지의 치료에 이용하려는 의료인이나 기관은 적절한 프로토콜과 훈련, 모니터를 시행하여 회복 가능성이 높은 환자에서 심정지가 발생한 경우 체외심폐소생술이 조기에 사용될 수 있도록 준비해야 하지만, 아직은 조기 체외심폐소생술 적용이 좋은 효과를 개선하기 위해서는 추가적인 연구가 필요하다[29].
정확한 신경학적 예후 예측은 소생 가능한 환자에 대한 부적절한 치료 중단을 방지하고, 소생가능성이 없는 환자에 대한 불필요한 치료를 줄이기 위해 매우 중요하다. 하지만 현재까지는 예후를 완벽하게 예측 가능한 검사가 확정되지 않았고, 치료에 사용된 약물(진정제와 신경근차단제)과 목표체온유지치료의 영향을 받을 수 있기 때문에 자발순환회복 후 충분한 시간이 지난 다음에 신경학적 예후를 예측하는 과정이 진행되므로 여러가지 신경학적 예후 검사결과들을 통합하여 예측 과정으로 접근하도록 권장하고 있다[2].
(1) 심정지 후 혼수환자에서 예후 예측은 소생 후 치료 중에 사용한 약물 효과나 심정지 회복기의 오류를 최소화하는 데 적절한 시간이 지난 후에 시행한다. (2) 심정지 후 혼수환자에서 예후 예측 검사들은 권고된 적정 기간에 맞추어 검사를 진행하더라도 이들의 결과를 종합하여 판단하는 것은 최소한 목표체온유지치료에서 정상 체온으로 회복 후 72시간 이후(자발순환회복 후 5일)에 다각적인 접근 방식으로 시행하도록 한다. (3) 예후 예측은 한가지 검사결과만으로 판단하지 말고, 신경학적 검사, 생체표지자 검사, 감각유발전위 검사, 뇌파검사, 신경 영상검사 및 근간대경련 지속여부 등 다각적으로 접근(multimodal approach)하여 판단하도록 한다[30].
소생 후 예후 판정은 Table 1의 신경기능지표를 가장 많이 사용하고, 5단계 중 양호한 회복(good recovery), 중등도 장애(moderate disability)인 경우를 좋은 신경학적 예후로 평가하고 나머지 장애나 사망은 나쁜 예후로 평가한다(Table 1). 평가는 2020년 한국심폐소생술가이드라인에 근거하여 아래의 6가지의 검사결과 중에 최소한 2개 이상의 소견이 관찰되면 나쁜 신경학적 예후를 추정할 수 있으며, 그렇지 않은 경우에는 추가 관찰 후 재평가하여 여러가지 소견들을 종합적으로 판단하여 예후를 결정한다. (1) 초기 뇌전산화단층촬영에서 회백질/백질 밀도비 감소 혹은 2-7일째 겉보기 확산계수를 포함한 확산강조 자기공명영상에서 광범위한 확산 제한[31,32]; (2) 24시간 이후 감각유발전위검사에서 양측N20 피질반응 소실[33]; (3) 72시간 이후 뇌파에서 돌발 억제 발생 혹은 뇌파감시에서 36시간 이내에 정상 파형이 발견되지 않음; (4) 24-72시간에 측정한 신경특이에 놀라제(neuron specific enolase: NSE) 고농도 혈청 값; (5) 72시간 이내 근간대경련 지속증 관찰; (6) 72시간 이후 양측 동공반사 및 각막반사의 소실.
주로 사용하는 신경 영상검사 중 컴퓨터단층촬영(computed tomography, CT)인 경우 심정지 발생 24시간 이내 적용이 가능하여 많이 사용하는데 기준 지표로 혼수환자에서 뇌 CT에서 감소된 회백질/백질 밀도비(gray matter/white matter ratio; 정상 1.3 정도)로 나타나는 뇌부종 정도를 평가하고, 뇌 자기공명영상(magnetic resonance imaging)은 2-7일 이내에서 관찰되는 확산 제한 및 확산 제한을 정량화 할 수 있는 겉보기확산계수(apparent diffusion coefficient, 정상 700-800×10-6 mm2/s)의 감소로 예측 가능하다.
심정지 후 목표체온유지치료에 대해 새로 추가된 근거리뷰에서 33℃의 목표체온유지치료와 37.5℃ 이하의 체온 유지법(발열 예방)을 비교한 무작위대조연구(targeted temperature management 2)에서 생존퇴원, 퇴원 180일째 생존율 및 퇴원 180일째 신경학적 예후의 차이가 관찰되지 않았다[38]. 10개의 무작위대조연구를 대상으로 목표 체온의 효과를 비교한 네트워크 메타분석 연구에서도 정상 체온(37-37.8°C)에 비해 31-32°C, 33-34°C, 35-36°C 모두 생존이나 좋은 신경학적 예후에 영향을 주지 못하였고, 이를 근거로 저체온이나 정상 체온 유지보다는 발열 예방이라는 용어를 사용하도록 권고하고 있다[39]. 하지만 후향적 연구들은 심정지로 인한 손상이 클수록 저체온 치료가 좋은 신경학적 예후와 관련이 있음을 제시하고 있다[40,41]. 따라서 현재는 소생 후 목표체온유지치료를 할 때 2020년 한국심폐소생술가이드라인에서 권고한 바와 같이 중심체온을 32-36℃로 유지할 것을 권고하고 있다[42].
심정지 후 치료도 생존사슬의 핵심 요소로 강조되고 있다. 소생 후 통합치료에는 자발순환회복 후 기도 확보, 호흡 유지, 순환 유지를 포함하는 초기 안정화 조치와 심장정지 유발 원인에 대한 진단 및 치료, 목표체온유지요법, 추가적인 뇌 손상을 완화하기 위한 집중치료, 신경학적 예후 예측, 생존자를 위한 지속적인 재활 치료가 포함된다. 앞서 설명된 체계화된 다학제 중재술들을 통해 잠재적으로 더 많은 심정지 환자가 좋은 신경학적 기능을 유지하고 퇴원할 수 있게 된다. 또한, 심정지 생존자를 위한 2차 예방 및 사회재활 등 지속적인 관리계획, 일정 기간이 지나도 의식이 회복되지 않는 환자에 대한 신경학적 예후 등이 새롭게 포함된다. 이러한 새로운 과학적 근거에 기반한 소생 후 통합치료 적용이 심정지 환자의 생존에 기여하기를 기대한다.
Figure 1.
Chain of survival in 2010 vs. 2020 cardiopulmonary resuscitation (CPR) guidelines. EMS, emergency medical system. Reproduced and adapted from Hwang SO et al. Clin Exp Emerg Med 2021;8(S):S8-S14, according to the Creative Commons license [1].

Figure 3.
2020 Korean cardiopulmonary resuscitation algorithm for integrated post-cardiac arrest care. ECG, electrocardiography; PCI, percutaneous coronary intervention; VF/VT, ventricular fibrillation/ventricular tachycardia; TTM, targeted temperature management; CT, computed tomography; EEG, electroencephalography. Adapted from Kim YM et al. Clin Exp Emerg Med 2021;8(S):S41-S64, according to the Creative Commons license [2].
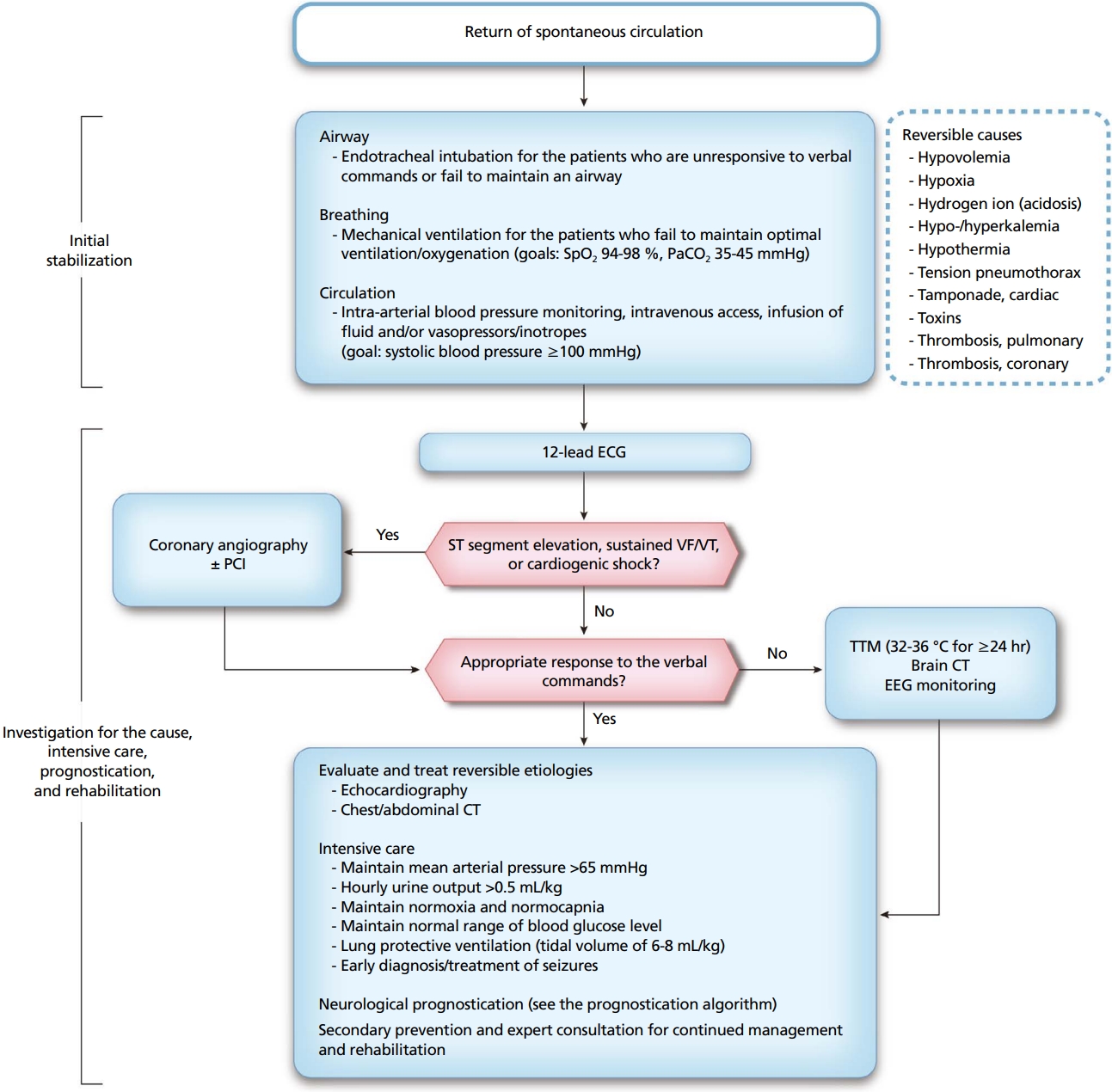
Table 1.
Comparison of neurologic recovery scoring systems between Glasgow-Pittsburgh CPCs and GOS scores
References
1. Hwang SO, Cha KC, Jung WJ, et al. 2020 Korean Guidelines for Cardiopulmonary Resuscitation. Part 2. Environment for cardiac arrest survival and the chain of survival. Clin Exp Emerg Med 2021;8((S):S8-S14.




2. Kim YM, Jeung KW, Kim WY, et al. 2020 Korean Guidelines for Cardiopulmonary Resuscitation. Part 5. Post-cardiac arrest care. Clin Exp Emerg Med 2021;8((S):S41-S64.




3. Neumar RW, Nolan JP, Adrie C, et al. Post-cardiac arrest syndrome: epidemiology, pathophysiology, treatment, and prognostication: a consensus statement from the International Liaison Committee on Resuscitation (American Heart Association, Australian and New Zealand Council on Resuscitation, European Resuscitation Council, Heart and Stroke Foundation of Canada, InterAmerican Heart Foundation, Resuscitation Council of Asia, and the Resuscitation Council of Southern Africa); the American Heart Association Emergenc y Cardiovascular Care Committee; the Council on Cardiovascular Surgery and Anesthesia; the Council on Cardiopulmonary, Perioperative, and Critical Care; the Council on Clinical Cardiology; and the Stroke Council. Circulation 2008;118:2452-2483.

4. Chalkias A, Xanthos T. Pathophysiology and pathogenesis of post-resuscitation myocardial stunning. Heart Fail Rev 2012;17:117-128.



5. Adrie C, Adib-Conquy M, Laurent I, et al. Successful cardiopulmonary resuscitation after cardiac arrest as a “sepsis-like” syndrome. Circulation 2002;106:562-568.


6. Lee MJ, Shin TY, Lee CH, et al. 2020 Korean Guidelines for Cardiopulmonary Resuscitation. Part 9. Education and system implementation for enhanced chain of survival. Clin Exp Emerg Med 2021;8((S):S116-S124.




7. Nunnally ME, Jaeschke R, Bellingan GJ, et al. Targeted temperature management in critical care: a report and recommendations from five professional societies. Crit Care Med 2011;39:1113-1125.


8. Hypothermia after Cardiac Arrest Study Group. Mild therapeutic hypothermia to improve the neurologic outcome after cardiac arrest. N Engl J Med 2002;346:549-556.


9. Bernard SA, Gray TW, Buist MD, et al. Treatment of comatose survivors of out-of-hospital cardiac arrest with induced hypothermia. N Engl J Med 2002;346:557-563.


10. Nolan JP, Laver SR, Welch CA, Harrison DA, Gupta V, Rowan K. Outcome following admission to UK intensive care units after cardiac arrest: a secondary analysis of the ICNARC Case Mix Programme Database. Anaesthesia 2007;62:1207-1216.


11. Suffoletto B, Peberdy MA, van der Hoek T, Callaway C. Body temperature changes are associated with outcomes following in-hospital cardiac arrest and return of spontaneous circulation. Resuscitation 2009;80:1365-1370.


12. Hwang SO. Therapeutic hypothermia after cardiac arrest. Int J Arrhythm 2010;11:31-34.
13. Madden LK, Hill M, May TL, et al. The implementation of targeted temperature management: an evidence-based guideline from the Neurocritical Care Society. Neurocrit Care 2017;27:468-487.



14. Choi HA, Badjatia N, Mayer SA. Hypothermia for acute brain injury: mechanisms and practical aspects. Nat Rev Neurol 2012;8:214-222.



15. Hassager C, Schmidt H, Møller JE, et al. Duration of device-based fever prevention after cardiac arrest. N Engl J Med 2023;388:888-897.


16. Arrich J; European Resuscitation Council Hypothermia After Cardiac Arrest Registry Study Group. Clinical application of mild therapeutic hypothermia after cardiac arrest. Crit Care Med 2007;35:1041-1047.


17. Jakkula P, Reinikainen M, Hästbacka J, et al. Targeting two different levels of both arterial carbon dioxide and arterial oxygen after cardiac arrest and resuscitation: a randomised pilot trial. Intensive Care Med 2018;44:2112-2121.




18. Roberts BW, Kilgannon JH, Hunter BR, et al. Association between elevated mean arterial blood pressure and neurologic outcome after resuscitation from cardiac arrest: results from a multicenter prospective cohort study. Crit Care Med 2019;47:93-100.



19. Spaulding CM, Joly LM, Rosenberg A, et al. Immediate coronary angiography in survivors of out-of-hospital cardiac arrest. N Engl J Med 1997;336:1629-1633.


20. Yannopoulos D, Bartos JA, Raveendran G, et al. Coronary artery disease in patients with out-of-hospital refractory ventricular fibrillation cardiac arrest. J Am Coll Cardiol 2017;70:1109-1117.


21. Thiele H, Akin I, Sandri M, et al. PCI strategies in patients with acute myocardial infarction and cardiogenic shock. N Engl J Med 2017;377:2419-2432.


22. Backman S, Westhall E, Dragancea I, et al. Electroencephalographic characteristics of status epilepticus after cardiac arrest. Clin Neurophysiol 2017;128:681-688.


23. Beretta S, Coppo A, Bianchi E, et al. Neurologic outcome of postanoxic refractory status epilepticus after aggressive treatment. Neurology 2018;91:e2153-e2162.


24. Oksanen T, Skrifvars MB, Varpula T, et al. Strict versus moderate glucose control after resuscitation from ventricular fibrillation. Intensive Care Med 2007;33:2093-2100.



25. Sunde K, Pytte M, Jacobsen D, et al. Implementation of a standardised treatment protocol for post resuscitation care after out-of-hospital cardiac arrest. Resuscitation 2007;73:29-39.


26. Salciccioli JD, Cocchi MN, Rittenberger JC, et al. Continuous neuromuscular blockade is associated with decreased mortality in post-cardiac arrest patients. Resuscitation 2013;84:1728-1733.



27. François B, Cariou A, Clere-Jehl R, et al. Prevention of early ventilator-associated pneumonia after cardiac arrest. N Engl J Med 2019;381:1831-1842.


28. Jeong D, Lee GT, Park JE, et al. Extracorporeal life-support for out-of-hospital cardiac arrest: a nationwide multicenter study. Shock 2022;57:680-686.


29. Suverein MM, Delnoij TS, Lorusso R, et al. Early extracorporeal CPR for refractory out-of-hospital cardiac arrest. N Engl J Med 2023;388:299-309.

30. Kim JH, Kim MJ, You JS, et al. Multimodal approach for neurologic prognostication of out-of-hospital cardiac arrest patients undergoing targeted temperature management. Resuscitation 2019;134:33-40.


31. Lee KS, Lee SE, Choi JY, et al. Useful computed tomography score for estimation of early neurologic outcome in postcardiac arrest patients with therapeutic hypothermia. Circ J 2017;81:1628-1635.


32. Oh JH, Choi SP, Zhu JH, et al. Differences in the gray-to-white matter ratio according to different computed tomography scanners for outcome prediction in post-cardiac arrest patients receiving target temperature management. PLoS One 2021;16:e0258480.



33. Choi SP, Park KN, Wee JH, et al. Can somatosensory and visual evoked potentials predict neurological outcome during targeted temperature management in post cardiac arrest patients? Resuscitation 2017;119:70-75.


34. Tiainen M, Poutiainen E, Oksanen T, et al. Functional outcome, cognition and quality of life after out-of-hospital cardiac arrest and therapeutic hypothermia: data from a randomized controlled trial. Scand J Trauma Resusc Emerg Med 2015;23:12.




35. Schweickert WD, Pohlman MC, Pohlman AS, et al. Early physical and occupational therapy in mechanically ventilated, critically ill patients: a randomised controlled trial. Lancet 2009;373:1874-1882.



36. Fertl E, Vass K, Sterz F, Gabriel H, Auff E. Neurological rehabilitation of severely disabled cardiac arrest survivors. Part I. Course of post-acute inpatient treatment. Resuscitation 2000;47:231-239.


37. Kim DY, Kim YH, Lee J, et al. Clinical practice guideline for stroke rehabilitation in Korea 2016. Brain Neurorehabil 2017;10((Suppl 1):e11.
38. Dankiewicz J, Cronberg T, Lilja G, et al. Hypothermia versus normothermia after out-of-hospital cardiac arrest. N Engl J Med 2021;384:2283-2294.

39. Fernando SM, Di Santo P, Sadeghirad B, et al. Targeted temperature management following out-of-hospital cardiac arrest: a systematic review and network meta-analysis of temperature targets. Intensive Care Med 2021;47:1078-1088.



40. Sandroni C, Natalini D, Nolan JP. Temperature control after cardiac arrest. Crit Care 2022;26:361.




41. Nutma S, Tjepkema-Cloostermans MC, Ruijter BJ, et al. Effects of targeted temperature management at 33 °C vs. 36 °C on comatose patients after cardiac arrest stratified by the severity of encephalopathy. Resuscitation 2022;173:147-153.


42. Chung SP, Sohn Y, Lee J, et al. Expert opinion on evidence after 2020 Korean cardiopulmonary resuscitation guidelines. Clin Exp Emerg Med 2023;Aug. 25. [Epub]. https://doi.org/10.15441/ceem.23.102

Peer Reviewers’ Commentary
이 논문은 심정지 환자에서 심폐소생술 후 발생할 수 있는 심정지 후 증후군의 치료에 대해 최신 문헌을 정리한 논문이다. 급성 심정지 환자에서 심폐소생술 후 자발 순환이 회복되면 심정지 동안이나 자발 순환이 회복된 직후부터 진행되는 전신 허혈 및 재관류에 따른 복잡한 병태생리적 변화가 진행되면서 여러 장기 손상이 초래될 수 있는데, 이를 심정지 후 증후군이라 한다. 심정지 후 치료의 근본적인 목표는 소생 후 증후군에서 나타나는 광범위한 장기 손상을 정상화하고, 좋은 신경학적 예후로 회복시키기 위한 통합적 치료를 제공하는 것이다. 이 논문에서는 심정지 후 좋은 예후와 함께 성공적으로 사회에 복귀하기 위해 궁극적으로 3요소가 필수적임을 강조하고, 이 3개 요소인 중환자 치료, 예후 평가, 통합적 의학-사회 재활 제공에 관하여 자세하면서 이해하기 쉽게 설명하고 있다. 이 논문은 새로운 과학적 근거에 기반한 심정지 후 증후군 환자의 다학제적 통합 치료 적용의 중요성을 잘 설명하고 있어, 심정지 환자를 치료하는 임상 현장에 많은 도움이 될 것으로 판단된다.
[정리: 편집위원회]
-
METRICS

-
- 0 Crossref
- Scopus
- 1,732 View
- 192 Download
-
Related articles in
J Korean Med Assoc -
Management of patients with neuropathic pain2022 August;65(8)
Management of severe pediatric obesity2021 June;64(6)
Management of antithrombotic agents for gastrointestinal endoscopy2020 November;63(11)
Management of Prostate Disorder in Aging Male1998 September;41(9)







