|
 |
- Search
| J Korean Med Assoc > Volume 65(5); 2022 > Article |
|
Abstract
Background: Among the types of gastric cancer, the proportion of early gastric cancer has shown a steady increase because the national screening programs have been conducted in Korea. Accordingly, the paradigm shift of the treatment procedure from surgical gastrectomy to endoscopic resection for selected early gastric cancer has accelerated recently. For successful treatment of early gastric cancer, early detection is essential to accurately predict the histological type, depth of invasion, and horizontal margins of the tumor.
Current Concepts: The diagnosis of early gastric cancer and selection of treatment procedures comprises the following steps: (1) presence diagnosis, (2) qualitative diagnosis, and (3) quantitative diagnosis. Presently, early gastric cancer diagnosis is based on the endoscopic detection of a demarcated lesion and irregularity of the mucosal surface or color pattern. If a lesion is diagnosed as early gastric cancer, qualitative and quantitative diagnostic processes should be conducted. Qualitative diagnosis predicts the histological type (differentiated vs. undifferentiated), whereas quantitative diagnosis predicts the invasion depth and horizontal margins of the lesion. The diagnostic processes are based on the macroscopic morphology and color of the lesion, while sometimes using chromoendoscopy, image-enhanced endoscopy, and magnifying endoscopy.
Discussion and Conclusion: If gastric cancer is detected at an early stage, most cases can be treated only by endoscopic resection. Therefore, endoscopists should have systematic knowledge regarding the findings of early gastric cancer for timely detection and appropriate selection of the treatment procedure.
Current Concepts: The diagnosis of early gastric cancer and selection of treatment procedures comprises the following steps: (1) presence diagnosis, (2) qualitative diagnosis, and (3) quantitative diagnosis. Presently, early gastric cancer diagnosis is based on the endoscopic detection of a demarcated lesion and irregularity of the mucosal surface or color pattern. If a lesion is diagnosed as early gastric cancer, qualitative and quantitative diagnostic processes should be conducted. Qualitative diagnosis predicts the histological type (differentiated vs. undifferentiated), whereas quantitative diagnosis predicts the invasion depth and horizontal margins of the lesion. The diagnostic processes are based on the macroscopic morphology and color of the lesion, while sometimes using chromoendoscopy, image-enhanced endoscopy, and magnifying endoscopy.
Discussion and Conclusion: If gastric cancer is detected at an early stage, most cases can be treated only by endoscopic resection. Therefore, endoscopists should have systematic knowledge regarding the findings of early gastric cancer for timely detection and appropriate selection of the treatment procedure.
위암은 전 세계적으로 5번째로 흔한 암이며, 위암으로 인한 사망은 암사망률 4위에 해당한다[1]. 특히 진단이 늦어져 위암이 진행된 상태에서 발견되는 경우에는 5년 생존율이 급격히 낮아지기 때문에, 가급적 조기에 위암을 발견하는 것이 무엇보다 중요하다[2-4]. 조기 위암(early gastric cancer)은 국소 림프절 전이 여부와 상관없이 점막층 또는 점막하층에 국한된 위암으로 정의되며, 예후는 매우 좋다[5]. 최근에는 국가암검진사업의 일환으로 만 40세 이상부터 2년 주기로 받는 위암 검진 내시경검사가 보편화되면서, 전체 위암 환자 중 조기 위암이 차지하는 비율이 꾸준히 증가되고 있고, 동시에 위암으로 인한 사망률도 점점 낮아지는 추세이다[2,4,6].
또한 전체 위암 중 조기 위암이 차지하는 비율이 증가하면서, 위암 치료의 패러다임이 기존의 외과적 수술에서 내시경적 절제술로 전환되고 있다[2]. 내시경적 절제술 중, 내시경 점막하 박리술(endoscopic submucosal resection, ESD)은 특수 절개도를 사용하여 위암을 절제하는 술기로, 현재 임상에서 가장 선호되는 방법이다. 크기가 큰 병변이나 궤양이 있는 병변도 일괄적으로 절제할 수 있기 때문에 기존의 내시경 점막 절제술(endoscopic mucosal resection)이 가진 한계를 극복했을 뿐만 아니라, 우수한 치료 성적과 함께 위를 보존할 수 있어 환자들의 삶의 질이 향상된다는 장점들을 가진다[7,8]. 이러한 장점들로 인해 ESD는 현재 조기 위암의 표준치료 중 하나로 포함되었으며[2], 최근에는 많은 장기간 성적들을 토대로 ESD의 적응증이 확대되고 있다[7,9]. ESD의 확대 적응증은 (1) 병변의 크기와 상관없이 궤양이 없는 분화형 점막암, (2) 궤양 병변이 있는 경우 크기가 3 cm 이하인 분화형 점막암, (3) 크기가 3 cm 이하이면서 점막하 침윤 깊이가 500 μm 이하인 분화형 암, 그리고 (4) 2 cm 이하의 궤양 병변이 없는 미분화형 점막암이다[10,11].
상기 확대 적응증에서 알 수 있다시피, 조기 위암의 성공적인 내시경 치료를 위해서는 종양의 크기, 침윤 깊이, 궤양의 유무뿐만 아니라 조직형에 대해서도 정확하게 예측하는 것이 중요하다. 이러한 목적을 위해 내시경 생검, 내시경 초음파검사(endoscopic ultrasonography), 확대 내시경(magnifying endoscopy, ME) 등이 사용되고 있지만, 실제 임상에서 가장 기본이 되는 진단 방법은 백색광 내시경검사이다. 이 논문에서는 ESD 시대에서 조기 위암을 발견하기 위한 내시경적 접근법에 대해 살펴보고자 한다.
내시경 영상 기술의 발전으로 과거에 비해 조기 위암을 발견하는 것이 더 쉬워졌다. 하지만 점막 표면에 부착되어 있는 거품과 점액이 그대로 남아있다면, 위점막의 미세한 변화를 놓칠 수밖에 없다. 따라서 점액 용해제와 기포 제거제를 적절하게 사용하여 위점막에 부착되어 있는 점액과 거품들을 잘 씻어내는 것이 필요하다[14,15]. 한편 위장관의 연동 운동으로 인해 자세한 내시경 관찰이 힘든 경우에는 진경제의 사용을 고려해야 한다[14]. 비록 진경제가 조기 위암의 발견을 높인다는 연구 결과는 없지만, 더 나은 시야를 확보하는 것이 조기 위암의 발견율을 높일 수 있어 일부 가이드라인에서는 심한 연동 운동으로 내시경 관찰이 어려운 경우에는 진경제를 사용할 것을 권고하고 있다[14].
내시경검사에서 위암을 놓치는 가장 중요한 원인은 위 내부의 관찰이 불충분하기 때문이다. 위는 내강이 넓은데다 굽어 있기 때문에 시야의 사각 지대가 필연적으로 발생하게 된다. 들문부는 내시경을 반전하여 검사 시 내시경 자체가 시야를 방해하기 때문에 병변을 놓치기 쉽다. 위체부 후벽과 궁륭부도 주요한 맹점 부위이며, 체부 대만 역시 공기를 충분히 주입하여 주름을 펴지 않는다면 숨겨진 병변을 놓칠 수 있다. 비록 내시경검사 시 관찰하는 순서와 방법은 병원이나 내시경검사자에 따라 다르지만, 조기 위암을 놓치지 않으려면 위 내부를 철저하고 체계적으로 관찰하는 것이 필요하다. 이외에도 남아있는 위액을 흡인하고, 공기 주입량을 조절하는 등 기본적인 내시경 조작을 익히는 것이 조기 위암의 발견에 필수적이다.
일부 조기 위암은 점막의 미세한 표면구조 및 색조 변화만을 동반하기 때문에, 내시경검사 시 주의 깊은 관찰을 필요로 한다. 최근의 체계적인 문헌고찰과 메타분석에 따르면 내시경검사 중 위암을 놓치는 비율이 9.4%로 알려져 있어 실제 임상에서는 적지 않은 수의 조기 위암을 놓치고 있을 가능성이 많다[16]. 여러 연구에서 내시경의 관찰시간과 위암 발견과의 연관성을 보고하고 있는데, 15,763명을 대상으로 조기 위암의 발견율을 조사한 연구에 의하면 관찰시간이 5분 미만인 경우가 5분 이상인 경우에 비해 조기 위암의 발견율이 절반 정도로 낮았다[17]. 또한 최근에 발표된 후향적 관찰연구에서도 충분한 내시경 관찰시간이 고위험 병변을 발견하는데 중요한 인자임을 밝힌 바 있다[18]. 유럽소화기내시경학회(European Society of Gastrointestinal Endoscopy)에서도 처음으로 내시경을 시행 받거나 장상피화생이 동반되어 있는 환자에서는 7분 이상 동안 관찰하는 것을 내시경의 질지표로 포함한 바 있다[19]. 이렇듯 충분한 시간 동안 내시경검사를 시행하는 것이 조기 위암의 발견에 필수적이다. 아직까지 이상적인 내시경 관찰시간에 대한 명확한 합의는 없지만, 위암을 놓치는 비율을 낮추기 위해 일반적으로 5-7분간의 내시경 관찰시간을 권고하고 있다.
조기 위암은 (1) 주변 정상 점막과 잘 구분되는 병변(demarcated lesion)과, (2) 색조와 표면구조의 불규칙성, 이 두 가지 내시경 소견을 기반으로 발견할 수 있다[20]. 조기 위암은 Borrmann 위암 분류에서 0형으로 분류되며, 0-I에서 0-III으로 세분화된다. 0-I형은 융기형, 0-II형은 표면형, 0-III형은 함몰형이며, 0-II형은 0-IIa (표면 융기형), 0-IIb (표면 평탄형) 및 0-IIc (표면 함몰형)의 세 가지 아형으로 다시 나뉜다(Figures 1, 2) [6]. 이 중 가장 흔한 유형은 0-IIc형이지만 많은 조기 위암들이 여러 형태의 혼합으로 나타나며, 이러한 경우에는 보다 범위가 넓은 병변부터 순서대로 주형태+부형태 순으로 기술하고 있다(예시: 0-IIb+IIc). 만약 병변의 면적으로 우열을 가리기 어렵다면, 육안적으로 보았을 때 좀 더 두드러지는 유형을 먼저 기재한다.
0-I형의 조기 위암은 내시경검사 시 눈에 잘 띄기 때문에 비교적 진단을 내리기 쉽다. 하지만 0-I형 조기 위암의 발생률은 낮으며, 위용종과의 감별이 어려운 경우도 종종 있다. 위용종의 경우에도 크기가 1 cm 이상인 경우에는 암성 변화가 동반되어 있을 가능성이 있으므로, 내시경 생검을 하거나 용종 절제술을 시행하여 전체 조직을 검사하는 것이 바람직하다[21,22]. 반면 0-IIa형 조기 위암은 선종(adenoma)과 유사해서 주의 깊게 관찰하지 않는 한 감별하기 어렵다. 0-IIa형 조기 위암은 표면에 미란, 융기, 색조 변화 등 주변의 정상 점막과 다른 구조가 동반되어 있고, 쉽게 출혈하는 경향을 가진다. 특히 0-IIa+IIc형 조기 위암은 융기성 미란과 감별하기 어려운데, 일반적인 융기성 미란은 대개 다발성으로 모양이 대칭적이며, 미란의 중심에 염증성 변화가 동반되어 있고 병변이 점막 주름의 중심에 위치하는 것과는 달리, 0-IIa+IIc형 조기 위암은 주로 단발성이고 부정형의 경계를 보이며, 병변이 점막 주름의 한쪽으로 치우친 경우가 많다는 점으로 감별할 수 있다[6,22].
0-IIb형 조기 위암은 주변의 정상 점막과 높이 차이가 없기 때문에 발견하기 어렵다. 색조 변화, 광택 소실, 미세표면구조의 변화를 동반하거나, 공기를 넣고 뺄 때 쉽게 출혈하는 경향을 가지는 병변이 관찰될 때 의심해 볼 수 있다. 그러나 이러한 소견 중 일부는 위축성 위염 및 염증성 병변에서도 관찰되기 때문에 0-IIb형 조기 위암만의 전형적인 특징은 아니다. 일반적으로 0-IIb형 조기 위암은 만성 염증에 비해 크기가 작고 경계가 명확하며, 미세표면구조가 불규칙하다. 0-IIb형 조기 위암은 적색조, 퇴색조, 정상 색조로 관찰되는데, 이 중 적색조 병변이 가장 흔하며 날문부에서 주로 발견되는 반면, 퇴색조 병변은 체부에서 주로 발견된다[6]. 정상 색조 병변은 약간의 불규칙한 표면만을 가지기 때문에 발견하기가 매우 어렵고 우연히 조직검사에서 확인되는 경우가 많다. 전형적인 0-IIb형 조기 위암은 대부분 크기가 2 cm 이하이지만, 크기가 2 cm보다 큰 경우에는 0-IIc형과 같이 다른 형태의 병변과 동반되어 있는 경우가 많다. 이러한 경우에는 영상강화내시경(image-enhanced endoscopy)이나 색소내시경(chromoendoscopy)을 사용하는 것이 정확한 측면 경계를 예측하는 데에 도움이 된다[22].
함몰형 조기 위암은 전체 조기 위암의 70-80%를 차지하기 때문에 조기 위암을 진단하는 데 있어 가장 중요한 병변으로, 미란, 양성 위궤양, 진행성 위암 등 다양한 병변과의 감별이 필요하다[6]. 0-IIc형 조기 위암은 함몰 변연의 재생상피가 고르게 분포하지 않으며, 함몰의 경계가 잠식상을 보인다. 점막 주름의 집중이 동반된 조기 위암에서는 점막 주름의 갑작스러운 단절과 팽대, 가늘어짐, 융합이 관찰되고, 점막 주름들의 연장선이 한 점으로 집중되지 않는 소견을 보인다. 함몰면은 다소 불규칙하고 점막 섬, 요철 부종, 출혈, 부정형 백태 등의 소견을 보이기 때문에, 치유기나 반흔기의 양성 위궤양과 감별할 수 있다[22,23]. 순수한 0-III형 조기 위암은 상대적으로 드물다. 대개 0-IIc형과 동반되어 있는 경우가 많고 뚜렷한 궤양이 관찰되는 경우는 수술 후 병리에서 진행위암으로 나오는 사례가 많기 때문이다. 0-III형 조기 위암에서 암세포는 궤양의 경계에 국한하여 침윤되어 있기 때문에 활동기 또는 치유기의 양성궤양과 구별하기 어려운 경우가 많지만, 궤양의 형태가 불규칙하고 궤양의 바닥면이 주변 점막보다 높고 섬 모양의 종양 점막이 관찰되며 불규칙한 백태로 지저분하게 덮여 있다는 점에서 양성궤양과 어느 정도 감별이 된다. 종종 출혈이나 응고된 혈액들도 관찰되며, 궤양의 경계면은 단단하고 집중된 점막 주름의 변이가 심하고 점막 주름들의 연장선이 한 점에서 만나지 않는다[22,23].
물론 조기 위암의 조직형은 대개 내시경 생검 결과를 통해 확인하지만, 내시경 생검 결과가 병변 전체의 조직형을 정확히 대표할 수 없어 ESD나 외과 수술 후 최종 병리조직검사 결과와 차이가 있는 경우도 적지 않다[26,27]. 이러한 경우에는 육안적으로 보이는 내시경 소견이 조기 위암의 분화도를 예측하는 단서가 될 수 있다.
첫 번째는 색조 변화이다. 내시경의는 위점막의 색조 변화를 통해 크기가 작은 편평 병변이나 함몰 병변을 발견할 수 있을 뿐만 아니라, 위암의 조직형도 어느 정도 예측할 수 있기 때문에, 내시경검사 시 관찰되는 점막의 색조는 위암의 내시경 진단에 매우 중요하다[28]. 조기 위암에서의 색조 변화는 암 병변 점막 내 혈관 밀도와 연관이 있어[29], 일반적으로 분화형 암은 주변 정상 점막과 비교 시 점막 내의 혈관 밀도가 비슷하거나 높기 때문에 동일한 색조 또는 적색조로 보이는 반면, 미분화형 암은 점막 내의 혈관 밀도가 상대적으로 감소되기 때문에 주변 점막에 비해 퇴색조로 관찰된다[6,20,28]. 두 번째는 병변의 육안적 형태이다. 대부분의 융기형(0-I, 0-IIa) 조기 위암은 분화형 암이다. 반면 평탄형(0-IIb) 또는 함몰형(0-IIc, 0-III) 조기 위암은 분화형 암뿐만 아니라 미분화형 암에서도 관찰될 수 있기 때문에, 병변의 색조 변화를 같이 고려하여 조직형을 예측해야 한다[6,20,30]. 마지막으로 배경 점막을 확인하는 것도 조기 위암의 분화도를 예측하는 데 도움을 줄 수 있다. 배경 점막이 심한 위축을 보이거나 장상피화생을 동반하고 있다면 분화형 암인 경우가 많고, 위축이 없거나 경한 경우는 미분화형 암을 고려해야 한다.
조기 위암의 침윤 깊이를 예측하기 위해서는 우선 조기 위암의 육안적 형태 분류를 염두에 두어야 한다. 또한 내시경 검사 시 위 내 공기량을 조절하고, 연동 운동 중 조기 위암의 형태 변화 여부를 관찰하는 것이 중요하다[31].
융기형 조기 위암에서 표면구조가 균일하고 궤양이 동반되어 있지 않다면 점막암의 가능성이 많다. 그리고 융기가 형성된 부위를 면밀하게 관찰하는 것도 위암의 침윤 깊이 예측에 중요한데, 융기 부위가 종양이라면 점막암의 가능성이 높지만 융기 부위가 정상 점막으로 덮여 있고 완만한 융기를 보인다면 심부 점막층 또는 점막하층 이하로 침윤하였을 가능성이 높다. 이외에도 병변 내에 함몰이나 강한 발적이 동반되어 있거나 크기가 2 cm 이상인 경우는 점막하암인 경우가 많다[4,6].
함몰형 조기 위암에서는 강한 발적, 깊은 함몰, 함몰 내 융기가 관찰되거나 변연부 융기가 동반되어 있다면 점막하암의 가능성이 많다[14,32]. 만약 함몰 병변 주변으로 점막 주름의 집중이 동반되어 있다면, 점막 주름 끝의 형태학적 변화가 침윤 깊이를 예측하는 데 중요한 단서가 된다. 함몰된 깊이가 얕고 점막 주름의 끝 부분에서만 불규칙적인 가늘어짐을 보이거나 갑작스러운 주름의 단절을 보인다면 점막암일 가능성이 높다. 반면 함몰면이 딱딱하고 함몰의 경계면에 불규칙적인 형태의 결절이 보이거나 점막 주름들의 곤봉상 비대 또는 융합이 관찰된다면 점막하암인 경우가 많다[6,33,34].
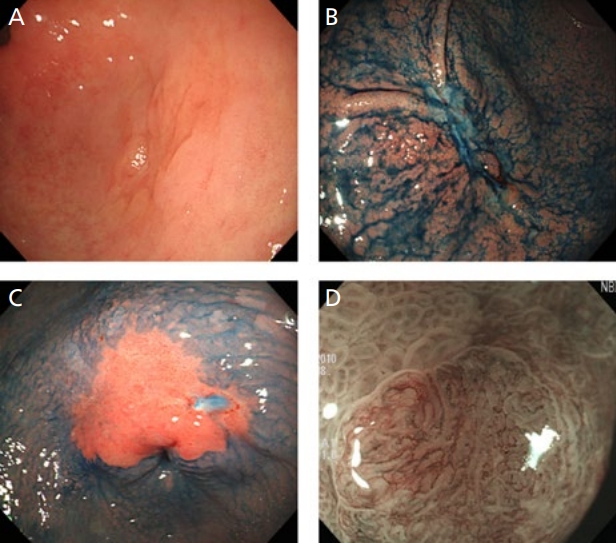
조기 위암의 측면 경계는 주로 백색광 내시경으로 확인하지만, 종양의 높이가 주변 정상 점막과 거의 동일하거나 유사한 색조를 보이는 경우에는 백색광 내시경만으로는 한계가 있다(Figure 3). 실제로 350명의 조기 위암 환자를 대상으로 한 후향적 관찰연구에서 조기 위암의 18.9%에서 측면 경계가 불분명하였으며, 대부분의 경우가 0-IIb형 병변이었다[35]. 바꾸어 말하면 조기 위암의 약 20%에서 ESD 시술 시 불완전 절제의 위험성을 내포하고 있는 것이다.
백색광 내시경으로 측면 경계가 불분명한 경우는 색소내시경이 도움이 된다. 색소내시경을 위해서는 인디고카민(indigo carmine)이 30여 년 전부터 가장 흔히 사용되고 있는데, 이는 점막에 흡수되지 않아 점막 구조의 불규칙성을 잘 보여준다[36,37]. 하지만 색소가 단순히 종양 표면의 불규칙성만을 강조하기 때문에, 심한 장상피화생이 동반된 상황에서는 요철이 지나치게 강조되어 오히려 종양의 경계를 판단하기 어려워진다는 단점이 있다[38]. 여러 연구들에 따르면 조기 위암의 측면 경계 예측에 대한 인디고카민 색소내시경의 정확도는 75.6-85.7%였다[35,39-41]. 일부에서는 바렛식도의 원주 상피를 관찰하기 위해 사용되었던 아세트산의 사용도 보고하고 있지만[42], 조기 위암의 약 42-53%에서만 유용하다고 알려져 있어 실제 사용에는 제한이 있다[43]. 아세트산 분무 후 인디고카민을 산포하는 아세트산-인디고카민 색소내시경도 일부 병원에서 사용되고 있는데, 이는 조기 위암의 측면 경계 진단을 위한 아세트산과 인디고카민의 장점을 합친 검사법으로, 분화형 암의 측면 경계 진단에 정확성이 높다[4,41,44]. 하지만 상기 방법 모두 미분화형 암에서는 정확도가 높지 않아 미분화형 암의 측면 경계를 예측하기 위해서는 병변 주위의 정상으로 보이는 점막을 생검하여 조직병리학적으로 암이 없는지를 확인한 후에 ESD를 위한 절제면을 결정하는 것이 필요하겠다[20].
최근에는 협대역 영상을 이용한 확대 내시경(ME with narrow-band imaging, ME-NBI)이 현 시점에서 위암을 확인하고 측면 경계를 파악하는 데 가장 유용한 방법으로 제시되고 있다[37,45]. ME-NBI와 인디고카민 색소내시경을 비교한 무작위 대조연구에서 위암의 측면 경계를 예측하는 정확도는 ME-NBI에서 유의하게 높았으며(97.4% 대 77.8%, P=0.009) [46], 또 다른 전향적 연구에서도 ME-NBI가 색소내시경에 비해 높은 정확도를 보였다(89.4% 대 75.9%, P=0.0071) [39]. 뿐만 아니라 ME-NBI는 색소내시경과 달리 미분화형 암에서도 유용하게 적용될 수 있음도 보고되고 있다[47,48].
국가암검진사업의 일환으로 검진 상부 소화관 내시경검사가 보편화되고, 또한 내시경 영상 기술이 발전하면서 조기위암의 발견율이 높아지고 있다. 하지만 여전히 적지 않은 수의 조기 위암이 간과되고 있다는 점을 감안한다면 내시경 의사의 세심한 관찰과 함께 위암의 내시경 소견에 대한 지식이 필수적이다. 또한 조기 위암의 치료가 외과적 수술에서 ESD로 패러다임이 전환되고 있는 상황에서 조기 위암을 성공적으로 치료하기 위해서는 단순히 위암을 발견하는 것에서만 그치는 것이 아니라, 이 논문에서 언급한 바와 같이 위암의 질적 및 양적 진단을 통해 적절한 치료 방침을 설정하는 것이 중요하다(Figure 4).
Figure 1.
Macroscopic classification of early gastric cancers. Adapted from Kim GH. Gut Liver 2021;15:811- 817, according to the Creative Commons license [6].
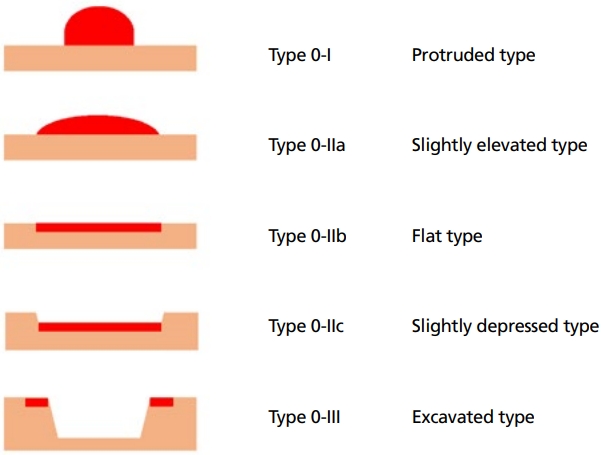
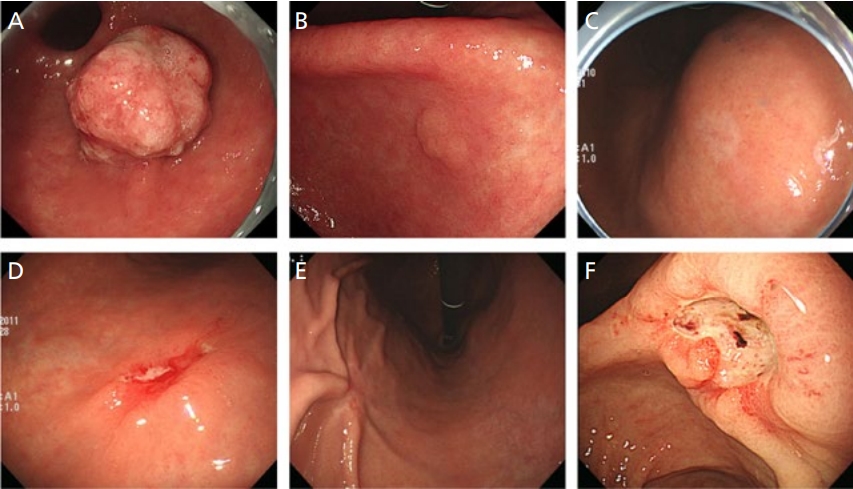
Figure 2.
Examples of early gastric cancers. (A) Type 0-I. (B) Type 0-IIa. (C) Type 0-IIb. (D) Type 0-IIc without ulceration. (E) Type 0-IIc with ulceration. (F) Type 0-III.
References
1. Sung H, Ferlay J, Siegel RL, Laversanne M, Soerjomataram I, Jemal A, Bray F. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin 2021;71:209-249.



2. Lee SH, Kim MC, Jeon SW, Lee KN, Park JJ, Hong SJ. Risk factors and clinical outcomes of non-curative resection in patients with early gastric cancer treated with endoscopic submucosal dissection: a retrospective multicenter study in Korea. Clin Endosc 2020;53:196-205.




3. Park JM. Quality indicator for gastric cancer detection based on Helicobacter pylori status. Clin Endosc 2020;53:629-630.




4. Sumiyama K. Past and current trends in endoscopic diagnosis for early stage gastric cancer in Japan. Gastric Cancer 2017;20((Suppl 1):20-27.


5. Ono H, Kondo H, Gotoda T, Shirao K, Yamaguchi H, Saito D, Hosokawa K, Shimoda T, Yoshida S. Endoscopic mucosal resection for treatment of early gastric cancer. Gut 2001;48:225-229.



6. Kim GH. Systematic endoscopic approach to early gastric cancer in clinical practice. Gut Liver 2021;15:811-817.



7. Jeon HK, Kim GH, Lee BE, Park DY, Song GA, Kim DH, Jeon TY. Long-term outcome of endoscopic submucosal dissection is comparable to that of surgery for early gastric cancer: a propensity-matched analysis. Gastric Cancer 2018;21:133-143.



8. Kim SG, Ji SM, Lee NR, Park SH, You JH, Choi IJ, Lee WS, Park SJ, Lee JH, Seol SY, Kim JH, Lim CH, Cho JY, Kim GH, Chun HJ, Lee YC, Jung HY, Kim JJ. Quality of life after endoscopic submucosal dissection for early gastric cancer: a prospective multicenter cohort study. Gut Liver 2017;11:87-92.



9. Palacios-Salas F, Benites-Goni H, Marin-Calderon L, Bardalez-Cruz P, Vasquez-Quiroga J, Alva-Alva E, Medina-Morales B, Asencios-Cusihuallpa J. Efficacy and safety of endoscopic submucosal dissection for superficial gastric neoplasms: a Latin American cohort study. Clin Endosc 2022;55:248-255.




10. Park CH, Yang DH, Kim JW, Kim JH, Kim JH, Min YW, Lee SH, Bae JH, Chung H, Choi KD, Park JC, Lee H, Kwak MS, Kim B, Lee HJ, Lee HS, Choi M, Park DA, Lee JY, Byeon JS, Park CG, Cho JY, Lee ST, Chun HJ. Clinical practice guideline for endoscopic resection of early gastrointestinal cancer. Clin Endosc 2020;53:142-166.




11. Lee J, Kim BW, Huh CW, Kim JS, Maeng LS. Endoscopic factors that can predict histological ulcerations in early gastric cancers. Clin Endosc 2020;53:328-333.




12. Quach DT, Hiyama T. Assessment of endoscopic gastric atrophy according to the Kimura-Takemoto classification and its potential application in daily practice. Clin Endosc 2019;52:321-327.




13. Bang BW, Kim HG. Endoscopic classification of intestinal metaplasia. Korean J Helicobacter Up Gastrointest Res 2013;13:78-83.

14. Yao K, Uedo N, Kamada T, Hirasawa T, Nagahama T, Yoshinaga S, Oka M, Inoue K, Mabe K, Yao T, Yoshida M, Miyashiro I, Fujimoto K, Tajiri H. Guidelines for endoscopic diagnosis of early gastric cancer. Dig Endosc 2020;32:663-698.



15. Kim GH, Cho YK, Cha JM, Lee SY, Chung IK. Effect of pronase as mucolytic agent on imaging quality of magnifying endoscopy. World J Gastroenterol 2015;21:2483-2489.



16. Pimenta-Melo AR, Monteiro-Soares M, Libanio D, DinisRibeiro M. Missing rate for gastric cancer during upper gastrointestinal endoscopy: a systematic review and metaanalysis. Eur J Gastroenterol Hepatol 2016;28:1041-1049.


17. Kawamura T, Wada H, Sakiyama N, Ueda Y, Shirakawa A, Okada Y, Sanada K, Nakase K, Mandai K, Suzuki A, Kamaguchi M, Morita A, Nishioji K, Tanaka K, Mochizuki N, Uno K, Yokota I, Kobayashi M, Yasuda K. Examination time as a quality indicator of screening upper gastrointestinal endoscopy for asymptomatic examinees. Dig Endosc 2017;29:569-575.



18. Ishibashi F, Kobayashi K, Fukushima K, Tanaka R, Kawakami T, Kato J, Sugihara K. Quality indicators for the detection of Helicobacter pylori-negative early gastric cancer: a retrospective observational study. Clin Endosc 2020;53:698-704.




19. Bisschops R, Areia M, Coron E, Dobru D, Kaskas B, Kuvaev R, Pech O, Ragunath K, Weusten B, Familiari P, Domagk D, Valori R, Kaminski MF, Spada C, Bretthauer M, Bennett C, Senore C, Dinis-Ribeiro M, Rutter MD. Performance measures for upper gastrointestinal endoscopy: a European Society of Gastrointestinal Endoscopy (ESGE) Quality Improvement Initiative. Endoscopy 2016;48:843-864.


20. Yao K, Nagahama T, Matsui T, Iwashita A. Detection and characterization of early gastric cancer for curative endoscopic submucosal dissection. Dig Endosc 2013;25 Suppl 1:44-54.


22. Shim KN. Endoscopic finding of early gastric cancer. Korean J Gastrointest Endosc 2007;34 Suppl 1:254-257.
23. Jee SR. Differential diagnosis of benign and malignant gastric ulcer. Korean J Gastrointest Endosc 2010;42:79-82.
24. Isobe T, Hashimoto K, Kizaki J, Murakami N, Aoyagi K, Koufuji K, Akagi Y, Shirouzu K. Characteristics and prognosis of synchronous multiple early gastric cancer. World J Gastroenterol 2013;19:7154-7159.



25. Lee HJ, Lee YJ, Lee JY, Kim ES, Chung WJ, Jang BK, Park KS, Hwang JS, Cho KB. Characteristics of synchronous and metachronous multiple gastric tumors after endoscopic submucosal dissection of early gastric neoplasm. Clin Endosc 2018;51:266-273.




26. Noh CK, Jung MW, Shin SJ, Ahn JY, Cho HJ, Yang MJ, Kim SS, Lim SG, Lee D, Kim YB, Cheong JY, Lee KM, Yoo BM, Lee KJ. Analysis of endoscopic features for histologic discrepancies between biopsy and endoscopic submucosal dissection in gastric neoplasms: 10-year results. Dig Liver Dis 2019;51:79-85.


27. Kim Y, Yoon HJ, Kim JH, Chun J, Youn YH, Park H, Kwon IG, Choi SH, Noh SH. Effect of histologic differences between biopsy and final resection on treatment outcomes in early gastric cancer. Surg Endosc 2020;34:5046-5054.



28. Kim GH, Kim KB, Lim EK, Choi SH, Kim TO, Heo J, Kang DH, Song GA, Cho M, Park DY. Analysis of endoscopic electronic image of intramucosal gastric carcinoma using a software program for calculating hemoglobin index. J Korean Med Sci 2006;21:1041-1047.



29. Honmyo U, Misumi A, Murakami A, Mizumoto S, Yoshinaka I, Maeda M, Yamamoto S, Shimada S. Mechanisms producing color change in flat early gastric cancers. Endoscopy 1997;29:366-371.


30. Moon HS. Improving the endoscopic detection rate in patients with early gastric cancer. Clin Endosc 2015;48:291-296.




31. Sano T, Okuyama Y, Kobori O, Shimizu T, Morioka Y. Early gastric cancer. Endoscopic diagnosis of depth of invasion. Dig Dis Sci 1990;35:1340-1344.

32. Kim SJ, Park BS, Choi CW, Kim HW, Kang DH, Park SB. Endoscopic features of submucosal invasion in undifferentiated -type early gastric cancer less than 20 mm in size without ulceration. Korean J Helicobacter Up Gastrointest Res 2021;21:127-134.

34. Ono H, Yoshida S. Endoscopic diagnosis of the depth of cancer invasion for gastric cancer. Stomach Intest 2001;36:334-340.
35. Nagahama T, Yao K, Maki S, Yasaka M, Takaki Y, Matsui T, Tanabe H, Iwashita A, Ota A. Usefulness of magnifying endoscopy with narrow-band imaging for determining the horizontal extent of early gastric cancer when there is an unclear margin by chromoendoscopy (with video). Gastrointest Endosc 2011;74:1259-1267.


36. Okabayashi T, Gotoda T, Kondo H, Ono H, Oda I, Fujishiro M, Yachida S. Usefulness of indigo carmine chromoendoscopy and endoscopic clipping for accurate preoperative assessment of proximal gastric cancer. Endoscopy 2000;32:S62.

37. Lee W. Application of current image-enhanced endoscopy in gastric diseases. Clin Endosc 2021;54:477-487.




38. Park JH, Lee JH, Lim YJ, Rhee PL, Kim JJ, Paik SW, Rhee JC, Park CK. Is chromoendoscopy with indigocarmine useful for detecting additional lesions in patients referred for endoscopic resection of gastric adenoma or cancer? Korean J Gastrointest Endosc 2005;30:1-6.
39. Asada-Hirayama I, Kodashima S, Sakaguchi Y, Ono S, Niimi K, Mochizuki S, Tsuji Y, Minatsuki C, Shichijo S, Matsuzaka K, Ushiku T, Fukayama M, Yamamichi N, Fujishiro M, Koike K. Magnifying endoscopy with narrow-band imaging is more accurate for determination of horizontal extent of early gastric cancers than chromoendoscopy. Endosc Int Open 2016;4:E690-E698.



40. Nagahama T, Yao K, Uedo N, Doyama H, Ueo T, Uchita K, Ishikawa H, Kanesaka T, Takeda Y, Wada K, Imamura K, Arima H, Shimokawa T. Delineation of the extent of early gastric cancer by magnifying narrow-band imaging and chromoendoscopy: a multicenter randomized controlled trial. Endoscopy 2018;50:566-576.


41. Iizuka T, Kikuchi D, Hoteya S, Yahagi N. The acetic acid + indigocarmine method in the delineation of gastric cancer. J Gastroenterol Hepatol 2008;23:1358-1361.


42. Guelrud M, Herrera I. Acetic acid improves identification of remnant islands of Barrett’s epithelium after endoscopic therapy. Gastrointest Endosc 1998;47:512-515.


43. Sakai Y, Eto R, Kasanuki J, Kondo F, Kato K, Arai M, Suzuki T, Kobayashi M, Matsumura T, Bekku D, Ito K, Nakamoto S, Tanaka T, Yokosuka O. Chromoendoscopy with indigo carmine dye added to acetic acid in the diagnosis of gastric neoplasia: a prospective comparative study. Gastrointest Endosc 2008;68:635-641.


44. Lee BE, Kim GH, Park DY, Kim DH, Jeon TY, Park SB, You HS, Ryu DY, Kim DU, Song GA. Acetic acid-indigo carmine chromoendoscopy for delineating early gastric cancers: its usefulness according to histological type. BMC Gastroenterol 2010;10:97.




45. Kim JW. Usefulness of narrow-band imaging in endoscopic submucosal dissection of the stomach. Clin Endosc 2018;51:527-533.




46. Kiyotoki S, Nishikawa J, Satake M, Fukagawa Y, Shirai Y, Hamabe K, Saito M, Okamoto T, Sakaida I. Usefulness of magnifying endoscopy with narrow-band imaging for determining gastric tumor margin. J Gastroenterol Hepatol 2010;25:1636-1641.


47. Horiuchi Y, Fujisaki J, Yamamoto N, Shimizu T, Miyamoto Y, Tomida H, Omae M, Ishiyama A, Yoshio T, Hirasawa T, Yamamoto Y, Tsuchida T, Igarashi M, Takahashi H. Accuracy of diagnostic demarcation of undifferentiated-type early gastric cancers for magnifying endoscopy with narrow-band imaging: endoscopic submucosal dissection cases. Gastric Cancer 2016;19:515-523.



Peer Reviewers’ Commentary
이 논문은 상부 소화관 내시경 검사 시 간과될 수 있는 조기 위암의 내시경 소견 및 진단법을 최신 문헌을 기반으로 잘 정리하여 설명해 주고 있다. 조기 위암 진단율이 증가함에 따라 내시경 치료의 적응증이 확대되고 있으며, 이를 통해 진단된 조기 위암의 내시경 절제술이 성공적으로 수행되기 위해서는 발견된 병변의 조직학적 유형, 침윤도, 그리고 병변의 경계를 정확히 예측하는 것이 필수적이다. 이러한 목적을 위해 다양한 검사법들이 사용되고 있지만, 이 논문에서는 가장 기본이 되는 백색광 내시경 검사 시 고려해야 할 사항과 조기 위암을 발견하기 위한 관찰법을 체계적 검사법과 병변의 분류에 따라 설명하고 있다. 또한, 조직형 예측을 통한 질적 진단과 조기 위암의 침윤 깊이와 측면 경계를 진단하는 양적인 진단까지 제시하고 있어 임상 현장에 많은 도움이 될 것으로 판단된다.
[정리: 편집위원회]
-
METRICS

-
- 1 Crossref
- Scopus
- 4,295 View
- 238 Download
-
Related articles in
J Korean Med Assoc -
Endoscopic treatment of colorectal polyps and early colorectal cancer2023 November;66(11)
Classification and endoscopic diagnosis of colorectal polyps2023 November;66(11)
Clinical guidelines for diagnosis of hematuria2023 June;66(6)
Transthoracic needle biopsy for diagnosis of lung cancer2023 March;66(3)