 |
 |
- Search
| J Korean Med Assoc > Volume 63(9); 2020 > Article |
|
Abstract
Chronic obstructive pulmonary disease (COPD) is the third most common cause of death worldwide. It has a prevalence of 14% among Koreans aged above 40 years and a prevalence of 31% among those aged above 65 years. However, only 6% of the COPD patients receive treatment. Most of the patients do not seek medical attention, as they think that dyspnea, cough, and productive sputum, which are the common symptoms of COPD, are normal aging phenomena. Smoking is a major risk factor for COPD, but environmental hazards and genetic susceptibility are also involved. With aging, lung injuries due to these risk factors accumulate, leading to increased prevalence of COPD. The major concerns regarding perioperative management of COPD patients include preoperative evaluation of cardiopulmonary risks, optimization of lung function, and evaluation of COPD-related physiological functions that are easily aggravated during anesthesia. These include respiratory muscle dysfunction, dynamic hyperinflation and auto-positive end-expiratory pressure, hypoxia-hypercarbia, and pulmonary hypertension-associated heart failure. Therefore, anesthesia for COPD patients should focus on preoperative evaluation, risk reduction measures, and prevention of postoperative pulmonary complications.
만성폐쇄성폐질환은 담배, 운동부족, 수명증가에 따라 점점 증가하고 있으며 40세 이상 한국인의 14%, 65세 이상인 경우 31%의 유병률을 보이며(국내 추정 환자 수: 340만 명), 세계적으로 사망원인 3위, 국내 사망원인 8위를 차지하고 있다[1]. 그러나 만성폐쇄성폐질환 환자의 6%(국내 약 20만명)만 치료를 받고 있는데 그 이유로는 환자들이 만성폐쇄성폐질환의 증상인 호흡 곤란, 기침, 가래를 정상적인 노화현상이라고 생각하고, 개인병원에서는 대부분 폐기능검사 장비를 갖추고 있지 않아 진단이 되지 않기 때문이다. 만성폐쇄성폐질환은 폐기능검사를 실시하여 1초강제호기량/강제 폐활량이 예측치의 70% 이하인 경우 진단할 수 있다.
만성폐쇄성폐질환 환자는 수술 후 폐렴, 재기관삽관, 48시간 이상의 장기 기관삽관, 재원일수 증가 및 사망 등의 합병증을 증가시키는 것으로 알려져 있으나[2], 환자 본인이 자신의 질환을 모르고 있는 경우가 많으므로 수술 및 마취를 담당하는 의사들의 주의가 필요하다. 이번 주제에서는 만성폐쇄성폐질환 환자의 수술 전 평가, 수술에 따른 위험을 감소시키기 위한 조치 및 마취관리에 대해 알아보고자 한다.
만성폐쇄성폐질환은 유해한 입자와 가스의 흡입에 의한 만성적으로 진행되는 폐의 염증성 질환으로 제일 중요한 생리학적 특징은 호기 시의 공기 흐름의 제한이다[3]. 가장 중요한 원인은 흡연으로 만성폐쇄성폐질환 환자의 80%가 흡연과 관계가 있다[4]. 1초강제호기량은 흡연의 정도에 비례하여 급격히 감소한다. 흡연 이외에도 호흡기 감염, 탄광 및 금광, 면직물 제조 과정에서의 직업 관련 먼지, 그리고 최근에는 공해도 그 원인으로 알려져 있다. 유전학적 요소로는 FAM13A variant [5], alpha-1 anti-trypsin deficiency [6]가 관련이 있다.
기도폐쇄의 주 부위는 직경 2 mm 이하의 소기도이며 폐의 염증과 파괴가 지속되면 표피세포막과 점액섬모제거장치(mucociliary clearance apparatus)가 훼손되어 염증세포가 기도벽에 침투하고, 술잔세포(goblet cell)와 점액샘이 증가하며, 염증성 가래가 소기도에 정체되고, 결체조직이 기도벽에 증식한다. 염증성 손상의 복구와 이에 따른 기도의 리모델링은 기도벽을 두껍게 하여 기도내경을 좁게 하며 흡기 시의 정상적인 기도확장도 저해한다. 만성폐쇄성폐질환이 진행되면서 폐고혈압이 동반되고 나중에는 우심실 부전이 발생한다.
특징적인 호기 시의 공기 흐름의 제한은 폐쇄세기관지염(obstructive bronchiolitis)으로 인한 소기도 저항의 증가와 폐포의 파괴와 확장으로 인한 폐포의 탄성수축 감소 때문에 발생한다. 이런 현상이 폐기능검사에서 1초강제호기량과 1초강제호기량/강제폐활량 비율의 감소로 나타난다. 이미 소기도의 리모델링이 진행되었기 때문에 천식과 달리 기도폐쇄가 비가역적이며 시간이 지남에 따라 악화된다. 흡입기관확장제에 잘 반응하지 않으며 1초강제호기량의 호전은 평균 15% 정도에 불과하다. 호기와 달리 흡기의 장애는 뚜렷하지 않다.
만성폐쇄성폐질환 환자는 기도저항의 증가와 폐포의 탄성수축력 감소 때문에 호기유속이 감소하여 점진적으로 폐의 과팽창과 공기축적이 발생한다. 따라서 만성폐쇄성폐질환 환자에서 인공호흡기 세팅을 할 때 호기 기간을 줄이면 충분한 호기가 일어나기 전에 다음 번 흡기가 개시되어 매 호흡마다 점점 폐가 팽창하게 되는데 이를 동적 과팽창이라고 한다. 동적 과팽창은 환기관류불균형의 악화, 고탄산혈증, 폐압력손상, 특히 심한 저혈압을 일으킬 수 있다[8]. 이 경우 인공호흡을 중단하고 호흡회로 연결부를 분리하여 흉곽내 감압을 시행해야 한다. 만약 이렇게 해도 혈압이 회복되지 않으면 만성폐쇄성폐질환 환자에게서 흔히 동반하는 큰공기집의 파열로 인한 긴장성기흉을 의심해야 한다. 심한 만성폐쇄성폐질환 환자에서 적절한 흡기:호기 비율은 1:3 이상이다[8].
정상인은 호기말 소기도의 압력이 0 cmH2O이나 만성폐쇄성폐질환 환자는 호기 동안 양압을 유지하여 소기도가 호기 중간에 허탈되는 것을 막는데 이것을 내인성 호기말양압이라고 한다. 마취 시에는 호흡근 이완으로 내인성 호기말양압을 유지할 수 없어 소기도가 허탈 되는데 인공호흡 중 내인성 호기말양압 정도의 압력으로 외부에서 호기말양압을 가하면 소기도의 개방을 유지하여 동적 과팽창을 막고 흡기말 고평부압을 낮출 수 있다[9]. 수술장에서 사용하는 마취기로는 내인성 호기말양압을 측정할 수 없고 각 환자의 내인성 호기말양압이 다 다르므로 환자의 흡기말 고평부압이 높아지지 않는 범위에서 환자의 반응을 잘 관찰하면서 호기말양압을 세팅한다[9]. 외부 호기말양압을 적용하면 환자가 자발 호흡 시 호흡일(work of breathing)도 줄일 수 있다[10].
폐의 과팽창 상태는 횡경막을 아래로 밀고 정상적인 횡경막의 돔 구조를 소실시킨다. 이것은 횡격막의 하방 이동거리를 감소시켜 흡기 시 파워를 약화시킨다. 또한 흡기를 시작할 때 내인성 호기말양압까지 흉강내압을 상승시켜야 하므로 만성폐쇄성폐질환 환자는 만성적으로 호흡일이 증가되어 있고 쉽게 호흡근의 피로와 부전이 발생할 수 있다.
만성폐쇄성폐질환 환자는 소기도의 폐쇄 및 폐포의 파괴로 환기관류불균형(ventilation-perfusion mismatch)이 발생하여 저산소증과 고이산화탄소혈증이 흔하다. 수술 전 동맥혈 산소분압의 감소는 1초강제호기량 <50% 시 나타나며 동맥혈이산화탄소의 증가는 1초강제호기량 <25% 시 나타난다. 수술 전 정상이던 환자에게서 고이산화탄소혈증이 나타난다면 환기관류불균형이 악화되었거나 저호흡을 의미한다. 수술 후에는 일반적으로 무기폐 등이 잘 발생하므로 저산소증 시 산소치료가 도움이 된다. 산소포화도는 환자의 수술 전 상태를 목표로 하고 산소 투여 시에는 맥박산소포화도 88-92% 유지를 목표로 한다. 자발호흡을 하고 있는 만성폐쇄성폐질환 환자에게 고농도의 산소를 투여하는 것은 조직의 산소공급을 증가시키지 못하며 오히려 고이산화탄소혈증을 일으킬 수 있다[11]. 이는 고농도의 산소가 환자의 호흡동인을 약하게 만들고, 폐포의 흡수성 허탈을 일으켜 션트를 증가시키고, 저산소증에 대한 정상적 대응기전인 저산소성 폐혈관수축을 억제하고[11], Haldane effect로 헤모글로빈에서 이산화탄소를 분리시키기 때문이다[12].
수술 전에 최선의 폐기능 상태를 유지하는 것이 중요하다. 첫째, 수술 4-8주 전에 금연이 권장된다[15,16]. 그러나 단지 이틀만 금연을 하여도 일산화탄소 헤모글로빈을 감소시키고 기관섬모운동을 개선할 수 있다. 둘째, 수술을 기다리며 적극적으로 폐질환을 치료한다. 장기지속형 머스카린대항제(long-acting muscarinic antagonists) [17]를 근간으로 장기지속형 베타항진제(long acting beta agonists)와 흡입스테로이드 제제로 치료한다. 예방적 항생제는 권장되지 않으나 감염이 의심되면 항생제로 치료한다. 이러한 치료는 수술 당일 아침까지 유지하고 수술 후 빠른 시일 내에 재개한다. 수술 중 기관지경련이 발생하였을 때는 속효성 베타항진제(salbutamol, terbutaline, levalbuterol)를 사용한다. 거담제의 효과는 확실치 않으나 객담이 많은 환자에게 도움이 될 수 있다. 만약 고용량으로 스테로이드를 흡입 또는 전신투여 받고 있던 환자라면 시상하부 뇌하수체 축 억제 및 부신기능부전이 나타날 수 있으므로 지난 6개월 동안 3주 이상 투여 받고 큰 수술이 예정되어 있다면 수술 전 스테로이드를 투여한다. 셋째, 흉부 물리치료, 운동 및 영양 처방과 교육을 시행하는 것이 도움이 된다[18]. 기침, 심호흡, 인센티브 폐활량 측정, 호기말양압, 지속적 양압 등을 시행할 수 있다.
수술 전 폐기능검사는 잘 조절되고 있는 만성폐쇄성폐질환 환자에게 꼭 필요한 것은 아니다. 그러나 임상적 판단만으로는 환자의 폐기능의 적정성을 판단하기 어려울 때 그리고 환자가 호흡곤란과 운동부하를 견디지 못할 때 시행하고 폐수술인 경우 대부분 시행해야 한다. 폐기능검사 상 수술에 금기가 되는 기준은 확립되어 있지 않다. 다만 폐수술을 받는 환자의 폐기능에 따른 처치 가이드라인은 Figure 1과 같다. 먼저 문진으로 환자의 운동 능력을 파악하고 대사등가물 2를 기준으로 그 이하면 수술적 치료를 피한다. 대사등가물 2 이상이면 폐기능검사를 시행한다. 1초 강제호기량과 일산화탄소확산능이 모두 수술 후 예상치의 60%를 넘는 경우 더 이상의 추가검사가 필요 없고, 둘 중 하나라도 30-60% 사이에 있으면 6분걷기테스트 등의 간단한 운동검사를 시행한다. 둘 중 하나라도 30% 미만이면 정식 운동부하검사를 시행한다. 이 경우 최대산소소모량 10 mL/kg/min을 기준으로 수술 여부를 결정한다.
동맥혈가스분석은 대부분 필요하지 않으나 큰 수술을 받거나 3시간 이상의 수술을 받는 만성폐쇄성폐질환 3, 4기의 경우 필요하다[19]. 동맥혈가스분석은 환자의 기저 산소 및 이산화탄소의 혈중농도에 맞추어 인공호흡기를 세팅하는데 도움이 된다. 또한 수술 후 산소치료나 인공호흡기의 필요성을 판단하는데 도움을 준다.
만성폐쇄성폐질환 증상이 갑자기 악화되거나 상기도 감염이 의심되는 경우 수술 시 합병증이 크게 증가하므로 가능한 수술을 미루는 것이 좋다. 미루는 기간은 환자의 증상이 원래 기저 수준으로 돌아갈 때까지로 환자마다 다르다. 그 기간 동안 주로 흡입기관지확장제와 머스카린대항제 그리고 짧은 기간의 전신 스테로이드, 항생제 치료가 시행된다[21].
마취 전 진정 및 진통 목적으로 벤조다이아제핀계 항불안제 및 마약성제제의 투여는 저산소증과 고이산화탄소혈증에 대한 호흡반응을 둔화시키기 때문에 주의해야 한다. 마취는 수술의 종류와 환자 및 집도의의 선호가 반영되어야 하지만 전신마취는 피하는 것이 좋다[22]. 전신마취와 이에 사용되는 마취제 및 인공호흡기 회로는 표면활성물질의 생산을 방해하고, 점액섬모 청소율을 낮추고, 폐포-모세관 장벽의 투과성을 높인다[23]. 또한 기관삽관에 따른 후두 및 기도 경련, 폐손상, 수술 후 폐렴, 기관발관 실패와 장기간의 인공호흡의 위험을 높인다[22]. 그러나 환자가 전신마취가 필요한 수술, 장시간의 수술, 심한 호흡곤란, 불안, 앙와위를 취할 수 없거나 기침이 지속적일 때는 전신마취를 시행해야 한다.
마취 유도는 부드럽게 하여 기도의 자극을 최소화하고 마취가 얕은 상태에서 기관삽관을 하는 것을 피해야한다. 만성폐쇄성폐질환 환자의 기관삽관 시 후두경련을 피하기 위해 기관튜브 보다는 후두마스크가 선호되나 이 두가지를 비교한 연구는 없다[24]. 흡입가스로 인한 기도 자극을 방지하기 위해 흡입마취보다는 정맥마취로 마취를 유도하는 것이 권장된다. 또한 흡입마취는 폐포의 파괴와 환기관류불균형 때문에 마취유도에 오랜 시간이 걸린다[25]. 다만 마취유지는 흡입마취제가 기관확장 작용이 있으므로 선호된다(예: 세보플루란). 소량의 마약성 진통제를 추가하면 마취 심도를 높이고 기침반사를 억제할 수 있다(예: 펜타닐). 마취 중 기관경련이 일어나면 즉시 마취심도를 깊게 하고 흡입기관지확장제를 투여한다.
전신마취 동안 인공호흡은 동적 과팽창과 내인성 호기말양압을 막는데 집중하여야 한다. 이를 위해서 폐보호환기법을 사용하는데 일회호흡량(5-8 mL/kg 예상체중)과 호흡수를 줄이고 호기시간을 늘려야 한다[26]. 흡기 고평부압은 15-20 cmH2O 이하로 유지한다. 흡기시간을 줄이는 것은 최고 흡기유속을 증가시켜 전체 폐포의 환기를 좋게 한다[27]. 그러나 이러한 환기법은 분당 호흡량의 감소로 고탄산혈증을 일으킬 수 있는데 어느 정도의 고탄산혈증은 환자에게 특별한 문제를 일으키지 않으므로 pH ≥7.25 이상이라면 허용한다. 다만 뇌압이 높거나 폐고혈압/우심부전이 있는 환자에서는 고탄산혈증을 피해야 한다.
만성폐쇄성폐질환 환자는 인공호흡동안 긴장성기흉이 발생하기 쉬운데 이는 큰공기집이 양압환기로 파열되기 때문이다. 긴장성기흉은 동적 과팽창과 유사한 증상으로 나타나나 동적 과팽창은 일시적으로 호흡회로를 분리하여 흉곽 내 압력을 감소시키면 1분 이내에 혈압이 정상화되나 긴장성기흉는 지속적인 저혈압을 보인다
만성폐쇄성폐질환 환자는 수술 중 저혈압이 발생하기 쉬운데 이는 폐의 과팽창이 직접적으로 심장 및 폐동맥을 압박하고, 흉곽 내 압력 증가로 전신정맥 환류가 감소하고 폐혈관저항이 상승하기 때문이다. 이것은 우심실의 스트레스를 증가시키고 심실중격의 좌측 이동을 만들어 좌심실의 충만을 저해하고 심박출량을 떨어뜨린다[26].
수술 종료 시 환자의 상태는 수술 전 상태와 가깝게 최적화되어야 한다. 신경근차단제는 완전하게 역전하고 반드시 말초신경 자극기로 평가한다. 잔류 신경근차단은 상기도의 폐쇄, 횡격막 부전, 점막섬모 제거의 부전, 저호흡을 일으킨다[28]. 기관발관 직전 흡입기관지확장제를 투여하는 것이 도움이 되고 고위험 환자에게는 발관과 동시에 비침습적 환기보조를 실시하여 호흡일을 줄이고 소기도의 폐쇄를 막는다. 수술 직후 환자가 덜 깨거나 근이완 역전이 불충분 하거나 통증이 있거나 마약성 제제의 사용으로 심호흡을 하지 못하고 기침을 잘 못하는 경우, 가래가 축적되고 무기폐가 생기며 저산소증이 발생할 수 있다. 호흡곤란을 보이는 환자는 증상의 악화 여부를 관찰하며 기다리기 보다 증상의 초기에 즉시 비침습적 환기보조를 시행하여야 한다[29].
수술 후에는 다양한 진통제를 병용하여 통증효과의 상승작용과 함께 단독 약물의 부작용(진정, 호흡억제, 메스꺼움 및 구토)을 줄일 수 있다. 주로 마약성진통제, 파라세타몰 및 비스테로이드 항염증제의 병용이 권장된다. 경막외진통은 마약성진통제의 사용을 줄여 호흡억제를 감소시키므로 적극적으로 고려한다[30].
저농도의 국소마취제와 마약제제를 병용하는 흉부 경막외마취는 통증자극을 차단하고 교감신경의 활성화를 차단한다. 그리하여 호흡근의 활동성을 보존하고 저산소성 폐혈관수축 반응을 보존한다. 호흡기의 저항과 호흡일을 줄이고 흡기 및 호기 폐용적을 더 잘 보존하며 환자가 스스로 객담을 배출할 수 있게 한다[31]. 단점은 사용된 국소마취제가 늑간근을 약화시킬 수 있고 교감신경차단은 저혈압을 일으키고 부교감신경을 항진시켜 호흡근경련을 일으킬 수 있다는 것이다[22]. 요추 부위에 제한된 척추 및 경막외 마취는 호흡근에 큰 영향을 미치지는 않으나 고도비만 환자의 경우 복근의 움직임을 차단하여 1초강제호기량과 강제폐활량을 20-25% 감소시켜 기침을 하거나 가래를 배출하는데 장애를 일으킬 수 있다[32]. 심한 만성폐쇄성폐질환 환자에게서 척추 경막외 병용마취와 진정 하 비침습적 호흡보조를 시행하여 성공적으로 수술을 시행한 보고들이 있어[33] 전신마취를 피하고자 하는 고도의 폐쇄성폐질환 환자에게 대안이 될 수 있다.
횡경막 근처의 수술(흉부 및 상복부)은 폐의 움직임을 제한하여 총폐용적과 기능적 잔기용량의 30%, 1초강제호기량의 40-60%를 감소시켜[36] 무기폐, 환기관류불균형의 악화, 저산소증 및 호흡부전을 일으킬 수 있다.
Figure 1.
Management of patients undergoing thoracic surgery according to pulmonary function tests. METS, metabolic equivalent of task; ppoDLCO, predicted postoperative diffusion for carbon monoxide; ppoFEV1, predicted postoperative forced expiratory volume in 1 second; 6MWT, 6 minute walk test distance in meters; VO2max, maximum rate of oxygen consumption.
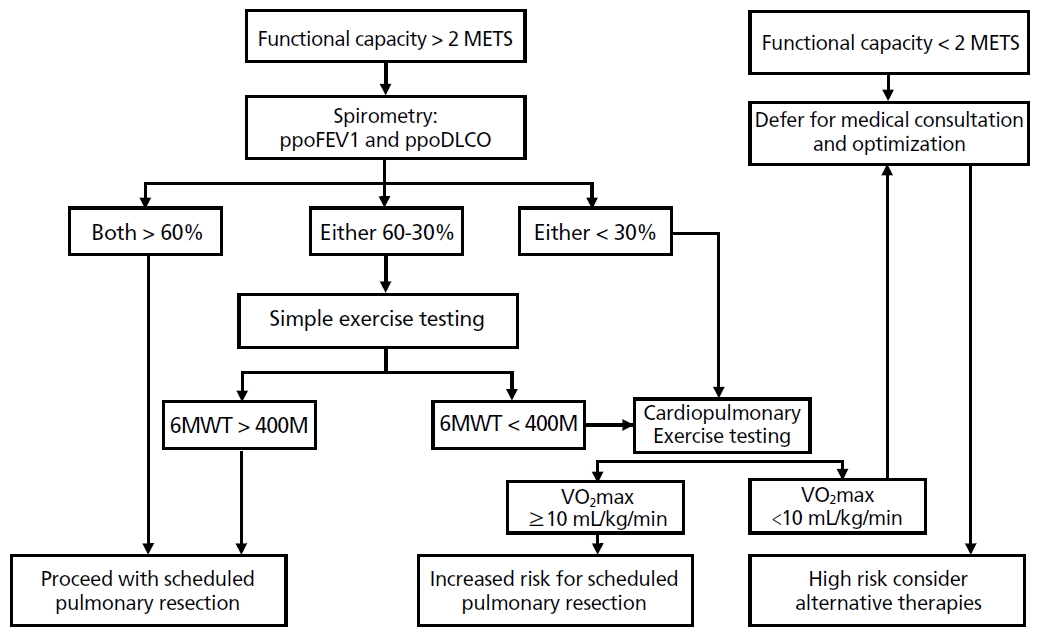
Table 1.
Classification of chronic obstructive pulmonary disease (American Thoracic Society/European Respiratory Society 2004 guideline for chronic obstructive pulmonary disease)
| Classification | FEV1/FVC after bronchodilator | FEV1 (%) |
|---|---|---|
| At risk | >0.7 | ≥80 |
| Mild: grade 1 | ≤0.7 | ≥80 |
| Moderate: grade 2 | ≤0.7 | 50-79 |
| Severe: grade 3 | ≤0.7 | 30-49 |
| Very severe: grade 4 | ≤0.7 | <30 |
References
1. Korea Centers for Diseases Control and Prevention. 2014 Korean National Health and Nutrition Examination Survey. Sejong: Ministry of Health and Welfare; 2015.
2. Fields AC, Divino CM. Surgical outcomes in patients with chronic obstructive pulmonary disease undergoing abdominal operations: an analysis of 331,425 patients. Surgery 2016;159:1210-1216.


3. Pauwels RA, Buist AS, Calverley PM, Jenkins CR, Hurd SS; GOLD Scientific Committee. Global strategy for the diag-nosis, management, and prevention of chronic obstructive pulmonary disease. NHLBI/WHO Global Initiative for Chronic Obstructive Lung Disease (GOLD) Workshop summary. Am J Respir Crit Care Med 2001;163:1256-1276.


5. Cho MH, Boutaoui N, Klanderman BJ, Sylvia JS, Ziniti JP, Hersh CP, DeMeo DL, Hunninghake GM, Litonjua AA, Sparrow D, Lange C, Won S, Murphy JR, Beaty TH, Regan EA, Make BJ, Hokanson JE, Crapo JD, Kong X, Anderson WH, Tal-Singer R, Lomas DA, Bakke P, Gulsvik A, Pillai SG, Silverman EK. Variants in FAM13A are associated with chronic obstructive pulmonary disease. Nat Genet 2010;42:200-202.




6. Brode SK, Ling SC, Chapman KR. Alpha-1 antitrypsin deficiency: a commonly overlooked cause of lung disease. CMAJ 2012;184:1365-1371.



7. Celli BR, Decramer M, Wedzicha JA, Wilson KC, Agusti A, Criner GJ, MacNee W, Make BJ, Rennard SI, Stockley RA, Vogelmeier C, Anzueto A, Au DH, Barnes PJ, Burgel PR, Calverley PM, Casanova C, Clini EM, Cooper CB, Coxson HO, Dusser DJ, Fabbri LM, Fahy B, Ferguson GT, Fisher A, Fletcher MJ, Hayot M, Hurst JR, Jones PW, Mahler DA, Maltais F, Mannino DM, Martinez FJ, Miravitlles M, Meek PM, Papi A, Rabe KF, Roche N, Sciurba FC, Sethi S, Siafakas N, Sin DD, Soriano JB, Stoller JK, Tashkin DP, Troosters T, Verleden GM, Verschakelen J, Vestbo J, Walsh JW, Washko GR, Wise RA, Wouters EF, ZuWallack RL; ATS/ERS Task Force for COPD Research. An official American Thoracic Society/European Respiratory Society statement: research questions in COPD. Eur Respir J 2015;45:879-905.


8. Yamakage M, Iwasaki S, Namiki A. Guideline-oriented periope-rative management of patients with bronchial asthma and chronic obstructive pulmonary disease. J Anesth 2008;22:412-428.



9. Caramez MP, Borges JB, Tucci MR, Okamoto VN, Carvalho CR, Kacmarek RM, Malhotra A, Velasco IT, Amato MB. Paradoxical responses to positive end-expiratory pressure in patients with airway obstruction during controlled ventilation. Crit Care Med 2005;33:1519-1528.



10. Cabrini L, Nobile L, Plumari VP, Landoni G, Borghi G, Mucchetti M, Zangrillo A. Intraoperative prophylactic and therapeutic non-invasive ventilation: a systematic review. Br J Anaesth 2014;112:638-647.



12. Hanson CW 3rd, Marshall BE, Frasch HF, Marshall C. Causes of hypercarbia with oxygen therapy in patients with chronic obstructive pulmonary disease. Crit Care Med 1996;24:23-28.


13. MacNee W. Pathophysiology of cor pulmonale in chronic obstructive pulmonary disease. Part One. Am J Respir Crit Care Med 1994;150:833-852.


14. Lemaire F, Teboul JL, Cinotti L, Giotto G, Abrouk F, Steg G, Macquin-Mavier I, Zapol WM. Acute left ventricular dysfunction during unsuccessful weaning from mechanical ventilation. Anesthesiology 1988;69:171-179.



15. Vaporciyan AA, Merriman KW, Ece F, Roth JA, Smythe WR, Swisher SG, Walsh GL, Nesbitt JC, Putnam JB Jr. Incidence of major pulmonary morbidity after pneumonectomy: association with timing of smoking cessation. Ann Thorac Surg 2002;73:420-425.


16. Henzler D, Dembinski R, Kuhlen R, Rossaint R. Anesthetic considerations in patients with chronic pulmonary diseases. Minerva Anestesiol 2004;70:279-284.

17. Woods BD, Sladen RN. Perioperative considerations for the patient with asthma and bronchospasm. Br J Anaesth 2009;103 Suppl 1:i57-i65.



18. Warner DO. Preventing postoperative pulmonary complications: the role of the anesthesiologist. Anesthesiology 2000;92:1467-1472.



19. Smetana GW, Lawrence VA, Cornell JE; American College of Physicians. Preoperative pulmonary risk stratification for noncardiothoracic surgery: systematic review for the American College of Physicians. Ann Intern Med 2006;144:581-595.


20. Canet J, Gallart L, Gomar C, Paluzie G, Valles J, Castillo J, Sabate S, Mazo V, Briones Z, Sanchis J; ARISCAT Group. Prediction of postoperative pulmonary complications in a population-based surgical cohort. Anesthesiology 2010;113:1338-1350.



21. Duggappa DR, Rao GV, Kannan S. Anaesthesia for patient with chronic obstructive pulmonary disease. Indian J Anaesth 2015;59:574-583.



22. Hausman MS Jr, Jewell ES, Engoren M. Regional versus general anesthesia in surgical patients with chronic obstructive pulmonary disease: does avoiding general anesthesia reduce the risk of postoperative complications? Anesth Analg 2015;120:1405-1412.


23. Licker M, Schweizer A, Ellenberger C, Tschopp JM, Diaper J, Clergue F. Perioperative medical management of patients with COPD. Int J Chron Obstruct Pulmon Dis 2007;2:493-515.


24. Kim ES, Bishop MJ. Endotracheal intubation, but not laryngeal mask airway insertion, produces reversible bronchocon-striction. Anesthesiology 1999;90:391-394.



25. Eger EI 2nd, Severinghaus JW. Effect of uneven pulmonary distribution of blood and gas on induction with inhalation anesthetics. Anesthesiology 1964;25:620-626.



26. Edrich T, Sadovnikoff N. Anesthesia for patients with severe chronic obstructive pulmonary disease. Curr Opin Anaesthesiol 2010;23:18-24.


27. Maddali MM. Chronic obstructive lung disease: perioperative management. Middle East J Anaesthesiol 2008;19:1219-1239.

28. Grosse-Sundrup M, Henneman JP, Sandberg WS, Bateman BT, Uribe JV, Nguyen NT, Ehrenfeld JM, Martinez EA, Kurth T, Eikermann M. Intermediate acting non-depolarizing neuro-muscular blocking agents and risk of postoperative respiratory complications: prospective propensity score matched cohort study. BMJ 2012;345:e6329.



29. Faria DA, da Silva EM, Atallah AN, Vital FM. Noninvasive positive pressure ventilation for acute respiratory failure following upper abdominal surgery. Cochrane Database Syst Rev 2015;(10):CD009134.

30. van Lier F, van der Geest PJ, Hoeks SE, van Gestel YR, Hol JW, Sin DD, Stolker RJ, Poldermans D. Epidural analgesia is associated with improved health outcomes of surgical patients with chronic obstructive pulmonary disease. Anesthesiology 2011;115:315-321.



31. Groeben H, Schäfer B, Pavlakovic G, Silvanus MT, Peters J. Lung function under high thoracic segmental epidural anesthesia with ropivacaine or bupivacaine in patients with severe obstructive pulmonary disease undergoing breast surgery. Anesthesiology 2002;96:536-541.



32. Regli A, von Ungern-Sternberg BS, Reber A, Schneider MC. Impact of spinal anaesthesia on peri-operative lung volumes in obese and morbidly obese female patients. Anaesthesia 2006;61:215-221.


33. Yi JW, Choi SE, Chung JY. Laparoscopic cholecystectomy performed under regional anesthesia in patient who had undergone pneumonectomy: a case report. Korean J Anesthesiol 2009;56:330-333.



34. Sanchez M, Malhotra N, Lin L. End-stage pulmonary disease and brachial plexus regional anesthesia: their implications on perioperative pulmonary function. Semin Cardiothorac Vasc Anesth 2012;16:59-64.


35. Long TR, Wass CT, Burkle CM. Perioperative interscalene blockade: an overview of its history and current clinical use. J Clin Anesth 2002;14:546-556.


36. Hedenstierna G, Edmark L. The effects of anesthesia and muscle paralysis on the respiratory system. Intensive Care Med 2005;31:1327-1335.



37. Tanskanen P, Kytta J, Randell T. The effect of patient positioning on dynamic lung compliance. Acta Anaesthesiol Scand 1997;41:602-606.


38. Mure M, Domino KB, Lindahl SG, Hlastala MP, Altemeier WA, Glenny RW. Regional ventilation-perfusion distribution is more uniform in the prone position. J Appl Physiol (1985) 2000;88:1076-1083.


39. Johnson N, Barlow D, Lethaby A, Tavender E, Curr L, Garry R. Methods of hysterectomy: systematic review and meta-analysis of randomised controlled trials. BMJ 2005;330:1478.



40. Numata T, Nakayama K, Fujii S, Yumino Y, Saito N, Yoshida M, Kurita Y, Kobayashi K, Ito S, Utsumi H, Yanagisawa H, Hashimoto M, Wakui H, Minagawa S, Ishikawa T, Hara H, Araya J, Kaneko Y, Kuwano K. Risk factors of postoperative pulmonary complications in patients with asthma and COPD. BMC Pulm Med 2018;18:4.



Peer Reviewers’ Commentary
만성폐쇄성폐질환은 담배, 운동부족, 수명 증가에 따라 우리 주위에서 흔히 볼 수 있으며, 65세 이상에서 31%의 유병률을 보이는 질환이다. 최근 인구 고령화와 환경 오염으로 인해 만성폐쇄성폐질환의 유병률이 증가하고 있어, 이 기저질환을 지닌 채 다른 수술을 받으러 오는 환자의 비율도 함께 증가할 것으로 예상된다. 이 논문은 만성폐쇄성폐질환을 동반한 환자의 마취관리에 대한 최신 지식을 정리하여 소개해 주고 있다. 만성폐쇄성 폐질환 환자에게 수술이 필요한 경우, 수술 외에도 마취로 인한 합병증의 발생 가능성은 진료의들에게 큰 부담이 아닐 수 없다. 이 논문은 이러한 상황에서 마취 및 수술의 중요한 변수, 수술 후 부작용 감소를 위한 처치, 수술 전 검사, 수술 연기, 마취유도 마취유지 및 수술 후 통증관리, 그리고 수술 등에 대하여 포괄적이면서도 심도 있게 설명하고 있어, 수술을 앞둔 만성폐쇄성폐질환을 동반한 환자를 돌보는 의사들에게 환자에 대한 이해와 관리에 많은 도움을 줄 것으로 판단된다.
[정리: 편집위원회]
-
METRICS

-
- 0 Crossref
- Scopus
- 8,127 View
- 187 Download
-
Related articles in
J Korean Med Assoc -
Treatment of Mycobacterium abscessus complex pulmonary disease2024 January;67(1)
Treatment of Mycobacterium avium complex pulmonary disease2024 January;67(1)
Increasing burden of nontuberculous mycobacterial pulmonary disease2024 January;67(1)
Management of patients with neuropathic pain2022 August;65(8)
Diagnosis and treatment of patients with heat-related illnesses2021 April;64(4)






