갑상샘 수술치료의 새로운 개념: 구강내시경수술 및 로봇수술
Current concepts in thyroid gland surgery: transoral endoscopic and robotic surgical procedures
Article information
Trans Abstract
The increased incidence of thyroid cancer in young females may raise concerns about visible hypertrophic scarring on the center of the neck after thyroid gland surgery. Therefore, endoscopic surgical procedures have attracted significant interest from patients with thyroid cancer, leading to the development of various endoscopic and robotic approaches. Although the cosmetic outcomes of current endoscopic and robotic thyroid surgeries have been excellent, all the procedures still require a large incision and extensive flap elevation. Transoral endoscopic thyroid surgery is a newly developed surgical method performed by inserting an endoscope through a mucosal opening created in the mouth, obviating the need for a skin incision. Additionally, the dissection area is relatively small and no dressings are required. Showering or shaving may resume the day after surgery and the port created within the oral mucous membrane generally heals within one week. Importantly, this approach is markedly less invasive than other endoscopic approaches. Although transoral endoscopic thyroid surgery has not yet been universally accepted, it may emerge as the preferred method for thyroid surgery in the near future.
서론
1. 갑상샘 내시경수술의 시작
갑상샘암은 우리나라에서 가장 많이 발생하는 암 중에 하나이다. 특히 여성에게 많이 발생하는 암으로 알려져 있으며 지속적으로 증가하고 있다. 예후가 매우 좋으므로 초기암의 경우에는 경과관찰을 하기도 하지만 아직까지 가장 확실한 치료방법은 수술적 절제이다. 일반적인 갑상샘암 수술방법은 쇄골과 흉골 상부에 약 5 cm 정도의 절개를 하고 갑상샘의 한쪽 또는 양쪽 엽을 제거하는 것이다. 이 수술방법은 19세기 후반에 스위스의 외과의사인 Theodor Kocher가 처음으로 정립하였으며, 오랜 기간동안 갑상샘암의 가장 확실한 치료방법으로 인정받고 있지만 수술 후에 목에 흉터가 남는다는 단점이 있다. 갑상샘암 환자들은 비교적 젊고 예후가 좋아 수술 후에도 사회활동을 주로 활발하게 하므로 수술 흉터에 관심을 가지고 흉터를 줄이는데 많은 비용을 지출하고 있다[1-3]. 특히, 동양인의 피부는 백인에 비해 비후성 흉터가 더 잘 생기므로 우리나라 환자들이 수술 흉터에 더욱 민감할 수밖에 없다.
이러한 이유로 각국의 많은 연구자들이 갑상샘 수술 흉터를 줄이기 위해 노력을 하였지만 한계에 부딪치게 되었고, 그 대신에 흉터를 옷으로 가려지는 부위로 옮기는데 성공을하여 지금의 내시경 수술법들을 개발하게 되었다. Gagner등[4]과 Huscher 등 [5]이 처음으로 갑상샘 내시경수술을 하고 결과를 보고하였고, 이후에 일본의 연구자들을 중심으로 다양한 수술법들을 개발하게 되었다[6-8]. Ikeda등[7]과 Ikeda등[8]이 axillary approach 방법을, Ohgami등[6]이 breast approach 방법을 처음 개발하였다. 하지만, 현재는 한국의 의료진들이 세계적으로 가장 활발하게 다양한 수술법들을 개발하여 보고하고 있다. 겨드랑이에 절개를 하여 접근하는 겨드랑이 접근법(transaxillary approach), 가슴과 겨드랑이의 네 개의 구멍을 통해 접근하는 BABA접근법(bilateral axillo-breast approach, BABA), 귀 뒤쪽 헤어 라인 안쪽에 절개를 해서 접근하는 귀뒤접근법(retroauricular approach)이 지금까지 국내외적으로 가장 많이 사용되어 왔던 수술법들이다[9-16]. 이러한 여러 수술방법들은 흉터를 숨기기 위해 절개 길이가 더 길어지고 더 광범위한 면적의 피부 아래 조직을 박리해야만 했으므로, 미용적으로는 우수한 결과를 보이지만 더 침습적인 수술법이라는 비판을 받기도 했다.
2. 로봇을 이용한 갑상샘 수술의 시작
의료용 로봇은 군사적인 목적으로 미국 국방부에서 처음 개발하기 시작하였다. 로봇을 원격으로 조정해서 전쟁터에서 바로 수술을 하려고 개발하였고[17,18], 이후에 민간업체가 시장성에 초점을 맞추어서 다목적 수술로봇으로 변형하여 개발하였다. 현재는 인튜이티브서지컬(Intuitive Surgical Inc.)의 다빈치 로봇(da Vinci surgical system)이 미국 식품의약국의 승인을 받고 전 세계 시장을 석권하고 있다. 다빈치 로봇은 지금까지는 주로 비뇨기과와 산부인과 수술에 활발하게 사용되었기 때문에 장비와 기구가 주로 복부 수술용으로 개발되었다. 따라서 입안과 목의 좁은 공간에서 두경부외과 수술을 하기에는 기구들이 다소 크고 불편한 점들이 많았다. 하지만 몇몇 연구자들이 갑상샘 수술과 편도암 수술에 다빈치 로봇을 이용하기 시작하였으며, 2010년대에 여러 병원에서 다빈치 로봇을 구입하면서 이비인후과 영역에서도 로봇수술이 급격히 증가하였다. 내시경으로 하고 있었던 겨드랑이 접근법, BABA접근법, 귀뒤접근법 등의 다양한 방법의 갑상샘 수술을 다빈치 로봇을 이용하여 할 수 있게 되었다[11,15,19]. 3차원 수술 시야에서 관절이 있는 로봇 팔을 이용해 보다 편리하게 수술을 할 수 있다는 점에서 주목받기 시작하였다.
3. 구강내시경수술과 로봇수술의 시작
노츠 수술(NOTES, natural orifice transluminal endoscopic surgery)이란 피부에 상처를 만들지 않고, 신체의 자연개구부(입, 항문, 질, 요로 등)를 통해 내시경기구를 삽입하여 하는 수술법으로, 2000년대에 복강수술에 이 신개념 수술을 처음으로 시작하고 발표를 하였다[20,21]. 갑상샘 수술에는 국내에서 2014년에 처음으로 사체와 동물에서 구강으로 내시경을 넣어 갑상샘 수술을 시도하고 발표를 하였다[22,23]. 그 후 2016년에 태국의 외과 의사인 Anuwong [24]이 60명의 환자에서 구강으로 내시경과 기구를 넣어 갑상샘절제술을 성공적으로 하고 국제학술지에 TOETVA (transoral endoscopic thyroidectomy vestibular approach)라는 수술명으로 보고하여 학계에 큰 이슈가 되었다. 이후로 세계 각국의 많은 의료진들이 이 수술방법을 배우고 도입하기 시작하였으며, 우리나라에서도 2015년부터 갑상샘 구강내시경 또는 로봇 수술을 시작하였으며 최근에는 많은 병원에서 활발하게 하고 있다[25-29].
갑상샘 구강내시경수술과 로봇수술의 대상
어떤 환자에게 구강내시경수술과 로봇수술을 추천하면 좋을까? Razavi 등[30]과 Razavi와 Russell [31]에 의하면 일반적으로 양성이거나 중등도인 경우(Bethesda II, III, IV)에는 직경 6 cm 미만, 악성이 의심되는 경우(Bethesda V, VI)에는 직경 2 cm 미만의 결절이면 수술이 가능하다. 여기에 저자의 의견을 추가하면 갑상샘 상엽에 위치한 악성종양의 경우에는 1 cm 이하 결절만 하는 것이 좋다. 왜냐하면 갑상샘보다 위쪽인 입에서부터 접근하므로, 가장 가까운 곳인 갑상샘 상엽 부위가 시야가 좋지 않고 기구가 잘 닿지 않는다. 따라서 이 부위에 큰 종양이 있으면 노출시키기가 쉽지 않고 조작을 하는 과정에서 종양이 주변으로 파급될 수 있다. 그외에 이전에 두경부 수술이나 방사선치료를 받은 환자, 급성 갑상샘기능항진증, 반회후두신경 마비, 갑상샘 흉골하 확장, 수술 전 림프절전이, 갑상샘 외 확장, 구강 농양, 그리고 위에서 언급한 적응증을 만족하지 않는 환자는 금기이다. 위 문헌에서는 수술 전 림프절전이가 있을 때는 권유하지 않았지만, 저자의 의견으로는 중심경부림프절에만 전이가 있다면 수술이 충분히 가능하다고 판단된다.
수술을 결정하기 전에 환자가 어떠한 이유로 이 수술을 원하는지, 환자에게 어떠한 도움이 되고, 어떠한 어려움이 예상되는지를 잘 확인할 필요가 있다. 예를 들어 켈로이드 체질의 환자는 수술 후에 보기 흉한 수술 흉터가 발생할 가능성이 높으므로 구강내시경수술이나 로봇수술을 더 적극적으로 권유해볼 수 있겠다. 구강위생이 좋지 않아 절개할 부위에 점막염 또는 농양이 있다면 이를 먼저 치료하고 나서 수술을 하는 것이 안전하다. 또 입으로 접근하므로 턱이 돌출되어 있거나 갑상연골이 돌출되어 있으면(Prominent Adam’s apple) 수술에 방해가 될 수도 있다. 수술 중 예측하지 못한 병의 진행 소견을 보일 경우나 출혈 등의 합병증이 발생할 경우 고식적인 갑상샘 절제술로 전환할 수 있다는 것도 미리 설명해야 한다.
전반적인 수술과정
갑상샘 구강내시경수술과 로봇수술의 방법은 거의 비슷하다. 단지 수술도구로 내시경장비와 로봇장비 중 어떤 것을 사용하는 지의 차이이며 각각의 장단점은 후반부에 다시 정리하고자 한다. 본 논문에서는 갑상샘 구강내시경수술의 전반적인 과정만을 간단하게 요약하였으며, 자세한 수술 술기와 동영상이 필요한 독자들은 저자의 선행논문들을 참고하면 된다[26,32].
1. 수술공간 만들기
환자의 입술 안쪽과 볼점막에 세 개의 구멍을 뚫고 카메라와 기구들을 삽입하여 수술을 한다. 목의 앞쪽은 수술을 할 수 있는 공간이 없으므로 인위적으로 피부 아래에 충분한 공간을 만들어야 한다. 입술 중앙의 안쪽에 대략 2.5 cm의 절개를 가하고 절개 부위로 날카롭지 않은 수술기구들(vascular tunneller 등)을 삽입하여 목의 앞쪽에 수술공간을 만들어 준다. 그 다음 CO2 가스를 주입하거나 외부 견인기를 삽입하여 수술공간을 유지시킨다. 양측 볼점막에 5 mm 정도의 절개를 가하고 각각 캐뉼라를 삽입한다. 가운데 캐뉼라를 통해 내시경을 삽입하고 양측 캐뉼라로 수술기구들을 삽입하여 수술을 한다(Figure 1).
2. 갑상샘절제술
집도의는 환자의 머리 쪽 의자에 앉아서 반대편에 위치한 모니터를 보면서 수술을 한다. 제1 수술 보조의가 내시경을 잡고 수술 부위가 잘 보이도록 조정하고 집도의는 양손으로 수술기구들을 조정하여 수술을 진행한다(Figure 2).

Operating room. During surgery, the main operator is positioned at the patient's head, with an assistant surgeon and a nurse positioned to the side of the patient. Informed consent for publication of the image was obtained from the participants.
1) 1단계: 피대근 접합부의 분리 및 갑상샘 노출
갑상샘은 피대근(strap muscle) 아래에 위치해 있으므로 단극전기소작기(hook type monopolar electrocautery)와 초음파절삭기(ultrasonic device)를 이용하여 양측 피대근 접합부를 정중선에서 분리한다. 갑상샘이 노출되면 피대근을 갑상샘의 외측면으로부터 분리하여 박리한다.
2) 2단계: 갑상샘 협부 절제
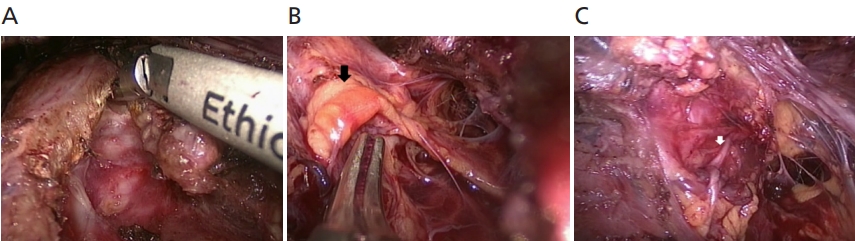
갑상샘의 협부를 위쪽부터 아래 방향으로 초음파절삭기를 이용하여 절개를 한다(Figure 3A).
3) 3단계: 갑상샘 상극 절제 및 상부갑상샘 보전
구강을 통한 갑상샘 수술을 하면서 시야확보가 가장 어려운 부분이다. 갑상샘을 내하측 방향으로 당겨서 갑상샘 상엽을 충분히 노출시킨다. 상갑상동맥과 정맥이 확인되면 초음파절삭기를 이용하여 결찰을 한다. 상부갑상샘을 확인하고 보존한다.
4) 4단계: 갑상샘 하부갑상샘과 반회 후두신경 보전
갑상샘 전체를 내측으로 견인한 상태에서 하부갑상샘과 반회후두신경을 확인한다. 하부갑상샘은 공급하는 주위 혈관을 최대한 보존하면서 갑상샘에서 분리한다. 반회후두신경의 주행을 확인하면서 박리하여 보존한다(Figure 3B,3C).
5) 5단계: Berry 인대 주변 절제
반회후두신경이 후두 내로 들어가는 부위에서 신경을 갑상샘으로부터 조심스럽게 분리시키고 berry 인대 주변을 적절히 지혈하면서 갑상샘을 기관으로 부터 분리시킨다.
6) 6단계: 절제된 시료의 체외 배달과 봉합
검체를 플라스틱 주머니에 넣어서 입술 아래 정중앙의 절개부를 통해서 몸 밖으로 제거한다. 볼점막의 측면 절개부를 통해 배액관을 삽입하고 흡수성 봉합사로 세 개의 절개부를 봉합한다.
3. 수술 후 관리
술 후 환자의 경부(특히 턱 아래 부위를 충분히)를 압박 드레싱을 하고 출혈, 혈종, 장액종, 피하기종 등이 발생하는지 관찰해야 한다. 저자는 초기에는 배액관을 삽입하지 않았으나 장액종을 몇차례 경험한 후 24시간동안 배액관을 유지시킨 후 제거한다. 수술 후 후두내시경 검사를 통하여 성대운동성을 확인하는 것이 좋다. 현재까지 구강내시경 수술 후 반회후두신경 손상에 의한 일시적 혹은 영구적 성대마비의 발생빈도, 고음 발생장애 빈도는 고식적인 수술에 비해 높지 않았다[26,33,34]. 구강 식이는 수술 당일이나 다음 날부터 가능하다. 환자들에게 무거운 것을 들거나 힘을 쓰는 일은 피하도록 교육한다. 구강 내 봉합사 제거는 보통 첫 번째 외래 방문 시에 한다(약 7-10일). 일반적으로 수술 후 한 달 뒤에 방문하여 음성과 갑상샘기능 검사를 시행하고 수술 부위를 다시 한번 확인한다.
갑상샘 구강내시경수술 대 로봇수술
환자들이 갑상샘 로봇수술과 내시경수술의 차이를 질문할 때가 많다. 앞에서 언급했듯이 사용하는 장비가 다를 뿐이지 기본적으로는 같은 방법의 수술이다. 목적지는 같은데 타고 가는 자동차가 다르다고 생각하면 이해하기가 쉽다. 목적지와 경로는 차이가 없으므로 결국 운전자가 가장 익숙하게 다룰 수 있는 자동차가 좋다. 내시경수술과 비교하여 로봇수술의 장점은 다음과 같다. 첫째, 3차원의 보다 좋은 시야에서 수술할 수 있다. 둘째, 다빈치 로봇이 수술자의 손 떨림을 보정을 해준다. 셋째, 관절이 있는 로봇 팔을 이용하여 좁은 공간에서도 좀 더 자유롭게 수술을 할 수 있다.
반면 다음과 같은 이유로 다빈치 로봇보다 내시경을 선호하는 경우도 많다. 첫째, 다빈치 로봇 장비와 기구들이 복강 내 수술을 하기 위해 개발되어서 아직까지 갑상샘 수술을 하기에 다소 크다. 둘째, 수술자가 수술을 하면서 손으로 느끼는 감각이 중요한데 이러한 촉각을 느낄 수 없다. 셋째, 수술 도중 기구들을 교체하는 것이 번거롭다. 넷째, 고가의 장비와 기구가 필요하다. 이러한 로봇의 단점을 극복하기 위해 앞으로 두경부외과 수술에 특화된 로봇 장비와 기구들이 개발될 것으로 기대한다.
결론
갑상샘 구강내시경수술과 로봇수술의 가장 큰 장점은 피부 절개가 전혀 없이 입 속에 점막 절개만으로 수술을 할 수 있다는 점이다. 따라서 흉터가 전혀 없고, 드레싱을 하지 않아도 되며, 수술 다음날부터 샤워나 면도가 가능하고, 점막은 일주일 이내에 치유가 된다. 또한, 기존의 다른 내시경 수술 접근법에 비해 갑상샘에서 가까운 구강에서부터 접근하기 때문에 상대적으로 덜 침습적이고 카메라가 구강의 정중앙으로 들어가므로 반대측의 수술 시야도 좋아 갑상샘 전절제술에 가장 적합하다. 아직은 장기간 치료결과에 대한 연구가 미흡하지만 기존의 내시경수술 접근법들과 비교해 볼 때 장점이 많아, 향후 갑상샘 치료의 ‘게임 체인저(game changer)’가 될 것으로 전망된다.
Notes
Conflict of Interest
No potential conflict of interest relevant to this article was reported.
References
Peer Reviewers’ Commentary
이 논문은 갑상샘 수술 방법의 하나인 구강을 통한 내시경 및 로봇수술에 대해 소개하고 있다. 전통적인 갑상샘 수술 후 발생하는 목의 흉터가 보이지 않도록 개발된 기존의 다양한 내시경 및 로봇수술 접근법들을 소개한 후, 피부에 별도의 상처를 내지않고 입술 안쪽과 볼점막을 통해 기구를 삽입하는 구강 내시경 및 로봇수술 방법이 기존의 수술법에 비해 갖는 장점들을 잘 기술하고 있다. 수술 방법과 단계를 그림과 사진을 통해 설명하고 어떤 환자들이 이 수술법의 적절한 대상이 되는지, 그리고 어떤 제한점이 있는지도 제시해 주고 있다. 이 논문은 갑상샘의 구강 내시경 및 로봇수술을 이해할 수 있게 하는 좋은 교육 자료이며, 임상현장에서 적절한 갑상샘 수술법을 결정하는데 좋은 지침을 제공할 것으로 판단된다.
[정리: 편집위원회]