 |
 |
- Search
| J Korean Med Assoc > Volume 64(5); 2021 > Article |
|
Abstract
The clinical outcome in advanced cancer has improved since the development of targeted therapies and immune checkpoint inhibitors. We can expect better overall survival after a combination treatment with these therapeutic agents. Classical cytotoxic chemotherapeutic agents directly kill tumor cells by destroying the cell structure and DNA of tumor cells or inhibiting their metabolism. Targeted therapy also directly affects tumor cells by inhibiting the cell growth signaling system. Conversely, immune checkpoint inhibitors can enhance immune responses by using the host immune system in the tumor microenvironment, leading to the direct killing of tumor cells. Therefore, immune checkpoint inhibitors are less toxic and have longer response durations. Even in solid tumors with nonimmunogenic backgrounds, cytotoxic chemotherapy or targeted treatment can induce immune responses to place the tumor microenvironment in an immunogenic state. Synergistic anticancer effects can be expected when immune checkpoint inhibitors are added during this state. Moreover, drug resistance may be overcome by combination therapies. If patients with cancer are treated with a combination of these therapeutic agents and the characteristics of each tumor are identified with data from next generation sequencing, personalized treatments can be tailored, making it possible to control cancers as a curable disease just like other benign chronic diseases.
최근 20년 동안 고형암의 치료는 전통적으로 이용되던 세포독성 항암제의 신약개발 이외 표적치료제와 면역 항암요법의 개발이 이루어지면서 빠른 속도로 발전되어 왔다. 특히 완치가 불가능한 전이 재발암의 경우 과거 6개월의 생존기간에서 평균 1년 6개월 이상의 연장을 기대할 수 있게 되었다. 또한 고형암에서는 종양의 크기가 줄어듦에 따라 수술이 불가능한 상태에서 절제가 가능한 정도까지 기대할 수 있을 뿐 아니라, 전이 병변의 절제술을 고려할 수 있게 되었고, 이로 인해 전이가 동반된 4기 암에서도 드물지만 완치를 기대할 수 있게 되었다. 세포독성 항암제가 암세포의 DNA 혹은 세포의 파괴나 대사작용에 영향을 미쳐 암세포를 사멸시키는 동시에 정상세포에 대한 손상이 발생하기 때문에 독성이 심했다면, 2000년대 이후 표준치료로 사용되고 있는 표적치료제는 종양의 성장과 진행에 중요한 역할을 하는 분자 물질을 표적으로 하기 때문에 정상세포에 미치는 영향이 상대적으로 적어 세포독성 항암제와 병합 혹은 단독요법으로 사용되고 있다. 그러나 고형암의 성장은 하나의 세포전달체계의 활성화로 이루어지는 것이 아니며, 종양이 진행함에 따라 종양세포 내 새로운 변이가 발생하면서 진화하는 양상을 보이기 때문에 표적치료제를 이용한 치료방법에는 한계가 발생하였다.
암에 대한 면역반응을 이용하는 치료는 과거부터 시도되었으나 좋은 결과를 보이지는 않아 실험적인 이용만 있던 중 면역관문억제제(immune checkpoint inhibitors)가 개발되면서 고형암의 치료효과는 한 단계 발전하였으며 고형암 또한 당뇨나 고혈압처럼 만성질환으로 조절할 수 있는 질병임을 가능하게 하였다. 이제 고형암의 약물치료는 서로 다른 기전의 세 가지 약물, 즉 세포독성 항암제, 표적치료제 그리고 면역관문억제제의 단독 순차적 혹은 병합요법으로 암 정복을 위한 목표에 좀 더 가까워졌다고 할 수 있다.
종양에 대한 환자의 면역체계를 활성화함으로써 면역세포가 종양을 치료하도록 하는 면역치료의 개념은 과거부터 연구되어 왔으나, 이는 주로 환자의 면역 관련 세포 특히 자연살해세포(natural killer cell, NK cell)나 수지상세포와 같은 면역반응에 직접 관여하는 세포를 증폭시켜 재주입하는 방식이었다. 이러한 방법의 면역치료는 이론적으로는 효과가 있을 것으로 생각되었으나 실제 진료 현장에서는 매우 제한적인 효과를 보였다. 그 이유는 종양의 복합 다양성과 종양세포의 진화, 그리고 종양을 둘러싼 종양 미세 환경과 종양 사이의 다양한 상호작용에 대한 점이 고려되지 않은 상태에서 주로 면역에 관여하는 세포 수만을 증가시켜 면역반응을 극대화시키려고 했기 때문일 것이다[1-4]. 종양에서의 유전자 발현을 밝히고자 하는 연구와 기술이 발달하면서 다양한 유전자 변화형태와 함께 이로 이한 종양과 종양 주위 미세환경의 변화, 그리고 종양 주위에서의 면역반응에 대한 이해가 깊어지면서 이를 이용한 새로운 면역치료인 면역관문억제제가 개발되었다.
신체 내에서 어떠한 이유로든 비정상세포가 발행하였을 때 정상적인 면역체계에서는 이를 비정상으로 인지하고 면역세포들이 활성화되면서 비정상세포를 제거하게 된다. 그러나 악성종양은 자체의 유전자 변화뿐 아니라 종양 미세환경에서의 변화 등 여러 방법을 통해 환자의 면역체계가 종양세포를 비정상적인 것으로 인지할 수 없도록 하면서 면역체계의 감시에서 벗어나게 된다. 면역체계가 정상적으로 작동하기 위해서는 비정상적인 세포, 즉 종양세포를 항원으로 인지하여 활성화되어야 하는데 악성종양은 이러한 면역학적 인지가 저하되면서 면역시스템이 작동하지 않도록 한다[5]. 종양세포에 대해서는 적응면역(adaptive immunity)와 고유면역(선천면역, innate immunity)이 모두 관여하게 되는데 적응면역체계에서는 세포독성 T림프구인 CD4+, CD8+ T세포가 중요한 역할을 하며, 고유면역체계에서는 자연살해세포가 주 역할을 한다[6-9]. Figure 1에서 보듯이 항원제시세포(antigen presenting cell, APC)가 종양세포를 인지하면 불활성화되어 있던 T세포가 활성화되고 활성화된 T세포는 증식하고 분화되면서 종양세포를 공격하는 살해세포로 작용하게 된다[10].
이때 종양세포는 1) APC가 종양세포를 항원으로 인지하지 못하도록 하거나, 2) T세포나 자연살해세포와 같이 직접적으로 종양세포를 공격하는 면역세포의 기능을 억제하기도 하며, 3) 종양세포 자체에서 유발산화질소합성효소(inducible nitric oxide synthase), 혈관내피성장인자(vascular endothelial growth factor), 베타형질전환성장인자(transforming growth factor), 인터루킨-10(interleukin-10)과 같은 면역억제 물질을 발현하거나 분비하고, 4) 종양 주위 환경으로 면역을 억제하는 다양한 세포와 물질들을 불러모아 면역학적 반응이 억제되도록 한다[11-17].
T세포의 기능을 억제 혹은 조절하는 면역체계 중 대표적인 것은 cytotoxic T lymphocyte antigen-4 (CTLA4), programmed death 1 (PD-1), programmed deathligand 1 (PD-L1), lymphocyte activation gene-3 (LAG3)이다. T세포의 CTLA-4가 APC의 CD80/86과의 작용으로 활성화된 T세포를 억제하는 피드백 시스템에서 항CTLA-4 제제를 주입하게 되면 이것이 T세포와 결합하여 T세포가 억제되지 않고 활성 상태를 유지하게 된다. 항CTLA-4 항체인 ipilimumab은 수술 불가능하거나 전이된 흑색종을 대상으로 한 3상 임상연구에서 의미 있게 생존기간을 연장시키는 결과를 보여주었다. PD-1은 T세포의 표면에서 발현되어 있는 상태에서 종양세포의 표면에 발현된 PD-L1/PD-L2와 결합함으로써 종양에 대한 T세포와 다른 세포들의 기능을 억제한다. PD-1 억제제인 pembrolizumab이나 nivolumab은 T세포의 PD-1에 결합하여 종양과 T세포의 결합을 방해함으로써 T세포의 기능이 활성화된 상태를 만들어준다. 이렇듯 면역관문억제제는 정상세포에 미치는 독성이 적고 종양세포에 직접적인 항종양 작용을 하는 것이 아니면서 종양에 대한 면역반응을 활성화시키는 효과를 나타낸다. 현재 pembrolizumab과 nivolumab은 이미 진료현장에서 다양한 고형암의 치료에 이용되고 있으며 T세포뿐 아니라 종양의 PD-L1을 억제하는 새로운 면역관문억제제로 duvalumab 이나 atezolimumab 등과 같은 새로운 면역관문억제제들이 개발되어 표준치료에도 이용되고 있다[18-21]. 특히, 폐암, 흑색종, 신세포암과 비뇨기 종양에서 좋은 효과가 보고되고 있으나 초기 기대와 달리 모든 종양에서 좋은 결과가 있는 것은 아니다. 특히 위장관 종양의 경우 위암과 식도암의 일부, 고빈도-현미부수체불안정성(microsatellite instabilityhigh, MSI-H) 대장암, 간암의 일부에서만 효과를 보이고 있는데 이는 위장관 종양 주위 미세환경의 복합 다양성과 함께 미세환경으로의 면역세포 침투가 저하되어 있어서 적절한 면역반응을 일으키지 못한 것 등이 원인으로 제시되고 있다[20].
최근 다양한 종양의 유전자 변화를 한 번에 검출할 수 있는 차세대염기서열분석법(next generation sequencing)과 같은 방법들이 진료현장에서 이용되면서 이러한 유전자 변화를 이용하여 표적이 맞는 표적치료제를 선택하여 치료에 시도하기도 한다. 면역관문억제제의 경우에도 종양의 성질만 가지고 치료에 대한 반응을 예측할 수 없기 때문에 어떠한 환자에게 약제를 적용하면 좋을지 예측할 수 있는 생체 표지자가 큰 도움이 될 수 있겠지만 현재까지 보고된 결 과로는 동일 약제가 종양마다 서로 다른 결과를 나타내기도하고 동일 종양 내에서도 지속적이고 반복적인 효과를 보이는 것은 아니어서 치료 선택을 위한 표지자는 연구 중에 있으며 대체로 1) 종양에서의 PD-L1 발현 정도, 2) 반복서열 불안정성(MSI), 3) 종양의 돌연변이 정도(tumor mutation burden, TMB) 등이 이용되고 있다. Pembrolizumab의 경우 비소세포폐암 환자를 대상으로 하는 3상 임상연구에서 종양에서 PD-L1의 발현이 50% 이상 높은 경우에서 좋은 결과를 보였기 때문에[22], 다른 고형암에서도 PD-L1의 발현이 있을 때 pembrolizumab을 고려하기도 한다. 그러나 같은 PD-1 억제제인 nivolumab의 경우 같은 비소세포암 환자를 대상으로 한 3상 연구에서 PD-L1의 발현은 치료효과와 관계없음을 보였으며[21,23], 종양의 PD-L1 발현을 검사하는 방법 또한 표준화되어 있지 않아 종양의 PD-L1 발현이 적절한 생체 표지자라고 할 수는 없다[24]. MSI의 경우 MSI-H 혹은 MMR 결핍형이 많이 존재하는 대장암에서 면역관문억제제의 효과를 기대할 수 있음이 보고되어 미국식 품의약국에서는 이러한 유형의 대장암에서 pembrolizumab과 nivolumab을 승인한 바 있다[25-28]. TMB는 특정 범위 내 종양 DNA를 분모로 하고 그 중 돌연변이가 일어난 숫자를 분자로 한 지표로 면역학적 환경을 잘 만드는 조건, 즉 돌연변이가 자주 일어나는 환경인 경우 면역 항암요법의 효과를 기대할 수 있다는 개념으로 접근하였을 때 TMB 또한 새로운 생체 표지자 후보일 수 있다. 폐암에서 PD-L1의 발현과 함께 TMB 정도를 종합적으로 평가하였을 때 면역 항암제에 대한 치료효과를 예측하는 것이 더 정확하다는 보고가 있었으나[29,30], 이에 대한 분석방법이 표준화되어 있지 않으며 시간과 비용이 많이 소모된다는 점에서 진료현장에서 쓰이지 않는다.
면역관문억제제는 초기 임상연구에서 시도되었을 당시에 단독요법 혹은 서로 다른 기전의 두 가지 면역관문억제제를 병합하는 연구가 주를 이루었다. 그러나 여러 실험실 연구에서 기존의 세포독성 항암제, 표적치료제 등의 약물뿐 아니라 방사선 요법 등의 다양한 치료들이 치료 직후 종양 주위 미세환경에서 면역학적 환경 변화를 유발할 수 있으며 이 때 면역관문억제제를 주사하였을 때 면역반응이 극대화되면서 항암효과가 상승할 수 있다는 결과들이 보고되면서 임상 연구에서도 활발하게 병합요법이 시도되고 있다. 또한 종양이 약제에 대해 발생하는 내성 기전을 극복할 수 있을 것으로도 기대하고 있다. 특히 그동안 위장관 종양에서 상대적으로 면역학적 반응이 잘 일어나지 않는 상태라고 하더라도 표준 세포독성 항암제와의 병합효과를 통해 효과를 나타낼 수 있음이 확인되어 위장관 종양에서도 활발한 연구가 이루어지고 있다(Table 1). 최근 간세포암에 대한 atezolimumab과 bevacizumab의 병합요법에서 1년 생존율이 67.2%로 10년 이상 일차 요법의 표준치료로 사용된 sorafenib 54.6%와 비교하여 좋은 결과를 보였으며, 무진행 생존값은 6.8개월로 역시 sorafenib의 4.3개월보다 좋은 효과를 나타내어 국내에서도 일차 요법으로 승인된 바 있다[31].
면역관문억제제의 사용은 물론 병합요법으로 인한 독성이 문제가 될 수는 있겠지만 최근 종양으로 약물을 전달하면서 주위 정상세포의 손상을 적게 할 수 있는 최신 기법들이 개발되고 있어 이를 극복할 수 있을 것으로 기대된다. 또한, 차세대염기서열분석법을 이용한 종양의 유전자 표현형에 대한 진단검사가 활성화하면서 환자 개인의 종양 유전자 표현형에 따라 선택적으로 약제를 선택하는 방법이 시도되고 있다[32]. 향후 고형암의 치료에서는 종양의 유전자형에 따라 효과를 기대할 수 있는 표적치료제를 선택하거나 독성을 예측하는 유전자 검사에 따라 적절한 세포독성 항암제를 선택할 수 있으며 여기에 약물로 인해 발생하는 면역학적 반응을 최대한 항암효과로 이어지게 할 수 있는 면역관문억제제의 추가로 암 정복에 한발 더 나아갈 수 있는 맞춤치료전략을 세울 수 있을 것으로 기대된다.
Figure 1.
T cell response to cancer cell. APC, antigen-presenting cell. Adapted from Pennock et al. Oncologist 2015;20:812-822, with permission from John Wiley and Sons [10].
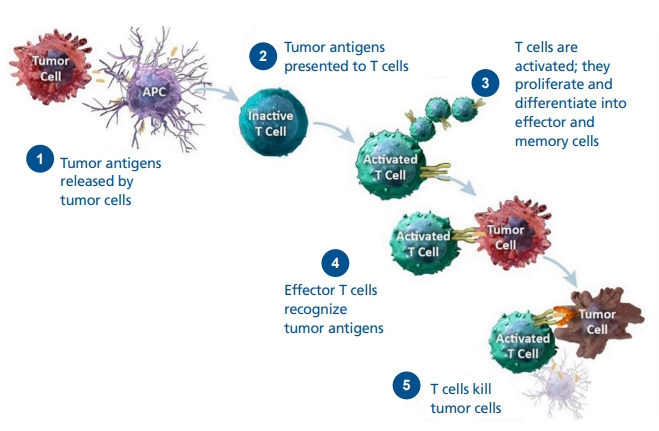
Table 1.
Current clinical trials with immune check point inhibitor in gastrointestinal cancer
References
1. Gajewski TF, Woo SR, Zha Y, Spaapen R, Zheng Y, Corrales L, Spranger S. Cancer immunotherapy strategies based on overcoming barriers within the tumor microenvironment. Curr Opin Immunol 2013;25:268-276.


2. Lawrence MS, Stojanov P, Polak P, Kryukov GV, Cibulskis K, Sivachenko A, Carter SL, Stewart C, Mermel CH, Roberts SA, Kiezun A, Hammerman PS, McKenna A, Drier Y, Zou L, Ramos AH, Pugh TJ, Stransky N, Helman E, Kim J, Sougnez C, Ambrogio L, Nickerson E, Shefler E, Cortes ML, Auclair D, Saksena G, Voet D, Noble M, DiCara D, Lin P, Lichtenstein L, Heiman DI, Fennell T, Imielinski M, Hernandez B, Hodis E, Baca S, Dulak AM, Lohr J, Landau DA, Wu CJ, MelendezZajgla J, Hidalgo-Miranda A, Koren A, McCarroll SA, Mora J, Crompton B, Onofrio R, Parkin M, Winckler W, Ardlie K, Gabriel SB, Roberts CWM, Biegel JA, Stegmaier K, Bass AJ, Garraway LA, Meyerson M, Golub TR, Gordenin DA, Sunyaev S, Lander ES, Getz G. Mutational heterogeneity in cancer and the search for new cancer-associated genes. Nature 2013;499:214-218.



4. Kirkwood JM, Butterfield LH, Tarhini AA, Zarour H, Kalinski P, Ferrone S. Immunotherapy of cancer in 2012. CA Cancer J Clin 2012;62:309-335.



5. Dunn GP, Bruce AT, Ikeda H, Old LJ, Schreiber RD. Cancer immunoediting: from immunosurveillance to tumor escape. Nat Immunol 2002;3:991-998.


6. Finn OJ. Immuno-oncology: understanding the function and dysfunction of the immune system in cancer. Ann Oncol 2012;23 Suppl 8(Suppl 8):viii6-viii 9.

7. Vesely MD, Kershaw MH, Schreiber RD, Smyth MJ. Natural innate and adaptive immunity to cancer. Annu Rev Immunol 2011;29:235-271.


8. Godet Y, Fabre E, Dosset M, Lamuraglia M, Levionnois E, Ravel P, Benhamouda N, Cazes A, Le Pimpec-Barthes F, Gaugler B, Langlade-Demoyen P, Pivot X, Saas P, Maillere B, Tartour E, Borg C, Adotevi O. Analysis of spontaneous tumorspecific CD4 T-cell immunity in lung cancer using promiscuous HLA-DR telomerase-derived epitopes: potential synergistic effect with chemotherapy response. Clin Cancer Res 2012;18:2943-2953.


9. Mlecnik B, Bindea G, Pages F, Galon J. Tumor immunosurveillance in human cancers. Cancer Metastasis Rev 2011;30:5-12.



10. Pennock GK, Chow LQ. The evolving role of immune checkpoint inhibitors in cancer treatment. Oncologist 2015;20:812-822.



11. Drake CG, Jaffee E, Pardoll DM. Mechanisms of immune evasion by tumors. Adv Immunol 2006;90:51-81.


12. Kerkar SP, Restifo NP. Cellular constituents of immune escape within the tumor microenvironment. Cancer Res 2012;72:3125-3130.



13. Aerts JG, Hegmans JP. Tumor-specific cytotoxic T cells are crucial for efficacy of immunomodulatory antibodies in patients with lung cancer. Cancer Res 2013;73:2381-2388.


15. Pardoll DM. The blockade of immune checkpoints in cancer immunotherapy. Nat Rev Cancer 2012;12:252-264.



16. Flies DB, Sandler BJ, Sznol M, Chen L. Blockade of the B7-H1/PD-1 pathway for cancer immunotherapy. Yale J Biol Med 2011;84:409-421.


17. Whiteside TL. The role of death receptor ligands in shaping tumor microenvironment. Immunol Invest 2007;36:25-46.


18. Eggermont AM, Chiarion-Sileni V, Grob JJ, Dummer R, Wolchok JD, Schmidt H, Hamid O, Robert C, Ascierto PA, Richards JM, Lebbe C, Ferraresi V, Smylie M, Weber JS, Maio M, Konto C, Hoos A, de Pril V, Gurunath RK, de Schaetzen G, Suciu S, Testori A. Adjuvant ipilimumab versus placebo after complete resection of high-risk stage III melanoma (EORTC 18071): a randomised, double-blind, phase 3 trial. Lancet Oncol 2015;16:522-530.


19. Borghaei H, Paz-Ares L, Horn L, Spigel DR, Steins M, Ready NE, Chow LQ, Vokes EE, Felip E, Holgado E, Barlesi F, Kohlhaufl M, Arrieta O, Burgio MA, Fayette J, Lena H, Poddubskaya E, Gerber DE, Gettinger SN, Rudin CM, Rizvi N, Crino L, Blumenschein GR Jr, Antonia SJ, Dorange C, Harbison CT, Graf Finckenstein F, Brahmer JR. Nivolumab versus docetaxel in advanced nonsquamous non-small-cell lung cancer. N Engl J Med 2015;373:1627-1639.



20. Wang D, Lin J, Yang X, Long J, Bai Y, Yang X, Mao Y, Sang X, Seery S, Zhao H. Combination regimens with PD-1/PD-L1 immune checkpoint inhibitors for gastrointestinal malignancies. J Hematol Oncol 2019;12:42.



21. Mok TSK, Wu YL, Kudaba I, Kowalski DM, Cho BC, Turna HZ, Castro G Jr, Srimuninnimit V, Laktionov KK, Bondarenko I, Kubota K, Lubiniecki GM, Zhang J, Kush D, Lopes G; KEYNOTE-042 Investigators. Pembrolizumab versus chemotherapy for previously untreated, PD-L1-expressing, locally advanced or metastatic non-small-cell lung cancer (KEYNOTE-042): a randomised, open-label, controlled, phase 3 trial. Lancet 2019;393:1819-1830.

22. Udall M, Rizzo M, Kenny J, Doherty J, Dahm S, Robbins P, Faulkner E. PD-L1 diagnostic tests: a systematic literature review of scoring algorithms and test-validation metrics. Diagn Pathol 2018;13:12.



23. Bylicki O, Barazzutti H, Paleiron N, Margery J, Assie JB, Chouaid C. First-line treatment of non-small-cell lung cancer (NSCLC) with immune checkpoint inhibitors. BioDrugs 2019;33:159-171.


24. Burtness B, Harrington KJ, Greil R, Soulieres D, Tahara M, De Castro G Jr, Psyrri A, Rotllan NB, Neupane PC, Bratland A, Fuereder T, Hughes BGM, Mesia R, Ngamphaiboon N, Rordorf T, Wan Ishak WZ, Roy A, Cheng J, Jin F, Rischin D. KEYNOTE-048: Phase III study of first-line pembrolizumab (P) for recurrent/metastatic head and neck squamous cell carcinoma (R/M HNSCC) [abstract]. Ann Oncol 2018;29 Suppl 8:VIII729.
25. Guinney J, Dienstmann R, Wang X, de Reynies A, Schlicker A, Soneson C, Marisa L, Roepman P, Nyamundanda G, Angelino P, Bot BM, Morris JS, Simon IM, Gerster S, Fessler E, De Sousa E Melo F, Missiaglia E, Ramay H, Barras D, Homicsko K, Maru D, Manyam GC, Broom B, Boige V, Perez-Villamil B, Laderas T, Salazar R, Gray JW, Hanahan D, Tabernero J, Bernards R, Friend SH, Laurent-Puig P, Medema JP, Sadanandam A, Wessels L, Delorenzi M, Kopetz S, Vermeulen L, Tejpar S. The consensus molecular subtypes of colorectal cancer. Nat Med 2015;21:1350-1366.



26. Boyiadzis MM, Kirkwood JM, Marshall JL, Pritchard CC, Azad NS, Gulley JL. Significance and implications of FDA approval of pembrolizumab for biomarker-defined disease. J Immunother Cancer 2018;6:35.



27. Le DT, Uram JN, Wang H, Bartlett BR, Kemberling H, Eyring AD, Skora AD, Luber BS, Azad NS, Laheru D, Biedrzycki B, Donehower RC, Zaheer A, Fisher GA, Crocenzi TS, Lee JJ, Duffy SM, Goldberg RM, de la Chapelle A, Koshiji M, Bhaijee F, Huebner T, Hruban RH, Wood LD, Cuka N, Pardoll DM, Papadopoulos N, Kinzler KW, Zhou S, Cornish TC, Taube JM, Anders RA, Eshleman JR, Vogelstein B, Diaz LA Jr. PD-1 blockade in tumors with mismatch-repair deficiency. N Engl J Med 2015;372:2509-2520.



28. Overman MJ, McDermott R, Leach JL, Lonardi S, Lenz HJ, Morse MA, Desai J, Hill A, Axelson M, Moss RA, Goldberg MV, Cao ZA, Ledeine JM, Maglinte GA, Kopetz S, Andre T. Nivolumab in patients with metastatic DNA mismatch repairdeficient or microsatellite instability-high colorectal cancer (CheckMate 142): an open-label, multicentre, phase 2 study. Lancet Oncol 2017;18:1182-1191.



29. Rizvi H, Sanchez-Vega F, La K, Chatila W, Jonsson P, Halpenny D, Plodkowski A, Long N, Sauter JL, Rekhtman N, Hollmann T, Schalper KA, Gainor JF, Shen R, Ni A, Arbour KC, Merghoub T, Wolchok J, Snyder A, Chaft JE, Kris MG, Rudin CM, Socci ND, Berger MF, Taylor BS, Zehir A, Solit DB, Arcila ME, Ladanyi M, Riely GJ, Schultz N, Hellmann MD. Molecular Determinants of response to antiprogrammed cell death (PD)-1 and anti-programmed deathligand 1 (PD-L1) blockade in patients with non-small-cell lung cancer profiled with targeted next-generation sequencing. J Clin Oncol 2018;36:633-641.



30. Kim HS, Cha H, Kim J, Park WY, Choi YL, Sun JM, Ahn JS, Ahn MJ, Park K, Lee SH. Genomic scoring to determine clinical benefit of immunotherapy by targeted sequencing. Eur J Cancer 2019;120:65-74.


31. Finn RS, Qin S, Ikeda M, Galle PR, Ducreux M, Kim TY, Kudo M, Breder V, Merle P, Kaseb AO, Li D, Verret W, Xu DZ, Hernandez S, Liu J, Huang C, Mulla S, Wang Y, Lim HY, Zhu AX, Cheng AL; IMbrave150 Investigators. Atezolizumab plus bevacizumab in unresectable hepatocellular carcinoma. N Engl J Med 2020;382:1894-1905.










