소아청소년 고도비만의 관리
Management of severe pediatric obesity
Article information
Trans Abstract
Background
Pediatric obesity has increased over the decades, and in particular, severe pediatric obesity has become a serious public health problem. A concern has arisen that the COVID-19 pandemic may exacerbate the incidence of childhood obesity.
Current Concepts
The consequences of severe pediatric obesity are more devastating than those of moderate obesity. Children with severe obesity are at a greater risk for hypertension, type 2 diabetes, metabolic syndrome, non-alcoholic fatty liver disease, atherosclerosis, and adult obesity. Correct assessment and diagnosis of a child with severe obesity is key to successful therapy. A thorough history and physical examination are important in identifying monogenic obesity or metabolic syndrome. Eating behaviors and psychosocial factors should be assessed to improve weight management outcomes. Treatment options for severe pediatric obesity include lifestyle modification, pharmacotherapy, and metabolic and bariatric surgery. Even though progress has been made with regard to the treatment of obesity, safe and effective treatment of severe pediatric obesity is challenging.
Discussion and Conclusion
More efforts and innovations are needed to find a solution for the huge medical and emotional burden the children with severe obesity and their families are enduring.
서론
소아청소년 비만의 유병률은 국내는 물론 전 세계적으로 지난 40년간 급격히 증가했다[1,2]. 최근 연구 자료에 따르면 소아청소년 비만의 발생 증가 속도가 둔화되고 전반적인 유병률이 안정되기 시작했지만, 소아청소년 고도비만은 지속적으로 증가하고 있다[3,4]. 코로나바이러스감염증-19(coronavirus disease 2019, COVID-19) 범유행 이후 학생들의 학교 등교 및 외출이 제한됨으로 인해 활동량이 감소되어 COVID-19가 소아청소년 비만의 확산을 심화시키고 비만 위험의 격차를 증가시킬 수 있다는 우려의 소리가 들려오고 있다[5]. 실제로 COVID-19 제한조치기간 동안에 소아청소년의 몸무게가 증가하였다는 연구들이 각지에서 보고되고 있다. 소아청소년 비만은 성인 비만과 마찬가지로 고혈압, 이상지질혈증, 제2형 당뇨병, 비알콜성 지방간 질환, 폐쇄성 수면 무호흡증, 다낭난소증후군, 우울증을 포함한 정신 질환과 같은 다양한 동반 질환의 발생과 관련이 있다[6-11]. 과체중 및 비만 아동과 비교했을 때, 고도비만인 아동에서는 심근경색증의 초기 징후와 무증상 단계의 동맥경화증 등 보다 심각한 심혈관대사 질환의 위험도가 보고되고 있다[12-14]. 아동에서부터 성인까지의 체질량지수의 궤적을 추적하였을 때, 비만 상태를 유지하는 정도는 고도비만에서 더 강하였다[15]. 그러므로, 소아청소년 고도비만의 예방과 치료는 심혈관대사 질환의 위험을 약화시키기 위해 매우 중요하다. 이 논문에서는 고도비만인 소아청소년 환자를 평가하는 방법과 생활습관 수정요법, 약물요법, 대사 및 비만수술 등의 주요 치료법을 중점적으로 다루고자 한다.
소아청소년 비만과 고도비만의 정의
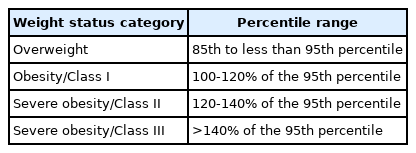
성인 비만의 대부분은 어린 시절에 시작되기 때문에, 소아청소년 비만에 대한 우려가 커지고 있으며, 의료진들에게 예방과 치료를 위한 적극적인 노력의 필요성이 대두되고 있다[16]. 비만평가에서 체질량지수는 소아와 성인에서 모두 인정된 지수이며, 소아의 경우 체질량지수를 나이와 성별에 대한 체질량지수 성장 곡선과 비교하며 동일 연령, 성별의 체질량지수 85백분위수와 95백분위수 사이를 과체중으로, 95백분위수 이상을 비만으로 정의한다[17]. 비만은 체질량지수 백분위수에 따라 3단계로 분류되는데, 95백분위수의 100%와 120% 사이가 비만 1단계, 체질량지수 95백분위수의 120%와 140% 사이가 비만 2단계, 140% 이상이 비만 3단계이다(Table 1) [18]. 소아청소년 고도비만은 비만 2단계과 3단계로 정의된다. 이러한 분류를 통해 비만도의 증가에 따라 심장혈관-대사질환의 위험도가 증가함을 볼 수 있고, 비만 2단계와 3단계가 이러한 위험도과 밀접한 관련이 있음을 보여준다[19,20].
소아청소년 고도비만이 대사에 미치는 영향
대사 및 심혈관 합병증이 소아기부터 관찰되며 이는 비만의 가장 흔한 생화학적 변화인 인슐린 저항성 발달과 밀접한 관계가 있다[21]. 비만과 관련하여 초기 소아기부터 발생하는 동반 질환은 포도당불내성, 이상지질혈증, 고혈압이다. 이러한 의학적 이상 상태의 집합을 대사증후군이라고 한다. 여기에는 제2형 당뇨병, 고혈압, 이상지질혈증, 관상동맥 심장질환 등이 포함된다[22].
중증 소아청소년 비만 평가
소아청소년 고도비만 치료에 성공하는 비결은 합병증을 포함한 정확한 진단이다. 출생부터 현재까지의 자세한 병력을 청취하는 것이 중요하다. 출생 체중, 양친의 체질량지수, 임신성 당뇨에 대한 노출, 산모 비만, 미숙아, 모유 수유 이력, 신생아 합병증, 신경 발달 이상, 이상 징후, 그리고 약물, 특히 당질부신피질호르몬, 항우울증 약물, 항자간증 약물 등의 질문이 포함되어야 한다. 정형외과적 통증, 두통, 코골이에 대하여서도 반드시 평가해야 한다. 비만은 이질적인 질병이기 때문에 기저의 에너지 대사 조절 이상의 잠재적 이상을 찾는 것이 치료에 있어 중요한 열쇠이다[23]. 신체검사에서 정상적인 성장 곡선을 보이는 경우에는 비만의 기질적인 원인을 배제할 수 있다. 그러나, 인슐린혈증과 인슐린 저항성은 성장을 가속화시키는데 이는 인슐린 유사 성장인자-1 (insulin like growth factor-1) 수용체와 인슐린의 교차반응에 의해 일어난다[24]. 흑색가시세포증(acanthosis nigricans)과 허리둘레는 인슐린 저항성과 대사증후군과 관련이 있기 때문에 중요한 신체적 특징이다[25].
혈액검사에서 아스파트산아미노기전달효소, 알라닌아미노기전달효소, 지질, 공복 포도당, 당화혈색소 등 비만 관련 동반 질환에 대해 검사해야 한다. 황체형성호르몬, 난포자극호르몬, 테스토스테론 수치는 남성의 사춘기가 지연되거나 여성의 다낭난소증후군이 의심되는 경우에 평가해야 한다. 가족 위험인자가 존재하는 경우 제2형 당뇨병에 대한 평가를 위해 경구 포도당 부하 시험이 필요하다.
1. 생물학적 요인
유전자는 비만에 가장 큰 기여를 하고 있으며, 체질량지수의 변이의 30-90%는 유전된다[26]. 단순 비만은 비만과 관련된 여러 유전자의 부가적인 영향으로 인해 발생한다[27]. 반면에 약 5%에서 10%의 소아에서는 과식증과 함께 5세 이전의 어린 나이에 비만이 발생하게 되는데, 이런 경우에는 단일유전자 질환으로 인한 비만을 고려해 보아야 하며, 이러한 사례의 대부분은 렙틴-멜라노코틴 경로(leptin-melanocortin pathway)의 단일유전인자 장애로 인해 발생한다[28]. 따라서 어린 나이에 발생한 고도비만이거나 비만과 동반하여 발달 지연이 있는 경우에는 유전자 평가를 고려하여야 한다. 단일유전자에 의한 비만의 확인은 멜라노코틴-4 수용체(melanocortin-4 receptor) 돌연변이에 대한 세타멜라노타이드 또는 렙틴 수용체 결핍에 대한 렙틴과 같은 특정 약리학적 치료의 대상자를 찾고 장기 이상을 포함한 다른 동반 질환에 대한 추가 평가를 위한 단서를 제공할 것이다[29]. 다른 생물학적인 요인으로는 성장호르몬 결핍증이나 쿠싱증후군과 같은 내분비장애가 있다.
식습관은 비만을 결정짓는 중요한 요인이다. 일반적인 식이 평가인 패스트푸드 섭취 빈도나 당이 포함된 음료의 소비 빈도를 조사하는 것을 넘어서, 식습관에 대한 철저하고 상세한 조사는 비만의 원인 파악을 위한 정보를 제공할 수 있다[30]. 예를 들어, 항상 음식을 입에 물고 있거나, 성인이 먹는 양을 먹거나, 식사 사이에 간식을 먹는 것으로 조사되는 아이들은 항상성 식욕 조절에 문제가 있을 수 있다[31]. 항상성 식욕 조절과는 반대로 비항상성(쾌락추구성) 식욕 조절 기전은 부정적인 감정이나 스트레스를 받는 상황에 적응하기 위해 감정적으로 과식을 하는 환자들에 의해 제안되었다.
낮은 신체활동 수준은 소아청소년 비만의 또 다른 생물학적 요인이다. 비만인 아이들이 운동을 망설이는 이유는 아마도 근골격계 통증, 총운동의 발달 지연, 심폐소생술의 건강 악화 또는 우울증 때문일 것이다. 불충분한 수면양은 주로는 심야에 스마트폰 등의 전자 기기를 사용함으로써, 또는 폐쇄성 수면 무호흡증후군이나 중추성저환기증후군에 의해서 발생하게 되는데, 이로 인해 그렐린과 코르티솔의 증가와 렙틴에 대한 반응의 감소가 일어나게 되고 비만 발생에 영향을 주게 된다[32,33].
2. 심리사회적 요인
비만 치료를 원하는 비만 아동은 정상체중 아동보다 우울증, 불안, 주의력결핍과다활동장애, 섭식장애 등 정신건강에 문제가 있는 경향이 더 높다. 고도비만 청소년은 우울증 발생률이 중등도 비만 청소년에 비해 3배, 불안은 5배 높은 것으로 보고되고 있다[34]. 폭식의 유병률은 비만(10%)보다 고도비만(17%) 아동에서 더 높게 보고되었다[35]. 따라서, 진료현장에서 동시에 발생하는 증상에 대한 평가와 적절한 치료를 제공하는 것은 더 나은 체중관리 결과를 위해 중요하다. 우울증, 불안, 주의력결핍과다활동장애, 섭식장애에 대한 간단한 선별검사는 설문지를 통해 평가할 수 있다. 양성 반응을 보이는 환자는 정신건강 관리를 위해 진료 의뢰를 고려하여야 한다.
고도비만은 신체적 건강 외에도 정신 사회적 건강에 부정적인 영향을 미친다. 233명의 청소년을 대상으로 한 다기관 관찰 연구에서, 피실험자들에게 신체적 편안함, 신체 존중감, 사회생활, 가족관계에 대한 설문지를 통해 조사하였다. 그 결과에 따르면 체질량지수의 증가는 삶의 질에 부정적인 예측변수임을 보여주었다[36]. 체중감량 치료를 원하는 361명의 청소년을 대상으로 한 연구에서 체중을 기반으로 한 괴롭힘은 체중이 증가함에 따라 증가되었다[37]. 아이가 희생을 경험하고 있는지를 확인하는 것과 학교와 집에서 관련 지지나 자원을 제공하는지를 확인하는 것은 계획에 필수적이어야 한다.
치료
1. 생활습관 교정
소아청소년 비만 치료에는 생활습관 개선요법이 필수적이다. 고도비만인 소아청소년에게도 일차 치료방법이다[18]. 현재까지 식이조절, 신체활동 증가, 자기감시, 자극조절, 양성강화, 사회지원, 인지행동치료 등 행동변화 전략을 적용한 수많은 치료프로그램이 이용되어왔다. 소아청소년 비만 치료에 있어 필수적인 요소는 건강한 행동에 대한 지원과 부모의 참여이다. 가족 기반 프로그램은 가장 성공적인 체중관리 프로그램이다. 하지만, 이 프로그램이 일차 치료에 적합하여도, 그 효과는 고도비만인 어린이들에게 제한적으로 나타난다. 가장 효과적인 프로그램을 통해 고도비만인 어린이들의 체질량지수가 약간 감소하는(5-20%) 결과를 보였지만, 시간이 지남에 따라 효과가 지속되지 않는 양상을 보인다[18].
기본 식단 권장사항은 대부분 저지방 식단에 기초하고 있으며, 최근에는 저탄수화물 식단이 인기를 끌고 있다[38]. 107개 연구로 진행한 체계적 문헌고찰 결과에서 저탄수화물 식이는 혈청 지질, 금식 혈청 포도당 및 인슐린 수치, 혈압에는 유의미한 악영향을 미치지 않았으며 저지방 다이어트에 상응하는 체중감소 결과를 보였다[38]. 저탄수화물 식이의 변형 가운데 단백질 저장 변형 식이(protein-sparing modified fast)는 특히 고도비만 소아청소년을 중심으로 체중감소가 두드러졌다. 이 식이요법은 케톤증(ketosis)을 촉진하여 체중감량을 개선하는 방법으로 저칼로리, 저탄수화물, 고단백 식단으로 이루어져있다. 이 실험에 참여한 환자들은 13주에 기준치에서 8 kg의 평균 체중감소를, 36주에 11%의 순 체중감소를 보였다[39].
저칼로리 냉동식사, 쉐이크, 바 등이 포함된 식사대체요법은 고도비만 청소년에서 단기적으로는 효과가 있어 사용되고 있다[40]. 이런 종류의 식사는 식사량 조절을 용이하게 하지만, 치료 종료와 정상 다이어트 재개에 따라 체중이 다시 증가하고, 장기간으로 진행하기가 어려운 점이 있다. 어린이들에서 치료는 제한적이며 부모와 환자들이 이러한 치료를 받아들이지 않음으로 인해 치료에 있어 제한이 있을 수 있다.
신체활동은 두 번째로 중요한 행동 개입이다. 미국소아청소년과학회(American Academy of Pediatrics)와 유럽내분비학회와 소아내분비학회는 체중상태에 관계없이 모든 아동에게 신체활동을 권장하고 있다. 학회는 매일 60분씩 중등도 내지는 격렬한 신체활동을 권장하고 스크린을 보는 시간은 하루에 1-2시간 이하로 제한하도록 권고하고 있다[41,42]. 고도비만인 아이들을 포함한 대부분의 어린이들은 이러한 권고사항을 달성하지 못한다. 특히 대근육발달 지연이나 근골격계 통증에 의해 움직임이 제한될 때, 운동 생리학자와 물리치료사는 개별적인 운동 계획을 개발함으로써 이러한 아이들을 도울 수 있다[43,44].
2. 약물요법
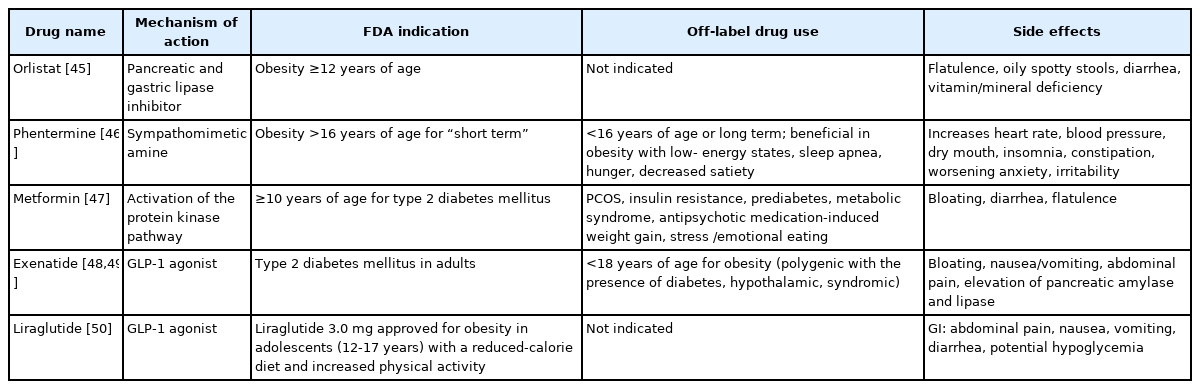
소아청소년 비만의 일차 치료방안은 생활습관 개선요법이다. 약물요법은 생활습관 개선요법의 부차적인 방법으로서, 생활습관 개선요법만으로는 성공을 거두지 못한 환자에서 선택되는 이차 치료법이다(Table 2) [45-50]. 소아청소년 비만 약물요법의 적응증은 10세 이상 연령과 체질량지수가 성별연령대비 95백분위수 이상이면서 체중과 관련된 동반 질환이 있는 경우, 동반 질환 유무와 관계없이 체질량지수가 95백분위수의 120% 이상인 경우가 포함되며, 생활습관 개선요법에 적절하게 반응하지 않는 경우를 포함한다[42]. 올리스타트(orlistat)는 식이에서 지방의 흡수를 막는 지방분해효소 억제제이며, 미국식품의약국에서 유일하게 승인된 소아청소년 비만치료제이며 장기간 사용도 가능하다. 12세 이상에서 사용이 가능하며, 1년 치료 후 약 -2.61 kg 감소가 확인되었다. 하지만 배에 가스가 차거나, 기름변을 보거나 설사를 하는 등의 부작용으로 인해 임상 사용이 상당히 제한적이며, 대다수의 청소년에서 이러한 부작용은 견디기 힘들 수 있다[45]. 노르에피네프린 재흡수억제제인 펜터민은 미국식품의약국에서 16세 이상의 환자들을 대상으로 단기간 치료를 위해 사용할 수 있도록 승인된 약물이다. 펜터민의 효과는 중간 정도이며 체질량지수는 약 4% 감소한다. 펜터민은 심박수를 높이며, 혈압, 불안감, 어지러움, 불면증 등의 증가를 유발할 수 있는 교감신경유사체이다[46].
주로 혈당 조절에 사용되는 비구안화물인 메트포민(metformin)은 제2형 당뇨병에 대해 미국식품의약국의 10세 승인을 받았다. 체중감소를 위해 메트포민과 위약의 사용을 비교한 616명의 소아청소년 환자를 대상으로 시행한 메타분석(체질량지수 기준 36.0 kg/m2, 메트포민 투여량은 하루 1-2 g)에서 메트포민 치료는 체질량지수 z-score (-0.10 [95% 신뢰구간, -0.17에서 -0.03])와 체질량지수(-0.86 [95% 신뢰구간, -1.44에서 -0.29)를 줄였다. 공복 혈장 포도당 및 인슐린 저항성에 있어서는 개선을 보였지만 지질 수준은 감소시키지 못하였다[47].
엑세나타이드(exenatide)와 리라글루타이드(liraglutide)는 글루카곤유사펩타이드-1 수용체(glucagon-like peptide-1, GLP-1) 작용제이다. 엑세나타이드는 성인 제2형 당뇨병 미국식품의약국 승인을 받았으며, 리라글루타이드 3.0 mg 주사는 성인 비만에 대한 미국식품의약국 승인 약물이다. 최근 리라글루타이드 3.0 mg 주사는 체중 60 kg 이상, 초기 체질량지수 30 kg/m2 이상인 12세 이상의 소아청소년의 비만 치료에 미국식품의약국 승인을 획득하였으며, 이 치료는 저칼로리 식이요법 및 운동요법과 병행하여야 한다. GLP-1 작용제 관련 체중감소는 위 비움 감소와 포만감 및 식욕 억제 증가와 관련이 있는 것으로 보인다. 고도비만 소아청소년을 대상으로 한 두 번의 무작위 대조군 실험을 통해 3개월간의 엑세나타이드 치료로 체질량지수와 체중의 상당한 감소를 이끌어낼 수 있음을 보여주었다[48]. 고도비만 청소년의 주간 엑세나타이드에 대한 6개월 무작위, 이중맹검 실험은 체질량지수의 상당한 감소와 당저항성과 콜레스테롤 수치에 있어서의 호전이 있음을 보고하였다[49]. 최근, 비만 소아청소년을 대상으로 56주간 치료를 진행한 리라글루타이드의 무작위 통제 실험에서 생활습관 개선과 함께 치료하였을 때 체질량지수 z-score의 상당한 감소가 있었음이 보고되었다[50]. GLP-1 작용제 치료는 증후군성 비만이나 시상하부성 비만에 있어서도 체중감소의 효과를 볼 수 있는 가능성을 가지고 있다[51,52].
3. 대사 및 비만 수술
소아청소년 비만에서 수술치료는 아직 공인된 공통적 수술 권고안은 없다. 성장과 사춘기 성숙이 완료된 경우에 고려되며 성장 중인 소아청소년에서 수술치료는 엄격한 기준 하에 제한적으로 고려되고 있다. 다면적 치료와 약물 치료 등 이전 단계 치료에 대한 평가가 선행되어야 한다. 수술치료가 소아청소년의 성장과 발달에 미치는 영향에 대한 연구는 부족하다. 그러나 최근에 대사 및 비만 수술(metabolic bariatric surgery, MBS)이 청소년 고도비만에서 효과적인 치료임이 인정되었고, 비만 관련 동반 질환에 대한 유의한 호전이 보고되었다[53]. 미국 대사 및 비만수술학회 소아위원회(American Society for Metabolic and Bariatric Surgery Pediatric Committee)에 의해 최근에 발표된 지침에서 체중 관련 동반 질환이 있는 10세 이상의 체질량지수가 95백분위수의 120% 이상을 보이는 소아청소년에 대해 MBS가 고려될 수 있음이 제안되었다. 체중 관련 동반 질환에는 당뇨병, 고혈압, 무알코올성 지방간 질환, 폐쇄성 수면 무호흡증 등이 포함된다. 그리고 동반 질환 여부와 관계없이 95백분위수의 140% 이상의 경우에도 MBS를 고려할 수 있다[53]. 지침에 따르면 이전의 체중감량 시도, 낮은 성성숙도 단계, 미숙한 골성장 등은 치료에 있어서 금지조항이 될 수 없다고 한다[53]. 성성숙도 단계, 성장 또는 키가 MBS에 의해 부정적인 영향을 받는다는 연구결과가 없기 때문에 MBS가 아동의 사춘기 성장에 미치는 영향에 대한 추가 연구가 수행되어야 한다. MBS를 진행하기 전에 청소년과 그 가족은 심리적 안정성과 역량이 있음을 확인해야하고, 적절한 사후 관리를 받을 수 있는 가용성에 대한 평가와 건강한 식생활과 활동 습관을 준수할 수 있는 검증된 능력을 갖춰야 한다. 또한 전 과정 동안 신체적, 정신적 지원을 할 수 있는 믿을 만한 관리인이 필요하다는 사실도 매우 중요하다.
일차적으로 평가된 MBS의 주요한 두 가지 방법은 Rouxen-Y 위 우회술과 수직슬리브위절제술(vertical sleeve gastrectomy)이었다. 고도비만 청소년들을 대상으로 한 전향적 연구에서 중간기간 체중감소(1-3년)는 30-40% 정도이고, 장기 체중감소(5-8년)는 약 30% 정도의 체질량지수 감소를 보여주어 지속 가능성을 보여준다[54,55]. 게다가 유전적 결함이 있는 희귀 소아청소년 고도비만 환자(Prader–Willi 증후군 및 멜라노코틴-4 수용체 돌연변이)의 MBS 연구에서 MBS는 상당한 체질량지수 감소와 동반 질환의 호전을 보여주었다[56,57].
MBS는 부작용의 발생 가능성이 있는 수술로 거대 및 미세영양소의 결핍과 단백질, 철분, 칼슘, 비타민 등을 평생 보충해야 할 가능성이 있다. Roux-en-Y 위 우회술은 체중감량을 위한 작용의 제한적 및 비흡수적 기전을 모두 포함하며, 이러한 기전으로 인해 결함이 발생할 가능성이 더 높다[45]. MBS의 또 다른 합병증은 위장 역류이며, 복강경수직슬리브위절제술(laparoscopic vertical sleeve gastrectomy)보다 더 빈번하게 발생하며 수술을 받은 환자의 12-30%에서 양성자펌프억제제의 장기간 사용이 보고되었다[58]. 모든 수술적 처치에 있어 환자들은 문합 부위 누출, 탈장, 협착, 상처 감염의 노출의 위험이 있지만, 이러한 합병증은 성인 환자들보다 소아청소년 환자에서 적게 발생한다.
결론
소아청소년 고도비만은 많은 즉각적이고 장기적인 건강 문제들과 연관되어 있기 때문에 중요한 공중 보건 문제이다. 최근 자료에 따르면 고도비만 소아청소년의 수는 증가하고 있지만, 유행과 추세를 보다 정확하게 설명하기 위해서는 더 많은 데이터가 필요하다. 현재까지 축적된 증거를 바탕으로 소아청소년 고도비만이 비만과 과체중인 소아청소년들과 비교하였을 때 대사 이상과 더 많이 관련이 있다는 것을 알 수 있다. 소아청소년 고도비만의 치료 방안은 생활습관 개선요법, 약물요법, 비만수술 등이 있지만, 이 질환에 시달리는 소아청소년에 대한 결과 개선을 위해서는 점진적이고 더 집약적인 혁신적인 치료법을 개발하고 평가할 필요가 있다. 의미있는 진전을 이루려면 소아청소년 비만 분야 전문가들은 고도비만의 심각성과 그 생물학적 배경을 인지하고 집중적인 치료 접근법을 평가하는 추가 연구의 시급성을 인정해야 한다. 또한 소아청소년 비만예방 프로그램을 개발하고 유지하기 위한 지역사회 기반 접근방식을 육성하기 위해 소아청소년과 의사와 공공보건의의 협력이 필요하다.
Notes
Conflict of Interest
No potential conflict of interest relevant to this article was reported.
Peer Reviewers’ Commentary
소아청소년에서의 비만이 최근에 매우 폭발적으로 증가하고 있어 비만에 대해 사회적으로 많은 관심이 필요한 시기이다. 이 논문은 소아청소년 고도 비만의 원인과 비만으로 발생하는 문제점, 비만의 관리 및 치료에 대한 최신 논문을 체계적으로 정리하여 설명해 주고 있다. 비만을 개선하기 위해서 식이 조절 및 신체 활동의 증가가 중요한 부분이라는 점을 잘 설명하고 있다. 또한, 최근 미국 식품의약국의 승인을 받은 글루카곤 유사 펩타이드-1 수용체 작용제를 포함하는 소아청소년에서 사용 가능한 약제의 종류, 기전, 부작용 등을 표로 잘 정리하여 제시해 주고 있어 소아청소년 비만 관리와 치료에 많은 도움을 줄 것으로 판단된다.
[정리: 편집위원회]