 |
 |
- Search
| J Korean Med Assoc > Volume 64(11); 2021 > Article |
|
Abstract
Background: The incidence of osteoporotic vertebral compression fracture (OVCF) is increasing with the increase in the elderly population. Kümmell’s disease following OVCF occurrence is not a rare complication and is frequently associated with severe pain or neurologic deficit with progressive kyphotic deformity. Kümmell’s disease initially meant post-traumatic delayed vertebral collapse, but now it is also termed nonunion, osteonecrosis, or intravertebral vacuum cleft, all of which suggest the disruption of the healing process.
Current Concepts: The major pathogenesis of Kümmell’s disease is a vascular compromise caused by mechanical stress or intravascular pathology. The key radiologic sign to diagnose Kümmell’s disease is the presence of intravertebral vacuum cleft, observed using simple X-ray, computed tomography, or magnetic resonance imaging. Magnetic resonance imaging is the most useful diagnostic tool showing gas or fluid signals. The risk factors for the progression of Kümmell’s disease after OVCF include middle-column injury, confined low signal intensity on T2-weighted image, posterior wall combined fracture, kyphotic angle >10°, and a height loss >15%. Its treatment can be broadly classified as conservative treatment, bone cement injection, and surgical treatment. The appropriate treatment method is selected based on the pain intensity, neurological symptoms, and the severity of the kyphotic deformity.
Discussion and Conclusion: Kümmell’s disease usually develops along with osteoporosis. Therefore, the treatment should be focused on relief from symptoms associated with Kümmell’s disease and osteoporosis. It is recommended that an anabolic agent should be administered after the diagnosis of Kümmell’s disease, regardless of the treatment modality.
Current Concepts: The major pathogenesis of Kümmell’s disease is a vascular compromise caused by mechanical stress or intravascular pathology. The key radiologic sign to diagnose Kümmell’s disease is the presence of intravertebral vacuum cleft, observed using simple X-ray, computed tomography, or magnetic resonance imaging. Magnetic resonance imaging is the most useful diagnostic tool showing gas or fluid signals. The risk factors for the progression of Kümmell’s disease after OVCF include middle-column injury, confined low signal intensity on T2-weighted image, posterior wall combined fracture, kyphotic angle >10°, and a height loss >15%. Its treatment can be broadly classified as conservative treatment, bone cement injection, and surgical treatment. The appropriate treatment method is selected based on the pain intensity, neurological symptoms, and the severity of the kyphotic deformity.
Discussion and Conclusion: Kümmell’s disease usually develops along with osteoporosis. Therefore, the treatment should be focused on relief from symptoms associated with Kümmell’s disease and osteoporosis. It is recommended that an anabolic agent should be administered after the diagnosis of Kümmell’s disease, regardless of the treatment modality.
우리나라 사회가 점차 고령화됨에 따라 골다공증의 유병률 또한 높아지고 있다. 골다공증은 고령에서 골절을 유발하는 비교적 흔한 질환으로 그 자체로는 증상이 없지만 뼈의 강도를 약하게 하여 골절을 유발하는 질환이다. 골격계 중 척추는 이와 같은 골다공증성 골절이 가장 흔히 발생하는 부위이며, 이를 골다공증성 척추 압박 골절이라고 부른다. 골다공증성 척추 압박 골절은 대개의 경우 큰 치료 없이 유합되어 통증이 경감되나, 약 7-13%의 환자에서는 시간이 흘러도 골절이 유합되지 않고 척추체 내부에 균열을 동반하는 소견을 보이게 되는데, 이를 쿰멜씨병(Kümmell’s disease)이라고 일컫는다[1-9].
1895년 독일의 의사였던 Kümmell이 경미한 척추 외상 후에 척추체의 지연성 붕괴(delayed post-traumatic vertebral collapse)를 보고하면서 이를 쿰멜씨병이라고 명명하였다[10,11]. 하지만 추후 쿰멜씨병의 병태생리에 대한 연구가 진행되면서 현재 쿰멜씨병은 척추체 내 가관절증, 추체 내진공틈새(intravertebral vacuum cleft, IVC), 척추체 괴사, 압박 골절의 불유합 등의 용어와 같은 의미로 사용되고 있다[12-16].
쿰멜씨병은 보통의 골다공증성 척추 압박 골절과는 다르게 통증이 지속되고 후만 변형이 증가하며 때로는 신경학적 이상 소견을 보일 수 있는 질환이기 때문에 치료법뿐만 아니라 위험인자, 병태생리 등에 대한 이해도 같이 필요하다. 우선, 본 논문에서는 척추를 전공하지 않는 일반 의사들에게 도움이 될 만한 쿰멜씨병의 임상 양상, 병태생리, 영상학적 소견 등을 살펴보고자 한다. 일단 쿰멜씨병이 발생하면 대개의 경우 증상이 수반되기 때문에 치료를 요하게 된다. 이의 치료는 보존적 치료, 척추성형술(vertebroplasty)이나 후만성형술(kyphoplasty) 등의 시멘트 주입술, 수술적 치료 등으로 크게 나누어 볼 수 있다. 치료 방법은 통증의 정도, 신경학적 증상의 유무, 후만 변형의 정도 등을 고려하여 치료 방법을 선택하게 된다. 이처럼 쿰멜씨병의 치료에 있어서 고려할 사항이 다양하고 그 임상 양상이 각기 다르기 때문에 확실히 정립된 치료가 있는 것은 아니다. 이 논문에서는 기존에 알려진 쿰멜씨병의 치료 방법에 대한 최신 지식을 정리하여 설명하였다.
쿰멜씨병의 가장 중요한 임상적 특징은 작은 외상력 이후 지연적으로 발생하는 척추체의 붕괴이다[10,17,18]. 그러나 많은 경우에서 초기에는 증상이 경미하거나 없기 때문에 검사 시기가 늦어져 병이 진행된 후 발견하게 된다[19,20]. 외상 이후 언제 척추체의 붕괴가 발생하여 증상이 생기는지는 다양하게 보고되고 있다[20]. 병의 진행 단계에 대해 여러 저자에 의해 연구가 되었지만 Steel [10]과 Benedek과 Nicholas [18]의 분류 체계가 많이 인용되는 것이다. 1951년 Steel [10]은 쿰멜씨병을 다섯 단계로 구분하였다. 첫 번째 단계(initial injury)에는 허리에 다양한 정도와 방법에 의한 초기 외상이 있게 되는데, 그 정도가 약해서 영상학적 검사 상 큰 이상 소견이 발견되지 않는다. 두 번째 단계(posttraumatic period)는 외상 후 단계로, 환자는 약간의 불편함을 느끼지만 기능적으로 제한은 없는 상태이다. 세 번째 단계(latent interval)는 잠복 단계로, 수개월 동안 일상생활이 가능한 기간이 지속된다. 네 번째 단계(recrudescent stage)는 재발 단계로 환자는 압박 골절 부위에 국한된 통증 악화를 경험하게 된다. 다섯 번째 단계(terminal stage)는 마지막 단계로, 점진적으로 후만 변형이 나타나기 시작한다. 이때 신경학적 이상 소견이 동반되기도 하지만 초기에는 드물며 대개 마지막 단계 즉, 통증이 동반되고 후만 변형이 진행될 때 같이 나타나는 경우가 많다[18,21,22]. 1981년 Benedek과 Nicholas는 Steel의 다섯 단계를 간소화하여 세 단계로 구분하였다. 첫 번째 단계에서는 경도의 허리 외상이 일어나고 그 정도는 약해서 무증상 기간이 수개월에서 수년 동안 지속될 수 있으며 영상학적 진단이 어려운 시기이다. 두 번째 단계에서는 추가적인 외상력 없이 점진적으로 통증이 발생하고 악화된다. 마지막 세 번째 단계에서는 척추체 붕괴와 점차 진행하는 후만 변형이 나타나게 된다.
쿰멜씨병은 골다공증성 척추 압박 골절과 마찬가지로 주로 노년층에서, 그리고 여성에서 조금 더 많이 발생하는 것으로 알려져 있다. 쿰멜씨병이 호발하는 부위는 흉요추부 이행부이며, 이 또한 골다공증성 척추 압박 골절이 호발하는 부위와 같다[20,23]. 일부 저자들은 쿰멜씨병과 골다공증성 척추 압박 골절은 연속성에 있는 질환이 아니고 상이한 손상 기전과 다른 임상 양상 및 영상 소견을 보이는 다른 질환으로 인식되기도 한다[20,23]. 하지만 골다공증성 척추 압박 골절은 초기에 발견되고, 쿰멜씨병은 비교적 나중에 발견되지 때문에 위와 같은 상이한 소견들이 나오는 것은 당연한 것으로 생각된다. 현재까지의 정론은 쿰멜씨병은 골다공증성 척추 압박 골절의 연속성 상에서 이해되고 있는 것으로 보인다.
쿰멜씨병의 발생에 가장 대표적인 원인으로 제시되고 있는 것이 골절된 척추체의 골괴사에 의한 불유합이다[21,24,25]. 척추체 골괴사의 병태생리 기전은 크게 둘로 나누어 생각할 수 있다. 우선 골절로 인한 형태학적 변형 때문에 발생하는 기계적 손상으로 인하여 척추체 내로의 혈류가 감소될 수 있다. 정상적으로는 흉요추부 척추체로의 혈류 공급은 한 쌍의 분절 동맥과 전방, 후방 중심 동맥으로부터 받고 있으며, 이는 각각 척추체의 전방 1/3과 후궁과 척추체의 후방 2/3의 혈액 공급을 담당한다. 척추체의 골괴사는 척추체의 전방 1/3 부근에 많이 발생하는데, 이는 전방 중심 동맥이 주위의 우회 동맥이 적어 허혈성 손상에 취약한 것으로 설명될 수 있다[25]. Kim 등[25]은 척추체의 중간 부분에서 골절이 발생하면 골절편이 방출되려는 성질 때문에 척추체의 단면적이 넓어지고 이것이 혈류 공급을 차단한다고 하였다. Sugita 등[26]도 척추체의 중간 부분에서의 골절이 종판 근처에 발생하는 골절에 비하여 혈관 손상이 더 많음을 관찰하여 골절의 형태에 따라 혈류 공급이 다르게 영향을 받을 수 있음을 보고하였다. 두 번째 척추체 골괴사의 병태생리는 척추체에 혈액을 공급해주는 혈관 자체의 이상이다. 알코올 중독증, 장기간의 스테로이드 치료 병력, 헤모글로빈병증 등은 모두 혈관 손상을 유발할 수 있는 위험인자로써 쿰멜씨병의 위험인자로 작용하게 된다. 혈관에 손상이 발생되면 혈관 내벽에 지방이 침착되고 동맥경화가 발생하여 혈류 공급이 더욱 차단된다[25]. 또한 골절 시 발생하는 지방 색전증도 작은 동맥을 막아 혈류를 차단하는 역할을 한다. 위와 같은 병태생리로 인하여 척추체의 골절후에 신생 혈관이 자라나오지 못하게 되어 결국 골절이 치유되지 못하고 불유합을 유발하게 된다. 골다공증이 심한 환자일수록 골모세포의 숫자도 적고 혈류 압박에도 취약하게 되어 골절의 유합을 더디게 할 수 있다는 보고도 있다[27]. 이러한 혈류 손상에 의한 기전과는 반대의 의견을 내는 연구도 보고되고 있다. 몇몇 저자들은 골괴사는 골절되지 않은 척추체에도 발견될 수 있음을 보고하였고 이들은 혈류 장애보다는 흉요추부 이행부의 생역학적 특성이 척추체 내의 불안정성을 유발시켜 쿰멜씨병을 유발하는 데 더 중요하다고 보고하고 있다[14,28]. 이상의 병태생리를 정리하면 쿰멜씨병의 발생에는 혈류 차단이라는 내인성 요소와 생역학적으로 불안정한 외인성 요소가 모두 작용하고 있다고 이해할 수 있다.
쿰멜씨병의 영상 진단에서 가장 중요한 소견은 IVC이다(Figure 1). IVC 소견은 척추체의 중심이나 인접한 종판에 가스가 축적되어 발생한다. IVC는 쿰멜씨병의 진단적 가치가 있는 소견이기도 하지만 지연성 척추체 붕괴를 예측하는 예후인자도 되기 때문에 이와 관련된 연구들이 많이 진행되어 왔다. Maldague 등[21]이 처음 IVC를 언급하였고, 그는 이러한 소견은 종양이나 감염에는 잘 발견되지 않는다고 하였다. 하지만 그 이후 다른 연구들에서는 감염이나 종양에서도 발견될 수 있다고 보고하였다[22,29,30]. IVC는 쿰멜씨병 전의 단계인 일반적인 골다공증성 압박 골절에서도 발견될 수 있다고도 보고되지만, 대개의 경우 수상 초기의 단계에서는 잘 관찰되지는 않는다[29,31]. IVC 소견이 쿰멜씨병에 얼마나 진단적 가치가 있는가에 대한 연구로 Libicher 등[29]은 IVC가 압박 골절 후 발생하는 골괴사의 진단에 특징적인 소견이라고 보고하면서 그 진단적 가치는 85%의 민감도, 99%의 특이도, 91%의 양성 예측률을 보인다고 하였다. IVC가 형성되는 기전은 척추체의 공간에 가스가 채워지거나 추간판 내의 가스가 골절된 척추체로 들어가는 것으로 설명된다. 가스의 성분은 대개는 질소이며 공간에 액체 성분이 차있을 경우 그 성분은 활막액과 유사한 성분이다. 가스 성분과 액체 성분은 자세에 따라서 그 위치가 바뀔 수 있다[30].
쿰멜씨병을 진단하기 위한 영상검사로는 단순 방사선 사진(X-ray), 컴퓨터단층촬영(computed tomography, CT), 자기공명영상(magnetic resonance imaging, MRI) 등이 있다. 우선 가장 쉽고 흔히 시행되는 검사는 X-ray이다. 초기 단계에서는 X-ray만으로 쿰멜씨병을 진단하기는 어렵다. X-ray 진단에서 쿰멜씨병의 진단에 가장 중요한 소견은 IVC sign이다. IVC는 대개 가로로 선모양으로 형성되며 측면 X-ray뿐만아니라 전후방 X-ray에서도 잘 관찰된다. IVC는 척추체 내의 불안정성을 시사하는 소견이기 때문에 굴곡-신전 X-ray나 누워서 찍는 X-ray에서 잘 관찰된다[23,32,33]. CT는 X-ray보다 뼈의 상태를 더 정밀하게 관찰할 수 있다. CT에서 IVC 소견이 더 명확히 관찰되며, 특히 후방 피질골의 연속성을 관찰할 수 있는데, 이는 치료가 필요한 경우 시멘트 주입술 시 시멘트가 척추관 쪽으로 유출될 수 있기 때문에 반드시 확인해야 하는 소견이다. 다음으로는 MRI 검사가 있다. MRI에서는 IVC 소견 및 내부의 액체 성분이 잘 관찰되어 쿰멜씨병에 진단적 가치가 높은 검사이며, 또한 신경 조직의 압박 유무도 관찰할 수 있다. MRI 상골절된 부분은 초기에는 T1 강조 영상에서 저신호 강도, T2 강조 영상에서 고신호 강도로 보이지만, 시간이 지남에 따라 골부종이 감소하고 이러한 신호 강도는 중간 신호 강도로 점차 바뀌게 된다[34]. Young 등[20]은 골괴사된 척추체 부분은 MRI 상 T1 강조 영상에서 고신호 강도로, T2 강조 영상에서는 저신호 강도로 관찰된다고 보고하였다. 하지만 대부분의 연구에서는 골괴사된 부분은 T1 강조 영상에서 저신호 강도로 T2 강조 영상에서는 다양하게 관찰된다고 보고되고 있고, 이는 척추체 내의 가스와 액체 성분의 비율에 따라서 달라진다고 보고되고 있다[29,30,34,35]. T2 강조 영상에서 병변 내부의 고신호 강도 부위를 둘러싼 주위의 저신호 강도를 보이는 부위를 볼 수가 있는데 이는 double-line sign이라 불리고, 중심의 새로운 육아조직이 주위의 경화된 조직으로 둘러싸인 것을 의미하며, IVC 소견과 연관성이 있는 것으로 알려져 있다(Figure 1) [35]. 이 소견은 대퇴골두 무혈성 괴사에서 관찰되는 crescent sign과 비슷한 소견으로 이해되고 있다[25]. IVC 소견 외에도 초기의 골다공증성 압박 골절에서 지연성 척추체 붕괴의 가능성을 시사하는 여러 소견을 MRI에서 관찰할 수 있다. Ahn 등[34]은 골절 초기 MRI에서 관찰된 골수 음영 패턴이 T1 강조 영상에서 저신호 강도로 보일 때 지연성 척추 붕괴의 가능성이 높아진다고 보고하였다. Tsujio 등[36]은 흉요추 접합부에서 발생한 골절, 중주(middle column) 손상, T2 강조 영상에서 저신호 강도가 국소적 혹은 넓게 분포하는 소견을 나쁜 예후인자로 보고하였다. 특히 T2 강조 영상에서 저신호 강도가 국소적으로 분포하는 것은 인장력과 전단력으로 인한 반복적인 기계적 압박을 의미하므로, 저신호 강도가 넓게 분포하는 것보다 불유합의 가능성이 더 클 수 있다. Ha와 Kim [37]은 척추체의 가운데 부분을 침범한 골절, 후벽 골절이 동반된 경우, 척추 후만각이 10도 이상, 척추체의 높이 감소가 15% 이상일 때, 그리고 IVC 징후가 보일 때를 나쁜 예후인자로 보고하였다.
다른 척추질환과 마찬가지로 우선적으로 해야 할 치료는 보존적 치료이다. 쿰멜씨병이 발생하여도 그 형태와 부위에 따라서 통증의 정도가 달라지기 때문에 신경학적 이상 소견이 없이 통증이 주 증상인 경우에는 보존적 치료를 시도하여야 한다. 보존적 치료의 방법은 골다공증성 척추골절에서와 같이 단기간의 침상 안정, 통증 조절을 위한 약물치료, 보조기 등이 주를 이루게 된다[12,31,38]. 하지만 이러한 치료들은 이미 불유합된 척추체에 구조적인 변화를 기대할 수는 없기 때문에 치료에 한계가 있을 수밖에 없다. 보존적 치료에서 빠져서는 안 되는 것이 바로 골다공증 자체의 치료이다. 쿰멜씨병이 발생하면 대개 정형외과나 신경외과의 척추 전문의를 만나게 되는데, 이 질환으로 인한 증상 즉, 통증이나 신경학적 이상만 해결하는데 집중하다 보면 골다공증 자체에 대한 치료를 소홀히 할 수 있다. 골다공증 자체를 치료해야 하는 이유는 다른 후속 골절을 예방하는 데 그 우선적인 목적이 있지만, 최근 연구에 따르면 골다공증 치료가 쿰멜씨병 자체의 healing에도 도움이 될 수 있다는 보고들이 있다[39,40].
2012년 Fabbriciani 등[39]은 증례 논문을 통해 L1의 쿰멜씨병으로 진단받은 81세 여자 환자에서 teriparatide를 12개월 투여하였을 때 환자의 통증이 완전히 사라지고, 후만 변형도 더 증가하지 않았으며, CT 상 보이는 IVC의 크기도 줄어들었음을 보고하였다(Figure 2). 또한 Gou 등[40]의 중국 정형외과 의사들은 최근 Osteoporosis International에 쿰멜씨병으로 진단받고, teriparatide로 1년간 치료한 21명의 환자를 모아서 그 결과를 발표하였다. 그들의 결과에 의하면 모든 환자에서 통증 점수는 유의하게 감소하였고, CT 상 보이는 IVC의 크기도 줄었다고 보고하였다. 21명의 환자 중 8명은 골가교도 형성된 것을 관찰할 수 있어 불유합이라고 진단되었지만, 유합도 도모할 수 있을 것으로 보고하였다. 이와 같이 신경학적 증상이 없는 경우라면 일반적인 보존적 치료에 teriparatide와 같은 골형성 촉진제를 사용하여 추가 골절을 막음과 동시에 쿰멜씨병 자체의 치료 효과도 기대해볼 수 있겠다. 반면 비스포스포네이트(bisphosphonate) 계열의 약제는 골유합을 저해할 가능성이 있기 때문에 골다공증성 척추 골절 후 쿰멜씨병이 발생할 가능성을 높일 수 있다고 보고되고 있다[41]. 따라서 골다공증성 척추 골절이 발생하였다면 쿰멜씨병의 발생 여부와는 상관없이 비스포스포네이트 계열의 약제를 끊거나 골형성 촉진제로 바꾸는 것을 고려해야 한다.
통증 치료 및 골다공증 치료 등의 보존적 치료에도 불구하고 통증이 지속될 경우 시멘트 주입술을 고려할 수 있다. 시멘트 주입술은 단순히 시멘트만 주입하는 척추성형술과 balloon을 이용하여 공간을 만들어 준 후 시멘트를 주입하는 후만성형술로 나눌 수 있다[42-48]. 이러한 치료는 대개 국소마취 하에 시행된다. 일반적인 골다공증성 척추 압박 골절의 초기 치료로서 척추성형술이나 후만성형술의 역할은 논란의 여지가 있어왔다. 시멘트 주입이 골유합을 촉진시켜주는 것이 아니며 오히려 골유합을 방해한다는 반대 의견과 그래도 통증 감소를 기대할 수 있다는 찬성 의견이 현재까지도 모두 존재한다[42,43]. 쿰멜씨병에서 시멘트 주입술의 효과에 대하여도 여러 연구에서 다르게 보고하고 있다. 쿰멜씨병에서 IVC 소견이 보일 때 시멘트를 주입하여도 인접 정상 척추체에 시멘트가 결합되기 힘들기 때문에 주입된 시멘트가 이탈되거나 인접 정상 척추체의 골절을 유발하는 등 좋지 않은 결과를 보고한 연구가 있다[12]. 또한 IVC가 있을 때 시멘트 누출의 위험이 높아진다는 연구도 보고되고 있다[49]. 본 저자는 골다공증성 척추 압박 골절의 일차 치료로 척추성형술이나 후만성형술은 고려하지는 않는다. 하지만 쿰멜씨병이 발생하였을 때는 이미 불유합이 발생한 것이기 때문에 일반적인 보존적 치료만으로 통증이 개선되지 않을 경우에는 신경학적 이상만 없다면 이러한 시멘트 주입술을 적극적으로 고려하고 있다. 척추성형술은 비용이나 부작용 대비 통증 개선 효과는 매우 좋은 편으로 보고되고 있어 소위 가성비가 매우 좋은 술식으로 생각되며, 침습적인 수술적 치료의 전 단계로써의 역할을 충분히 수행한다고 생각된다. 가장 흔한 부작용은 시멘트 누출로 보고되고 있으며, 후방 피질골에 연속성이 끊어진 경우에는 경막 외로 시멘트가 누출될 위험이 있으니 주의를 요한다[49]. 시멘트 누출과 관련한 가장 심각한 부작용으로는 폐색전증이 있으나 그 빈도는 매우 낮게 보고되고 있다. 척추성형술은 엎드려 있는 자세에서 시멘트만 주입하기 때문에 후만 변형을 교정하는 정도는 시술 시 자세에서 교정되는 정도이다. 반면 후만성형술은 balloon을 이용하여 추체의 높이를 높인 후에 시멘트를 주입하기 때문에 자연히 후만 변형의 교정을 척추성형술보다는 더 기대할 수 있다. 또한 balloon으로 만들어진 공간에 시멘트가 주입되기 때문에 척추성형술보다는 낮은 압력으로 시멘트를 주입할 수 있어 시멘트 누출의 위험이 적다고 보고되고 있다. 여러 방사선학적 지표는 후만성형술이 척추성형술보다는 우수하다고 보고되고 있으나 대부분의 연구에서 임상 증상의 호전 정도는 비슷하다고 보고되고 있다[42]. 비용이나 효과 등을 고려하여 어떤 시술을 할지를 결정하게 되며, 저자는 개인적으로 통증 개선에는 척추성형술만으로 충분하다고 판단되어 주로 척추성형술만을 시행하고 있다. 쿰멜씨병에서 척추성형술이나 후만성형술 후에 시술과 관련한 합병증 외에 고려해야 할 것으로는 시멘트 주입술한 척추체의 나머지 부분이 유지되지 못하고 다시 무너지는 경우, 인접 마디에 새로운 골다공증성 압박 골절이 발생하는 경우 등이 있다. 따라서 시술 전에 이러한 것이 발생한 가능성이 있다는 것을 의사도 인지할 뿐 아니라 환자에게도 설명하여야 할 것으로 생각된다.
약물치료 등의 보존적 치료나 시멘트 주입술과 같은 최소 침습적 치료를 시행하였음에도 불구하고 통증이나 후만 변형이 악화되거나 처음부터 신경학적 이상 소견이 발생한 경우에는 수술적 치료를 고려할 수밖에 없다. 쿰멜씨병에서 수술적 치료는 항상 최후의 치료 옵션으로 생각하는 것이 좋다. 그 이유는 이러한 질환의 환자군들이 비교적 고령으로 기저질환이 많고, 골질이 좋지 않기 때문에 수술과 관련한 합병증의 위험이 상주하기 때문이다. 일단 수술을 고려할 상황이 되면 이러한 수술과 합병증의 위험을 줄이려는 노력을 기울여야 하겠다. 수술의 방법은 후만 변형의 정도, 신경학적 이상의 유무 등을 생각해서 선택해야 하나 여기서도 그나마 덜 침습적인 방법을 우선적으로 고려하는 것이 좋을 것으로 생각된다. 즉, 후만 변형이 있는 경우 삼주 절골술(three column osteotomy)을 하지 않고 후만 변형 교정이 가능한지, 신경 압박이 있는 경우 추체 제거술을 하지 않고 후방 감압술로만 신경 압박을 해소할 수 있을지, 추체 제거술이 필요할 경우 측방 수술 없이 후방에서만 수술이 가능할지 등을 순차적으로 고려하게 된다. 신경학적 이상이 없다면 대부분 후방 수술로 충분하며, 이러한 경우 후만 변형과 그에 연관된 통증이 주 증상이기 때문에 불안정한 분절의 안정화와 후만 변형의 교정에 초점을 맞추어 치료 전략을 세워야 하겠다. 누우면 펴지는 비교적 유연한 후만증은 후방에서 후관절 제거 및 다분절에 걸친 후방 유합술 정도만 하여도 변형을 교정할 수 있다. 이때 쿰멜씨병이 있는 병소를 어떻게 처리할지를 결정해야 하는데, 척추체 제거술을 하기도 하나, 이는 대개 신경학적 이상이 있는 경우에 시행하게 되고, 신경학적 이상이 없다면 병소에 시멘트를 주입하거나 소파술 후 골이식 또는 cage를 척추경을 통해서 삽입하여 전방지지를 도모할 수 있다. 만약 누워도 잘 펴지지 않는 유연하지 않은 후만 변형일 경우에는 어쩔 수 없이 후만 변형의 첨부(apex)에서 삼주 절골술을 고려해야 한다(Figure 3). 다음으로 신경학적 이상이 있을 경우에는 후만 변형의 동반 여부를 고려하여 신경 감압의 방법을 선택한다. 후만 변형이 심하지 않은 경우에는 추체 제거를 시행하지 않고 후궁절제술만 해도 신경 감압을 충분히 시행할 수 있다(Figure 4). 만약 후만 변형이 동반되어 있고 전방에서 신경을 누르는 정도가 심하다고 판단될 경우에는 추체 제거술을 고려해야 한다. 추체 제거술은 일반적으로 측방 접근을 통해서 시행하나 쿰멜씨병이 호발하는 흉추부나 흉요추부 같은 경우에는 후방 접근(posterior vertebral column resection)만으로도 충분히 추체를 제거할 수 있어 전방 접근 없이 완전한 신경의 감압 및 척주 재건을 동시에 시행할 수 있다(Figure 5). 요추부에 발생한 쿰멜씨병의 경우에는 요추 신경근 때문에 후방 접근만으로는 추체 제거가 힘들기 때문에 어쩔 수 없이 측방으로 접근해야 한다. 쿰멜씨병 환자에서 수술적 치료 시 적합한 수술 방법을 택하여도 필수적으로 필요한 기기 고정술 시 골질이 좋지 않아 고정력이 약해질 가능성 있어 이에 대한 대책도 생각해야 한다. 대표적으로는 척추경 나사 주위에 시멘트로 보강을 하는 것과 pullout을 막기 위하여 근위부나 원위부에 hook를 사용하는 방법이 있다(Figures 4, 5). 수술 후에도 골다공증의 약물치료는 지속해야 하며, 이러한 상황에서는 빠른 골질의 회복과 유합률을 동시에 올릴 수 있는 골형성 촉진제를 사용하는 것이 추천된다.
골다공증성 척추 압박 골절 환자가 늘어감에 따라 쿰멜씨병의 빈도 역시 증가하고 있다. 그 동안의 많은 연구를 통하여 이 질환의 병태생리를 잘 이해할 수 있게 되었고, 방사선학적 위험인자도 많이 알려져 있어 이 부분에 대해서 숙지할 필요가 있겠다. 일단 쿰멜씨병이 발생하게 되면 일반적인 골다공증성 척추 압박 골절에 비해서 보존적 치료에 잘 반응하지 않을 가능성이 높다. 신경학적 이상이나 극심한 통증과 같은 경우가 아니라면 보존적 치료를 우선적으로 시도해야 하며 여기서 빠지면 안 되는 것이 골형성 촉진제와 같은 골다공증 치료이다. 보존적 치료에 반응하지 않을 경우에는 신경학적 증상이 없다면 시멘트 주입술을 적극적으로 고려한다. 수술적 치료는 보존적 치료에 실패할 경우에 고려되며, 신경학적 이상 소견이나 후만 변형의 정도에 따라 그 방법을 선택하면 되겠으나 수술과 관련한 합병증에 특히 주의를 기울여야 하겠다.
Figure 1.
The intravertebral vacuum cleft sign was confirmed on the 12th thoracic vertebra on a standing lateral X-ray taken 4 months after the injury in a 77-year-old female patient (A). Intravertebral vacuum cleft sign is also found in magnetic resonance imaging, showing low signal intensity on T1 weighted image (B). On T2 weighted image, a band-shaped, high-signal intensity lesion is seen suggesting fluid in the center of the fractured vertebral body and a low-signal intensity “double-line sign” suggesting the surrounding granulation tissue (C). Informed consent for publication of the clinical images was obtained from the patient.
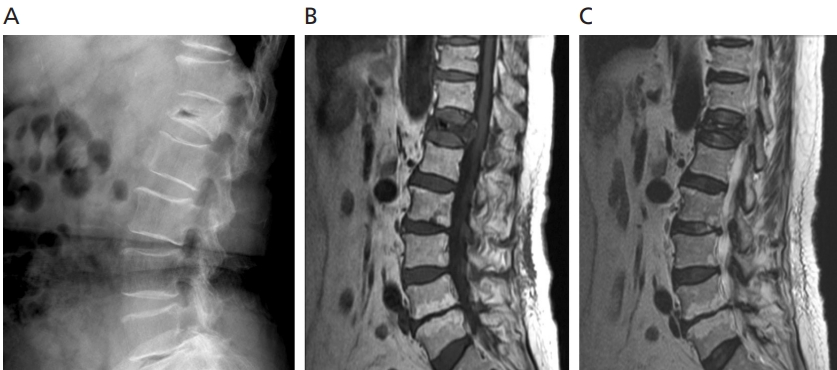
Figure 2.
Case of an 81-year-old female patient. Initial computed tomography images (A,B) and follow-up computed tomography images taken 12 months after teriparatide treatment (C,D). Adapted from Fabbriciani G, et al. Rheumatol Int 2012;32:1371-1374, with permission from Springer [39].

Figure 3.
A 78-year-old female patient came to the hospital with severe back pain and kyphosis that had persisted for several years. She did not suffer from any neurologic symptom. On X-ray, kyphosis was observed with the apex of 12th thoracic vertebra (A), and there was no evidence of nerve compression (B). A mild form of Kümmell’s disease was suspected as air density was seen in the vertebrae and adjacent intervertebral discs (C). A pedicle subtraction osteotomy was performed on the 12th thoracic vertebra to correct the kyphosis, and thereafter the pain was much improved (D). Informed consent for publication of the clinical images was obtained from the patient.
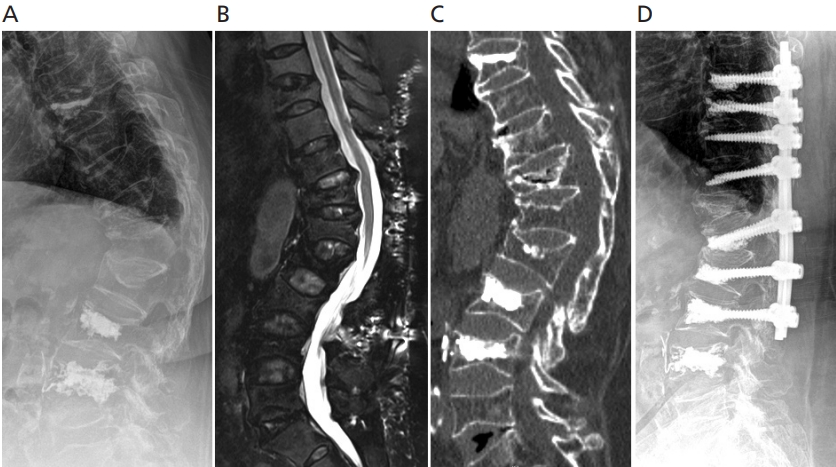
Figure 4.
An 82-year-old female patient who underwent vertebroplasty at L2 and T12 4 months ago at a hospital, but she was unable to walk due to worsening back pain and radiating pain in the lower extremities (A). On magnetic resonance imaging, Kümmell’s disease was observed in the L2 vertebra, and her dural sac was severely compressed (B-D). She underwent posterior decompression by performing laminectomy of L2 and posterior instrument and fusion from T12 to L3 (E,F). During the surgery, the screws were reinforced with bone cement and a laminar hook at L3 to prevent screw pull-out (E,F). Informed consent for publication of the clinical images was obtained from the patient.
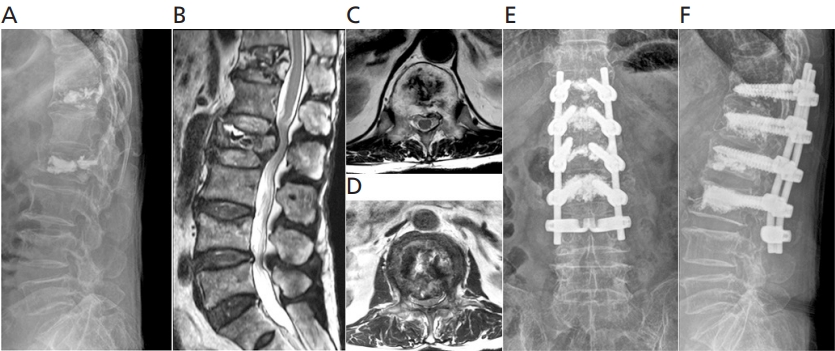
Figure 5.
A 78-year-old female patient came to the hospital with complaints of inability to walk due to the weakness in her legs for 2 days. X-ray shows compression fracture and suspicious Kümmell’s disease at T12 (A). On magnetic resonance imaging, spinal cord was compressed by the posteriorly bulged bone fragment showing the high signal intensity at the compression level (arrow) (B). After removing the whole vertebral body of T12 through a posterior approach without an anterior approach (so called posterior vertebral column resection), anterior support was performed using expandable cage, and then posterior fusion was performed. The distal screw was reinforced with a laminar hook (C). It is observed that the fusion was successful 2 years after surgery (D). Informed consent for publication of the clinical images was obtained from the patient.

References
1. Xiao YP, Bei MJ, Yan CQ, Chang JZ. Analysis of the effect of percutaneous vertebroplasty in the treatment of thoracolumbar Kummell’s disease with or without bone cement leakage. BMC Musculoskelet Disord 2021;22:10.


2. Adamska O, Modzelewski K, Stolarczyk A, Kseniuk J. Is Kummell’s disease a misdiagnosed and/or an underreported complication of osteoporotic vertebral compression fractures? A pattern of the condition and available treatment modalities J Clin Med 2021;10:2584.



3. Wang W, Liu Q, Liu WJ, Li QB, Cai L, Wang ZK. Different performance of intravertebral vacuum clefts in Kummell’s disease and relevant treatment strategies. Orthop Surg 2020;12:199-209.



4. Lim J, Choi SW, Youm JY, Kwon HJ, Kim SH, Koh HS. Posttraumatic delayed vertebral collapse: Kummell’s disease. J Korean Neurosurg Soc 2018;61:1-9.


5. He D, Yu W, Chen Z, Li L, Zhu K, Fan S. Pathogenesis of the intravertebral vacuum of Kummell’s disease. Exp Ther Med 2016;12:879-882.


6. Ranjan M, Mahadevan A, Prasad C, Sommana S, Susarla Krishna S. Kummell’s disease--uncommon or underreported disease: a clinicopathological account of a case and review of literature. J Neurosci Rural Pract 2013;4:439-442.


7. Matzaroglou C, Georgiou CS, Wilke HJ, Assimakopoulos K, Karageorgos A, Konstantinou D, Velissaris D, Panagiotopoulos E, Kafchitsas K. Kummell’s disease: is ischemic necrosis or vertebral “microcracking” the first step in the sequence? Med Hypotheses 2013;80:505.


8. Li H, Liang CZ, Chen QX. Kummell’s disease, an uncommon and complicated spinal disorder: a review. J Int Med Res 2012;40:406-414.


9. Ma R, Chow R, Shen FH. Kummell’s disease: delayed posttraumatic osteonecrosis of the vertebral body. Eur Spine J 2010;19:1065-1070.


12. Lee SH, Kim ES, Eoh W. Cement augmented anterior reconstruction with short posterior instrumentation: a less invasive surgical option for Kummell’s disease with cord compression. J Clin Neurosci 2011;18:509-514.


13. Jang JS, Kim DY, Lee SH. Efficacy of percutaneous vertebroplasty in the treatment of intravertebral pseudarthrosis associated with noninfected avascular necrosis of the vertebral body. Spine (Phila Pa 1976) 2003;28:1588-1592.


14. Kim DY, Lee SH, Jang JS, Chung SK, Lee HY. Intravertebral vacuum phenomenon in osteoporotic compression fracture: report of 67 cases with quantitative evaluation of intravertebral instability. J Neurosurg 2004;100((1 Suppl Spine):24-31.

15. Pappou IP, Papadopoulos EC, Swanson AN, Cammisa FP Jr, Girardi FP. Osteoporotic vertebral fractures and collapse with intravertebral vacuum sign (Kummel’s disease). Orthopedics 2008;31:61-66.


16. Van Eenenaam DP, el-Khoury GY. Delayed post-traumatic vertebral collapse (Kummell’s disease): case report with serial radiographs, computed tomographic scans, and bone scans. Spine (Phila Pa 1976) 1993;18:1236-1241.

17. Nicholas JJ, Benedek TG, Reece GJ. Delayed traumatic vertebral body compression fracture; part I: clinical features. Semin Arthritis Rheum 1981;10:264-270.


18. Benedek TG, Nicholas JJ. Delayed traumatic vertebral body compression fracture; part II: pathologic features. Semin Arthritis Rheum 1981;10:271-277.


19. Matzaroglou C, Georgiou CS, Assimakopoulos K, Giannakenas C, Karageorgos A, Saridis A, Kafchitsas K, Wilke HJ. Kummell’s disease: pathophysiology, diagnosis, treatment and the role of nuclear medicine. Rationale according to our experience. Hell J Nucl Med 2011;14:291-299.

20. Young WF, Brown D, Kendler A, Clements D. Delayed posttraumatic osteonecrosis of a vertebral body (Kummell’s disease). Acta Orthop Belg 2002;68:13-19.

21. Maldague BE, Noel HM, Malghem JJ. The intravertebral vacuum cleft: a sign of ischemic vertebral collapse. Radiology 1978;129:23-29.


22. Sarli M, Perez Manghi FC, Gallo R, Zanchetta JR. The vacuum cleft sign: an uncommon radiological sign. Osteoporos Int 2005;16:1210-1214.


23. Matzaroglou C, Georgiou CS, Panagopoulos A, Assimakopoulos K, Wilke HJ, Habermann B, Panos G, Kafchitsas K. Kummell’s disease: clarifying the mechanisms and patients’ inclusion criteria. Open Orthop J 2014;8:288-297.



24. Chongyan W, Zhang X, Li S, Liu J, Shan Z, Wang J, Chen J, Fan S, Zhao F. Mechanism of formation of intravertebral clefts in osteoporotic vertebral compression fractures: an in vitro biomechanical study. Spine J 2018;18:2297-2301.


25. Kim YC, Kim YH, Ha KY. Pathomechanism of intravertebral clefts in osteoporotic compression fractures of the spine. Spine J 2014;14:659-666.


26. Sugita M, Watanabe N, Mikami Y, Hase H, Kubo T. Classification of vertebral compression fractures in the osteoporotic spine. J Spinal Disord Tech 2005;18:376-381.


27. D’Ippolito G, Schiller PC, Ricordi C, Roos BA, Howard GA. Age-related osteogenic potential of mesenchymal stromal stem cells from human vertebral bone marrow. J Bone Miner Res 1999;14:1115-1122.


28. Antonacci MD, Mody DR, Rutz K, Weilbaecher D, Heggeness MH. A histologic study of fractured human vertebral bodies. J Spinal Disord Tech 2002;15:118-216.


29. Libicher M, Appelt A, Berger I, Baier M, Meeder PJ, Grafe I, Dafonseca K, Noldge G, Kasperk C. The intravertebral vacuum phenomen as specific sign of osteonecrosis in vertebral compression fractures: results from a radiological and histological study. Eur Radiol 2007;17:2248-2252.


31. Nakamae T, Fujimoto Y, Yamada K, Takata H, Shimbo T, Tsuchida Y. Percutaneous vertebroplasty for osteoporotic vertebral compression fracture with intravertebral cleft associated with delayed neurologic deficit. Eur Spine J 2013;22:1624-1632.



32. Cho JH, Shin SI, Lee JH, Yeom JS, Chang BS, Lee CK. Usefulness of prone cross-table lateral radiographs in vertebral compression fractures. Clin Orthop Surg 2013;5:195-201.



33. McKiernan F, Faciszewski T. Intravertebral clefts in osteoporotic vertebral compression fractures. Arthritis Rheum 2003;48:1414-1419.


34. Ahn SE, Ryu KN, Park JS, Jin W, Park SY, Kim SB. Early bone marrow edema pattern of the osteoporotic vertebral compression fracture : can be predictor of vertebral deformity types and prognosis? J Korean Neurosurg Soc 2016;59:137-142.



35. Yu CW, Hsu CY, Shih TT, Chen BB, Fu CJ. Vertebral osteonecrosis: MR imaging findings and related changes on adjacent levels. AJNR Am J Neuroradiol 2007;28:42-47.


36. Tsujio T, Nakamura H, Terai H, Hoshino M, Namikawa T, Matsumura A, Kato M, Suzuki A, Takayama K, Fukushima W, Kondo K, Hirota Y, Takaoka K. Characteristic radiographic or magnetic resonance images of fresh osteoporotic vertebral fractures predicting potential risk for nonunion: a prospective multicenter study. Spine (Phila Pa 1976) 2011;36:1229-1235.


37. Ha KY, Kim YH. Risk factors affecting progressive collapse of acute osteoporotic spinal fractures. Osteoporos Int 2013;24:1207-1213.


38. Chen L, Dong R, Gu Y, Feng Y. Comparison between balloon kyphoplasty and short segmental fixation combined with vertebroplasty in the treatment of Kummell’s disease. Pain Physician 2015;18:373-381.

39. Fabbriciani G, Pirro M, Floridi P, Callarelli L, Manfredelli MR, Scarponi AM, Mannarino E. Osteoanabolic therapy: a nonsurgical option of treatment for Kummell’s disease? Rheumatol Int 2012;32:1371-1374.


40. Gou P, Wang Z, Zhao Z, Wang Y, Jiang Y, Xue Y. Restoration of the intravertebral stability in Kummell’s disease following the treatment of severe postmenopausal osteoporosis by 1-34PTH-a retrospective study. Osteoporos Int 2021;32:1451-1459.


41. Ha KY, Park KS, Kim SI, Kim YH. Does bisphosphonate-based anti-osteoporosis medication affect osteoporotic spinal fracture healing? Osteoporos Int 2016;27:483-488.


42. Zhang B, Chen G, Yang X, Fan T, Chen Z. Percutaneous kyphoplasty versus percutaneous vertebroplasty for neurologically intact osteoporotic Kummell’s disease: a systematic review and meta-analysis. Global Spine J 2021;Feb. 5. 2192568220984129.
43. Dai SQ, Qin RQ, Shi X, Yang HL. Percutaneous vertebroplasty versus kyphoplasty for the treatment of neurologically intact osteoporotic Kummell’s disease. BMC Surg 2021;21:65.


44. Kim WJ, Ma SB, Shin HM, Song DG, Lee JW, Chang SH, Park KY, Choy WS, Oh TH. Correlation of sagittal imbalance and recollapse after percutaneous vertebroplasty for thoracolumbar osteoporotic vertebral compression fracture: a multivariate study of risk factors. Asian Spine J 2021;Aug. 20. [Epub]. https://doi.org/10.31616/asj.2021.0062

45. Nakamae T, Yamada K, Tsuchida Y, Osti OL, Adachi N, Fujimoto Y. Risk factors for cement loosening after vertebroplasty for osteoporotic vertebral fracture with intravertebral cleft: a retrospective analysis. Asian Spine J 2018;12:935-942.



46. Han S, Jang IT. Analysis of adjacent fractures after two-level percutaneous vertebroplasty: is the intervening vertebral body prone to re-fracture? Asian Spine J 2018;12:524-532.



47. Elnoamany HA. Influence of vertebral bone marrow edema on outcome in non-acute osteoporotic patients treated with percutaneous vertebroplasty. Asian Spine J 2016;10:436-442.



Peer Reviewers’ Commentary
이 논문은 골다공증 척추 압박 골절 이후 발생되는 쿰멜씨병의 임상 양상 및 역학, 다양한 병태 생리, 특징적인 영상학적 소견, 임상 양상에 따른 여러 치료 방법 등에 대한 최신 문헌을 정리한 논문이다. 질환의 진행에 따른 다양한 분류 체계를 소개하고 있으며 단계별로 나타나는 임상 양상을 잘 기술하고 있다. 척추체내 진공 균열을 확인하기 위한 검사 방법을 단순히 소개하는데 지나지 않고 진단에 도움이 되는 촬영 자세, 치료에 중요한 검사 소견 등을 함께 제시하며 이해하기 쉽게 설명하고 있다. 또한 골형성 촉진제의 사용이 쿰멜씨병의 치료에 도움이 됨을 제시해 주고 있다. 이 논문은 쿰멜씨병의 임상 양상에 따른 다양한 치료 방법 및 각각의 적응증을 제시하고 있어 치료 방법의 선택에 좋은 지침이 될 것으로 판단된다.
[정리: 편집위원회]
-
METRICS

-
- 1 Crossref
- Scopus
- 6,937 View
- 187 Download
-
Related articles in
J Korean Med Assoc -
Evidence-based treatment of osteoporotic vertebral compression fracture2021 March;64(3)
Minimally Invasive Treatment of Painful Osteoporotic Vertebral Fractures2009 April;52(4)






