박출률 감소 심부전의 치료
Treatment of heart failure with reduced ejection fraction
Article information
Trans Abstract
Background
Heart failure with reduced ejection fraction (HFrEF) is a syndrome consisting of typical symptoms and/or signs of heart failure (HF) due to left ventricular systolic dysfunction (ejection fraction ≤40%) caused by various underlying cardiac diseases. We report conventional and recently established pharmacologic and nonpharmacologic treatments of HFrEF in this review article.
Current Concepts
So far, various pharmacologic treatments have been proven beneficial in reducing HF-associated hospitalization or cardiac death. The mainstay of the treatments is renin-angiotensin-aldosterone system inhibitors, which are sympathetic nervous system blockers on top of the diuretics to relieve symptoms of systemic or pulmonary congestion. Recently, new treatment targets for natriuretic peptide and sodium-glucose cotransporter have emerged in HFrEF, allowing the use of these novel drugs in addition to the optimal conventional medications. Device therapies, such as implantable cardioverter-defibrillator and cardiac resynchronization therapy, can improve the outcome in a special population. Heart transplantation is the final treatment for patients with advanced HF. However, due to the limitation of the donor pool, mechanical circulatory support is necessary.
Discussion and Conclusion
Current guidelines recommend using the four pillars of medications in HFrEF, including angiotensin-converting enzyme inhibitors (angiotensin-neprilysin inhibitors or angiotensin receptor blockers), beta-blockers, mineralocorticoid receptor antagonists, and sodium-glucose cotransporter inhibitors. Appropriate device therapy, mechanical circulatory support, and heart transplantation can enhance survival in advanced HF patients. Balanced treatment, including conventional and newer therapies, is necessary.
서론
심부전은 다양한 원인으로 인하여 심장의 수축기능 또는 이완기능의 장애와 함께 전형적인 증상과 징후가 나타나는 질환이다[1-4]. 심부전의 여러 분류 방법이 있으나 좌심실의 박출률(ejection fraction)에 따른 분류를 가장 많이 활용한다. 박출률 감소 심부전(heart failure with reduced ejection fraction, HFrEF)은 박출률 ≤40%인 경우이며, 박출률 경한 감소 심부전(heart failure with mildly reduced ejection fraction)은 40%< 박출률 <50%, 박출률 보존 심부전(heart failure with preserved ejection fraction)은 박출률 ≥50%인 심부전을 지칭한다[4-6]. HFrEF의 상태 및 동반 질환에 따라 적절한 약물적, 비약물적 치료를 통해서 환자의 증상을 완화하고, 삶의 질을 개선시키며, 임상 예후의 호전 또한 기대할 수 있다. 최근 다양한 치료방법의 발전에 따른 HFrEF의 최신지견을 정리하고 이에 대한 고찰을 하고자 한다.
박출률 감소 심부전의 정의와 진단
심부전은 심장의 구조적 또는 기능적 이상에 따른 심부전의 전형적인 증상과 징후를 보이면서 나트륨배설펩타이드(natriuretic peptide)의 증가 소견 또는 폐와 전신 울혈의 객관적 증거를 보일 때 진단하며, 수축기능 장애(박출률 ≤40%)를 동반하는 경우 박출률 감소 심부전으로 정의한다(Figure 1) [1]. 심부전이 의심되는 환자의 진단에 있어서는 심전도, 나트륨배설펩타이드를 포함한 혈액학적 검사, 심초음파, 흉부 X선을 시행하는 것이 중요하다. 심전도 소견이 정상일 경우에는 심부전의 가능성이 낮음을 시사하며, 주된 심전도 이상 소견으로는 심방세동, Q파, 좌심실 비대, 넓은 QRS파 등이 있다. 바이오마커인 나트륨배설펩타이드 중에서는 B형-type 나트륨배설펩타이드(B-type natriuretic peptide, BNP)와 N-terminal proBNP를 주로 활용하는데 BNP 35 pg/mL 미만 또는 N-terminal proBNP 125 pg/mL 미만이라면 심부전이 아닐 가능성이 많다. 추가적으로 심부전의 동반 질환 파악 및 다른 진단과의 감별을 위해서 전해질, 크레아티닌(creatinine), 혈구수치, 간수치, 신장기능, 그리고 갑상선기능 평가를 시행할 수 있다. 심초음파는 심장기능 평가를 위한 가장 중요한 검사로 좌심실 박출률 측정을 통해서 심부전의 분류가 가능하며, 심장의 크기와 벽 두께 측정, 국소 벽운동 장애에 대한 평가, 우심실기능, 폐고 혈압 여부, 판막기능 및 이완기능 평가가 가능하다. 흉부 X선에서는 호흡곤란과 관련하여 폐질환에 대한 감별을 할 수 있으며, 추가적으로 폐부종이나 심비대와 같은 심부전의 추가적인 소견을 확인할 수 있다[1,4,6,7].
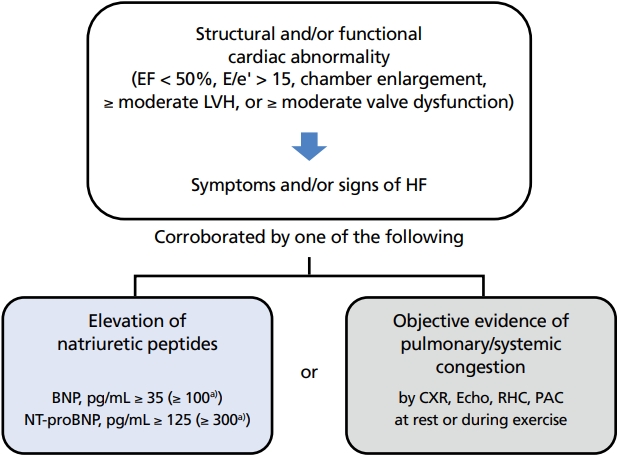
New universal definition of heart failure. EF, ejection fraction; LVH, left ventricular hypertrophy, HF, hypertrophy; BNP, B-type natriuretic peptide; NT-proBNP, N-terminal pro B-type natriuretic peptide; CXR, chest X-ray; RHC, right heart catheterization; PAC, pulmonary artery catheter. a)For hospitalized patients. Illustrated by the author.
박출률 감소 심부전의 약물치료
약물치료는 박출률 감소 심부전에서 가장 근간이 되는 치료이므로, 기구치료나 시술 또는 수술적 치료를 고려하기 전에 반드시 최적의 약물치료가 이루어질 수 있도록 노력해야 한다. 박출률 감소 심부전의 치료에 있어 사망률의 감소, 심부전 악화로 인한 재입원의 방지, 임상 상황과 신체기능 및 삶의 질 호전의 세 가지 목표를 달성하는 데 초점을 맞추고 있다[2,4,7,8].
약물치료의 근간은 안지오텐신전환효소억제제(angiotensin converting enzyme inhibitor) 또는 안지오텐신수용체-네프릴리신억제제(angiotensin receptor-neprilysin inhibitor), 베타차단제(beta blocker), 염류코티코이드수용체대항제(mineralocorticoid receptor antagonist)를 통하여 레닌-안지오텐신-알도스테론계(renin-angiotensinaldosterone system) 및 교감신경계를 조절하는 것이며, 박출률 감소 심부전에서 사망률을 줄이거나 심부전으로 인한 입원을 줄이고, 임상 증상을 호전시킬 수 있음을 보여주었다[4,5,8]. 안지오텐신전환효소억제제는 박출률 감소 심부전의 사망률과 이환율을 줄이고, 증상을 개선시킬 수 있는 가장 기본적인 약제이다[9-12]. 금기사항이나 불내성이 없는 모든 박출률 감소 심부전 환자에서 추천되며, 가능한 최고 용량까지 증량을 해야 한다. 베타차단제는 안지오텐신전환효소억제제와 이뇨제를 사용 중인 박출률 감소 심부전 환자에서 사망률과 이환율을 감소시킬 수 있으므로 진단받은 이후 안지오텐신전환효소억제제와 함께 가능한 빨리 사용하는 것이 권고된다[13-19]. 아직까지 안지오텐신전환효소억제제와 베타차단제 중에 어떤 약제를 먼저 사용해야 하는지에 대한 지침은 정해져 있지 않으므로, 임상 상황에 따라 선택해야 하지만 베타차단제의 경우에는 울혈이 해소된 이후 임상적으로 안정된 상태에서 사용해야 하고, 낮은 용량부터 시작하여 가능한 최고 용량까지 증량하도록 한다. 염류코티코이드수용체길대항제 는 박출률 감소 심부전에서 안지오텐신전환효소억제제와 베타차단제에 추가해서 사용할 경우 사망률을 줄이고, 심부전으로 인한 재입원을 감소시킬 수 있으며, 증상 또한 개선시킬 수 있다[20,21]. 에플레레논(eplerenone)은 스피로놀락톤(spironolactone)에 비해 보다 선별적으로 작용하므로 여성형 유방의 빈도가 더 낮다. 고칼륨혈증을 유발할 수 있으므로 신기능이 불량하거나 혈청 칼륨의 수치가 5.0 mmol/L 이상일 때에는 사용에 주의를 요한다. 안지오텐신수용체-네프릴리신 차단제(사쿠비트릴-발살탄, sacubitril-valsartan)는 PARADIGMHF (Prospective Comparison of Angiotensin II Receptor Blocker Neprilysin Inhibitor With Angiotensin-Converting Enzyme Inhibitor to Determine Impact on Global Mortality and Morbidity in Heart Failure) 연구를 통해 보행이 가능한 박출률 감소 심부전 환자에서 에날라프릴(enalapril)과 비교하여 심부전의 악화로 인한 입원과 심혈관계 사망, 그리고 전체 사망을 감소시켰으며, 삶의 질 또한 개선시키는 효과를 보여주었다[22]. 이후 진행된 PINONEER-HF (Comparison of Sacubitril–Valsartan versus Enalapril on Effect on NT-proBNP in Patients Stabilized from an Acute Heart Failure Episode) 연구에서 입원치료 후 안정된 박출률 감소 심부전에서 안지오텐신-네프릴리신 차단제를 사용하는 것 또한 임상적인 효과를 보였고, 안지오텐신전환효소억제제를 기존에 사용하지 않았던 환자에서도 이득이 있음을 증명하였다[23]. 안지오텐신수 용체대항제는 안지오텐신전환효소억제제 또는 안지오텐신 수용체-네프릴리신 차단제 사용 시 부작용이 있을 경우에 사용할 수 있다. 최근에는 sodium-glucose cotransporter 2 억제제(SGLT2 inhibitor, SGLT2i)인 다파글리플로진(dapagliflozin)과 엠파글리플로진(empagliflozin)이 당뇨병의 유무와 상관없이 심혈관계 사망과 심부전 악화를 감소시키는 효과를 입증하여 기존에 안지오텐신전환효소억제제/안지오텐신수용체-네프릴리신 차단제, 베타차단제, 염류코티코이드대항제를 사용하고 있는 박출률 감소 심부전에서 추가로 사용할 것을 권고하고 있다[24-26]. VICTORIA (Vericiguat Global Study in Subjects With Heart Failure With Reduced Ejection Fraction) 연구에서 경구 soluble guanylate cyclase stimulator인 베리시구아트(vericiguat)가 플래시보(placebo) 대비 일차결과변수인 심혈관계 원인으로 인한 사망과 심부전으로 인한 입원을 효과적으로 감소시켰으므로, 박출률 감소 심부전에서 기존 약제에 추가하여 사용할 수 있는 약제로 새롭게 대두되고 있다[27]. 철결핍(ferritin 수치 <100 μg/L, 또는 100-299 μg/L이면서 transferrin saturation <20%)을 동반한 박출률 감소 심부전에서 ferric carboxymaltose를 사용하는 것은 조혈 및 비조혈 조직에서 세포 에너지 대사를 향상시킬 수 있으며, 여러 연구를 통해 심혈관계 입원과 사망을 감소시키는 것을 입증하였다[28-30].
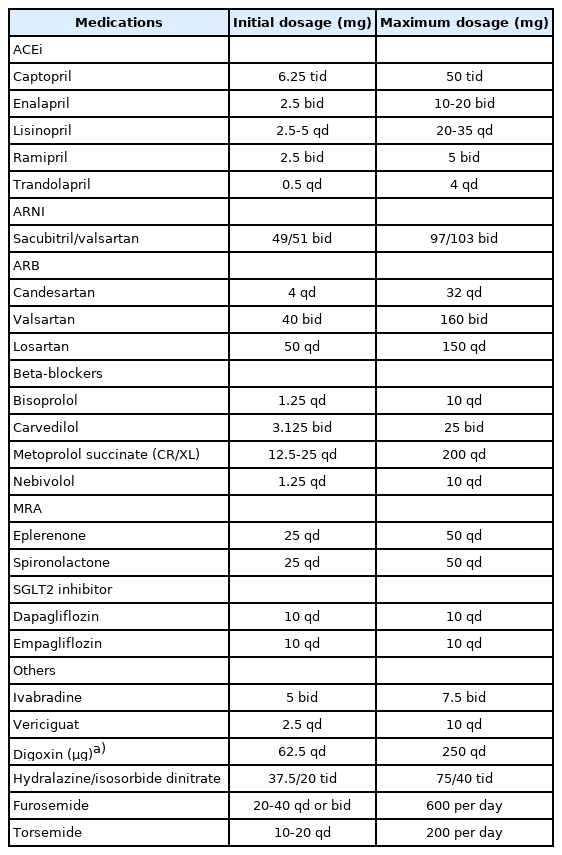
박출률 감소 심부전의 최신 약물치료는 네 가지의 핵심 약물인 안지오텐신전환효소억제제/안지오텐신수용체-네프릴리신억제제(사용이 어려울 경우 안지오텐신수용체 차단제), 베타차단제, 염류코티코이드대항제, SGLT2i를 가능한 빨리, 동시에 적용하고 이뇨제를 적절하게 사용하여 임상 예후를 호전시키고, 환자의 증상을 안정화하며 삶의 질을 호전시키는 것으로, 가능한 최고 용량을 사용하기 위해서 혈압과 증상에 따라서 약제를 증량해야 한다(Table 1) [4].
박출률 감소 심부전의 비약물적 치료
1. 기구치료
심부전 환자에서는 치명적인 부정맥으로 인하여 갑작스러운 사망의 빈도가 상승한다. 기저 심장질환에 대한 치료는 급사의 위험을 줄여줄 수는 있지만 부정맥이 발생한 이후에는 도움이 되지 않으므로 삽입형 제세동기(implantable cardioverter defibrillator, ICD) 치료가 필요하다. 박출률 감소 심부전에서 3개월 이상의 충분한 약물치료에도 좌심실 박출률이 35% 이상으로 호전되지 않는 경우에 ICD의 삽입을 권고한다[31-34]. 하지만 중증의 심부전에서는 ICD 삽입으로 인한 급사 위험의 감소가 심부전 악화에 따른 사망으로 인해서 상쇄되기 때문에 약물치료에 반응이 없는 New York Heart Association class IV의 환자에서 향후 심장 대체요법인 좌심실 보조장치나 심장이식을 계획하고 있는 상황이 아니라면 ICD 삽입을 권고하지 않는다[4]. 향후 안지오텐신수용체-네프릴리신 차단제 및 SGLT2i와 같은 새로운 약제의 사용이 부작용의 빈도를 효과적으로 감소시켜 ICD 치료의 필요성을 줄일 수 있을지에 대해서는 추가 연구가 필요하다.
적절한 환자에서 시행될 경우 심장 재동기화 치료(cardiac resynchronization therapy)는 사망률과 이환율을 감소시킬 수 있을 뿐 아니라, 심장기능을 호전시키고, 삶의 질 개선 효과 또한 기대할 수 있다[35-40]. 박출률 35% 이하의 환자에서 최적의 약물치료를 시행함에도 불구하고, 동성 리듬을 보이면서 QRS 간격이 150 ms 이상이고, 좌각차단(left bundle branch block)의 형태를 보이는 경우에 심장 재동기화 치료 시행의 이득이 가장 명확하다.
최근 경피적승모판막 성형술(transcatheter edge-to-edge repair, TEER)은 중증의 이차성 승모판막 역류증을 동반한 박출률 감소 심부전 환자에서 최적의 약물치료에도 불구하고 증상이 지속된다면 고려할 수 있다 [41]. 대조군 대비하여 심부전으로 인한 입원 및 전체 사망을 감소시켰던 COAPT (Cardiovascular Outcomes Assessment of the MitraClip Percutaneous Therapy for Heart Failure Patients With Functional Mitral Regurgitation) 연구에서의 등록 조건을 반영하여 특정 조건을 만족하는 경우(20%≤EF≤50%, 좌심실 추축기말 직경≤70 mm, 폐동맥 수축기압≤70 mmHg) 시행할 것을 권고한다[42].
2. 심장 대체요법
진행성 심부전은 중증의 지속되는 심부전 증상(진행성 New York Heart Association III 또는 IV)과 함께 좌심실 박출률 ≤30%, 단독의 우심실 기능부전, 수술이 불가능한 심각한 판막질환 또는 선천성 심장질환, 중증의 이완기능 장애 또는 구조적 장애를 동반한 상태에서 지속적으로 높은 나트륨배설펩타이드 수치를 보이며, 정주 이뇨제나 강심제, 혈관 수축제의 사용을 요하는 울혈 증상이 1년간 1회 이상 반복될 때로 정의할 수 있다[4]. 운동능력 역시 감소하는 상태로 6분 보행검사에서 300 m 미만의 보행이 가능하며, 심폐기능 운동부하검사에서 최대 산소 섭취량이 12 mL/kg/min 미만 또는 예측치의 50% 미만으로 감소되어 있다.
회복이 불가능한 진행성 심부전에서는 심장 대체요법을 고려할 수 있으며, 좌심실 보조장치와 심장이식 치료가 대표적이다. 좌심실 보조장치는 좌심실 첨부에 모터를 삽입하고 대동맥으로 혈류가 바로 분출될 수 있도록 연결하는 수술을 통해서 심박출량을 증가시킨다. MOMENTUM 3 (Multicenter Study of MagLev Technology in Patients Undergoing Mechanical Circulatory Support Therapy with HeartMate 3) 연구에서 HeartMate III 장치 삽입 이후 2년 생존율이 1년에 80%, 2년에 70% 정도로 보고된다[43]. HeartMate III 장치는 완전 자기부상 원심펌프로 이전 장치들에 비해서 펌프에 발생하는 혈전 및 관련 합병증을 유의하게 감소시키는 결과를 보여주었다[44].
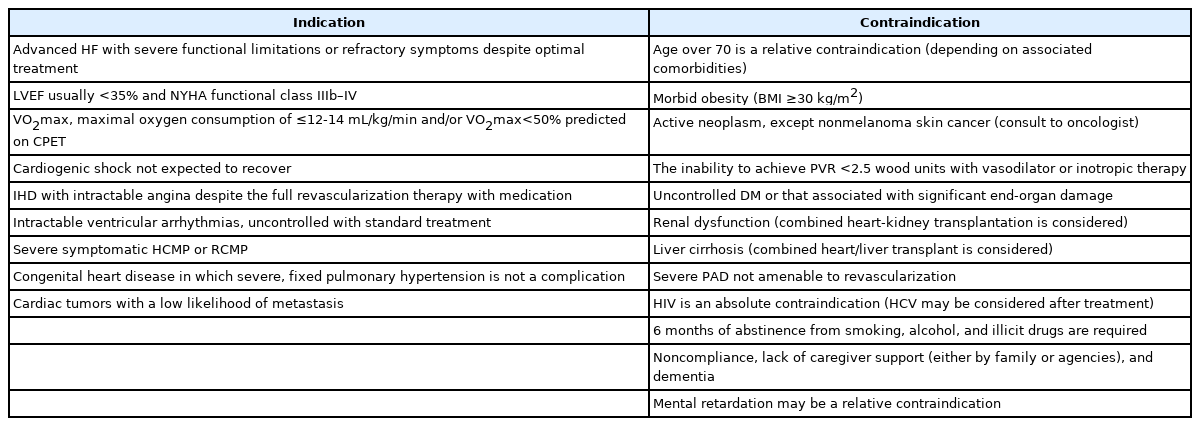
심장이식은 진행성 심부전에서 가장 근본적인 치료방법이며, 심장 이외에 다른 장기들의 기능이 잘 유지될 때 시행할 수 있다(Table 2) [45]. 그러나 공여자의 제한과 잠재적인 다른 수혜자의 기회를 고려할 때 신중하게 대상자를 선정하고, 치료 과정에서 다학제 진료를 통한 최선의 치료가 무엇보다 중요하다[46]. 국내에서도 좌심실 보조장치의 적용을 통해 심장이식의 한계점을 보완하고 진행성 심부전 환자의 생존율을 높이는 데 기여할 수 있을 것으로 기대된다.
3. 심장 재활
운동을 통하여 신체를 단련하는 것이 운동능력을 증가시키고, 건강과 관련된 삶의 질을 개선시킬 수 있다는 것은 다양한 임상연구를 통해서 잘 알려져 있다. 메타연구에서 심장 재활이 박출률 감소 심부전에서 전체 사망과 심부전으로 인한 입원을 감소시킬 수 있음을 보여주었지만, 사망에 대한 직접적인 효과는 아직 명확하지 않다[47-50]. 심부전으로 인한 재입원은 심장 재활의 순응도가 높을수록 더 낮으므로 꾸준한 운동이 더욱 도움이 된다는 것을 알 수 있다. 최대 산소 섭취량을 호전시키기 위해서는 고강도 인터벌 운동이 효과적이지만 고령 환자나 다양한 합병증을 동반하여 신체기능이 취약한 경우에는 주의를 요하며, 운동 시에는 전문가의 감독 하에 시행하는 것이 안전하다.
결론
박출률 감소 심부전은 다양한 원인과 함께 복합적인 기전으로 심장기능이 감소하여 여러 장기에 영향을 주게 되는 임상적 증후군이므로, 치료에 있어서도 총체적인 접근법이 필요하다. 세심한 병력 청취와 신체검진 및 적절한 검사를 통해서 정확한 심장 상태를 평가하고 동반 질환에 대한 점검을 해야 하며, 이를 기반으로 치료 전략을 잘 수립해야 한다. 약물치료로는 네 가지 핵심 약물인 안지오텐신전환효소억제제 또는 안지오텐신수용체-네프릴리신억제제(사용이 어려울 경우 안지오텐신수용체 차단제), 베타차단제, 염류코티코이드 길대항제, SGLT2i을 가능한 최대 용량으로 사용해야 하며, 이뇨제는 증상에 따라 용량을 조절한다. 심부전에 대한 교육과 심장 재활 역시 모든 환자의 치료 과정에 포함되는 것을 권고하며, 그 외의 약물 및 비약물적 치료는 상황에 따라 개별화하여 적용해야 한다(Figure 2). 다양한 치료법의 개발과 체계적 관리방법의 정착으로 박출률 감소 심부전의 예후가 향후 더욱 개선될 수 있을 것으로 기대한다.

Up-to-dated pharmacologic and non-pharmacologic treatment strategy in heart failure with reduced ejection fraction – unless contraindicated, four pillars of essential drugs need to be initiated and up-titrated to a maximal tolerable dose. HFrEF, heart failure with reduced ejection fraction; ACEi, angiotensin converting enzyme inhibitor; ARB, angiotensin receptor blocker; ARNI, angiotensin receptor-neprilysin inhibitor; BB, beta blocker; MRA, mineralocorticoid receptor antagonist; SGLT2i, sodium-glucose cotransporter 2 inhibitor; ISDN, isosorbide dinitrate; ICD, implantable cardioverter defibrillator; CRT, cardiac resynchronization therapy; VAD, ventricular assist device; DT, destination therapy; BTT, bridge to transplantation; TEER, transcatheter edge-to-edge repair. Illustrated by the author.
Notes
Conflict of Interest
No potential conflict of interest relevant to this article was reported.
References
Peer Reviewers’ Commentary
심부전은 증상, 징후 및 여러 객관적 검사들을 종합해서 진단하는 비교적 복잡한 질환이며, 치료에서도 여러 가지 고려할 부분들이 많아서 치료지침이 매우 중요하다. 이 논문에서는 박출률 감소 심부전 치료의 최신 지견을 정리하여 설명하고 있다. 박출률 감소 심부전의 진단, 약물치료, 기구 치료, 대체요법, 심장 재활에 이르기까지 광범위한 내용을 핵심적인 내용을 중심으로 요약하고 있다. 특히 심부전 치료에 새롭게 도입되어 4종류의 핵심 약물 중 하나로 정립된 sodium-glucose co-transporter 2 억제제와 최근 활발히 사용되고 있는 기구 요법에 관해 상세히 설명해 주고 있다. 이 논문은 박출률 감소 심부전을 다루는 임상 현장에 좋은 치료지침을 제공할 수 있을 것으로 판단된다.
[정리: 편집위원회]