 |
 |
- Search
| J Korean Med Assoc > Volume 65(8); 2022 > Article |
|
Abstract
Background: The antimicrobial stewardship program (ASP) is a coordinated intervention designed to improve and measure the appropriate antibiotics use by selecting an optimal antibiotic drug regimen, including dosing, therapy duration, and administration route. The implementation of ASPs decreases the consumption, cost, and adverse effects of antibiotic use. Additionally, it improves the clinical outcomes, and decreases Clostridium difficile infection and antimicrobial resistance.
Current Concepts: To overcome the antimicrobial resistance and implement ASPs worldwide, various efforts are underway, such as enacting ASP guidelines, developing core elements for ASP implementation, introducing ASPs to the healthcare accreditation system, and providing healthcare facilities with adequate incentives to implement ASPs. In Korea, ASP guidelines were published in September 2021, and core elements for ASP implementation are being developed at the time of writing. However, there is a shortage of personnel required for the ASP team, including healthcare workforce and infectious disease specialists for leading the team Moreover, financial support for ASP implementation in the National Health Insurance Service is not provided yet. The awareness of hospital leadership and clinicians prescribing antibiotics for ASP implementation is still low. The reimbursement system establishment and workforce for ASPs are prerequisite for the implementation of ASPs.
Discussion and Conclusion: At the national level, it is necessary to provide financial support for ASPs in healthcare facilities, nurture the healthcare workforce in performing ASPs, and advocate ASP education and publicity.
Current Concepts: To overcome the antimicrobial resistance and implement ASPs worldwide, various efforts are underway, such as enacting ASP guidelines, developing core elements for ASP implementation, introducing ASPs to the healthcare accreditation system, and providing healthcare facilities with adequate incentives to implement ASPs. In Korea, ASP guidelines were published in September 2021, and core elements for ASP implementation are being developed at the time of writing. However, there is a shortage of personnel required for the ASP team, including healthcare workforce and infectious disease specialists for leading the team Moreover, financial support for ASP implementation in the National Health Insurance Service is not provided yet. The awareness of hospital leadership and clinicians prescribing antibiotics for ASP implementation is still low. The reimbursement system establishment and workforce for ASPs are prerequisite for the implementation of ASPs.
Discussion and Conclusion: At the national level, it is necessary to provide financial support for ASPs in healthcare facilities, nurture the healthcare workforce in performing ASPs, and advocate ASP education and publicity.
항생제 사용관리 프로그램(antimicrobial stewardship program, ASP)은 항생제의 종류, 용량, 투여기간, 투여 경로를 포함하여 가장 적절한 항생제의 사용을 촉진하기 위해, 항생제 사용의 적정성을 측정하고, 개선하도록 고안된 통합적 중재활동이다[1]. ASP의 목적은 환자의 치료결과를 개선하고, 자원활용을 최적화하며, 항생제 내성을 감소시키는 것이다[2]. 항생제 내성은 전 세계적으로 심각한 문제 중 하나이며, 의료기관에서 ASPs를 활성화하여 항생제 사용을 최적화하는 것은 항생제 내성을 해결하기 위한 핵심전략 중 하나이다[3]. 세계보건기구를 포함하여, 유럽연합, 미국, 영국, 호주 등 많은 국가들이 항생제 내성 극복을 위한 전략으로 ASPs를 활성화하기 위해 노력하고 있다[3]. 우리나라도 항생제 내성을 극복하기 위한 전략으로 2016년에 제1차 국가 항생제 내성 관리대책을 수립하고 5년간 수행하였으며, 2021년 11월에는 제2차 국가 항생제 내성 관리대책을 수립하여 추진 중이다[4,5]. 제2차 국가 항생제 내성 관리대책의 첫 번째 주요 분야는 항생제 적정 사용이며, 의료기관에 ASP 도입 및 추진이 중점 분야에 포함되어 있다[5]. 2021년 9월에 대한항균요법학회, 대한감염학회 및 한국병원약사회가 협력하여 ‘한국에서의 ASP 적용 지침’을 출판하였으며, 의료기관에 이 지침을 성공적으로 도입하기 위한 핵심요소들을 개발하고 있다[3,6]. 또한 대한 항균요법학회와 대한감염학회는 질병관리청의 지원을 받아 항생제 사용관리에 대한 유트브 공개 교육자료를 개발하였으며, 일반인용, 의료인 기본, 의료인 심화, 한국형 ASP 지침 요약으로 구성하여 학회 홈페이지(https://www.ksat.or.kr/board/list.html?code=ss_basic)에서 제공하고 있다[7].
이 논문에서는 ASP의 개념과 필요성, 방법과 효과, 실행을 위한 핵심요소에 대해 고찰하고, 우리나라에서 ASPs가 효과적으로 실행되기 위한 전제조건을 살펴보고자 한다.
항생제 사용관리(antimicrobial stewardship)라는 용어는 1996년 McGowan과 Gerding [8]에 의해 미국에서 처음 사용되었다. McGowan과 Gerding에 따르면, 이 용어는 선한 steward(청지기)의 복음에 대한 주일 강론과 교회에 정기적으로 봉사하는 선한 청지기 되기 또는 청지기 직분이라는 용어의 사용에서 영감을 받았으며, 그들은 항생제를 사용할 때, 불필요한 사용을 피하여 적절하게 사용하고, 재생 불가능한 귀중한 자원으로 항생제를 고려해야 한다는 점을 강조하고 싶었다고 한다[9]. 이후에 미국과 유럽의 항생제 내성 예방에 대한 지침에 항생제 사용관리라는 용어가 포함되면서 널리 사용되게 되었다. 사전적 의미로는 (1) 청지기의 직분, 직무 및 의무, (2) 어떤 일을 지휘, 감독, 관리, 특히 신중하고 책임 있는 관리를 뜻한다. 항생제 사용관리는 (1) 항생제의 사용 통제와 용량, 기간, 투여 경로를 포함하여 가장 적절하게 선택하는 치료, (2) 부작용과 항생제 내성과 같은 의도하지 않은 결과를 최소화하면서 환자의 치료결과를 개선하는 목적, (3) 적절한 항생제 사용을 측정하고 개선 및 촉진하는 일련의 통합적 중재, (4) 정책, 지침, 감시, 교육, 감사와 같은 다면적 접근, (5) 항생제 내성 출현을 예방하는 핵심 구성요소, (6) 불필요한 사용을 방지하고, 표적화되고 제한된 치료를 제공하는 현명한 항생제 사용으로, 현재의 효과와 미래세대가 사용할 수 있는 기회를 극대화하는 책임 있는 사용 등의 의미로 여러 문헌들에서 사용되었다[9]. 이러한 항생제 사용관리를 실현하는 여러가지 통합적 중재활동을 항생제 사용관리 프로그램이라고 한다.
항생제 사용의 증가와 부적절한 항생제 사용은 항생제 내성의 증가로 이어지고, 증가된 항생제 내성은 다시 광범위 항생제의 사용과 부적절한 항생제 사용을 증가시키는 악순환을 반복한다. 이러한 악순환의 고리를 끊고, 적정한 항생제 사용을 유도하여 환자의 임상적 예후를 호전시키고, 비용 상승, 항생제 내성균 출현, Clostridioides difficile에 의한 장염 등과 같은 항생제 사용에 의한 부수적인 피해(collateral damage)를 최소화하기 위해서 항생제 사용관리 프로그램을 실행할 필요가 있다.
2019년에 400 병상 미만의 병원(6개 요양병원, 3개의 급성기 병원, 1개의 정형외과 병원)에 입원한 환자들을 대상으로 항생제 처방의 적정성을 평가하였을 때, 병원 간 항생제 처방 형태가 다양하였으며, 총 30.6%가 부적절하게 항생제를 사용하고 있는 것으로 평가되었다[10]. 그리고, 2018년에 국내 20개 의료기관의 입원 및 외래 환자를 대상으로, 투여 목적에 따른 항생제 처방의 적정성을 평가하였을 때, 수술의 예방적 항생제는 54.4%가 부적절하였고, 시술이나 장기 이식, 면역 억제제 투여에 대한 예방적 항생제는 29.5%가 부적절하였으며, 치료적 항생제는 20.5%가 부적절하였다[11]. 부적절한 항생제 처방은 환자의 치료결과에 악영향을 끼치고, 항생제 내성 문제를 일으킬 수 있어 개선되어야 하고, 항생제 처방 형태를 개선하기 위해서는 ASPs가 활성화되어야 할 필요가 있다.
항생제 처방의 적절성을 효과적으로 높일 수 있는 근거기반의 핵심 중재 전략은 항생제 제한과 사전 승인(restriction and preauthorization; front-end program)과 전향적 감사와 피드백(prospective audit with feedback: back-end program)이다[6]. 핵심 중재 전략 외에 부가적인 전략으로 악수 사용관리, 교육, 임상 진료지침, 항생제 투약 기간 최적화, 증후군 기반 항생제 관리, 주사 항생제의 경구 항생제로의 전환, 항생제의 치료적 약물농도 모니터링 등이 있다 (Table 1) [6].
항생제 제한과 사전 승인은 특정 항생제에 대하여 항생제를 처방하는 의료진이 항생제를 처방하기 전에 항생제 사용 관리 전담팀의 승인을 받아 처방할 수 있게 하는 전략이다. 환자에게 항생제 투약의 필요성을 처음부터 평가하여 적정한 항생제를 처방할 수 있도록 유도하기 때문에, 올바른 경험적 항생제가 투여될 확률을 높여서, 대상 항생제의 사용량과 투약 기간을 감소시키고, Clostridium difficile infection (CDI)을 줄이는 효과가 있다[12,13]. 하지만 이 전략이 실시간으로 24시간 동안 수행되려면 많은 인력이 필요하고, 항생제를 처방하는 의사와 제한하는 ASP팀 사이의 갈등이 발생할 수 있고, 사전 승인 대상이 아닌 항생제의 사용량의 늘어나는 풍선 효과를 유발할 수 있으며, 관리자의 숙련도에 따라 효과의 차이를 보이는 단점이 있다. 이러한 단점을 극복하기 위해, 항생제를 처방하는 의사의 불편함을 줄이고, 미생물 검사결과가 나오고 임상적인 평가가 가능한 시점인, 처방 후 3-5일에 제한을 시작하는 형태로 운영되기도 한다[14]. 전향적 감사와 피드백은 항생제가 처방되고 일정시간이 지난 후 관리자가 처방된 항생제의 적정성을 평가하여 처방한 의료진과 소통하는 전략이며, 항생제 사용의 적정성 향상, 유지 기간의 단축, 재입원율 감소, 항생제 내성과 CDI를 감소시키는 효과가 있었다[6]. 전향적 감사와 피드백의 한 형태로, 의사와 약사로 구성된 ASP 전담팀이 항생제를 처방하는 의료진과 함께 회진하면서, 항생제 처방에 대한 개별적인 피드백을 즉시 제공하는 악수 사용관리(Handshake stewardship)가 있다. 교육은 ASP의 핵심적인 요소로 항생제 처방 행위에 직접적인 영향을 줄 수 있으나, 수동적인 형태의 교육은 중재 기간 중에 나타나는 일시적인 효과를 보이 며, 능동적 중재를 함께 시행하지 않으면 그 효과가 크지 않은 것으로 알려져 있다[15,16]. 요로감염이나 지역사회획득 폐렴과 같은 특정 감염 질환에 대하여 항생제 사용에 대한 적정성을 평가하고 관리하는 방법이 있으며, 패혈증에도 항생제 사용관리를 적용할 수 있다[17,18].
ASPs를 의료기관에 성공적으로 도입하고 정착시키기 위해서는 ASPs를 실행할 구조와 절차가 필요하다. 2014년 미국 질병통제센터(Centers for Disease Control and Prevention, CDC)는 의료기관의 항생제 사용에 대한 개선이 시급하다고 판단하였고, 미국 내의 모든 급성기 병원에서 ASPs를 실행할 것을 권고하고, 이를 효과적으로 수행할 수있도록 7가지 핵심요소를 제시하였다[24,25]. 미국 CDC의 7가지 핵심요소는 리더십의 책무(leadership commitment), 책임자 임명(accountability), 담당 약사 임명(pharmacy expertise), 중재의 실행(action), 추적조사(tracking), 보고 (reporting), 교육(education)이다[3]. (1) 리더십의 책무는 의료기관의 경영자들이 의료기관에서 항생제 사용관리를 수행하는 데에 필요한 인적, 재정적, 정보자원 기술의 지원에 대한 내용이고, (2) 책임자 임명은 ASPs를 수행하는 전담팀을 구성하고 이러한 팀의 리더를 임명하는 것이며, (3) 담당 약사 임명은 항생제 사용관리를 전담할 약사를 임명하고 역할을 부여하고, (4) 중재의 실행은 항생제를 적절하게 사용할 다양한 중재 방법을 의료기관 실정에 맞게 활용하며, (5) 추적조사는 항생제 사용과 중재의 효과에 대한 다양한 지표를 지속적으로 감시하고 모니터링 하는 것이고, (6) 보고는 항생제 사용과 중재의 효과의 지표들을 경영자와 의료인을 포함하는 직원이 공유할 수 있도록 하는 것이며, (7) 교육은 ASPs를 경영자, 의료인을 포함하는 직원과 환자들에게 교육하는 것이다. 미국 CDC는 이러한 핵심요소를 병원에 가장 먼저 적용하였고, 이후 규모가 큰 병원뿐만 아니라, 장기 요양 시설, 외래, 소규모 급성기 병원, 자원이 제한된 의료기관을 위한 핵심요소를 각 기관의 수준에 맞게 조정하고 별도로 제시하여, 의료기관 전반에서 ASPs가 실행될 수 있는 기반을 마련하여 추진하고 있다. 미국의 의료기관 인증기관인 The Joint Commission은 의료기관 인증평가에도 이러한 ASP 실행을 위한 핵심요소를 도입하여 활용하고 있다[26].
영국은 Antimicrobial Self-Assessment Toolkit, Antimicrobial Stewardship Toolkit for English Hospitals, TARGET (Treat Antibiotics Responsibly, Guidance, Education, Tools) Toolkits이라는 형태로 미국 CDC의 Core Elements와 유사한 프로그램들을 국가적 차원에서 운영하고 있다[3]. 호주는 국가적인 차원에서 essential elements and strategies for antimicrobial stewardship programs이라는 명칭으로 항생제 사용관리를 실행하는 데 필요한 구조와 거버넌스 및 필수 전략을 제시하였다. 2019년에는 전 세계의 항생제 사용관리 전문가들이 합의하여 항생제 사용관리 프로그램 실행을 위한 필수요소와 체크리스트를 구체적으로 제정하여 발표하였다[27]. 세계보건기구는 소득 수준이 낮거나, 중간 정도 되는 국가의 의료기관에서 ASPs를 실행하기 위한 World Health Organization Practical Toolkit을 발표하였으며, 국가에서 필요한 필수요소와 체크리스트, 의료기관에서 필요한 필수요소와 체크리스트를 구분하여 제시하고 있다[28]. 국가에서 수행해야 할 필수요소는 의료기관에서 ASPs를 진행하는 데 필요한 의료인력 확보, 훈련, 인증 획득을 지원하는 인센티브를 제공하는 것을 포함하고 있다.
대한항균요법학회는 2021년 11월에 질병관리청의 연구비 지원을 받아 대한감염학회, 한국병원약사회와 함께 우리나 라에서 ASPs를 실행할 수 있는 핵심요소를 개발하고 있다. 국제 기구나 다른 나라의 핵심요소를 참고하여 우리나라 상황에 맞게 조정하고, 의료기관에서 ASPs를 활성화할 수 있도록 재정적 지원방안과 의료기관 인증평가의 인증기준을 고려하여, 건강보험심사평가원과 의료기관평가인증원의 자문을 받아서 개발을 추진중이다.
2020년에 전국 150 병상 이상 217개 병원에서 ASPs에 참여하고 있는 의사들을 대상으로 시행한 설문조사에서, 의료 기관의 ASP 활성화의 가장 큰 장애는 ASPs를 수행할 인력의 부족이고, 두 번째는 지침이나 매뉴얼 같은 도구의 부족이며, 세 번째는 ASP 수행에 대한 적절한 보상체계의 부족으로 확인되었다[29]. 이에 따라 ASP 활성화에 가장 필요한 지원은 ASP 수행 인력 확보이고, 두 번째는 ASP에 대한 보상체계 마련이며, 세 번째는 지침이나 매뉴얼 같은 ASPs를 위한 도구의 개발로 조사되었다.
ASPs를 실행하는 데에 필요한 가장 중요한 전제조건은 ASPs를 실행할 전담팀을 구성할 수 있는 전문 인력을 확보하는 것이다. ASPs를 성공적으로 구현하기 위해서는 의사, 약사, 간호사, 미생물 학자 및 감염 예방 전문가, 정보기술 전문가로 구성된 다학제 팀이 필요하고, 병원 경영진과 관련 위원회 구성원들은 이 팀과 협력하고 지원해야 한다(Figure 1) [6]. 그리고 이러한 다학제 ASP팀을 이끌고 ASPs를 수행하는 데에 핵심적인 역할을 할 감염내과나 소아청소년 감염 분과전문의가 필수적이고, 감염 약료 분과 전문 약사나 ASP 교육을 받은 간호사의 역할도 중요하다. 하지만 현재 우리 나라에서 ASPs를 책임지고 운영할 수 있는 감염 분과 전문의와 훈련된 임상 약사 인력은 턱없이 부족하다. 항생제를 투여하고 있는 모든 환자들에게 ASPs를 적용한다고 가정할 때, ASPs를 수행하는 데에 필요한 전문 인력(full-time equivalent, FTE)은 100 병상당 1.2명(사분범위, 1.02-1.38)이었고, 항생제를 사용하는 환자 100명당 필요한 FTE 는 2.28명(사분범위, 1.93-2.62)이었는데 반해, 전국적으로 84개의 500 병상 이상 병원을 대상으로 시행한 조사에서 ASPs를 수행할 FTE가 전혀 없는 기관이 94%로 조사되었다 [30,31]. 2020년 11월 기준으로 우리나라에서는 ASP 프로그램을 운영할 수 있는 내과/소아청소년과 감염 분과 전문의는 350여 명이었고, 감염 약료 분과 전문약사도 86명에 불과 했다[3]. 이를 극복하기 위해서는 ASPs를 운영할 전문가를 양성할 수 있는 제도적인 지원책을 마련하고, 체계적으로 교육하는 과정을 개발하여 운영할 필요가 있다.
의료기관이 ASPs를 도입하여 전담팀이나 위원회 같은 운영체계를 갖추고, 지속적으로 수행해 나가기 위해서는 국민건강보험에 ASP 활동에 대한 수가가 도입되는 등의 방법으로 재정적 지원이 반드시 마련되어야 한다. ASPs의 효과는 개별 의료기관의 수익으로 연결되기 보다는, 국가적인 공익으로 이어지기 때문 에, 재정적인 지원 없이 의료기관 자체적으로 ASPs를 수행하는 비용을 투입 하기에는 무리가 있다. 영국처럼 ASP 적용을 주기적으로 평가하여 그에 따른 인센티브를 제공하거나, 호주나 미국처럼 의료기관 인증기준에 ASP 항목을 구체적으로 제시하여, 의료기관이 ASPs 를 수행하도록 유도하는 방안을 고려할 수 있다. 또한, 의료 기관의 경영진이나 항생제를 처방하는 의료인들의 ASPs에 대한 인식도와 수용성을 높이기 위하여 홍보와 교육을 활성화할 필요도 있다.
ASP는 항생제의 종류, 용량, 투여기간, 투여 경로를 포함하여 가장 적절한 항생제의 사용을 촉진하기 위해, 항생제 사용의 적정성을 측정하고, 개선하도록 고안된 통합적 중재 활동이다. ASP는 항생제를 적정하게 사용하도록 유도하여, 항생제 사용량과 항생제 사용에 따른 비용을 감소시키고, 환자의 임상적 예후를 호전시키며, 항생제의 독성과 알레르기 같은 이상반응, CDI와 항생제 내성을 감소시키는 효과가 있어, 전 세계적으로 ASPs를 활성화하기 위해 다양한 노력을 하고 있다. 우리나라도 ASP 지침을 출판하고, ASP 실행을 위한 핵심요소를 개발하고 있다. 하지만 ASP 실행에 필요한 전문 인력이 매우 부족하고, 재정적 지원이 거의 없으며, 경영진이나 의료인들의 인식도도 낮아 ASPs를 위한 인프라는 척박하다. 이를 개선하기 위해 체계적으로 전문 인력을 양성할 수 있도록 제도적으로 뒷받침하여야 하고, ASPs에 대한 국민건강보험수가를 도입하고, ASPs에 대한 홍보와 교육을 강화해야 하겠다.
Figure 1.
Multidisciplinary team for implementation of antimicrobial stewardship program. Adapted from Yoon YK, et al. Infect Chemother 2021;53:617-659, according to the Creative Commons license [6].
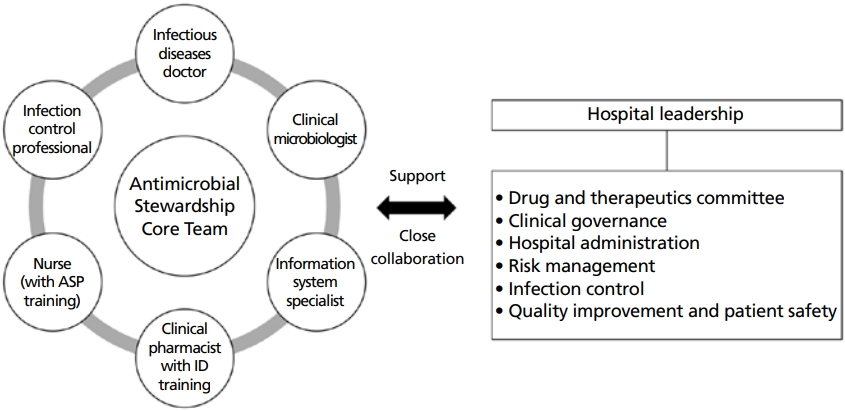
Table 1.
Important strategies for antimicrobial stewardship program
Adapted from Yoon YK, et al. Infect Chemother 2021;53:617-659, according to the Creative Commons license [6].
References
1. Society for Healthcare Epidemiology of America; Infectious Diseases Society of America; Pediatric Infectious Diseases Society. Policy statement on antimicrobial stewardship by the Society for Healthcare Epidemiology of America (SHEA), the Infectious Diseases Society of America (IDSA), and the Pediatric Infectious Diseases Society (PIDS). Infect Control Hosp Epidemiol 2012;33:322-327.


2. Barlam TF, Cosgrove SE, Abbo LM, MacDougall C, Schuetz AN, Septimus EJ, Srinivasan A, Dellit TH, Falck-Ytter YT, Fishman NO, Hamilton CW, Jenkins TC, Lipsett PA, Malani PN, May LS, Moran GJ, Neuhauser MM, Newland JG, Ohl CA, Samore MH, Seo SK, Trivedi KK. Implementing an antibiotic stewardship program: guidelines by the Infectious Diseases Society of America and the Society for healthcare epidemiology of America. Clin Infect Dis 2016;62:e51-e77.




3. Hwang S, Kwon KT. Core elements for successful implementation of antimicrobial stewardship programs. Infect Chemother 2021;53:421-435.




4. Ryu S. The new Korean action plan for containment of antimicrobial resistance. J Glob Antimicrob Resist 2017;8:70-73.


5. Ministry of Health and Welfare. National Action Plan on Antimicrobial Resisatnce [2021-2025] [Internet]. Sejong: Ministry of Health and Welfare. 2021 [cited 2022 Jul 15]. Available from: https://policy.nl.go.kr/search/searchDetail. do?rec_key=SH2_PLC20210279323
6. Yoon YK, Kwon KT, Jeong SJ, Moon C, Kim B, Kiem S, Kim HS, Heo E, Kim SW; Korean Society for Antimicrobial Therapy; Korean Society of Infectious Diseases; Korean Society of Health-System Pharmacist. Guidelines on implementing antimicrobial stewardship programs in Korea. Infect Chemother 2021;53:617-659.




7. Korean Society for Antimicrobial Therapy. Basic content of antimicrobial stewardship programs (ASP) [Internet]. Seoul: Korean Society for Antimicrobial Therapy. 2021 [cited 2022 Jul 15]. Available from: https://www.ksat.or.kr/board/list.html?code=ss_basic
8. McGowan JE Jr, Gerding DN. Does antibiotic restriction prevent resistance? New Horiz 1996;4:370-376.

9. Dyar OJ, Huttner B, Schouten J, Pulcini C; ESGAP (ESCMID Study Group for Antimicrobial stewardshiP). What is antimicrobial stewardship? Clin Microbiol Infect 2017;23:793-798.


10. Kim YC, Park JY, Kim B, Kim ES, Ga H, Myung R, Park SY, Lee MJ, Moon SM, Park SH, Song KH, Kim HB; Korea Study Group for Antimicrobial Ste wardship (KOSGAP). Prescriptions patterns and appropriateness of usage of antibiotics in non-teaching community hospitals in South Korea: a multicentre retrospective study. Antimicrob Resist Infect Control 2022;11:40.




11. Park SY, Moon SM, Kim B, Lee MJ, Park JY, Hwang S, Yu SN, Lee YM, Lee HJ, Hong KW, Park KH, Kwak YG, Moon C, Jeon MH, Park SH, Kim YK, Song KH, Kim ES, Kim TH, Kim HB; Korea Study Group for Antimicrobial Stewardship (KOSGAP). Appropriateness of antibiotic prescriptions during hospitalization and ambulatory care: a multicentre prevalence survey in Korea. J Glob Antimicrob Resist 2022;29:253-258.


12. Rattanaumpawan P, Sutha P, Thamlikitkul V. Effectiveness of drug use evaluation and antibiotic authorization on patients’ clinical outcomes, antibiotic consumption, and antibiotic expenditures. Am J Infect Control 2010;38:38-43.


13. Feazel LM, Malhotra A, Perencevich EN, Kaboli P, Diekema DJ, Schweizer ML. Effect of antibiotic stewardship programmes on Clostridium difficile incidence: a systematic review and meta-analysis. J Antimicrob Chemother 2014;69:1748-1754.


14. Kim HI, Kim SW, Chang HH, Kim HB. A survey of antimicrobial stewardship programs in Korean hospitals. Korean J Med 2014;87:173-181.

15. Bantar C, Sartori B, Vesco E, Heft C, Saúl M, Salamone F, Oliva ME. A hospitalwide intervention program to optimize the quality of antibiotic use: impact on prescribing practice, antibiotic consumption, cost savings, and bacterial resistance. Clin Infect Dis 2003;37:180-186.


16. Belongia EA, Knobloch MJ, Kieke BA, Davis JP, Janette C, Besser RE. Impact of statewide program to promote appropriate antimicrobial drug use. Emerg Infect Dis 2005;11:912-920.


17. Seok H, Jeon JH, Park DW. Antimicrobial therapy and antimicrobial stewardship in sepsis. Infect Chemother 2020;52:19-30.




18. Seok H, Park DW. Optimal antimicrobial therapy and antimicrobial stewardship in sepsis and septic shock. J Korean Med Assoc 2019;62:638-644.


19. Nathwani D, Varghese D, Stephens J, Ansari W, Martin S, Charbonneau C. Value of hospital antimicrobial stewardship programs [ASPs]: a systematic review. Antimicrob Resist Infect Control 2019;8:35.




20. Baur D, Gladstone BP, Burkert F, Carrara E, Foschi F, Döbele S, Tacconelli E. Effect of antibiotic stewardship on the incidence of infection and colonisation with antibiotic-resistant bacteria and Clostridium difficile infection: a systematic review and meta-analysis. Lancet Infect Dis 2017;17:990-1001.


21. Song YJ, Kim M, Huh S, Lee J, Lee E, Song KH, Kim ES, Kim HB. Impact of an antimicrobial stewardship program on unnecessary double anaerobic coverage prescription. Infect Chemother 2015;47:111-116.




22. Park SM, Kim HS, Jeong YM, Lee JH, Lee E, Lee E, Song KH, Kim HB, Kim ES. Impact of intervention by an antimicrobial stewardship team on conversion from intravenous to oral fluoroquinolones. Infect Chemother 2017;49:31-37.




23. Hwang H, Kim B. Impact of an infectious diseases specialistled antimicrobial stewardship programmes on antibiotic use and antimicrobial resistance in a large Korean hospital. Sci Rep 2018;8:14757.




24. Fridkin S, Baggs J, Fagan R, Magill S, Pollack LA, Malpiedi P, Slayton R, Khader K, Rubin MA, Jones M, Samore MH, Dumyati G, Dodds-Ashley E, Meek J, Yousey-Hindes K, Jernigan J, Shehab N, Herrera R, McDonald CL, Schneider A, Srinivasan A; Centers for Disease Control and Prevention (CDC). Vital signs: improving antibiotic use among hospitalized patients. MMWR Morb Mortal Wkly Rep 2014;63:194-200.


25. Pollack LA, Srinivasan A. Core elements of hospital antibiotic stewardship programs from the Centers for Disease Control and Prevention. Clin Infect Dis 2014;59 Suppl 3:S97-S100.



26. Vaughn VM, Greene MT, Ratz D, Fowler KE, Krein SL, Flanders SA, Dubberke ER, Saint S, Patel PK. Antibiotic stewardship teams and Clostridioides difficile practices in United States hospitals: a national survey in The Joint Commission antibiotic stewardship standard era. Infect Control Hosp Epidemiol 2020;41:143-148.


27. Pulcini C, Binda F, Lamkang AS, Trett A, Charani E, Goff DA, Harbarth S, Hinrichsen SL, Levy-Hara G, Mendelson M, Nathwani D, Gunturu R, Singh S, Srinivasan A, Thamlikitkul V, Thursky K, Vlieghe E, Wertheim H, Zeng M, Gandra S, Laxminarayan R. Developing core elements and checklist items for global hospital antimicrobial stewardship programmes: a consensus approach. 2019;25:20-25.

28. World Health Organization. Antimicrobial stewardship programmes in health-care facilities in low-and middle-income countries: a WHO practical toolkit [Internet]. Geneva: World Health Organization. 2019 [cited 2022 Jul 15]. Available from: https://www.who.int/publications/i/item/9789241515481
29. Lee MJ, Moon SM, Kim B, Park SY, Park JY, Koo H, Lee H, Song KH, Lee H, Park JS, Lee MS, Choi SM, Kim CJ, Chang HH, Kim TH, Park SH, Kim ES, Kim HB; Korea Study Group for Antimicrobial Stewardship (KOSGAP). Status of antimicrobial stewardship programmes in Korean hospitals including small to medium-sized hospitals and the awareness and demands of physicians: a nationwide survey in 2020. J Glob Antimicrob Resist 2021;26:180-187.


30. Park SY, Chang HH, Kim B, Moon C, Lee MS, Kim JY, Jung DS, Kim SW, Moon SM, Kim ES, Kim HB; for Korea Study Group For Antimicrobial Stewardship (KOSGAP). Human resources required for antimicrobial stewardship activities for hospitalized patients in Korea. Infect Control Hosp Epidemiol 2020;41:1429-1435.


31. Kim B, Lee MJ, Moon SM, Park SY, Song KH, Lee H, Park JS, Lee MS, Choi SM, Yeom JS, Kim JY, Kim CJ, Chang HH, Kim ES, Kim TH, Kim HB; Korea Study Group for Antimicrobial Stewardship (KOSGAP). Current status of antimicrobial stewardship programmes in Korean hospitals: results of a 2018 nationwide survey. J Hosp Infect 2020;104:172-180.


Peer Reviewers’ Commentary
항생제 내성에 대처하기 위한 2가지 전략으로 항생제의 적절한 사용과 오남용 방지, 그리고 내성균의 전파를 차단하기 위한 감염관리가 제시되고 있는데, 전자에 해당하는 내용이 이 논문에서 제시하고 있는 항생제 사용관리 프로그램이다. 항생제 사용 관리 프로그램은 약제의 적정성을 포함한 의료 질 향상 측면에서도 중요하지만, 항생제 내성균 대응을 위해서도 국내 의료기관에 반드시 정착되어야 할 활동이다. 기존 의료진들에게 아직은 다소 생소할 수 있는 개념이지만 제2차 국가 항생제 내성 관리대책에 따르면 2025년까지 국내 모든 상급종합병원과 종합병원에 항생제 사용관리 프로그램을 정착시키는 것을 목표로 하는 만큼 관련된 분야의 발전이 예상된다. 이 논문은 임상 현장의 의료진들이 항생제 사용관리 프로그램을 이해하는 데 많은 도움을 줄 것으로 판단된다.
[정리: 편집위원회]
-
METRICS

-
Related articles in
J Korean Med Assoc -
Implementation of DUR System and Participation of Clinicians2004 February;47(2)
Clinical Implementation of Therapeutic Hypothermia after Cardiac Arrest2009 December;52(12)
Prevention of myopia progression2016 January;59(1)
Current status of health and medical television programs2016 October;59(10)






