 |
 |
- Search
| J Korean Med Assoc > Volume 65(9); 2022 > Article |
|
Abstract
Background: Treatment for early colon cancer has progressed rapidly with endoscopic resection and minimally invasive surgery. Selection of patients without risk of lymph node metastasis is necessary before deciding on endoscopic resection for early colon cancer treatment. We aimed to review the optimal multidisciplinary treatment strategies for early colon cancer, including endoscopy and surgery.
Current Concepts: Pathological risk factors include histologic grade of cancer cell differentiation, lymphovascular invasion, perineural invasion, tumor budding, and deep submucosal invasion. These risk factors for predicting lymph node metastasis are crucial for determining the treatment strategy of endoscopic excision and radical resection for early colon cancer. Prediction of the depth of invasion in early colon cancer using endoscopic optical assessments is vital to determine the appropriate treatment method for endoscopic or surgical resection. Furthermore, optical assessment of pit and vascular patterns is useful for estimating the depth of submucosal invasion using magnifying chromoendoscopy and narrow-band imaging endoscopy. Performing an endoscopic and pathologic evaluation of the risk factors for lymph node metastasis is imperative when selecting endoscopic or surgical resection. Endoscopic treatments include cold snare polypectomy, endoscopic mucosal resection, and endoscopic submucosal dissection. In addition, appropriate surgical treatment should be recommended for patients with early colon cancer with a high risk of lymph node metastasis.
Discussion and Conclusion: A multidisciplinary approach should be recommended to establish an optimized treatment strategy, minimize the risk of complications, and obtain excellent oncologic outcomes via patient-tailored treatment in patients with early colon cancer.
Current Concepts: Pathological risk factors include histologic grade of cancer cell differentiation, lymphovascular invasion, perineural invasion, tumor budding, and deep submucosal invasion. These risk factors for predicting lymph node metastasis are crucial for determining the treatment strategy of endoscopic excision and radical resection for early colon cancer. Prediction of the depth of invasion in early colon cancer using endoscopic optical assessments is vital to determine the appropriate treatment method for endoscopic or surgical resection. Furthermore, optical assessment of pit and vascular patterns is useful for estimating the depth of submucosal invasion using magnifying chromoendoscopy and narrow-band imaging endoscopy. Performing an endoscopic and pathologic evaluation of the risk factors for lymph node metastasis is imperative when selecting endoscopic or surgical resection. Endoscopic treatments include cold snare polypectomy, endoscopic mucosal resection, and endoscopic submucosal dissection. In addition, appropriate surgical treatment should be recommended for patients with early colon cancer with a high risk of lymph node metastasis.
Discussion and Conclusion: A multidisciplinary approach should be recommended to establish an optimized treatment strategy, minimize the risk of complications, and obtain excellent oncologic outcomes via patient-tailored treatment in patients with early colon cancer.
대장암은 우리나라에서 가장 흔한 암 중 하나이다. 국가암검진 프로그램이 널리 시행됨에 따라 지난 수십 년 동안 조기 대장암의 진단율이 증가했다[1]. 조기 대장암의 치료는 내시경절제술과 최소 침습적 수술 등으로 빠르게 발전하고 있다. 내시경절제술은 전신마취 없이 시행할 수 있으며, 수술적 절제에 비해 회복이 빠르고 입원기간이 짧으며, 비용이 저렴한 장점이 있다[2]. 그러나 내시경절제술은 림프절 절제를 시행할 수 없고, 원발성 국소 병변만을 절제하기 때문에 조기 대장암 치료를 위해 내시경절제술을 결정하기 전에 림프절 전이의 위험이 없는 환자를 선택하는 것이 중요하다.
최소 침습 수술은 대장암 수술 분야에 큰 변화를 가져왔다[3-5]. 복강경 수술은 수술 후 통증, 배변 회복, 입원기간, 빠른 일상생활 복귀 등 수술 후 단기 결과를 개선했다[6]. 대규모 무작위임상연구에서는 장기 종양학적 결과의 안전성을 확립했다[7]. 따라서 복강경 수술은 대장암 환자에게 안전한 종양 수술로 받아들여지고 있다.
조기 대장암의 치료 전략을 수립하여 환자의 병기와 전신 상태에 최적화된 적절한 치료법을 선택하여 합병증의 위험을 최소화하고 우수한 종양학적 결과를 얻기 위해서는 다학제적 접근이 강조되고 있다. 이 논문에서는 조기 대장암에 대한 내시경 및 수술을 포함한 최적의 다학제적 치료 전략을 정리하여 제시하였다.
초기 대장암의 예후를 결정짓는 가장 중요한 인자는 림프절 전이이다. 수술 전 컴퓨터단층촬영(computed tomography, CT)은 원격전이 뿐만 아니라 림프절 전이를 감지하기 위해 일상적으로 사용된다. 불규칙한 경계, 조직의 이질성, 불규칙한 모양과 같은 림프절의 형태적 특징은 전이성 림프절을 구별 짓는 특징으로 간주된다. 밀도가 균일한 림프절은 전이 가능성이 적고, 경계가 분명하지 않거나, 모호하거나, 혹은 밀도가 혼합된 림프절은 전이성 림프절로 간주된다[8]. 림프절 전이는 다양한 방사선학적 특징을 이용하여 평가하지만 CT의 림프절 전이의 진단 정확도는 여전히 약 70%에 불과하다. 5 mm 이하의 림프절 중에서도 약 15-20%가 대장암에서 전이성 림프절로 보고되고 있다[9].
따라서 조기 대장암의 내시경절제술과 근치적 절제술의 치료 전략을 결정할 때 림프절 전이를 예측하는 병리학적 위험인자는 매우 중요하다. 병리학적 위험인자에는 암세포 조직 분화도, 림프관 침윤, 혈관 침윤, 신경주위 침윤, 종양발아, 깊은 점막하 침윤 및 수직 침윤 깊이(>1,000 μm)가 포함되므로 병리학적 평가에서 점막하 조직을 포함하는 것은 중요하다[10].
저분화 선암, 인환세포암종 및 점액성 선암은 불량한 조직학적 유형으로 분류될 수 있다[11]. 림프 및 정맥 침습도 림프절 전이의 독립적인 예측인자이다. 종양발아는 점막하 침윤의 침습면으로부터 분리된 단일 암세포 또는 5개 미만의 암세포군의 존재로 정의한다. 가장 깊은 침습면 부위에 5-10개 이상의 종양발아가 존재하면 조기 대장암에서 림프절 전이의 위험이 증가할 수 있다[12].
점막층에 국한된 대장암은 림프절 전이를 일으키지 않는다. 그러나 점막하층을 침범하면 약 6-20%에서 림프절 전이가 발생한다[13]. Haggitt 분류 방법은 유경성 병변의 점막하 침윤을 평가하는 데 사용되었다. 비경성 병변의 경우 Kudo 또는 Kikuchi 분류에 따라 점막하 침윤 깊이를 평가한다[14]. 점막하층 전체를 3등분으로 했을 때, 표층(SM1), 중층(SM2), 심층(SM3)으로 나눌 수 있다. Haggitt level 4와 Kikuchi SM 2-3의 깊은 점막하 침윤이 있는 경우 림프절 전이의 위험이 증가한다. 무경성 악성 용종에서 점막하층으로 수직 침윤 깊이가 1,000 μm 이상인 경우 림프절 전이의 위험이 3배 이상 증가한다[15]. 내시경절제술로 점막하층의 전체 두께를 절제할 수 없는 경우 점막하층을 3단계로 나누는 것은 부정확할 수 있다. 따라서 1,000 μm 이상의 수직 침습 깊이는 깊은 점막하 침습을 반영하는 특징으로 사용 할수 있다. 내시경적 제거 후 절제연을 침범하는 것도 위험인자이다. 이러한 위험요소가 있는 경우 추가적인 근치적 절제가 필요하다(Figure 1) [16].
내시경을 이용한 광학적 평가를 이용해 조기 대장암의 침윤 깊이를 예측하는 것은 내시경적 또는 수술적 절제의 치료 방법을 적절하게 결정하는 데 큰 도움이 된다. 병변의 경도, 깊고 불규칙한 함몰, 공기주입에 의한 형태의 불변, 점막주름의 수렴, non-lifting sign 등은 심부 점막하암을 시사하는 육안 소견이다. 특히 non-lifting sign은 점막하 섬유증 또는 깊은 점막하 침윤과 연관되어 있다. 그러나 육안적 형태에 의한 깊은 점막하암을 예측하는 것에 비해 민감도와 정확도가 낮아 non-lifting sign 만으로 점막하 침윤을 예측하는 것은 한계가 있다[17].
확대색소내시경과 협대역영상(narrow-band image, NBI) 내시경을 사용한 pit pattern과 혈관상의 광학적 평가는 점막하 침윤 깊이를 추정하는 데 유용하다. 깊은 점막하 침범도 Kudo pit pattern을 사용하여 예측할 수 있는데, 심부 점막하 침범은 pit pattern IIIL, IIIS 및 IV에서 각각 1%, 5% 및 8%에 불과했지만, 형태가 불규칙하거나(type VI), 조직화되지 않은 경우(type VN), 깊은 점막하 침윤의 확률은 각각 14%와 80%이다[18]. Indigo carmine 혹은 crystal violet 등의 염색액을 도포한 후 확대색소내시경을 이용하여 점막을 관찰하면 점막선 구멍(mucosal gland orifice or pit pattern)의 형태를 평가할 수 있는데, 두 염색법의 색소내시경 진단 정확도에는 차이가 없었다[19]. NBI는 빛의 파장을 선택적으로 조절하여 얕은 광투과율을 이용하여 점막 표면을 세밀하게 관찰할 수 있는데, 점막색, 표면 형태, 모세혈관상을 평가하여 침습성 대장암의 위험을 예측할 수 있다[20]. 확대색소내시경을 사용한 NBI는 점막 표면의 모세혈관상을 세심하게 탐색할 수 있는데 pit pattern이 깨지면서 두꺼운 미세혈관이 불규칙하게 있거나 무혈성 부위가 관찰되는 경우, 그리고 혈관 분포가 균일하지 않을 경우, 심부 점막하층을 침범했을 가능성이 있다.
일본에서는 Sano, Hiroshima, Showa, Jikei 분류와 같은 다양한 평가도구가 개발되었다. Japan Narrow Band Imaging Expert Team 분류는 전문가 회의에서 통합 분류 시스템으로 제안되었으며, 검증 연구를 통해 그 유용성이 입증되었다. 일본, 미국, 유럽의 내시경 전문가 그룹은 조기 대장암의 내시경 진단을 위해 Narrow Band Imaging International Colorectal Endoscopic classification (NICE) 분류를 개발했다[21]. NICE 분류는 내시경으로 관찰할 수 있는 점막의 미세한 변화에 따라 양성 선종, 점막내암, 표재성 점막하암, 심부 점막하암으로 구분된다(Table 1) [21]. 육안 내시경에서 심부 점막하암을 시사하는 소견이 있거나 Kudo 전구형이 V N 인 경우 또는 NBI 내시경에서 Sano class IIIB, Hiroshima class C3 또는 Japan Narrow Band Imaging Expert Team class 3에 해당하는 경우 깊은 점막하 침윤 가능성이 높다. 따라서 내시경을 이용한 광학 진단을 바탕으로 내시경적 치료와 수술을 적절하게 고려할 수 있다.
네덜란드 T1 대장암 연구 그룹은 큰 무경성 용종에서 NBI 를 사용하여 T1 대장암을 실시간 광학 진단하는 다기관 전향적 연구를 수행했다. 광학 진단의 민감도는 여전히 63.3%로 제한적이지만, 점막하층 침윤이 있는 내시경적으로 절제 불가능한 병변을 예측하는 데 대한 특이도는 99.0%로 정확했다[22]. 따라서 확대색소내시경, NBI 등을 포함한 첨단 내시경 영상 기술을 사용하여 조기 대장암의 표층 또는 깊은 점막하 침윤을 구별하는 정확도를 높여 내시경 절제가 가능한 병변에 대한 불필요한 외과적 의뢰를 줄일 수 있다. 반대로 즉각적인 수술적 절제가 필요한 심부 점막하 대장암의 불필요한 수술 전 내시경절제술을 줄이는 데 도움을 줄 수 있다.
점막층에 국한된 대장암은 림프절 전이의 위험이 없기 때문에 내시경절제술로 점막내 종양을 완전히 절제하면 재발 가능성이 없어 치료할 수 있다. 점막내 종양이나 표층 점막하 침윤이 있는 경우 내시경적 치료와 수술적 치료 간 재발률에는 차이가 없었다[23].
그러나 림프절 전이의 위험이 높은 점막하 대장암에서는 내시경절제술이 수술적 절제술보다 재발률이 높다. 점막하 침윤이 있는 초기 대장암에서, 내시경절제술은 국소 재발률이 2.3-6.4%인 반면, 외과적 절제술은 국소 재발률이 0.9-1.9%로 상대적으로 낮았다[24]. 조기 대장암의 림프절 전이 확률은 위험인자 유무에 따라 각각 15.5%, 7.1%였다. 따라서 림프절 전이의 위험인자가 높은 초기 대장암은 내시경 치료 후 추가적인 수술이 필요하다.
내시경 치료에는 콜드 올가미 용종 절제술(cold snare polypectomy), 내시경점막절제술(endoscopic mucosal resection, EMR), 내시경점막하박리술(endoscopic submucosal dissection, ESD)이 있다. 대장내시경에서 악성 대장 용종이 발견되면 Paris 분류에 따른 용종의 크기와 육안적 형태를 확인해야 한다. 유경성 악성 용종은 콜드 올가미 폴립 절제술을 사용하여 안전하게 제거할 수 있다. 무경성 용종의 경우 종양의 크기에 따라 적절한 내시경 절제방법을 선택할 수 있다. 크기가 2 cm 미만인 용종은 EMR을 통해, 2 cm 이상의 폴립은 ESD를 통해 안전하게 절제할 수 있다. 함몰이 있는 무경형 용종(유형 IIc)은 점막하 침윤과 관계가 있을 수 있기 때문에 내시경 치료의 선택에 세심한 주의가 필요하다[25].
암세포의 절제연 침범은 국소 절제의 종양학적 실패로 이어지는 가장 중요한 요인이다. 따라서 조기 대장암의 내시경 치료를 위해서는 절제연이 음성인 일괄 절제를 시행해야 한다. ESD는 EMR 기법보다 큰 무경성 병변의 일괄 절제에 더 유리할 수 있다. 그러나 ESD에는 높은 출혈 및 천공과 같은 합병증의 위험이 따른다[26]. 결장 병변에 대한 ESD는 난이도가 높기 때문에 합병증 발생률과 완전 절제율은 내시경 시술자의 경험과 기술에 따라 크게 달라진다. 점막하 박리 후 합병증의 대부분은 내시경으로 치료할 수 있으며, 응급수술이 필요한 경우는 점막하박리술을 받은 환자의 약 1% 정도이기 때문에 ESD의 안전성은 임상적으로 충분히 수용할 만하다. 따라서 대장의 ESD는 적절한 수련 후 충분한 경험을 가진 내시경 전문가가 시술과 관련된 합병증으로 인한 응급 상황에 대처할 수 있는 의료기관에서 시행되어야 한다[27].
얕은 점막하층에는 림프관이 없어 림프절 전이의 위험이 거의 없다. 그래서 조기 대장암에서 표재성 점막하 침범의 경우 내시경절제술을 안전하게 시행할 수 있다. 깊은 점막하 침범이 있으면 림프혈관 침범과 림프절 전이의 가능성이 높아지기 때문에 심부 점막하 침범이 의심되면 내시경으로 표적 생검만 시행하고 수술적 절제를 고려해야 한다[28]. 이와 같이 내시경적 절제술이나 외과적 절제술을 선택할 때 림프절 전이의 위험인자를 평가하는 것이 중요하다. 또한 림프절 전이의 위험이 높은 조기 대장암 환자에서 우수한 장기 종양학적 결과를 얻기 위해서는 내시경절제술 후 적절한 외과적 치료를 권고해야 한다.
절제된 조직에 림프절 전이의 위험인자가 있거나 절제연이 침범된 경우, 안전한 종양 치료를 위해 외과적 절제를 고려해야 한다. 대장암 치료를 위한 수술적 절제의 원칙은 온전한 결장간막평면, 광범위 림프절 절제, 종방향 절제연 확보의 세 가지 요소로 구성된다.
1982년 Heald는 직장간막에 퍼진 미세 전이 부위를 제거하기 위해 발생학적 평면을 따라 예리하게 박리함으로써 전직장간막절제술(total mesorectal excision, TME)을 제시했다. TME 수술은 직장암의 국소 재발률을 40%에서 10% 미만으로 감소시켰는데, 표준화된 TME는 수술의 질을 개선함으로써 직장암에 대한 종양학적 이점을 얻을 수 있었다[29]. 2009년 Hohenberger 등[30]은 대장암에 대한 전결장간막절제술(complete mesocolic excision, CME)이라는 개념을 제안했다. CME는 결장장간막평면 또는 결장간막면(mesocolic plane) 수술로서 Toldt씨 근막을 따라 예리한 박리를 시행하여 온전한 결장간막면을 유지한다는 점에서 TME와 유사한 개념을 가지고 있다. 결장간막면 수술의 질을 비교한 병리학적 연구에서, 고유근이 노출된 불완전한 결장간막에 비해 온전한 결장간막이 있는 경우에서 유의한 생존 차이가 보고되었다[31]. 메타 분석에서도 CME의 종양학적 이점을 보고했다[32].
CME의 개념화는 표준화된 수술의 질을 제공하고 수술 치료의 정량화를 통해 객관적인 분석을 가능하게 할 수 있다. 절제된 결장간막면의 병리학적 평가는 수술의 질에 대한 객관적인 분석을 가능하게 할 수 있으며, 이는 종양학적 예후 및 수술의 질에 대한 지표로 사용될 수 있다[33]. 따라서 외과 영역에서 CME의 임상적 적용은 대장암에 대한 근치적 수술기법의 표준화를 통해 수술의 질과 환자 생존율의 향상을 기대하고 있다.
집도의는 림프절의 박리 범위를 결정해야 한다. 림프절 전이를 예측하는 데 있어 수술 전 CT의 진단 정확도는 제한적이다. 림프절의 크기가 크고 질감이 이질적인 경우는 전이 가능성이 높지만, 림프절(N) 상태에 대한 CT 소견은 신뢰할 수 없다. 종양 침범의 깊이가 깊어질수록 림프절 전이의 위험도 증가한다[34]. 따라서 수술 전 T상태는 림프절 절제 범위를 결정하는 데 중요한 역할을 한다. 일본결장직장암학회(The Japanese Society of Cancer of the Colon and Rectum) 가이드라인에서는 T3-4에서 D3 림프절 전이의 가능성이 10%로 높기 때문에 진행성 대장암에서 D3 박리를 권장한다[35]. 중심 혈관 결찰(central vascular ligation)은 장간막 혈관 기시부까지 확장된 mesocolon의 완전한 절제를 위해 시행한다. 광범위 림프절 박리술을 위해서는 영양 동맥(feeding artery)의 기점에서 혈관 결찰을 수행해야 한다. 이 중심 혈관 결찰은 일본결장직장암학회 가이드라인에 따른 D3 림프절 박리의 개념과 유사하다.
결장의 림프관 경로는 20세기 초 Jamieson과 Dobson [36]에 의해 과학적인 실험을 토대로 최초로 기술되었다. 그들은 사체의 결장벽에 프러시안 블루(Prussian blue)를 주입하여 염료가 림프계를 따라 흐르고 림프절을 염색하는 것을 관찰했다. 이러한 연구는 대장암 세포가 결장벽에서 국소 림프절로 퍼질 수 있음을 보여주었으며, 이로써 광범위 림프절 박리의 필요성이 강조되었다.
광범위 D3 박리는 우측 결장절제술에서는 상장간막정맥(superior mesenteric vein, SMV)의 surgical trunk에 대한 Gillot의 개념을 기반으로 한다. 1964년 Gillot 등[37]은 SMV 우측의 위결장정맥간(gastrocolic trunk)과 회대장정맥(ileocolic vein) 사이의 부위를 surgical trunk라고 하는 해부학적 지표로 명명했다. 우측 결장의 림프액은 surgical trunk에 수집되어 중심 림프계로 배출되기 때문에 국소적 조절을 위해 surgical trunk를 포함하는 근치적 림프절 박리술이 인정되었다. 1995년 Toyota 등[38]은 우측 결장의 림프 흐름은 SMV의 우측면에 림프관 사슬을 형성하여 주변 림프계를 따라 흐르며 일부 림프관 연결은 중결장동맥(middle colic artery)의 기시부에 있는 림프절까지 확장된다고 설명했다. 그러나 조기 대장암에서 근치적 림프절 박리술의 종양학적 필요성과 이점에 대한 임상적 증거는 부족하다. 현재 종양학적으로 적절한 림프절 박리 범위와 D3 림프절 박리의 해부학적 범위를 결정하기 위하여 다양한 무작위 임상연구가 진행되고 있다[39,40].
림프절 절제 개수가 5개 미만인 환자보다 20개 이상인 환자에서 예후가 더 좋았다는 보고가 있다[41]. 림프절 절제가 불충분한 경우 전이성 림프절의 병리학적 진단은 불가능했을 수 있으며, 따라서 보조 항암치료에 대한 치료 기회를 놓쳤을 수 있다. 충분한 림프절 박리로 적절한 항암치료를 시행하면 보다 정확한 림프절 병기 결정으로 인해 생존율이 향상될 수 있다. 종양학적 관점에서 암의 병리학적 병기를 평가하기 위해서는 적어도 12개의 림프절을 적출해야 하며, 림프절 전이 여부에 따라 수술 후 적절한 항암치료를 선택할 수 있다.
종방향 절제연의 관점에서 볼 때, 대장암 수술의 근위부와 원위부 절제연의 길이에는 차이가 있다(Figure 2) [40]. 일부 술자는 10 cm 이상을 충분한 종방향 절제연으로 판단한다.
일본 연구에서 대부분의 전이 병소는 종양의 5 cm 이내에 분포했기 때문에, 양측에 5 cm의 절제연을 확보하는 것으로 충분하다고 하였다[42]. 또한 간 또는 비장 굴곡 부위는 이중 림프 배액이 있기 때문에 종방향 절제연을 확장하여 넓게 충분히 확보해야 한다고 주장했다. 그러나 대장암 수술에서 기존 근치적 절제술과 확장 근치적 절제술은 치료 효과에 유의한 차이가 없다는 연구결과가 많다[43].
따라서 온전한 결장간막면을 유지하는 것이 중요한 요소이지만, 종양의 위치와 병기, 섭식혈관과의 관계, 림프절 전이 정도에 따라 선택적으로 원발성 종양으로부터 5-10 cm 이상의 절제연을 고려할 수 있다.
최근에는 형광 림프절 매핑이 유망한 영상 유도 기술로 연구되고 있다. ICG (indocyanine green)는 인체에 무해한 형광염료로 결장벽에 주입되면 혈관주위 공간에서 림프계로 들어간다. 대장암 수술에서 형광 림프절 매핑은 특히 주요 surgical trunk 주변에서, 정확하고 안전한 림프절 박리를 위해서 림프 경로를 시각화하는 데 도움이 될수 있다(Figure 3) [44]. 최적의 ICG 용량을 대장내시경을 통해 점막하에 주사했을 때 형광 림프절 매핑의 성공률은 90% 이상이었다[44]. 형광 림프절 매핑 기술을 적용하여 획득 림프절 수를 증가시킬 수 있었다[45,46]. 림프절과 림프 배액 경로를 직접 시각화했을 때, 원발성 종양과 관련된 림프절을 쉽게 박리할 수 있다. 정확한 병리학적 병기 결정을 위해서는 충분한 수의 림프절을 회수하는 것이 중요하다. 종양학적 관점에서 볼 때, 환자가 수술 후 적절한 항암치료를 받을 수 있도록 병리학적 병기를 정확히 평가하기 위해 적어도 12개의 림프절을 회수해야 한다. 형광 림프절 매핑은 12개 이상의 림프절 회수율을 유의하게 향상시켰다[44].
감시 림프절 절제술은 근치적 절제술과 관련된 수술 후 합병증을 줄이기 위해 유방암 및 악성 흑색종에서 확립된 기술이다. 감시 림프절은 이론적으로 원발성 암에서 림프절로 최초 배액되는 부위이다. 방사성 동위원소, 청색 염료 및 형광 염료 등이 림프절 매핑에 사용된다[47]. 근적외선 카메라 시스템의 개발로 복강경 및 로봇 대장암 수술에서 감시 림프절을 감지하기 위해 형광 림프절 매핑이 적용되어왔다. 감시 림프절 매핑은 광범위 또는 선택적 림프절 박리를 결정하기 위한 예비 절차이다. 대장암에서 림프 흐름은 선형 연결을 통해서가 아니라 복잡한 림프 네트워크를 통해 다양한 경로로 퍼질 수 있다. 현재까지 감시 림프절 매핑은 림프절 전이를 평가하는 데 많은 한계가 있다[48]. 림프절 매핑과 관련된 많은 질문에 대해 명확한 답은 아직 없지만, 형광 염료 및 영상 장치의 추가 발전은 형광 림프절 매핑의 개선을 가속화하고 특히 초기 대장암에서 근치적 림프절 절제술로의 확장을 결정하는데 도움이 될 것이다[49].
Acknowledgement
The authors appreciate the multidisciplinary treatment team for colorectal cancer, Pusan National University Yangsan Hospital, Yangsan, Korea.
Figure 1.
Treatment strategies for pT1 cancer after endoscopic resection. Adapted from Hashiguchi Y, et al. Int J Clin Oncol 2020;25:1-42, according to the Creative Commons license [16]. SM, submucosa; BD, tumor budding degree.
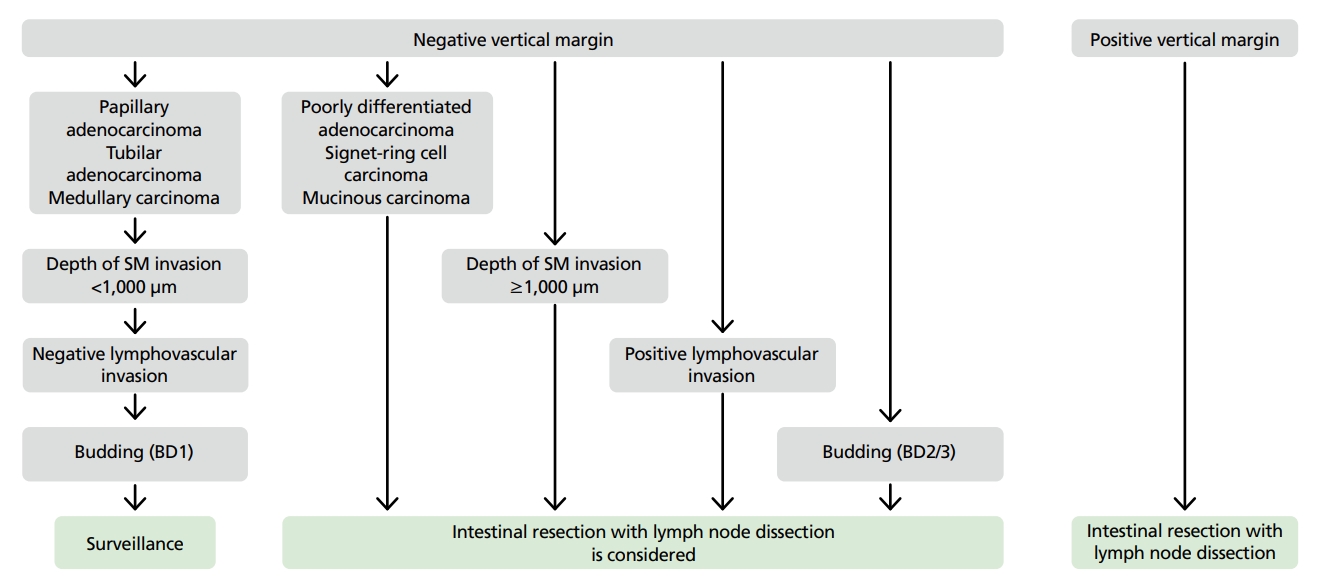
Figure 2.
Grouping of the retrieved lymph nodes (LNs). Adapted from Yang SY, et al. BMC Cancer 2020;20:657, according to the Creative Commons license [40].

Figure 3.
Fluorescence lymph node mapping using laparoscopic near infrared camera systems. (A-C) Stryker (1588 AIM camera system; Stryker, Kalamazoo, MI, USA). (D-F) Storz (IMAGE1 S; Karl Storz, Tuttlingen, Germany). (G-I) Olympus (CLV-S200-IR; Olympus, Tokyo, Japan). (A), (D), and (G) show the mesentery of the colon under white light. Green fluorescence-colored lymph nodes are seen using the endoscopic near-infrared visualization mode of the Stryker (B). isolating the indocyanine green-dyed lymph nodes from the specimen, which is fully resected from the surgical field (C). Blue-colored lymph nodes are seen under the conventional isolating the indocyanine green mode (E) and green-colored under the Spectra mode (F) of the Storz. Partial white light and infrared (IR) light at the same time were led to green-colored lymph nodes overlapping with original view as seen in the narrow-band imaging mode (H) of the Olympus; green-colored lymph nodes are seen in the IR mode (I). Adapted from Ahn HM, et al. Surg Endosc 2022;36:1152-1163, according to the Creative Commons license [44].

Table 1.
Narrow Band Imaging International Colorectal Endoscopic classification (NICE) for the endoscopic diagnosis of early colorectal cancer
Adapted from Wang Y, et al. World J Gastrointest Oncol 2021;13:58-68, according to the Creative Commons license [21].
References
1. Nam S, Choi YJ, Kim DW, Park EC, Kang JG. Risk factors for colorectal cancer in Korea: a population-based retrospective cohort study. Ann Coloproctol 2019;35:347-356.




2. Kim SG, Lyu DH, Park CM, Lee NR, Kim J, Cha Y, Jung HY. Current status of endoscopic submucosal dissection for early gastric cancer in Korea: role and benefits. Korean J Intern Med 2019;34:785-793.




3. Kim HH, Ihn MH, Lee YH, Lee J, Yun S, Cho SW. Effect of age on laparoscopic surgery and postoperative chemotherapy in elderly patients with colorectal cancer. Ann Coloproctol 2020;36:229-242.




4. Jaloun HE, Lee IK, Kim MK, Sung NY, Turkistani SAA, Park SM, Won DY, Hong SH, Kye BH, Lee YS, Jeon HM. Influence of the enhanced recovery after surgery protocol on postoperative inflammation and short-term postoperative surgical outcomes after colorectal cancer surgery. Ann Coloproctol 2020;36:264-272.




5. Nakamura Y, Hokuto D, Koyama F, Matsuo Y, Nomi T, Yoshikawa T, Kamitani N, Sadamitsu T, Takei T, Matsumoto Y, Iwasa Y, Fukuoka K, Obara S, Nakamoto T, Kuge H, Sho M. The prognosis and recurrence pattern of right- and left-sided colon cancer in stage II, stage III, and liver metastasis after curative resection. Ann Coloproctol 2021;37:326-336.




6. Park SJ, Lee KY, Lee SH. Laparoscopic surgery for colorectal cancer in Korea: nationwide data from 2013 to 2018. Cancer Res Treat 2020;52:938-944.




7. Fleshman J, Sargent DJ, Green E, Anvari M, Stryker SJ, Beart RW Jr, Hellinger M, Flanagan R Jr, Peters W, Nelson H; Clinical Outcomes of Surgical Therapy Study Group. Laparoscopic colectomy for cancer is not inferior to open surgery based on 5-year data from the COST Study Group trial. Ann Surg 2007;246:655-662. discussion 662-664.


8. Kim MC, Oh JH. Lateral pelvic lymph node dissection after neoadjuvant chemoradiotherapy in patients with rectal cancer: a single-center experience and literature review. Ann Coloproctol 2021;37:382-394.




9. Nam S, Hong Y, Choi YJ, Kang JG. Clinicopathologic analysis of lateral margin measured by whole-mount section in T3 rectal cancer. Ann Coloproctol 2020;36:172-177.


10. Son GM, Lee IY, Cho SH, Park BS, Kim HS, Park SB, Kim HW, Oh SB, Kim TU, Shin DH. Multidisciplinary treatment strategy for early rectal cancer: a review. Precis Futur Med 2022;6:32-48.
11. Han J, Hur H, Min BS, Lee KY, Kim NK. Predictive factors for lymph node metastasis in submucosal invasive colorectal carcinoma: a new proposal of depth of invasion for radical surgery. World J Surg 2018;42:2635-2641.



12. Yim K, Won DD, Lee IK, Oh ST, Jung ES, Lee SH. Novel predictors for lymph node metastasis in submucosal invasive colorectal carcinoma. World J Gastroenterol 2017;23:5936-5944.



13. Choi JY, Jung SA, Shim KN, Cho WY, Keum B, Byeon JS, Huh KC, Jang BI, Chang DK, Jung HY, Kong KA; Korean ESD Study Group. Meta-analysis of predictive clinicopathologic factors for lymph node metastasis in patients with early colorectal carcinoma. J Korean Med Sci 2015;30:398-406.




14. Kikuchi R, Takano M, Takagi K, Fujimoto N, Nozaki R, Fujiyoshi T, Uchida Y. Management of early invasive colorectal cancer. Risk of recurrence and clinical guidelines. Dis Colon Rectum 1995;38:1286-1295.

15. Bosch SL, Teerenstra S, de Wilt JH, Cunningham C, Nagtegaal ID. Predicting lymph node metastasis in pT1 colorectal cancer: a systematic review of risk factors providing rationale for therapy decisions. Endoscopy 2013;45:827-834.


16. Hashiguchi Y, Muro K, Saito Y, Ito Y, Ajioka Y, Hamaguchi T, Hasegawa K, Hotta K, Ishida H, Ishiguro M, Ishihara S, Kanemitsu Y, Kinugasa Y, Murofushi K, Nakajima TE, Oka S, Tanaka T, Taniguchi H, Tsuji A, Uehara K, Ueno H, Yamanaka T, Yamazaki K, Yoshida M, Yoshino T, Itabashi M, Sakamaki K, Sano K, Shimada Y, Tanaka S, Uetake H, Yamaguchi S, Yamaguchi N, Kobayashi H, Matsuda K, Kotake K, Sugihara K; Japanese Society for Cancer of the Colon and Rectum. Japanese Society for Cancer of the Colon and Rectum (JSCCR) guidelines 2019 for the treatment of colorectal cancer. Int J Clin Oncol 2020;25:1-42.




17. Hisabe T, Tsuda S, Hoashi T, Ishihara H, Yamasaki K, Yasaka T, Hirai F, Matsui T, Yao K, Tanabe H, Iwashita A. Validity of conventional endoscopy using “non-extension sign” for optical diagnosis of colorectal deep submucosal invasive cancer. Endosc Int Open 2018;6:E156-E164.



18. Tanaka S, Haruma K, Nagata S, Oka S, Chayama K. Diagnosis of invasion depth in early colorectal carcinoma by pit pattern analysis with magnifying endoscopy. Dig Endosc 2001;13:S2-S5.

19. Backes Y, Moss A, Reitsma JB, Siersema PD, Moons LM. Narrow band imaging, magnifying chromoendoscopy, and gross morphological features for the optical diagnosis of T1 colorectal cancer and deep submucosal invasion: a systematic review and meta-analysis. Am J Gastroenterol 2017;112:54-64.



20. Sano Y, Tanaka S, Kudo SE, Saito S, Matsuda T, Wada Y, Fujii T, Ikematsu H, Uraoka T, Kobayashi N, Nakamura H, Hotta K, Horimatsu T, Sakamoto N, Fu KI, Tsuruta O, Kawano H, Kashida H, Takeuchi Y, Machida H, Kusaka T, Yoshida N, Hirata I, Terai T, Yamano HO, Kaneko K, Nakajima T, Sakamoto T, Yamaguchi Y, Tamai N, Nakano N, Hayashi N, Oka S, Iwatate M, Ishikawa H, Murakami Y, Yoshida S, Saito Y. Narrow-band imaging (NBI) magnifying endoscopic classification of colorectal tumors proposed by the Japan NBI Expert Team. Dig Endosc 2016;28:526-533.


21. Wang Y, Li WK, Wang YD, Liu KL, Wu J. Diagnostic performance of narrow-band imaging international colorectal endoscopic and Japanese narrow-band imaging expert team classification systems for colorectal cancer and precancerous lesions. World J Gastrointest Oncol 2021;13:58-68.



22. Backes Y, Schwartz MP, Ter Borg F, Wolfhagen FHJ, Groen JN, de Vos Tot Nederveen Cappel WH, van Bergeijk J, Geesing JMJ, Spanier BWM, Didden P, Vleggaar FP, Lacle MM, Elias SG, Moons LMG; Dutch T1 CRC Working Group. Multicentre prospective evaluation of real-time optical diagnosis of T1 colorectal cancer in large non-pedunculated colorectal polyps using narrow band imaging (the OPTICAL study). Gut 2019;68:271-279.


23. Heo J, Jeon SW, Jung MK, Kim SK, Kim J, Kim S. Endoscopic resection as the first-line treatment for early colorectal cancer: comparison with surgery. Surg Endosc 2014;28:3435-3442.



24. Kim JB, Lee HS, Lee HJ, Kim J, Yang DH, Yu CS, Kim JC, Byeon JS. Long-term outcomes of endoscopic versus surgical resection of superficial submucosal colorectal cancer. Dig Dis Sci 2015;60:2785-2792.



25. Facciorusso A, Antonino M, Di Maso M, Barone M, Muscatiello N. Non-polypoid colorectal neoplasms: Classification, therapy and follow-up. World J Gastroenterol 2015;21:5149-5157.



26. Fujiya M, Tanaka K, Dokoshi T, Tominaga M, Ueno N, Inaba Y, Ito T, Moriichi K, Kohgo Y. Efficacy and adverse events of EMR and endoscopic submucosal dissection for the treatment of colon neoplasms: a meta-analysis of studies comparing EMR and endoscopic submucosal dissection. Gastrointest Endosc 2015;81:583-595.


27. Jeon HH, Lee HS, Youn YH, Park JJ, Park H. Learning curve analysis of colorectal endoscopic submucosal dissection (ESD) for laterally spreading tumors by endoscopists experienced in gastric ESD. Surg Endosc 2016;30:2422-2430.



28. Vleugels JLA, Koens L, Dijkgraaf MGW, Houwen B, Hazewinkel Y, Fockens P, Dekker E; DISCOUNT study group. Suboptimal endoscopic cancer recognition in colorectal lesions in a national bowel screening programme. Gut 2020;69:977-980.



29. Varela C, Kim NK. Surgical treatment of low-lying rectal cancer: updates. Ann Coloproctol 2021;37:395-424.




30. Hohenberger W, Weber K, Matzel K, Papadopoulos T, Merkel S. Standardized surgery for colonic cancer: complete mesocolic excision and central ligation--technical notes and outcome. Colorectal Dis 2009;11:354-364. discussion 364-365.


31. West NP, Morris EJ, Rotimi O, Cairns A, Finan PJ, Quirke P. Pathology grading of colon cancer surgical resection and its association with survival: a retrospective observational study. Lancet Oncol 2008;9:857-865.


32. Conti C, Pedrazzani C, Turri G, Fernandes E, Lazzarini E, De Luca R, Valdegamberi A, Ruzzenente A, Guglielmi A. Comparison of short-term results after laparoscopic complete mesocolic excision and standard colectomy for right-sided colon cancer: analysis of a western center cohort. Ann Coloproctol 2021;37:166-173.



33. Nagtegaal ID, van de Velde CJ, van der Worp E, Kapiteijn E, Quirke P, van Krieken JH; Cooperative Clinical Investigators of the Dutch Colorectal Cancer Group. Macroscopic evaluation of rectal cancer resection specimen: clinical significance of the pathologist in quality control. J Clin Oncol 2002;20:1729-1734.


34. Hong EK, Landolfi F, Castagnoli F, Park SJ, Boot J, Van den Berg J, Lee JM, Beets-Tan R. CT for lymph node staging of Colon cancer: not only size but also location and number of lymph node count. Abdom Radiol (NY) 2021;46:4096-4105.



35. Tomita N, Ishida H, Tanakaya K, Yamaguchi T, Kumamoto K, Tanaka T, Hinoi T, Miyakura Y, Hasegawa H, Takayama T, Ishikawa H, Nakajima T, Chino A, Shimodaira H, Hirasawa A, Nakayama Y, Sekine S, Tamura K, Akagi K, Kawasaki Y, Kobayashi H, Arai M, Itabashi M, Hashiguchi Y, Sugihara K; Japanese Society for Cancer of the Colon, Rectum. Japanese Society for Cancer of the Colon and Rectum (JSCCR) guidelines 2020 for the clinical practice of hereditary colorectal cancer. Int J Clin Oncol 2021;26:1353-1419.




36. Jamieson JK, Dobson JF. On the Injection of Lymphatics by Prussian Blue. J Anat Physiol 1910;45:7-10.


37. Gillot C, Hureau J, Aaron C, Martini R, Thaler G, Michels NA. The superior mesenteric vein, an anatomic and surgical study of eighty-one subjects. J Int Coll Surg 1964;41:339-369.

38. Toyota S, Ohta H, Anazawa S. Rationale for extent of lymph node dissection for right colon cancer. Dis Colon Rectum 1995;38:705-711.


39. Xu L, Su X, He Z, Zhang C, Lu J, Zhang G, Sun Y, Du X, Chi P, Wang Z, Zhong M, Wu A, Zhu A, Li F, Xu J, Kang L, Suo J, Deng H, Ye Y, Ding K, Xu T, Zhang Z, Zheng M, Xiao Y; RELARC Study Group. Short-term outcomes of complete mesocolic excision versus D2 dissection in patients undergoing laparoscopic colectomy for right colon cancer (RELARC): a randomised, controlled, phase 3, superiority trial. Lancet Oncol 2021;22:391-401.


40. Yang SY, Kim MJ, Kye BH, Han YD, Cho MS, Jeong SY, Cho HM, Kim H, Kang GH, Song SH, Park JS, Kim JS, Park SY, Kim J, Min BS. Prospective study of oncologic outcomes after laparoscopic modified complete mesocolic excision for nonmetastatic right colon cancer (PIONEER study): study protocol of a multicentre single-arm trial. BMC Cancer 2020;20:657.




41. Baxter NN, Ricciardi R, Simunovic M, Urbach DR, Virnig BA. An evaluation of the relationship between lymph node number and staging in pT3 colon cancer using population-based data. Dis Colon Rectum 2010;53:65-70.


42. Kobayashi H, West NP, Takahashi K, Perrakis A, Weber K, Hohenberger W, Quirke P, Sugihara K. Quality of surgery for stage III colon cancer: comparison between England, Germany, and Japan. Ann Surg Oncol 2014;21 Suppl 3:S398-S404.



43. Morarasu S, Clancy C, Cronin CT, Matsuda T, Heneghan HM, Winter DC. Segmental versus extended colectomy for tumours of the transverse colon: a systematic review and meta-analysis. Colorectal Dis 2021;23:625-634.



44. Ahn HM, Son GM, Lee IY, Shin DH, Kim TK, Park SB, Kim HW. Optimal ICG dosage of preoperative colonoscopic tattooing for fluorescence-guided laparoscopic colorectal surgery. Surg Endosc 2022;36:1152-1163.




45. Park SY, Park JS, Kim HJ, Woo IT, Park IK, Choi GS. Indocyanine green fluorescence imaging-guided laparoscopic surgery could achieve radical D3 dissection in patients with advanced right-sided colon cancer. Dis Colon Rectum 2020;63:441-449.


46. Son GM, Ahn HM, Lee IY, Ha GW. Multifunctional indocyanine green applications for fluorescence-guided laparoscopic colorectal surgery. Ann Coloproctol 2021;37:133-140.




47. Saha S, Philimon B, Efeson M, Helina A, Elgamal M, Kiya G, Hilkiah S, Arora M, Wiese D, Kitagawa Y. The role of sentinel lymph node mapping in colon cancer: detection of micro-metastasis, effect on survival, and driver of a paradigm shift in extent of colon resection. Clin Exp Metastasis 2022;39:109-115.



48. Nissan A, Protic M, Bilchik A, Eberhardt J, Peoples GE, Stojadinovic A. Predictive model of outcome of targeted nodal assessment in colorectal cancer. Ann Surg 2010;251:265-274.


49. Son GM, Lee IY, Lee YS, Kye BH, Cho HM, Jang JH, Kim CN, Lee KY, Lee SH, Kim JG; Korean Laparoscopic Colorectal Surgery Study Group. Is Laparoscopic Complete Mesocolic Excision and Central Vascular Ligation Really Necessary for All Patients With Right-Sided Colon Cancer? Ann Coloproctol 2021;37:434-444.




Peer Reviewers’ Commentary
이 논문은 조기 대장암 환자를 치료할 때 고려해야 할 내시경 치료부터 최소침습수술까지 다양한 치료전략과 임상적인 특성에 대해 최신 문헌을 정리하여 자세하게 소개해주고 있다. 조기 대장암의 경우 점막하 침윤 정도에 따라 대장내시경을 통한 점막하 박리술을 고려해볼 수 있으나 림프절 전이와 재발의 위험도를 신중히 고려해 치료 방법을 결정해야 한다. 조기 대장암의 진단과 치료에 대한 내시경적 및 병리학적 평가를 통해 치료에 대한 다학제적 접근은 매우 중요하다. 조기 대장암 치료에서 최소침습수술과 함께 최근 개발된 림프절 형광 매핑 영상기술을 이용할 경우 암 주변 림프 경로를 시각화하여 원발성 종양과 관련된 림프절 전이를 판단하는 데 많은 도움을 받을 수 있다. 이 논문은 조기 대장암 환자를 진단하고 치료하는 임상 현장에 많은 도움을 줄 것으로 판단된다.
[정리: 편집위원회]
-
METRICS

-
Related articles in
J Korean Med Assoc -
Surgical treatment of esophageal cancer2024 February;67(2)
Endoscopic treatment of colorectal polyps and early colorectal cancer2023 November;66(11)
Adjuvant treatment for resectable non-small cell lung cancer2023 March;66(3)
Healthcare response strategies for the long-COVID era2023 January;66(1)
Surgical treatment for metastatic colorectal cancer2022 September;65(9)






