 |
 |
- Search
| J Korean Med Assoc > Volume 66(1); 2023 > Article |
|
Abstract
Background: Glossopharyngeal neuralgia (GPN) is a rare type of cranial nerve rhizopathy that accounts for roughly 1% of trigeminal neuralgia cases and presents as extreme neuralgic pain in the ipsilateral deep throat, tongue base, or ear. Pain is usually intense and electric shock-like, occurring either without warning or triggered by swallowing. The purpose of this article is to provide a comprehensive review of the diagnosis and treatment of GPN and to differentiate it from trigeminal neuralgia.
Current Concepts: In this review, our experiences, including cases of misdiagnosis and diagnostic pitfalls, are presented in detail. Treatment of GPN with microvascular decompression (MVD) has a success rate of over 90%. The use of “off-the-root entry zone” MVD, which eliminates the need for an adjuvant rhizotomy, is the best treatment for GPN. In addition, although gamma knife radiosurgery is categorized as a destructive procedure, it can still be another option if a patient is ineligible for MVD.
Discussion and Conclusion: Practitioners must consider GPN when diagnosing patients with cranial nerve rhizopathy; it should be distinguished from other pain syndromes, especially trigeminal neuralgia. With an accurate diagnosis, an appropriate treatment plan can be developed.
Current Concepts: In this review, our experiences, including cases of misdiagnosis and diagnostic pitfalls, are presented in detail. Treatment of GPN with microvascular decompression (MVD) has a success rate of over 90%. The use of “off-the-root entry zone” MVD, which eliminates the need for an adjuvant rhizotomy, is the best treatment for GPN. In addition, although gamma knife radiosurgery is categorized as a destructive procedure, it can still be another option if a patient is ineligible for MVD.
Discussion and Conclusion: Practitioners must consider GPN when diagnosing patients with cranial nerve rhizopathy; it should be distinguished from other pain syndromes, especially trigeminal neuralgia. With an accurate diagnosis, an appropriate treatment plan can be developed.
혀인두신경통(glossopharyngeal neuralgia)은 드물기 때문에 상대적으로 흔한 삼차신경통(trigeminal neuralgia)으로 오진되기 쉬운 뇌신경 기능장애 질환의 하나이다[1-3]. 그 발병률은 삼차신경통의 1% 정도로 추정된다[4]. 혀인두신경통이라는 용어는 1921년 Harris가 혀 뒤쪽, 목구멍 등의 통증 발작을 설명하는 용어로 처음 사용했다[5]. 임상적으로는 설인신경통을 주고 사용하고 있으나, 이 논문에서는 대한의사협회 의학용어집에 따라 혀인두신경통으로 사용한다.
혀인두신경통은 국제두통학회(International Headache Society)의 분류에서 고전적, 속발성 및 특발성 등으로 분류된다[6]. 고전적 혀인두신경통의 경우에는 혀인두신경 뿌리를 혈관이 압박하는 소견이 자기공명영상(magnetic resonance imaging, MRI)에서 관찰된다. 이차성 혀인두신경통은 증상을 유발하는 기저 질환이 있다. 특발성 혀인두신경통은 기저 질환이나 뇌신경 혈관 압박 소견이 없는 경우로 정의되고 있다. 이차성 혀인두신경통을 제외하면, 주로 성인에게 발생하며, 오른쪽보다 왼쪽에, 남성보다 여성에 더 호발하는 경향이 있다[1-3,7].
혀인두신경의 외과적 해부와 혀인두신경통의 병태생리 이해는 치료를 이해하는 데 도움이 된다. 혀인두신경은 감각 운동이 혼합된 신경으로 가늘고 목 안쪽에 깊숙하게 자리 잡고 있어 해부학적으로 잘 보이지 않는다[12]. 혀인두신경 돌기는 하올리브(inferior olive)와 하소뇌각(inferior cerebellar peduncle) 사이의 뇌교(pons)의 측면에서 나온다. 혀인두신경의 신체 감각은 혀의 후방 2/3, 중이 및 인두에서 파생되는 반면 내장 감각은 경동맥체에서 입력을 받는다. 귀밑샘(parotid gland)에 대한 부교감 신경 섬유도 혀인두신경을 통해 이동한다. 그것들은 뇌교의 하부 타액 핵(inferior salivatory nucleus)에서 발생하고 혀인두신경을 고막 신경으로 남겨두고 소석체 신경(lesser petrosal nerve)과 합류한다. 혀인두신경의 운동 섬유는 수질의 모호한 핵에서 시작하여 스타일로 인두 근육을 자극한다[3,12,13].
미주신경은 자율 신경계의 일부로서 감각 신경과 운동 신경으로 구성되어 있다. 심장, 폐 및 위장관의 부교감 신경 제어와 연결된다. 이 신경은 숨골(medulla oblongata)에서 나오고 그 가지들은 올리브(olive)와 하소뇌각 사이에서 올리브 쪽 측면에서 나온다. 미주신경은 상완운동(branchial motor), 내장 감각(visceral sensory), 내장 운동(visceral motor), 특수 및 일반 감각(special and general sensory) 신경 등으로 구성된다. 미주신경의 상완 운동 섬유는 주로 인두, 후두, 연구개 및 심장 근육의 근육을 자극하여 발성 및 삼킴에 관여한다. 내장 운동 섬유는 식도, 위 및 대부분의 장을 포함한 소화관의 비자발적 수축을 자극한다. 미주신경의 체감각 섬유는 귀 뒤의 피부, 이도의 외부 부분 및 인후의 특정 부분으로부터 감각 정보를 받는 반면, 내장 감각 섬유는 후두, 식도, 폐, 기관으로부터 감각 입력을 전달한다. 심장 및 대부분의 소화관. 혀뿌리 부근의 미각은 미주신경의 특수 감각 섬유를 통해 전달된다[13].
혀인두신경과 미주신경은 삼차신경보다 더 가늘고 길다. 혀인두신경의 평균 직경은 약 1.2±0.3 mm인 반면 미주신경은 2.84 mm이며, 삼차신경이 메켈 동굴(Meckel’s cave) 근처 삼차신경절 부위에서는 최대 9.7 mm (4.6-9.3 mm)에 이를 수 있다[14,15]. 뇌간에서 출발한 혀인두신경은 16.2±1.9 mm 정도를 주행하며, 삼차신경의 뇌내 주행 길이는 9.66±1.71 mm 정도이다[16,17]. 미주신경은 5-6개의 신경 다발로 구성되며 그 중 혀인두신경측 2-3개가 감각 신경이고, 나머지 2-3개는 운동 신경으로 알려져 왔다[18]. 그러나 최근 전기 생리적 검사를 통해 신경의 기능을 확인한 보고에 의하면, 혀인두신경측 2-3개 감각신경이 실제 순수 감각 신경인 경우가 50% 정도일 뿐이며, 약 50% 정도의 경우에서 운동 반응을 같이 보였다. 이러한 검사 소견은, 감각 신경이라고 절단한 경우에 운동 기능장애가 초래될 수 있다는 의미이며, 미주신경의 운동 분지는 생명 유지에 중요한 뇌신경이라는 점을 고려할 때의 잘라서는 안된다는 점에서 중요한 의미가 있다[3,9].
혀인두신경 기시부에 대한 혈관 압박이 혀인두신경통의 원인으로 인정되고 있다[1,8,9]. 이차성 혀인두신경통의 원인으로, 소뇌교각부 종양, 감염, 다발성 경화증, 파제트병, 외상, 치과 시술 등이 보고되고 있다[19-21]. 특별한 원인이 없는 진성 특발성 혀인두신경통은 매우 드물다. 혀인두신경통이 워낙 드물다 보니, 어느 정도 퍼센트의 혀인두신경통 환자가 신경 혈관 압박에 기인하는지를 조사한 보고는 아직 없다.
혀인두신경통에서 신경근기시부(root entry zone, REZ)의 혈관 압박은, 안면경련증(반얼굴연축, hemifacial spasm)이나 삼차신경통의 경우와 유사하게 신경초(myelin)를 미세하게 파괴해서 전기연접전달(ephaptic transmission)을 유발할 수 있다[12,22]. 혈관 압박 그 자체가 혀인두신경과 관련된 핵 구조 변화를 유발할 수 있는지는 분명하지 않지만, 신경 과흥분성을 초래하는 탈수초화 및 결과적인 전기연접 전달이 혀인두신경통의 병인으로 보고 있다. 혀인두신경통에 대한 미세혈관감압술의 높은 수술 성공률(90-95% 이상)도 이러한 가설을 지지하는 소견이다[8,23]
진단은 임상 증상에 근거해서 이루어지며, 치료는 정확한 진단에서 시작한다. 드물게 발생하다 보니, 가능성을 염두에 두고 있지 않다면 삼차신경통으로 오진할 수도 있겠다. 진단이 되면, 질환의 자연 경과, 치료 옵션, 가능한 합병증 및 예후를 예측할 수 있다. 증상은 혀인두신경, 때때로 미주신경의 감각 분포 영역에서 나타나게 된다(Table 1).
증상 양상은 삼차신경과 같이 칼로 찌르는 듯한, 전기가 오는 듯한 짧은 발작적 통증이 특징적이다[6]. 통증은 혀인두신경이 분포하는 혀 후방부, 편도선, 인두 또는 아래턱 부근 및 깊은 귀속 부위 등에서 발생한다(Table 1) [1-3]. 환자의 절반 이상이 동측 귀 깊은 곳으로 향하는 듯한 방사성 신경통을 호소하는데, 묻지 않으면 환자가 얘기하지 않는 경우도 종종 있다. 또한, 눈, 코, 턱 또는 어깨를 포함한 다른 부위 방사통을 동반할 수 있고, 삼차신경통의 일부 증상과 유사하게 나타나서, 진단이 어려운 경우도 있다. 혀인두신경통과 삼차신경통은 씹기, 말하기 또는 양치질을 포함하여 동일한 유발 동작을 공유할 수 있지만 혀인두신경통에는 목구멍, 깊은 귀 또는 깊은 목구멍 등이 포함되는 특징이 있다. 혀인두신경통 증상은 치과 질환, 삼차신경통 또는 기타 다양한 비정형 안면 통증 증후군과 구분되어야 한다. 설인신경 분포의 일부가 삼차신경의 하악 분지 분포와 겹칠 수 있기 때문에 혀인두신경통과 삼차신경통의 구분이 어려운 경우도 있다[1-3].
혀인두신경통 증상에 미주신경의 감각 분지 증상을 포함하는 경우가 적지 않아서, 서맥, 심장무수축 또는 저혈압 등과 같은 심혈관 증상을 동반하다 보니 혀인두신경통이라는 진단명에 대한 논란이 있다[8,20,21]. 서맥, 실신, 저혈압 또는 심정지와 같은 미주신경 증상은 혀인두신경통 환자의 약 10%에서 발견된다[22,24,25]. 미주신경 증상으로, 삼키기 어려움, 쉰 목소리 또는 말하거나 마시는 동안 발작성 기침 등이 있고, 기침할 때 통증 발작이 발생하는 경우도 있다. 혀인두신경통의 가장 흔한 증상 중 하나인 깊은 목구멍의 통증이 혀인두신경과 미주신경의 체성 감각 성분 모두에 의해 설명될 수 있어 미주-혀인두신경통(vago-glossopharyngeal neuralgia)이라는 용어가 혀인두신경통보다 더 타당하다[26]. 30개의 증례 분석 결과, 혀인두신경과 미주신경이 동시에 원인인 경우가 혀인두신경 단독이 원인인 경우보다 더 많았다[1].
진단과 수술 전 검사로 MRI 영상 검사, 안면신경 및 청각 신경의 기능 검사 등이 필요하다. 안면신경의 기능을 미리 확인하기 위해, 운동신경전도속도(motor nerve conduction velocity)를 포함하는 근전도검사(electromyography)를 수술 전에 시행하고, 증상을 유발하는 말초 병변의 감별을 위해 순음청력검사, 음성청력검사, 임피던스 청력검사 등의 이비인후과적 평가도 필요하다. 증상을 유발하는 원인 혈관과 혀인두신경 및 미주신경과의 관계를 확인하기 위해 MRI 및 자기공명혈관조영(magnetic resonance angiography) 및 컴퓨터단층혈관조영(computed tomography angiography) 등이 필요하다. MRI는 1.5 T (Sigma EXCITE; General Electronics, Boston, MA, USA) 또는 3.0-T (Achieva; Philips, Best, The Netherlands) 등을 이용한 감사가 시행된다[1,3]. MRI 검사에서 원인 혈관이 혀인두 및 미주신경을 압박하는 원인 혈관이 관찰되는 경우가 대부분이지만, 원인 혈관이 분명하지 않은 경우도 있다(Figure 1).
한 환자에서 삼차신경통과 혀인두신경통의 동시에 발현될 수도 있다. 두 질환이 동반된 환자라고 해도 더 극심한 증상만 얘기하고, 나머지 한 질환의 증상은 무시하고 얘기하지 않을 수 있다. 통상 혀인두신경통 통증이 더 심하다 보니, 삼차신경통을 놓치는 경우가 있다. 둘 중 하나의 진단이 다른 하나의 자동 치료를 의미하는 것이 아니라는 점을 환자는 모르기 때문에, 두가지 질환의 동반 여부는 진료시에 확인할 필요가 있고, 증상이 시차를 두고 발현되는 경우도 있다. 두 질환이 동반된 환자는 두 질환에 대한 각각의 미세혈관감압술을 요하므로 다른 증상 여부도 미리 문진해야 한다. 혀인두신경통과 삼차신경통이 모두 있는 개인이 초기에 혀인두신경통 증상과 함께 전형적인 삼차신경통 증상을 보인다면 혀인두신경통 진단이 간과될 수도 있다. 비정형 혀인두신경통은 미세혈관감압술이 통상 도움이 되진 않지만, carbamazepine에 반응하는 제한된 경우에서 통증 완화에 효과가 있다는 보고가 있어, 경과를 보면서 치료 방향을 결정할 필요가 있다[27].
진단의 중요성은 아무리 강조해도 과하지 않다. 저자 병원에서도 혀인두신경통 환자를 삼차신경통으로 오진한 사례가 있다[3]. 그 환자는 혀인두신경통을 암시하는 전형적인 통증을 호소했지만, 삼차신경통으로 오진하여 삼차신경통 미세혈관감압수술을 받게 되었다. 통증은 수술 후에도 전혀 호전되지 않았으며, 자세한 재문진을 통해 그가 처음 설명했던 통증의 특징을 첫 진료에서 무시했던 것을 알게 되었다. 이 환자는 혀인두신경통에 중요한 진단적 가치가 있는 동측 귀 깊숙한 곳의 방사통도 동반된 전형적인 혀인두신경통 환자였지만, 그 가능성을 전혀 고려하지 않았던 것이 오진의 이유였다. 혀인두신경통에 대한 미세혈관감압수술을 받은 후 통증은 완치되었다. 환자는 같은 부위에 대한 개두수술을 2번 받게 된 것이다. 이 환자의 경험으로 얻은 교훈은 다음과 같다. (1) 안면 통증에 혀인두신경통도 있을 수 있다는 점을 항상 염두에 둬야 한다. (2) 극심한 안면 통증 환자에서 다른 안면 통증의 동반 여부를 확인해야 하며, 그 반대의 경우도 마찬가지이다. (3) 전형적인 혀인두신경통과 전형적인 삼차신경통은 통증 유발 요인이 있고, 통증 유발 요인이 없다면 비정형 혀인두신경통 또는 비정형 삼차신경통일 가능성이 높다. (4) 혀인두신경통과 삼차신경통의 구분은 중요하다. 주 증상이 혀 아래에 있을 경우에는 동반 증상의 특징과 통증 부위를 확인해야 한다. 동반되는 증상 부위가 혀인두신경통 진단에 중요하다. (5) 삼차신경통과 혀인두신경통의 공존도 염두에 두고 있어야 한다[3].
삼차신경통에 효과가 입증된 약물은 혀인두신경통에도 적용할 수 있다. 약물 치료의 목표는 신경병성 통증을 완화시키는 것일 뿐, 완치를 위한 것이 아니다. 통상, carbamazepine(300-1,000 mg)을 먼저 투여해 보고, oxcarbazepine(300-1,200 mg), gabapentin(1,800-3,600mg) 또는 pregabalin (150-600 mg) 등의 다른 요법을 시도할 수 있다[28,29]. 심혈관 증상이 동반된 경우 아트로핀(atropine)을 투여할 수 있지만 통증 완화에는 도움이 되지 않는다.
약물 치료는 삼차신경통에 사용하는 약제와 크게 다르지 않으므로, 여기서는 더 언급하지 않고, 대신 혀인두신경통에 대한 미세혈관감압술, 선택적 뇌신경근 절개술(selective cranial nerve rhizotomy) 및 감마나이프 방사선 수술(gamma knife radiosurgery, GKRS) 등과 같은 약물 치료에 반응하지 않는 환자에 적용 가능한 치료법을 소개하고자 한다.
미세혈관감압술은 수술현미경이 개발되면서 가능하게 된 신경외과 수술 치료법 중 하나이다. 뇌신경과 미세혈관과의 상호 관계로 인한 질병을 치료하는 정교한 치료법이다. 이 수술법은 Jannetta [5]에 의해 삼차신경통과 안면경련증에 적용되면서, 뇌신경과 혈관이 관련한 질환을 완치시키는 치료법으로 인정받게 되었다[23,25,30]. 삼차신경통과 안면 경련증에 적용한 미세혈관감압술 결과에 고무된 Jannetta 교수는 1977년에 혀인두신경통에 이 수술법을 적용하였다[9]. 혀인두신경통의 수술 완치율은 50-100%로 보고되나(2014), 장비, 수술자의 경험, 신경생리학적 모니터링 여부 등에 따라 성적이 크게 좌우된다[3,8,31].
혀인두신경 및 미주신경의 신경근기시부에 대한 감압이 핵심인, 미세혈관 감압 수술은 뇌신경과 혈관의 분리가 기본이지만, 궁극적으로 뇌신경에 전달되던 불필요하고 자극적인 혈관의 박동 신호(pulsating signal)를 제거해 주는 것이 그 목표이다. 완치된 상태를 장기적으로 유지하기 위해서는 뇌신경과 혈관의 물리적 분리를 유지하는 것이 필수적이다. 수술 성적은 뇌신경 주변의 미세동맥 여부이며, 이 미세동맥 존재 여부에 따라 영향을 받을 수 있다.
저자의 기관에서는 모든 미세혈관감압술에는, 컴퓨터단층촬영 유도 내비게이션 시스템을 활용한 후두하 개두술(retromastoid craniotomy)을 시행한다(Figure 2). 두개골 제거술과 비교할 때, 자가 두개골을 원위치에 다시 고정시켜 주므로, 수술 후 두통의 발생률이 현저하게 낮고, 제거된 두개골 부위 관련 합병증의 발생을 줄일 수 있다. 뇌간과 뇌신경의 기능을 확인하기 위해 수술 중 뇌간 청각유발전위와 감각유발전위(Viasys Healthcare, Conshohocken, PA, USA)를 이용한다. Lateral suboccipital infra-floccular approach는 충분한 수술 시야 확보에 충분하므로 더 큰 개두술이 필요 없었다[1,3,31]. Transcondylar fossa 접근법은, 절개 범위가 더 크지만 기존 수술법을 능가하는 장점이 없다. 수술 난이도와 성적은 미세 혈관의 존재 여부와, 그 혈관의 어려움을 극복하느냐 여부이며, 절개 규모는 무관하다[1,3]. 수술 부위 주변은 조직 건조를 방지하기 위해 식염수에 적신 거즈로 덮어 보호해 준다. 자세한 수술법은 기술하지 않지만, 수술에 대한 기본적인 원칙을 가지고 수술하는 것이 필요하다. 혀인두신경의 신경근기시부가 노출되면 4가지 수술 기법 중 하나를 적용하여 감압한다: (1) 테프론(Teflon)을 사용한 단순 혈관 전위, (2) 코팅된 테프론을 사용한 혈관 전위, (3) 테플론을 이용한 혈관 신경 분리(기존 방법과 유사하나 신경근기시부를 최대한 비워주는 방법), (4) 정맥이 원인인 경우, 정맥 소작. 저자의 경우에는 특발성 혀인두신경통의 경우, 신경 절단 또는 손상 유발은 치료 목적으로 수행하지 않는다[1-3].
혀인두신경과 미주신경이 삼차신경보다 가늘고 길어서, 이에 대한 미세혈관감압술은 삼차신경통보다 더 위험하다. 설인-미주 신경의 신경근기시부는 삼차신경보다 두개골 기저부 쪽으로 더 아래쪽에 위치하므로 개두 부위도 더 아래쪽으로 확장되어야 한다[1-3]. 설인신경과 미주신경의 이러한 해부학적 특징은 미세혈관감압술 수술 난이도에 영향을 주는 요인이다. 이러한 이유로 1차 수술로 인해 유착이 유발되어 있고, 테프론 등의 이물질이 들어가 있는 상태에서 시행되는 재수술은 더 위험할 수밖에 없다. 그래서 첫 수술이 중요하며, 재수술을 피하는 것이 좋다[1-3].
전치(transposition) 기반의 혀인두신경통 미세혈관감압술 결과에 대한 코호트 보고는 아직 없다. 자체 결과에 의하면, 본 기관에서 시행한 총 78개 증례의 혀인두신경통 환자(6개월 이상의 경과 추적) 분석에서, 76명(97.4%)에서 통증 없음(Barrow Neurological Institute grading scale 1, BNI 1 등급), 간헐적 통증(BNI 2 등급)의 소견을 보였다[3]. 5년 이상 추적된 49개 증례 중 48명(97.9%)이 1년 내에 BNI 1 또는 2 등급이 되었다. 예전 분석에서는 수술 직후에 BNI grade 3에 속한 경우가 8/48개 증례였지만, 그 중 7명은 1년 내에 BNI grade 1 또는 2로 호전되었다. 한 증례에서 BNI 3 등급에 머물면서 겨울과 계절이 바뀔 때 약물 복용이 필요했지만, 추적하면서 전형적인 통증은 호전되고, 남아 있는 증상은 비정형 통증이었다. 삼킴 곤란, 발성 장애, 청력 감소와 같은 일시적인 합병증을 경험한 환자가 3/78명 있었고, 수개월이 경과하면서 완전 회복되었다. 사망이나 영구적인 합병증이 발생한 증례는 없었고, 미주신경 관련 합병증도 없었다[3].
저자의 경우, 수술적 치료가 시행된 특발성 혀인두신경통 환자 78개 증례 중 76개 증례에서 혀인두신경 단독 또는 혀인두신경과 미주신경의 신경근기시부가 동시에 혈관에 의해 압박된 소견을 확인했다[3]. 미세혈관감압술 동안 2개 증례에서는 명확한 원인 동맥이 보이지 않았으나, 원인이 없다고 할 수는 없었다. 그 이유는 2개 증례 중 1명에서 지주막이후하소뇌동맥(posterior inferior cerebellar artery)을 신경근기시부에 묶여 있어서(tethering), 그 지주막이 고정된 것을 풀어준 후 후하소뇌동맥이 신경근기시부를 압박하지 않게 되었기 때문이다. 삼차신경 미세혈관감압술보다는 빈도가 낮지만, 뇌신경 주변의 지주막을 넓게 박리만 해 준 경우에도 환자가 증상이 호전된 경우가 있다는 점이 그러한 가정을 뒷받침한다[3]. 다른 한 증례는 신경근기시부 주변에 작은 동맥들이 존재했고, 이러한 세동맥을 분리해 증상이 호전된 것으로 생각되며, 4년 이상의 추적 기간 동안 재발은 없다. 특발성인 경우라도, 혀인두신경통 원인 혈관에 대한 탐색이 완전하지 못하여 그렇게 명명되었을 가능성도 있다. 미세혈관감압술 동안 혀인두신경과 미주신경 전체 주행을 확인하는 것은 수술 성공률을 높이는 데 중요하다. 미주신경 압박이 통증의 원인이 아니라고 판단하고, 혀인두신경만 감압해 주면 혀인두신경통 유무에 관계없이 삼키기 어려움이나 발작성 기침과 같은 미주신경 증상이 남을 수 있고, 혀인두신경 감압에 의해 유발된 혈관 주행의 변화에 의해 예상치 못하던 미주 증상이 더 심해질 수도 있고, 이러한 증상이 생명을 위협할 수도 있으므로, 미주신경의 주행까지 수술 시야에서 확인해야 한다[3].
코호트 연구에서 보고된 삼차신경통에 대한 미세혈관감압술의 성공률(80-85%)이 안면경련증(90%)보다 다소 낮지만, 혀인두신경통 미세혈관감압술 성공률은 95% 정도로 현저하게 높다[3,32-34]. 혀인두신경과 미주신경 관련 질환이므로 수술 위험도가 삼차신경통 수술보다 높지만, 혀인두신경 및 미주신경의 해부학적 특징과 경정맥공을 제외하고 이를 둘러싸는 뼈 구조가 단순하기 때문에 혀인두신경통에 대한 미세혈관감압술의 성공률이 높다고 볼 수 있다. 그래서, 수술 위험성을 잘 극복하면서 미세혈관감압술이 이루어진다면 삼차신경통보다 혀인두신경통의 대한 장기 치료 성적이 더 높을 가능성이 있다. 한편, 혀인두신경통 재수술은 혀인두신경 및 미주신경의 해부학적 특징을 고려할 때 반드시 피하려고 노력해야 한다. 왜냐하면 삼차신경에 비해 혀인두신경과 미주신경은 훨씬 더 가늘며, 이들 신경에 대한 손상은 돌이킬 수 없는, 때로는 생명을 위협하는 결과를 초래할 수 있다. 신경과 혈관 사이에 테프론을 삽입해 주는 수술법으로 대변되는 단순 interposition만으로 장기적인 완치 성적을 확보할 수 없기 때문에, 전치(transposition) 기법을 시행해야 한다. 어떤 수술법을 적용하든 미세동맥은 절대 보존해야 하며, 수술 중 혈관 경련을 예방하기 위해서는 혈관 조작을 최소한으로 제한해야 한다[3].
Jannetta 등은 원래 삼차신경통, 안면경련증 및 혀인두신경통에 대해 문제가 되는 동맥과 신경근기시부 사이에 절연 물질(insulating material)로 테프론을 삽입하는 interposition을 제안했다[5,9]. 절연 물질이 혈관의 위치, 즉 신경근기시부에서 이동되는 경우 interposition보다 전치 기법이 더 이상적이다. 다만, 원인이 되는 혈관의 힘 벡터가 변하지 않는, 절연 물질의 단순 삽입으로 혈관과 신경근기시부를 분리했다면 증상은 완치되기 어렵거나 재발할 수 있다[3]. 테프론을 이용한 전치수술(transposition using Teflon pieces)에 이용되는 전치 기법은 테프론 조각을 삽입해 분리시키는 것이 아니라 혈관의 위치와 혈류의 방향을 바꾸는 것이다. 원인 혈관의 물리적 압박뿐만 아니라 힘 벡터의 방향이 바뀌기 때문에, 원인 혈관의 박동성 힘으로부터 신경근기시부가 해제되므로, 증상은 완치되고 재발도 방지할 수 있다[3]. 이 기법은 ‘신경근기시부에서 벗어난 위치(off the REZ)’로 특징지을 수 있는데, 이는 원인 혈관이 신경근기시부에서 없어지게 되었기 때문이며, 테프론 조각이 off the REZ 상태를 유지하기 위해 사용될 때 테프론 조각도 off the REZ에 배치된다. 이 off the REZ 원칙은 ‘전위’의 기본 요건이다[3]. 테플론은 화학적으로 안정된 물성을 가지고 있으나, 수십 년 후에도 맥동하는 뇌척수액과 접촉해도 안정적으로 유지되는지는 분명하지 않기 때문에, 이 물질을 사용하더라도, 뇌신경 위에 올려 두지 말자는 것이다. 이러한 방법의 수술이 시행된 환자에서, 혀인두신경의 신경근기시부를 압박하는 원인 혈관이 테프론에 의해 분리되어 있는 소견을 확인할 수 있다(Figure 3) [3].
원인 혈관이 구불구불하거나 동맥 경화를 동반하거나, 큰 혈관인 경우 테프론 조각을 사용한 단순한 전위로는 충분한 감압이 어렵다. 이런 경우에, 테프론 슬링을 이용한 전치수술(transposition using a fibrin glue coated Teflon sling)이 적용된다[3]. 이 기법을 이용하면 신경근기시부가 어떠한 압박도 받지 않도록 혈관의 방향을 안정적으로 변경하고 경막 또는 뇌간의 상단에 고정해 줄 수 있다[3]. 이를 위해 접착제(bioglue, tisseel 등)로 코팅된 테프론 슬링을 수술 중에 집도의가 수작업으로 제작하여 사용한다(Figure 4) [3]. 과정을 간단히 설명하면(Figure 5), 여러 개의 테플론 섬유를 길게 준비한다. 정전기 발생을 줄이고 조작을 쉽게 하기 위해 물을 뿌린 천 위에 올린다, 피브린 접착제를 천 위에 올려둔 테프론 섬유에 뿌려 준 후, 손가락을 이용하여 꼬아 줘서 길쭉한 가닥을 만든다[3]. 슬링의 길이와 두께는 집도의의 의도와 환자의 상황에 따라 조정이 가능하다. 수술 부위가 좁고 공간이 좁은 곳에서의 전위를 위해 사용하게 되므로, 테프론이 질기고 탄성이 좋다는 점을 고려하여 슬링을 두껍게 만들지 말고, 신경근기시부에 압박의 2차 원인이 되지 않게 가늘게 만들면 된다. 슬링이 원인 동맥을 둘러싸게 하고, 슬링의 끝을 추체 경막을 포함하는 ‘신경근기시부에서 벗어난 위치(off the REZ)’ 또는 뇌간 위에 피브린 글루와 타코실(San Diego, CA, USA) 조각을 사용하여 고정해 주면 된다. 이런 고정이 충분하지 않다면 추체경막에 한두 개의 봉합을 포함한 추가 고정을 해 줄 수 있다. 또한 테플론 조각은 테플론 슬링을 지지하는 데에도 사용할 수 있으며 역시 ‘신경근기시부에서 벗어난 위치’에 배치해야 한다.
드물지만 신경근기시부를 압박하는 울혈된 정맥이 원인인 경우도 있다[3]. 정맥이 삼차신경통의 원인인 경우가 6-18% 정도로 보고되고 있지만, 동일한 병인이 예상되는 혀인두신경통의 원인으로 정맥이 기여할 수 있다. 정맥이 측부정맥들과 풍부하게 연결되어 있으므로, 신경근기시부에 있는 충혈된 정맥이 있다면, 소작 및 절단을 해 줘야 한다(Figure 6) [3]. 정맥 소작술 후 신경학적 이상 없이 증상이 없어지며[35], 출혈이나 허혈성 사건은 동반되지 않았다.
Dandy [8]는 1927년 처음 두개내 혀인두신경근절제술(Selective glossopharyngeal nerve rhizotomy)을 시행하고, 즉각적인 결과는 좋았으나 재발이 잦았다고 보고했다. 이러한 장기 결과를 개선하기 위해 그는 혀인두신경에 추가적으로 미주신경의 감각 분지의 일부를 잘라주는 수술법을 적용하기 시작했다[36]. 미주신경의 상부 감각 분지를 절제한 후 관련 합병 증상으로 자극성 기침, 인후의 이물감, 쉰 목소리, 연하곤란 등이 발생했다[37]. 그러나, 미세혈관감압술 454건과 혀인두신경절제술 157건에 대한 결과를 리뷰한 문헌 보고에서 수술의 영구적인 합병증(19.1%)이 혀인두신경절제술 없이 시행한 미세혈관감압술(5.1%)보다 3배 더 컸다고 보고했다[37]. 또한, 103명의 혀인두신경통 환자에서 부분적인 미주신경 절제술을 동반하거나 하지 않은 선택적 혀인두신경절제술 환자에 대한 분석 연구에서, 통증 완화와 즉각적인 합병증이 두 그룹 간에 유의미한 차이가 없다고 보고한 반면, 부분 미주신경 근절제술을 받은 혀인두신경절제술 후 장기적인 합병증은 35.8%로, 미주신경 rhizotomy 없이 혀인두신경절제술을 시행한 경우(3.8%)보다 훨씬 더 많았다[37]. 저자들은 미주신경 rhizotomy가 없는 혀인두신경절제술은 혀인두신경통에 대한 안전하고 효과적인 치료 옵션이라고 주장하지만, 높은 장기 합병증 발생률을 고려할 때, 그 결론에 동의할 수 없다. 한편, 수술 중 전기 생리학적 검사를 적용한 혀인두신경통 수술 환자에서, 미주신경의 해부학 특성에 대한 연구 보고에 의하면, 근위 2-3개의 가지가 감각신경 가지이고 나머지 3-4가지가 운동신경가지라는 일반적인 지식이 사실이 아닐 수 있음을 시사했다. 그들은 50%의 피험자에게 수행한 검사에서, ‘순수한 감각’ 잔뿌리가 없고 ‘순수한 감각’ 잔뿌리를 소유한 나머지 50%에서는 근위 2-3개가 아니라 가장 근위에 있는 한 개의 가지만 순수 감각신경일 가능성이 높다고 보고했다[9]. 이러한 연구 결과는, 미주신경의 일부를 치료 목적으로 자르거나, 파괴되기 전에 철저하고 주의 깊은 전기생리학적 검사가 선행되지 않으면, 매우 심각한 장애를 초래할 수 있다는 것을 의미한다. 이러한 보고를 고려할 때, 아무리 부분적일지라도 미주신경 신경근 절제술은 절대 시행하지 말아야 한다.
Lazorthes와 Verdie [10]의 첫 번째 보고를 시작으로 경피적 고주파 열응고술은 여러 저자들에 의해 시도되었으나 미주신경, 경정맥 및 내경동맥 주변의 시술이라 위험하며, 삼킴 곤란, 성대 마비, 심지어 심혈관 사건을 포함한 다양한 합병증 들이 발생할 수 있기 때문에 대중적인 시술이 되지 못했다[38-41]. 저자의 의견으로는 혀인두신경통 미세혈관감압술 동안 치료 보조 목적으로, 신경근절제술을 추가하는 것은 필요 없다고 생각한다[3]. 우리는 ‘off the REZ’ 원칙 하에 가장 단순한 방법의 미세혈관감압술을 시행해 주는 것이 비파괴적이며 완치 가능성이 높은 혀인두신경통에 대한 최선의 치료법이라고 믿고 있고 장기 추적 결과도 그러하다[3].
지난 20년 동안 삼차신경통에 대한 GKRS 경험을 바탕으로 Stieber 등[41]은 2005년에 혀인두신경통에 대한 GKRS 첫 치료 사례를 보고했다. 최근까지, 대규모 치료 성적을 보고한 사례는 없으며, 혀인두신경통이 매우 드물게 발생하기 때문이다[42-47]. 최근 22명의 혀인두신경통 환자가 6개의 학술 의료 센터에서 GKRS를 받은 국제 다기관 연구가 2016년에 발표되었다[44]. 단일 4 mm isocenter는 혀인두신경 고기 수준에서 혀인두신경을 대상으로 한 다음 중앙값 최대 선량 80 Gy (범위 80-90 Gy)로 방사선을 조사했다[44]. 그들은 방사선 치료 후 3개월 내에 완전 통증 완화(BNI 1등급)가 50% (11/22)에서, 개선된 결과(BNI 1,2, 3등급)가 73%(16/22)에서 관찰되었고 7년간 잘 유지된 환자는 28%였다. GKRS에 잘 반응한 16명 중 8명(50%)에서 증상이 재발하였다. 구개설궁의 감각 저하가 지속되었고 그 증상은 두 번째 GKRS 후에 발생했다. 21명 대상의 다른 연구에서 17/21명(81%)이 GKRS 후 통증이 사라졌으나 10/21명(58.8%)이 13개월 만에 재발했다[43]. 결국, 17명(81%)이 장기 추적(평균 5.2년)에서 통증 없이 혀 가장자리의 일시적인 감각 이상이 언급되었다. 치료 초기에 반응한 환자도 재발할 수 있으니, 추가적인 GKRS 치료가 필요할 수 있다.
우리나라에서는 2021년 12월부터 미세혈관감압술 대상이 되지 못하는 제한된 환자에서, 혀인두신경통의 대체 치료법으로 GKRS를 승인하고 있다[3]. GKRS가 혀인두신경통에 즉각적인 완치를 보장하지는 못하지만 통증 강도와 빈도를 감소시킬 수 있다는 점이 중요하다. 재치료가 필요할 수 있고 경과에 따라, 약물 치료도 필요하지만, GKRS는 전신 마취가 필요없이 국소마취 하에 시행할 수 있는 안전한 치료법이며, 재발률이 낮고 반복 치료가 가능하며 반복 치료가 안전하게 가능하다는 점에서 신경근 절제술보다 더 좋은 선택이 될 수 있다[3].
Figure 1.
Diagnostic magnetic resonance imaging (MRI) study. (A) pre-operative MR shows that the proximal PICA (red arrow) looped to the PICA (black arrowhead) compressing the IX nerve (yellow arrowhead). (B) Postoperative MRI shows that the position and trajectory of the PICA is altered (red arrow) and the root entry zone of the IX nerve became free from any vascular compression (yellow arrowhead). PICA, posterior inferior cerebellar artery; IX, glossopharyngeal nerve. Illustrated by the author.
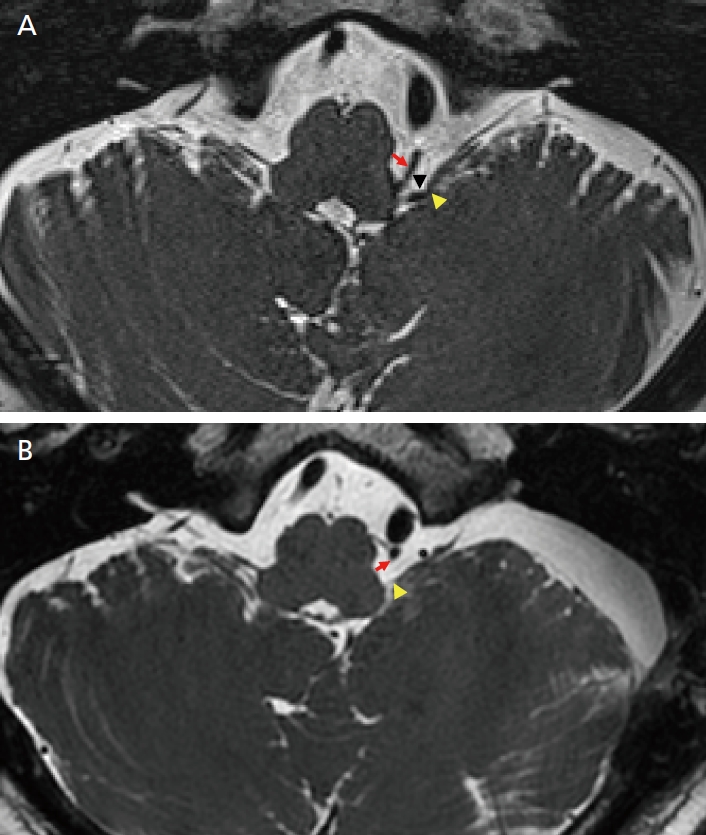
Figure 2.
Computed tomography (CT) navigation -guided craniotomy. (A) CT guided navigation for identification of the sigmoid sinus and mastoid air cells. (B) Postoperative 3-dimensional CT image showing the size and shape of the suboccipital craniotomy (yellow arrows), Scale bar: 1 cm. Illustrated by the author.

Figure 3.
Simple transposition using Teflon pieces. (A) Posterior inferior cerebellar artery (PICA) is compressing the root entry zone (REZ) (arrow) of the IX and X nerve. (B) The position and trajectory of the PICA is altered by the inserted Teflon, but Teflon is not located at the REZ (arrow) as an insulation material. Since Teflon was not used as an insulation material, we define this technique ‘transposition’. Informed consent for publication of the clinical images was obtained from the patient. IX, glossopharyngeal nerve; X, vagus nerve. Adapted from Park JS and Ahn YH. J Korean Neurosurg Soc 2023;66:12-23, according to the Creative Commons license[35].
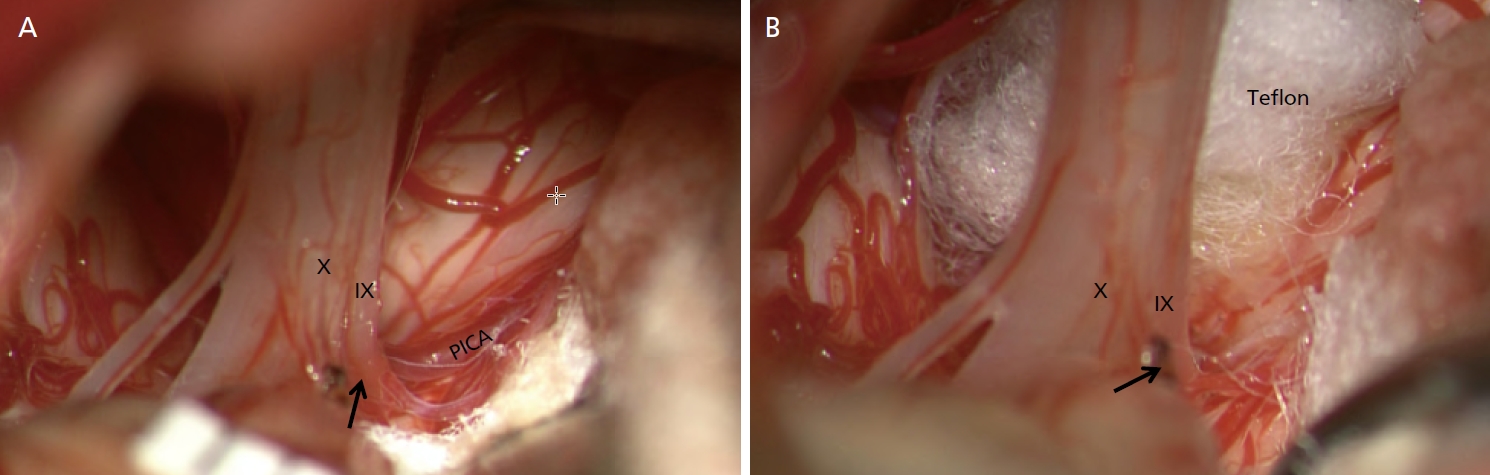
Figure 4.
Transposition using a Teflon sling. (A) Very tortuous Posterior inferior cerebellar artery (PICA) is compressing the root entry zone (REZ) of the IX and X nerves. (B) Tortuous PICA compressing the REZ and the cisternal portion of the CN IX-X complex. (C) A fibrin glue coated sling is lifting up PICA to change its position and trajectory off the REZ. We define this technique ‘transposition using a Teflon sling’. Informed consent for publication of the clinical images was obtained from the patient. IX, glossopharyngeal nerve; X, vagus nerve. Adapted from Park JS and Ahn YH. J Korean Neurosurg Soc 2023;66:12-23, according to the Creative Commons license[35].
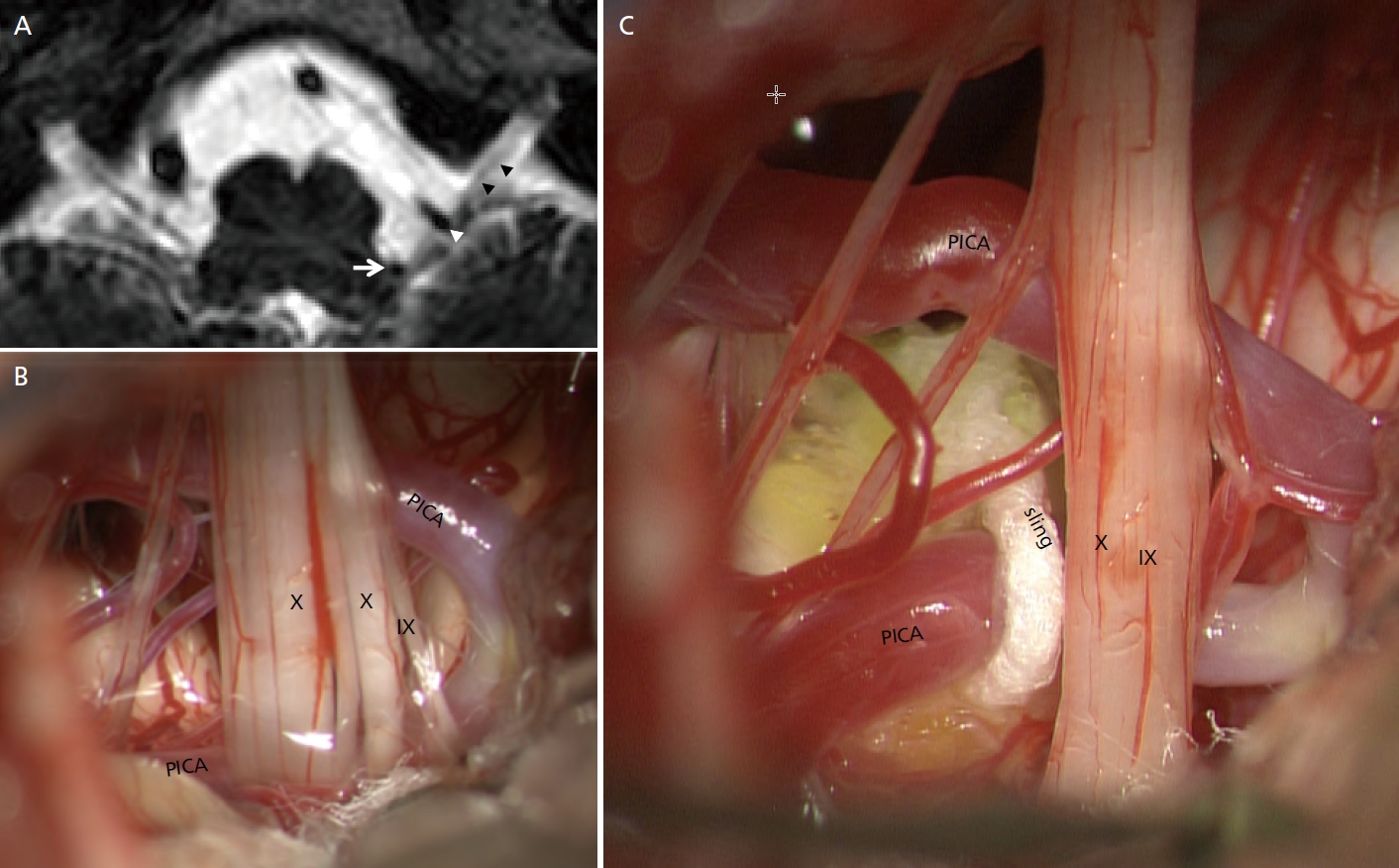
Figure 5.
Manual craft of bioglue-coated Teflon sling. (A) Dry pieces of Teflon fiber were prepared (one division of the visible ruler is 1 mm). A lot of lint from the Teflon fibers are observed. (B) A sling was made by spraying fibrin glue on a Teflon strand and twisting the fibrin glue coated Teflon. A Teflon sling became lintfree, smooth and easy to manipulate. Illustrated by the author.
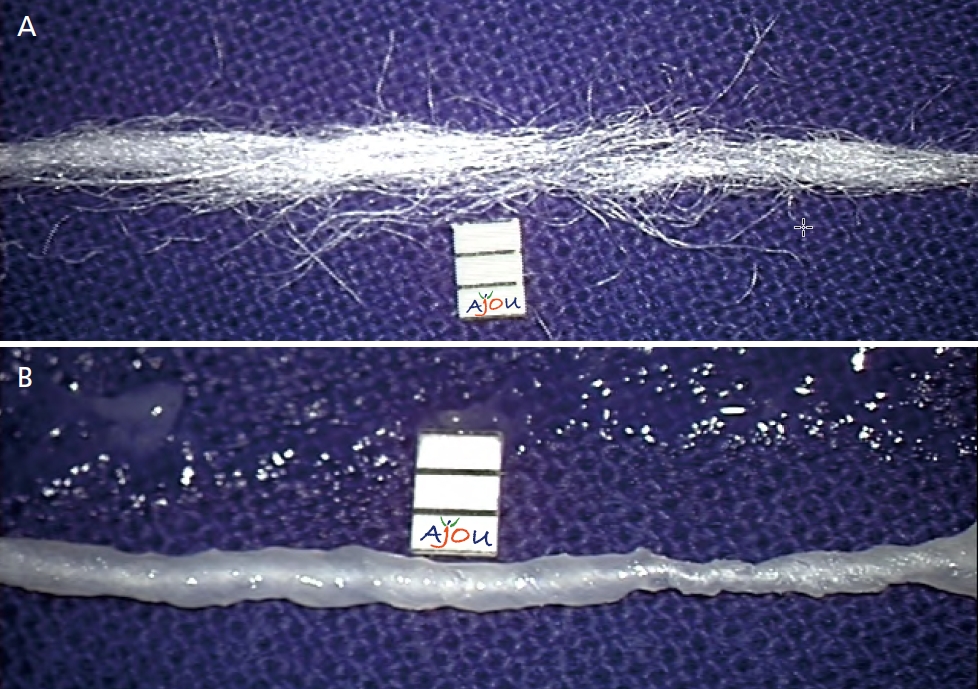
Figure 6.
Interposition of insulating material (IM). (A) Posterior inferior cerebellar artery (PICA) compressing the IX nerve. (B, C) While PICA being maneuvered, it appears unfeasible to transpose PICA to another position, owing to several perforators tethering PICA to the brain stem. (D) Teflon pieces are inserted between the root entry zone (REZ) and the vessel as an IM. Informed consent for publication of the clinical images was obtained from the patient. X, vagus nerve; IX, glossopharyngeal nerve. Adapted from Park JS and Ahn YH. J Korean Neurosurg Soc 2023;66:12-23, according to the Creative Commons license[35].
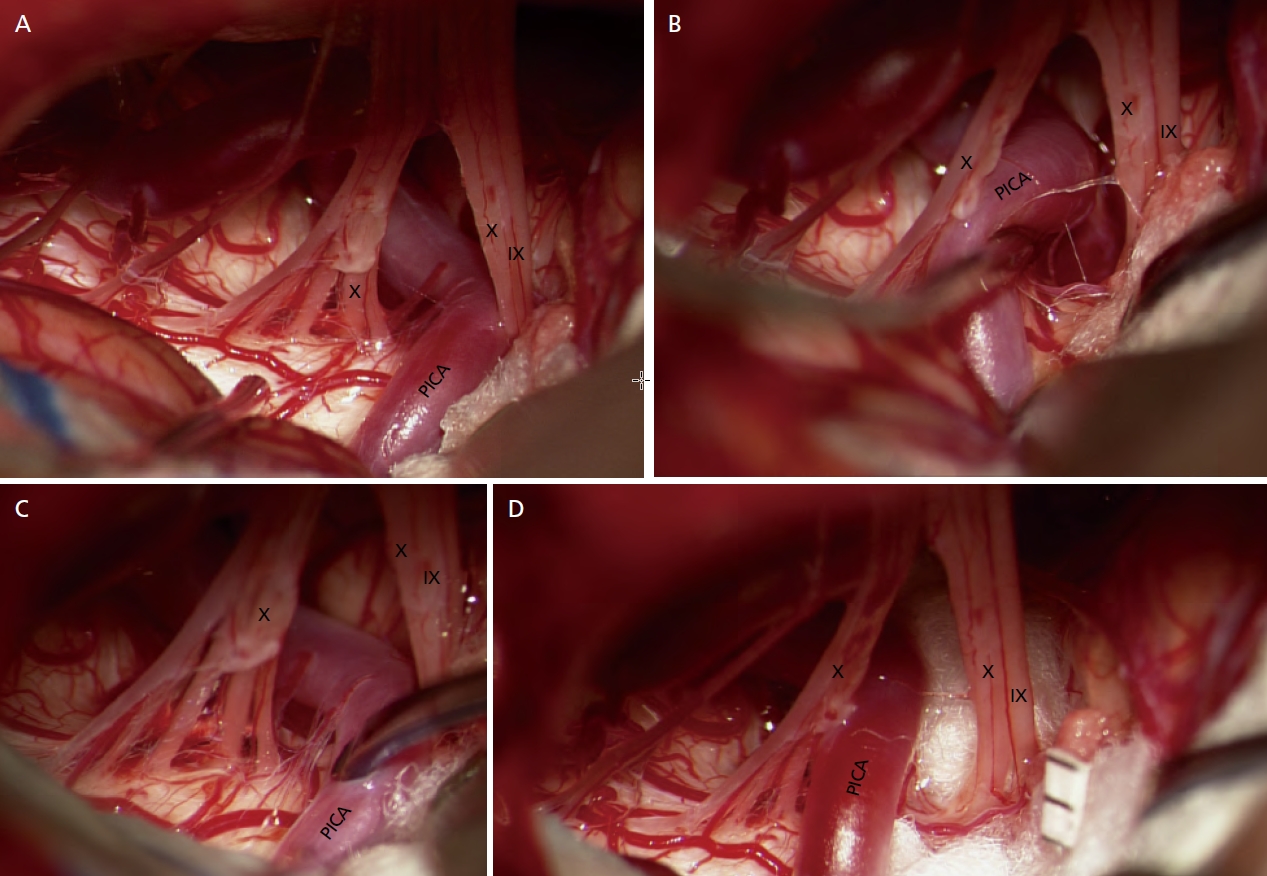
Table 1.
Diagnostic criteria of glossopharyngeal neuralgia
References
1. Kim MK, Park JS, Ahn YH. Microvascular decompression for glossopharyngeal neuralgia: clinical analyses of 30 cases. J Korean Neurosurg Soc 2017;60:738-748.




2. Lee SH, Park JS, Ahn YH. Bioglue-coated Teflon sling technique in microvascular decompression for hemifacial spasm involving the vertebral artery. J Korean Neurosurg Soc 2016;59:505-511.




4. Scholz J, Finnerup NB, Attal N, et al. The IASP classification of chronic pain for ICD-11: chronic neuropathic pain. Pain 2019;160:53-59.


5. Jannetta PJ. Microsurgical exploration and decompression of the facial nerve in hemifacial spasm. Curr Top Surg Res 1970;2:217-220.
6. Barbash GI, Keren G, Korczyn AD, et al. Mechanisms of syncope in glossopharyngeal neuralgia. Electroencephalogr Clin Neurophysiol 1986;63:231-235.


7. Rushton JG, Stevens JC, Miller RH. Glossopharyngeal (vagoglossopharyngeal) neuralgia: a study of 217 cases. Arch Neurol 1981;38:201-205.


8. Dandy WE. Glossopharyngeal neuralgia (tic douloureux): its diagnosis and treatment. Arch Surg 1927;15:198-214.

10. Lazorthes Y, Verdie JC. Radiofrequency coagulation of the petrous ganglion in glossopharyngeal neuralgia. Neurosurgery 1979;4:512-516.



11. Singh PM, Kaur M, Trikha A. An uncommonly common: glossopharyngeal neuralgia. Ann Indian Acad Neurol 2013;16:1-8.



12. Peris-Celda M, Oushy S, Perry A, et al. Nervus intermedius and the surgical management of geniculate neuralgia. J Neurosurg 2018;131:343-351.


13. Tew Jr J, Taha J; Percutaneous rhizotomy in the treatment of intractable facial pain (trigeminal, glossopharyngeal, and vagal nerves). Operative Neurosurgical Techniques: Indications, Methods, and Results. WB Saunders Co.; 1995.
14. Ajayi NO, Lazarus L, Satyapal KS. Trigeminal cave and ganglion: an anatomical review. Int J Morphol 2013;31:1444-1448.

15. Tubbs RS, Shoja MM, Loukas M. Anatomy of the glossopharyngeal nerve. In: Tubbs RS, Rizk E, Shoja MM, Loukas M, Barbaro N, Spinner RJ, editor. Nerves and Nerve Injuries; 2015. p. 371-383.
16. Kano H, Urgosik D, Liscak R, et al. Stereotactic radiosurgery for idiopathic glossopharyngeal neuralgia: an international multicenter study. J Neurosurg 2016;125(Suppl 1):147-153.

17. Wang C, Kundaria S, Fernandez-Miranda J, Duvvuri U. A description of the anatomy of the glossopharyngeal nerve as encountered in transoral surgery. Laryngoscope 2016;126:2010-2015. Nerves and Nerve Injuries.



18. Rey-Dios R, Cohen-Gadol AA. Current neurosurgical management of glossopharyngeal neuralgia and technical nuances for microvascular decompression surgery. Neurosurg Focus 2013;34:E8.

19. Krüger MT, Dong CC, Honey CR. Defining the anatomy of the vagus nerve and its clinical relevance for the neurosurgical treatment of glossopharyngeal neuralgia. Stereotact Funct Neurosurg 2019;97:244-248.



20. Sampson JH, Grossi PM, Asaoka K, Fukushima T. Microvascular decompression for glossopharyngeal neuralgia: longterm effectiveness and complication avoidance. Neurosurgery 2004;54:884-890.



21. Wang M, Chae R, Shehata J, et al. Comparative analysis of surgical exposure and freedom between the subtonsillar, endoscope-assisted subtonsillar, and far-lateral approaches to the lower clivus: a cadaveric study. J Clin Neurosci 2020;72:412-419.


25. Kakizawa Y, Seguchi T, Kodama K, et al. Anatomical study of the trigeminal and facial cranial nerves with the aid of 3.0-tesla magnetic resonance imaging. J Neurosurg 2008;108:483-490.


26. Sibilla L, Agarwal N. Cranial nerve IX: glossopharyngeal. In: Agarwal N, Port J, editor. Neuroimaging: anatomy meets function. Springer; 2018. p. 207-210.
27. Oishi M, Fukuda M, Noto Y, Kawaguchi T, Hiraishi T, Fujii Y. Trigeminal neuralgia associated with the specific bridging pattern of transverse pontine vein: diagnostic value of threedimensional multifusion volumetric imaging. Stereotact Funct Neurosurg 2011;89:226-233.



28. Giorgi C, Broggi G. Surgical treatment of glossopharyngeal neuralgia and pain from cancer of the nasopharynx: a 20-year experience. J Neurosurg 1984;61:952-955.

29. Nishihara K, Hanakita J, Kinuta Y, Kondo A, Yamamoto Y, Kishimoto S. Three cases of Eagle’s syndrome. No Shinkei Geka 1986;14(3 Suppl):441-445.
30. Harris W. Persistent pain in lesions of the peripheral and central nervous system. Br Med J 1921;2:896-900.



31. Sarlani E, Grace EG, Balciunas BA, Schwartz AH. Trigeminal neuralgia in a patient with multiple sclerosis and chronic inflammatory demyelinating polyneuropathy. J Am Dent Assoc 2005;136:469-476.


32. Chen J, Sindou M. Vago-glossopharyngeal neuralgia: a literature review of neurosurgical experience. Acta Neurochir (Wien) 2015;157:311-321.



33. Ma Y, Li YF, Wang QC, Wang B, Huang HT. Neurosurgical treatment of glossopharyngeal neuralgia: analysis of 103 cases. J Neurosurg 2016;124:1088-1092.


34. Patel A, Kassam A, Horowitz M, Chang YF. Microvascular decompression in the management of glossopharyngeal neuralgia: analysis of 217 cases. Neurosurgery 2002;50:705-711.


35. Yang KH, Na JH, Kong DS, Park K. Combined hyperactive dysfunction syndrome of the cranial nerves. J Korean Neurosurg Soc 2009;46:351-354.



36. Borius PY, Tuleasca C, Muraciole X, et al. Gamma Knife radiosurgery for glossopharyngeal neuralgia: a study of 21 patients with long-term follow-up. Cephalalgia 2018;38:543-550.



37. Manzoni GC, Torelli P. Epidemiology of typical and atypical craniofacial neuralgias. Neurol Sci 2005;26 Suppl 2:s65-s67.



38. Hardy DG, Rhoton AL Jr. Microsurgical relationships of the superior cerebellar artery and the trigeminal nerve. J Neurosurg 1978;49:669-678.


39. Kong Y, Heyman A, Entman ML, Mcintosh HD. Glossopharyngeal neuralgia associated with bradycardia, syncope, and seizures. Circulation 1964;30:109-113.


40. Sindou M, Henry JF, Blanchard P. Idiopathic neuralgia of the glossopharyngeal nerve: study of a series of 14 cases and review of the literature. Neurochirurgie 1991;37:18-25.

41. Stieber VW, Bourland JD, Ellis TL. Glossopharyngeal neuralgia treated with gamma knife surgery: treatment outcome and failure analysis: case report. J Neurosurg 2005;102 Suppl:155-157.

42. Linskey ME, Ratanatharathorn V, Peñagaricano J. A prospective cohort study of microvascular decompression and Gamma Knife surgery in patients with trigeminal neuralgia. J Neurosurg 2008;109 Suppl:160-172.


43. Stanic S, Franklin SD, Pappas CT, Stern RL. Gamma knife radiosurgery for recurrent glossopharyngeal neuralgia after microvascular decompression. Stereotact Funct Neurosurg 2012;90:188-191.



44. Breeze R, Ignelzi RJ. Microvascular decompression for trigeminal neuralgia: results with special reference to the late recurrence rate. J Neurosurg 1982;57:487-490.

46. White JC, Sweet WH. Pain and the neurosurgeon: a forty-year experience. CC Thomas; 1969.
Peer Reviewers’ Commentary
얼굴 부위 통증의 대표적인 원인은 5번 뇌신경의 문제인 삼차신 경통이고, 그보다 드물지만 9번과 10번 뇌신경의 문제로 발생하는 혀인두신경통이 있는데, 삼차신경통과 감별진단이 어려운 경우도 많다. 통증이 있는 부위가 중첩되기도 하고, 두 질환이 공존할 수도 있으며, 진단은 환자의 호소를 근거로 이루어지는데, 환자의 표현이 부정확하여 오진하기도 한다. 약물 치료로 상당 부분 초기에 증상 호전을 가져오지만, 시간이 지나며 약물 효과가 줄어들거나, 약물의 부작용이 심하여 충분한 용량을 쓰기가 힘든 경우가 많다. 이때 90% 이상의 성공률을 가진 신경외과적 수술을 시행해볼 수 있고, 미세혈관감압술이 대표적이다. 다른 뇌신경에 의한 질환에서의 미세혈관감압술에 비해 더 난이도가 높아, 혀인두신경통은 진단부터 치료까지 대부분 과정이 쉽지 않다. 이 논문은 기초 지식과 오랜 임상경험을 토대로 상세히 설명하고 있어, 머리 및 얼굴 부위 통증이라는 비교적 흔한 증상의 환자를 대하는 모든 의료인에게 혀인두신경통을 이해하는데 좋은 정보를 제공할 것으로 판단된다.
[정리: 편집위원회]
-
METRICS

-
- 0 Crossref
- Scopus
- 2,649 View
- 143 Download
-
Related articles in
J Korean Med Assoc -
Clinical features and treatment of rosacea2024 May;67(5)
Diagnosis and treatment of dyslipidemia in children and adolescents2024 May;67(5)
Surgical treatment of esophageal cancer2024 February;67(2)
Diagnosis and evaluation of nontuberculous mycobacterial pulmonary disease2024 January;67(1)
Guideline for the diagnosis and treatment of scabies2023 December;66(12)






