만성두드러기의 생물학적제제 치료
Treatment with biological products for chronic urticaria
Article information
Trans Abstract
Background
Chronic urticaria is characterized by repeatedly occurring itchy wheals and/or angioedema for at least six weeks. The prevalence of chronic urticaria is increasing globally, with variations observed among different regions. Chronic urticaria has a long duration and may recur over time. Effective and tolerable treatment for such patients is crucial due to unpredictable, recurrent, and disabling symptoms, as well as the significant impact on quality of life.
Current Concepts
Recent guidelines recommend the regular use of non-sedative second generation antihistamines as the first line of treatment for chronic urticaria. For patients whose urticarial symptoms persist or worsen with the approved dose of antihistamines, the guideline recommends the second line of treatment, which involves either increasing the dosage of the initial antihistamine or combining it with three other kinds of antihistamines. However, almost half of patients with chronic urticaria are refractory to antihistamines. Recently, treatment modulating immunoglobulin E (IgE) levels and activities was found to provide an efficient therapeutic approach. Omalizumab, the only approved anti-IgE treatment to date for patients with chronic urticaria, has demonstrated strong evidence of both efficacy and safety. Recent international guidelines recommend omalizumab as the first choice of treatment for antihistamine-refractory chronic spontaneous urticaria.
Discussion and Conclusion
As omalizumab is not a curative and disease-modifying agent, there is a subpopulation of patients with chronic spontaneous urticaria who partly or have never responded to omalizumab. To address this, ongoing research is exploring the therapeutic potential of other biological products that target various aspects, such as type 2 inflammation, complement system, and the c-kit pathway.
서론
두드러기는 가려움을 동반한 팽진(wheal)과 혈관부종(angioedema)을 특징으로 하며, 전 인구의 약 20%가 일생에 한 번은 경험할 정도로 매우 흔한 질병이다[1]. 팽진의 발생이 6주 이상 거의 매일 나타나는 만성두드러기의 유병률은 일반인구를 대상으로 진행된 연구들에서 0.5-5%로 보고된다[2]. 생명을 위협하는 질환은 아니지만 재발과 호전을 반복하며, 예측할 수 없이 악화되므로 삶의 질 저하를 초래한다[3,4]. 두드러기 증상의 중증도에 따라 차이가 있지만 평균 유병기간은 3-5년으로 보고하고 있으며[3], 최근 국내 조사에서도 평균 6.5년으로 보고하였다[5]. 증상이 심할수록 유병기간도 길어진다[6]. 최근 진료지침에서는 가능한 증상이 전혀 없고, 완전히 조절되어 일상생활에 불편함이 없도록 치료단계를 조정하도록 권고한다[7]. 그러나 병인기전이 불확실하고, 예후 또는 치료반응을 평가하기 위한 객관적인 지표가 없어 지속적인 관리가 어려운 경우가 많다.
2020년 대한천식알레르기학회와 피부면역학회 공동으로 근거 기반 만성두드러기 치료지침을 발표하였다[1,8]. 비진정성 2세대 항히스타민제를 1차 치료제로 사용하며, 4주 정도 경과를 확인하여 증상이 조절되지 않으면, 항히스타민제를 4배 용량 또는 4종 병용하여 치료단계를 높이도록 권고하였다[1]. 항히스타민제 증량에도 두드러기 증상이 조절되지 않는다면, 오말리주맙(omalizumab), 사이클로스포린(cyclosporine)을 추가 치료로 고려할 수 있다[8]. 만성두드러기 환자의 40-50%는 항히스타민제에 반응하지 않고, 항히스타민제로 두드러기가 조절되지 않는 환자에서 삶의 질이 더 현저하게 저하되는 것이 관찰되었다[4,7]. 이 논문에서는 만성두드러기 환자에서 사용 가능한 생물학적제제의 만성두드러기 치료 적용에 대해 정리하였다(Figure 1) [8].
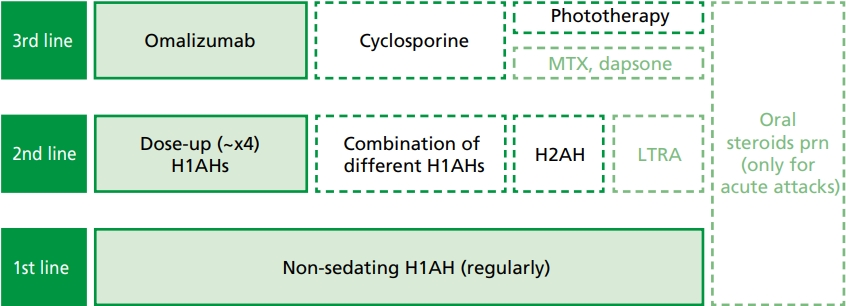
Stepwise treatment for patients with chronic spontaneous urticaria. Solid lines indicate strong recommendations, and broken lines are conditional recommendations. The pale boxes are conditional and against current recommendations. MTX, methotrexate; H1AH, H1-antihistamines; H2AH, H2-antihistamines; LTRA, leukotriene receptor antagonist. Adapted from Choi JH et al. Allergy Asthma Immunol Res 2020;12:750-770, according to the Creative Commons license [8].
두드러기 중증도 및 조절상태 평가
두드러기 증상의 중증도를 평가하기 위한 지표로 가려움의 정도와 24시간 동안 발생하는 팽진의 평균 개수를 점수화한 urticaria activity score (UAS, 0-6)가 있다. UAS를 매일 평가하여 최근 1주일간의 결과를 누적하여 계산한 UAS7(0-42)을 최근 임상연구에서 중요한 평가지표로 사용하고 있다. UAS, UAS7은 진료 당일 또는 7일 이내의 팽진, 가려움이 얼마나 심했는지를 평가할 수 있다[7]. UAS7 점수 6 이하이면, 경미한 두드러기 증상으로, 28 이상이면 심한 두드러기 증상으로 평가한다. 그러나 악화와 호전을 반복하는 만성두드러기의 임상경과와 약물치료에 대한 모니터링을 위해 최근 4주간의 두드러기 증상의 조절상태를 평가할 수 있는 urticaria control test (UCT, 0-16)가 개발되었다[9,10]. UCT 점수 16점을 완전 조절상태로, 12 이상을 잘 조절되는 상태, 12점 미만인 경우 조절되지 않는 두드러기로 평가한다[9,10]. 만성두드러기 특이형 삶의 질 측정도구를 통해 두드러기 증상이 환자들의 삶의 질에 미치는 영향을 평가할 수 있다(Table 1, Figure 2) [7,10,11].
오말리주맙의 치료 효과에 대한 주요 임상시험 결과
오말리주맙은 12세 이상의 만성 자발성 두드러기(chronic spontaneous urticaria) 환자의 치료를 위해 허가된 유일한 생물학적제제이다. 오말리주맙은 재조합 인간화 면역글로불린G1 (immunoglobulin G1, IgG1), 단클론 항면역글로불린 E 항체이다. 만성두드러기의 핵심 병인기전이 비만세포의 활성화 및 탈과립이며, 면역글로불린E (IgE)와 비만세포 표면의 IgE 수용체를 통한 활성화가 탈과립의 주요 요인이다. 오말리주맙은 혈청 유리 IgE에 결합하여 IgE가 비만세포, 호염기구 및 호산구 표면의 수용체와 결합하는 것을 저해하는 작용을 한다[12]. 또한 IgE 수용체의 세포 표면 발현을 낮추는 것으로 확인되었다[13]. 오말리주맙은 국내에서 2017년 항히스타민제 불응성 만성 자발성 두드러기에 대해 식약처의 적응증을 받았다.
만성두드러기에 대한 오말리주맙의 주요 3상 임상시험에서 4주 간격으로 오말리주맙 75 mg, 150 mg, 300 mg을 투여한 총 733명의 환자를 242명의 위약군과 비교하였다[14-16]. 항히스타민제로 조절되지 않는 만성두드러기 환자에서, 12주차에 가려움 점수의 감소를 일차 유효성 평가지표로 위약군과 비교한 결과 오말리주맙의 3가지 용량 모두 일차 유효성 평가지표를 충족하였다. 오말리주맙 300 mg군이 75 mg이나 150 mg군에 비해 더 짧은 기간에 가려움증의 개선을 보였다. 그러나 치료를 중단한 후 모든 치료군에서 두드러기 증상이 위약 수준으로 회복되었다. 이러한 여러 위약 대조 임상시험 결과를 종합하여 2021년 발표된 메타분석은 두드러기 중증도 점수의 감소와 삶의 질 개선에서 오말리주맙 300 mg이 모든 평가지표에서 임상적으로 의미 있는 개선을 보였지만 150 mg 치료군은 임상적으로 의미 있는 치료효과를 입증하지 못한 것으로 보고했다[17]. 그러나 우리 나라와 일본의 항히스타민제로 조절되지 않는 만성 자발성 두드러기 환자를 대상으로 진행된 3상 임상시험에서는 오말리주맙 150 mg과 300 mg 두 군 모두 위약 대비 유의한 치료효과를 확인하였다[18]. 이를 바탕으로 대한천식알레르기학회 및 대한피부면역학회는 항히스타민제 불응성 만성두드러기에 대해 오말리주맙 150 mg 또는 300 mg을 4주 간격으로 추가할 것을 권장하고 있다[8].
1. 항히스타민제 불응성 만성두드러기
1세대 항히스타민제는 중추신경계에 작용하여 소양증은 4-6시간 지속되는 데 비해 진정작용 및 항콜린효과는 12시간 이상 지속되며, 알코올, 수면진정제, 항우울증제 등과 약물상호작용도 큰 편이다. 또한 렘 수면을 방해하고, 학습 및 행동에도 영향을 미치는 것으로 나타나면서 더 이상 두드러기의 일차 약제로 권장되지 않는다. 국제 진료지침에는 2세대 항히스타민제를 2주 이상 규칙적으로 유지하여 증상이 호전되지 않으면 4배 용량까지 증가하는 방법을 우선적으로 권장하고 있다. 그러나 허가사항을 고려하여 국내에서는 1종의 항히스타민제로 잘 조절되지 않는 두드러기에 대해 용량 증량보다는 4종의 다른 항히스타민제를 병용하는 경우가 많다. 최근 발표된 국내 연구에서 표준용량 항히스타민제로 증상이 조절되지 않는 만성두드러기 환자에 대해 무작위 배정을 통해 표준용량 유지군(항히스타민제 2종 교체 또는 기존 항히스타민제에 H2 길항제를 추가)과 고용량 항히스타민제군(항히스타민제 4배 용량 증량 또는 4종 항히스타민제 병용)에서 4주 치료 후 두드러기 조절상태를 비교한 결과 고용량 항히스타민제군에서 증량 또는 병용 모두에서 표준용량 항히스타민제를 유지한 군에 비해 안전성 문제없이 유의한 두드러기 증상의 개선을 보였다[19]. 두드러기 증상의 완전완화(complete remission), 즉, UAS7 점수가 0에 도달하는 비율은 4배 증량군이 4종 병용에 비해 높았다. 한편, 모든 대상자들은 최소 2주 이상 표준용량 항히스타민제를 유지 중이나 두드러기 증상이 지속되어 연구에 등록되었으며, 표준 용량으로 4주 동안 유지치료를 지속한 55명 중 약 35%에서도 잘 조절되는 상태에 도달한 것으로 나타나 4주 이상 지속적인 항히스타민제 치료를 유지한 후 항히스타민제 불응성 여부를 판단할 필요가 있다.
항히스타민제 불응성 예측지표에 대한 다양한 연구결과가 있으나, 실제 진료현장에서 활용할 수 있고, 체계적 분석 결과에서 강한 수준의 근거가 확인된 것은 높은 중증도 점수(UAS7), 높은 C반응단백 수치와 d-dimer 수치였다[20]. 총 IgE가 높은 경우, 혈관부종이 동반된 경우, 만성 유발성 두드러기가 동반되거나, 전신스테로이드 치료를 받았던 경우 등도 항히스타민제 불응성 환자의 특징으로 보고되고 있으나, 아직은 그 근거가 부족한 것으로 나타났다[6,20].
2. 오말리주맙 치료의 적정 용량 및 투여간격
중증 알레르기 천식에서 오말리주맙의 최적 용량은 환자의 혈청 총 IgE 수치와 체중에 따라 결정된다. 그러나 만성 두드러기에 대해서는 혈청 IgE 수치 또는 체중과 무관하게 임상시험에서 효과와 안전성이 입증된 4주 간격 150 mg 또는 300 mg 피하주사를 사용할 수 있다. 오말리주맙 300 mg 투여 시 150 mg보다 더 빠르고 강력한 두드러기 증상의 개선을 보였으나, 국내에서는 비용 효용의 측면에서 대부분의 환자에게 150 mg을 투여하고 있다. 12주에 UAS7 ≤6에 도달한 환자의 비율을 비교하면, 위약군의 11-19%, 150 mg 오말리주맙군의 40%, 300 mg군의 52-66%를 보였다. 이후 추가 임상시험 결과 3개월에 잘 조절되지 않았던 환자에서 오말리주맙 치료를 6개월까지 유지한 결과 300 mg 용량군의 58%, 150 mg 용량군의 34%에서 추가로 잘 조절되는 두드러기 상태에 도달한 환자의 비율이 증가하였다[21]. 따라서 오말리주맙 추가치료를 시작한 경우 최소 6개월까지는 유지한 후 오말리주맙 치료에도 반응하지 않는지를 평가하도록 권장하고 있다[7,8].
모든 임상시험에서 오말리주맙을 중단하면, 16주 이내에 가려움증 및 팽진 점수가 위약 수준으로 증가했다. 오말리주맙이 항히스타민제 단독치료에 비해 증상 조절에 효과적이지만, 두드러기의 완화를 유도하지 못하며, 일부 환자에게는 장기간의 치료가 필요할 수 있다. 두드러기 증상이 잘 조절되면, 항히스타민제를 감량할 수 있다. 6개월의 오말리주맙 치료 후 3개월 이상 UCT=16, UAS7=0으로 완전한 조절상태를 유지한 환자에 대해서는 오말리주맙의 감량 또는 투여 간격을 1-2주씩 연장하여 치료단계를 낮추는 시도를 할 수 있다[7]. 두드러기 증상의 악화 없이 4개월 동안 매 8주 간격의 오말리주맙 치료에도 잘 조절된다면, 오말리주맙 치료의 중단을 고려할 수 있으나[21], 개인 환자의 증상 조절에 따른 맞춤 전략이 필요하다. 오말리주맙 치료를 중단한 후 두드러기 증상이 재발하는 경우라도 대부분의 환자는 이전의 유효 용량 및 간격으로 재치료 시 좋은 반응을 보였다[22].
3. 오말리주맙 치료반응 예측인자
만성두드러기 환자에서 오말리주맙에 대한 치료반응은 효과가 나타나는 시기와 증상 개선의 정도에 따라 분류한다. 오말리주맙에 대한 치료반응이 처음 4주 이내에 시작될 때 빠른 반응 또는 조기 반응으로 평가하며, 12-16주에 걸쳐 서서히 호전이 되는 경우 반응이 느리거나 늦는 것으로 정의한다. 오말리주맙에 대한 치료반응의 정도는 UAS7에 따라, 완전 반응은 치료 후 UAS7=0 또는 치료 전 UAS7 점수에 비해 90% 이상 개선된 경우에 해당한다. UAS7 감소가 치료 전에 비해 30% 미만으로 개선되거나, 치료 후 UAS7>6 또는 치료 중에도 가려움, 팽진이 악화된 경우로 정의한다[21,23].
오말리주맙 치료 후 만성 자발성 두드러기 환자의 약 70%는 치료 첫 4주 이내에 반응한다. 주요 임상시험 결과에서 4주차에 잘 조절된 두드러기(UAS7 ≤6)가 위약군의 2-5%, 오말리주맙 150 mg군의 21-28%, 300 mg군의 37-51%에서 보고되었다[14-16]. 완전 반응(UAS7=0)에 도달하는 시기는 오말리주맙 300 mg군에서 8-10주에 관찰된 반면, 150 mg군은 12-16주로 나타났다. 그러나 약 30%의 환자는 6개월간의 오말리주맙 치료에도 두드러기 증상의 개선이 없었다.
만성 자발성 두드러기의 병인기전 중 자가면역반응을 통한 IgE 수용체 경로의 활성화가 중요하며, 제1형 자가면역(자가알레르기)과 제2형 자가면역으로 구분한다[24]. 갑상샘 과산화효소(thyroid peroxidase)에 대해서 환자에 따라 IgE 또는 IgG 항체 각각에 양성을 보이는 경우가 20-30%에서 확인된다. 제1형 자가면역을 보이는 환자에서 오말리주맙에 대한 치료반응도 좋은 것으로 나타났다. 반면, 치료 전 혈청 총 IgE치가 40 IU/mL 미만으로 낮거나, 호염기구 히스타민 유리능 분석, 자가혈청 피부반응시험 및 IgE 또는 그 수용체에 대한 IgG 자가항체를 포함하는 제2형 자가면역반응을 보이는 환자에서 오말리주맙에 대한 반응이 느리거나 나쁜 것으로 보고되었다[25,26]. 그러나 자가혈청피부반응시험 양성 또는 갑상샘 자가항체가 양성인 환자의 경우에도 실제 비만세포에서 히스타민을 유리할 수 있는 환자의 비율은 낮으며, 182명의 만성 자발성 두드러기 환자 중 8% (18명)에서만 확실한 제2형 자가면역이 확인되었다[27]. 이 연구에서도 2형 자가면역반응을 보인 환자에서 유의하게 낮은 총 IgE가 확인되어[27], 현재 실제 진료현장에서 오말리주맙의 치료반응성을 예측할 수 있는 유일한 지표는 치료 전 혈청 총 IgE이다.
4. 오말리주맙 치료에 반응하지 않는 환자에 대한 치료
오말리주맙 300 mg에 부분 반응 또는 무반응을 보이는 만성두드러기 환자에서 오말리주맙을 450 mg 또는 600 mg까지 증량하거나, 투여간격을 4주에서 2주까지 단축하여 유의한 증상 개선을 보고한 연구들이 있다[28,29]. 2022년 국제 두드러기 가이드라인에서도 오말리주맙 300 mg을 4주 간격 투여로 부분 반응 또는 무반응을 보이는 환자에서 2주 간격 600 mg 투여까지 권장하고 있으나, 허가사항을 초과한 치료임을 강조하고 있다.
오말리주맙에 비해 임상연구 결과가 부족하지만, 사이클로스포린 또한 항히스타민제 불응성 만성두드러기 환자에서 효과가 있다는 메타분석 결과가 발표되었다[30]. 1일 용량 1-5 mg/kg로 투여한 결과 4주차 54%, 12주차 73%에서 반응을 보였고, 위장장애가 가장 흔한 부작용이었지만 약 5%의 환자에서 혈청 크레아티닌 상승 및 고혈압이 관찰되었다. 오말리주맙과 사이클로스포린 각각에 잘 반응하지 않은 환자들에 대해 두 치료를 병용하여 유의한 치료반응의 개선을 확인한 연구결과도 있다[31]. 또한, 오말리주맙으로 잘 치료되지 않는 낮은 혈청 IgE와 제2형 자가면역 내재형의 특징을 보이는 만성두드러기 환자에서 사이클로스포린에 좋은 치료 반응을 보인 연구결과도 있다[32].
5. 만성 유발성 두드러기 환자에서 오말리주맙 치료효과
만성 유발성 두드러기는 한랭, 체온 상승, 피부 마찰, 압력, 햇빛, 운동 등 일반적인 신체적 자극에 의해 유발되며, 지속 기간이 길고 유발 요인을 피하기 어렵기 때문에 삶의 질에 심각한 영향을 미친다. 만성 자발성 두드러기 환자 중 76%까지 만성 유발성 두드러기를 동반하는 것으로 나타났으며, 이 환자들이 더 높은 두드러기 중증도 및 긴 유병기간을 보인다[33]. 최근 메타분석에 따르면 오말리주맙 치료는 다양한 만성 유발성 두드러기 환자에서 유의한 증상 개선이 확인되었다[34]. 증상을 동반한 피부묘기증, 한랭두드러기, 햇빛 두드러기에 대한 유효성 평가는 가능한 정도였지만 압박, 콜린성, 진동, 물 접촉에 의한 만성 유발성 두드러기에 대한 근거는 여전히 부족하다. 콜린성 두드러기에 대한 오말리주맙의 효과는 국내 연구에서 완전 반응율이 4.8%로 낮았다[35]. 만성 유발성 두드러기의 유형에 따른 용량, 주사 간격 및 치료 기간을 설정하기 위해서는 더 많은 무작위 대조 시험 결과가 필요하다.
6. 오말리주맙의 안전성
모든 임상시험에서 오말리주맙의 안전성이 평가되었다. 전반적으로, 오말리주맙은 내약성이 매우 우수였으며, 가장 심각하게 고려되는 이상반응은 급성중증과민증(anaphylaxis)으로, 오말리주맙을 1회라도 투여 받은 총 39,510명 중 0.09%로 추정되었다[36]. 만성두드러기 환자에서 급성중증과민증의 발생 위험은 천식으로 오말리주맙을 투여 받은 환자보다 낮았으며, 용량 비례 효과도 관찰되지 않았다[37]. 오말리주맙은 만성두드러기로 치료를 받은 소아[38] 및 노인[39] 환자에서 모두 높은 내약성을 보였다. 임신 중 오말리주맙에 노출된 산모와 태아에서 안전성 문제는 관찰되지 않았다[40].
7. 기타 생물학적제제의 만성두드러기 치료 적용
만성두드러기에 허가된 생물학적제제는 아니지만 오말리주맙에 반응하지 않는 환자들을 대상으로 천식, 아토피피부염 등 중증 알레르기질환에 허가된 dupilumab, benralizumab, mepolizumab, reslizumab과 건선에 허가된 secukinumab을 사용 후 두드러기 증상의 개선을 보고한 증례들이 최근 발표되고 있으나, 아직은 그 근거가 매우 부족하다[41].
결론
오말리주맙은 유효성 및 안전성에 대한 강력한 근거를 바탕으로 최근 가이드라인에서 항히스타민제 증량에도 조절되지 않는 만성 자발성 두드러기 환자에서 우선적으로 고려할 치료제로 권장된다. 국내 허가사항에는 항히스타민제 불응성 만성 자발성 두드러기 환자에 대해 매 4주 150-300 mg을 피하주사하며, 6개월까지 지속 투여 후 치료반응을 확인하여 유지치료 또는 치료중단을 고려할 수 있다. 그러나 질병 조절제가 아니기 때문에 오말리주맙에 부분적으로 또는 전혀 반응하지 않는 환자들도 있으며, 더 연구가 필요하지만 자가면역 내재형에 따라 오말리주맙을 증량하거나, 사이클로스포린을 추가 또는 교체하는 치료가 필요하다. 치료 전 혈청 총 IgE가 40 미만으로 너무 낮거나, 갑상샘 자가항체와 혈청 C반응단백이 높고, 호염기구 히스타민 유리능이 증명된 자가혈청피부반응시험 양성 환자에서 오말리주맙에 대한 반응이 늦게 나타나거나 반응이 없는 경우가 있다. 만성 자발성 두드러기 동반 없이 만성 유발성 두드러기만 있는 환자에서의 유효성에 대한 근거는 아직 부족하다. 또한 최근 소아 및 노인 환자에서 오맙리주맙 추가치료의 성인 환자와 유사한 치료효과에 대한 증례보고가 발표되고 있으나, 유효성과 안전성에 대한 임상적 근거는 아직 충분하지 않다. 만성 두드러기의 병인에 대한 최근의 연구결과를 바탕으로 IgE 외의 다른 치료 타겟에 대한 다양한 생물학적제제들이 개발 중이다.
Notes
Conflict of Interest
No potential conflict of interest relevant to this article was reported.
Acknowledgements
This work was partly supported by the GRRC program of Gyeonggi-do Province (GRRC Ajou2023-B02) and a grant from the National Research Foundation of Korea (NRF) funded by the Korea government (MSIP) (NRF-2022R1A2C2095297).
References
Peer Reviewers’ Commentary
이 논문은 만성두드러기의 치료에서 관심이 높아지고 있는 유일한 생물학적제제인 오말리주맙에 대해 최신 문헌을 정리하여 잘 설명한 논문이다. 표준 용량 항히스타민제 치료에 반응하지 않는 만성두드러기 환자는 항히스타민제를 4배 용량 증량 또는 4종 병용하여 치료하지만, 이 중 절반 가까운 환자는 약물에 반응하지 않는다. 이러한 환자들에게 다음 단계 치료로 오말리주맙 혹은 사이클로스포린을 고려한다. 현재 국내에서 항히스타민제 불응성 만성두드러기 환자에게 사용이 가능한 생물학적제제는 오말리주맙이 유일하다. 이 논문은 만성두드러기 환자에서 오말리주맙의 주요 임상시험 결과와 치료 용량, 투여 간격, 치료반응 예측인자, 안정성 등에 대하여 정리하였다. 또한 만성유발성두드러기 환자에서의 오말리주맙 치료 효과도 기술하고 있어, 만성두드러기를 진료하는 임상 현장에 많은 도움이 될 것으로 판단된다.
[정리: 편집위원회]


