소아청소년 이상지질혈증의 진단 및 치료
Diagnosis and treatment of dyslipidemia in children and adolescents
Article information
Trans Abstract
Background
Atherosclerotic cardiovascular disease is a major cause of morbidity and mortality worldwide, including in South Korea. Dyslipidemia is an independent risk factor for the development of atherosclerotic cardiovascular diseases. There is strong evidence that atherosclerosis begins early in life and that elevated lipid levels in childhood predict elevated lipid levels into adulthood.
Current Concepts
A universal approach for cholesterol screening in all children is recommended. Lipid profiles should be studied for all children aged 9 to 11 years and then for those aged 17 to 21 years, as cholesterol levels may vary after puberty. The non-fasting lipid profile can be as useful in detecting severe genetic dyslipidemias as the fasting lipid profile and thus can be used as a first-line screening in children. The initial treatment for dyslipidemia in a child always begins with a 6-month trial of lifestyle modifications, such as improvements in dietary and physical activity patterns. Statins are as effective in children as in adults and can lower low-density lipoprotein cholesterol levels by up to 50%. Therefore, they are considered first-line therapy for children who meet the criteria for pharmacological therapy.
Discussion and Conclusion
Statins and non-statin lipid-lowering agents can lower cholesterol levels with minimal adverse effects in children and adolescents with hypercholesterolemia. However, limited data is currently available on the long-term safety and efficacy of lipid-lowering agents in the pediatric population. Furthermore, non-statin lipid-lowering agents are used far less frequently in children. Therefore, further long-term safety and efficacy studies on lipid-lowering agents in pediatric populations and clinical trials with non-statin lipid-lowering agents are required.
서론
전 세계적으로 소아청소년의 과체중 및 비만 유병률이 급속히 증가하면서, 제2형 당뇨병, 고혈압, 이상지질혈증과 같은 비만 관련한 대사질환의 유병률 또한 증가하는 추세를 보이고 있다[1-6]. 이러한 비만 관련 대사질환은 심뇌혈관질환 발생의 주 위험인자이다[7]. 그 중에서도 이상지질혈증은 죽상경화성 심혈관질환의 주 위험인자로 밝혀져 있는데, 이러한 이상지질혈증은 소아청소년기부터 시작되어 조기죽상경화증과 조기심혈관질환을 발생시킬 수 있어, 미국심장협회는 소아의 이상적인 심혈관계 건강에 있어 이상지질혈증이 중요한 요소라고 강조하였다[8-10]. 고콜레스테롤혈증이 확인된 청소년의 약 75%는 20대까지 고콜레스테롤혈증이 유지되고, 고콜레스테롤혈증, 높은 저밀도지단백질 콜레스테롤혈증(low-density lipoprotein [LDL] cholesterolemia)과 낮은 고밀도지단백질 콜레스테롤혈증(high-density lipoprotein [HDL] cholesterolemia)이 있는 소아청소년의 약 50%는 12년 후에도 여전히 지속된다고 보고된 바 있다[11]. 또한 비만, 고혈압, 이상지질혈증, 흡연 등의 위험요인이 증가할수록 죽상경화증 병변의 면적 또한 증가한다고 밝혀졌다[12]. 죽상경화성 심혈관질환에 의한 사망률은 전 세계적으로 전체 사망원인의 30%에 달하며, 한국은 27.6%를 차지하는 것으로 알려져 있다[13,14]. 따라서 성인기 심혈관질환 예방을 위해 소아청소년 시기부터 이상지질혈증을 관리하여 적절한 심혈관계 건강을 유지하는 것은 매우 중요하다. 이 논문에서는 소아청소년 이상지질혈증의 정의, 선별검사 및 진단, 치료방법을 함께 살펴보고자 한다.
소아청소년 이상지질혈증의 정의
이상지질혈증의 통일된 청소년기 진단기준은 현재까지 전세계적으로 정립되지 않았다. 1992년 미국 콜레스테롤 교육 프로그램(National Cholesterol Education Program, NCEP)과 미국 소아과학회(American Academy of Pediatrics)에서 6-19세 백인 소아청소년의 혈청 지질농도의 분포를 바탕으로 90-95백분위수에 해당하는 값을 고콜레스테롤혈증(≥200 mg/dL) 및 고 LDL 콜레 스테롤혈증(≥130 mg/dL)의 기준치로 제시하였다[15]. 또한 NCEP Adult Treatment Panel III를 소아의 실정에 맞게 변형하여 사용한 기준에서는 고중성지방혈증 ≥110 mg/dL, 저 HDL 콜레스테롤혈증 <40 mg/dL으로 정의하고 있다[16]. 한편, 국제당뇨병연맹(International Diabetes Federal)은 고중성지방혈증은 ≥150 mg/dL, 낮은 HDL 콜레스테롤혈증의 경우 성별과 연령에 따라 구분하여 10-15세 소아청소년에서는 HDL 콜레스테롤 <40 mg/dL을, 만 16세 이상 소아청소년에서는 HDL 콜레스테롤 <40 mg/dL (남아), <50 mg/dL (여아)를 기준치로 제시하였다[17]. 미국 소아과학회는 2011년 National Heart, Lung and Blood Institute (NHLBI)에서 개정한 내용을 바탕으로, 소아청소년에서 혈청 총콜레스테롤 ≥200 mg/dL, LDL 콜레스테롤 ≥130 mg/dL, non-HDL 콜레스테롤 ≥145 mg/dL, 중성지방 ≥130 mg/dL (10세 미만에선 ≥100 mg/dL), HDL 콜레스테롤 <40 mg/dL를 이상지질혈증으로 정의하고 있다[18]. 대한소아내분비학회에서 한국의 실정에 맞게 개발한 ‘소아청소년 이상지질혈증 진료지침 2017’에서는 NHLBI 2011의 정의에 따라 소아청소년 이상지질혈증을 정의하였다(Table 1) [19].
선별검사 및 진단
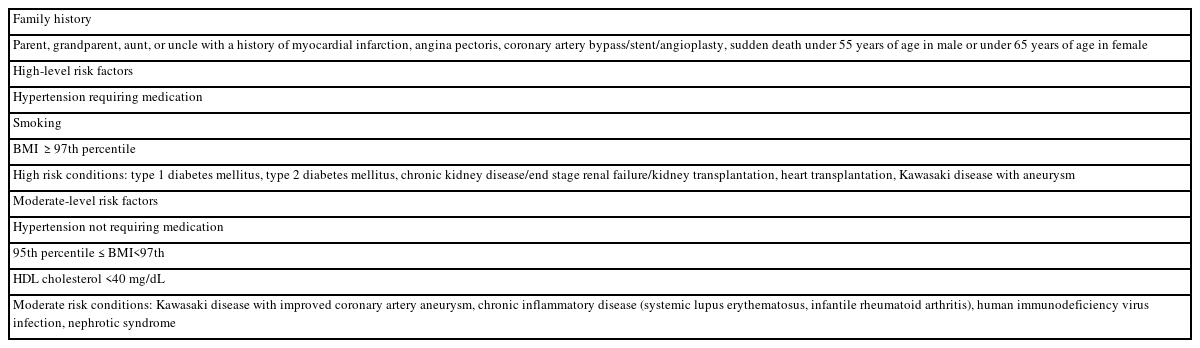
소아청소년 시기의 지질 선별검사는 이상지질혈증을 조기 진단하고 관리하여 성인기의 심혈관질환 발생 위험도를 낮추고 중증도를 감소시키기 위한 목적으로 시행된다. 과거 선별검사의 대상은 조기관상동맥질환이나 이상지질혈증의 가족력에 근거하여 시행하였으나 이 경우 전체 이상지질혈증 소아의 30-60%가 누락될 수 있다[20]. 심혈관질환의 가족력이 미래의 심혈관질환을 예측하는데 중요하지만, 가족력에 대한 정보의 정확도나 신뢰도가 떨어지고, 가족력이 없다고 해서 소아청소년에서 이상지질혈증이 없다고 할 수 없기 때문이다[21]. 또한 정상적인 콜레스테롤 농도의 변화 패턴은 생후 2세 이후에는 큰 변화가 없으나, 사춘기 동안에 10-20% 정도 지질 수치가 감소하며, 20대에 들어서는 다시 증가하게 된다[11]. 따라서 출생 이후 2세까지는 이상지질혈증에 대한 선별검사는 권고하지 않고, 모든 소아청소년에 대해서 9-11세와 17-21세에 non-HDL 콜레스테롤로써 선별검사 실시를 권고한다. 이상지질혈증의 위험인자가 있는 경우에는 2-8세, 12-16세에 공복상태(최소 9시간)의 지질 검사를 시행한다. 이상지질혈증의 위험인자는 가족력, 높은 수준의 위험인자, 중등도 수준의 위험인자로 나누어 볼 수 있다(Table 2) [19].
선별검사 방법으로 추천되는 non-HDL 콜레스테롤은 LDL 콜레스테롤보다 공복상태의 영향을 받지 않는다고 장점이 있어, 심혈관질환 발생을 예측할 수 있는 좋은 검사이며, LDL 콜레스테롤과 함께 성인기에서 이상지질혈증 발생의 예측인자로 평가된다. 공복지질검사는 3개월 이내 2주 이상의 간격으로 2회 실시하여 평균치를 구한다.
치료
소아청소년 이상지질혈증의 치료계획은 대상의 연령, 심혈관계 위험인자의 중증도 및 개수, 혈장 LDL 콜레스테롤, 중성지방 수치에 따라 달라진다. 일반적으로 치료계획에는 심혈관계의 건강을 목표로 한 식사요법, 생활습관 교정이 일차 관리 방법이며, 일차 관리가 실패하거나 충분치 못할 경우 이차적으로 약물요법을 고려한다. 비만아에서는 적절한 식사요법과 규칙적인 운동습관을 유지하여 체중을 유지 또는 조절하며 적절한 신체 성장을 하도록 한다. 치료의 일차지표는 LDL 콜레스테롤이며, NHLBI 가이드라인에서는 추가 목표 지표를 중성지방으로 하였다.
1. 식이요법
2015 미국 식이요법 지침에서는 만 2세 이상 일반 인구 대상으로 성장기에 필요한 영양공급과 동시에, 심혈관질환의 위험을 줄이기 위한 식이요법 지침을 제시하고 있다[22]. 이상지질혈증이 있는 소아청소년의 경우, LDL 콜레스테롤을 낮추기 위한 저지방 식이요법으로의 전환을 권장하며 먼저 1단계 식사요법(cardiovascular health integrated lifestyle diet-1, CHILD-1)을 3-6개월간 시도한다. 1단계 식사요법은 지방량을 총열량 섭취의 30%로 유지하고, 포화지방 섭취 10% 미만, 하루 콜레스테롤 섭취 300 mg 미만으로 제한하는 식사요법이다. 목표에 도달하지 못하면 이상지질혈증의 원인에 따라 2단계 식사요법 중 CHILD-2-LDL 또는 CHILD-2-triglyceride (TG) 식사요법을 선택하여 시행한다. CHILD-2-LDL 식사요법에서는 지방량은 총열량 섭취의 25-30%로 유지하고, 포화지방 섭취는 7% 미만, 하루 콜레스테롤 섭취는 200 mg 미만, 트랜스지방 섭취는 1% 미만으로 가능한 제한한다. 중성지방이 높은 경우에는 CHILD-2-TG 식사요법을 시행하는데, 단순탄수화물의 섭취를 줄이고 복합탄수화물로 대체하며, 오메가-3 지방산 섭취를 늘린다.
건강한 영아 인구집단에서의 모유 수유는 심혈관계 위험을 감소시키므로 생후 첫 6개월까지는 가능한 완전 모유 수유가 권장된다[23]. 지방은 유아기 뇌와 인지 발달에 중요한 영양 성분이기 때문에 12개월 미만의 영아에서 의학적 적응증 없이 지방 섭취를 제한해서는 안 된다.
우유는 식사에서 제공되기 힘든 단백질, 칼슘, 마그네슘, 비타민D 등 필수 영양소를 제공한다[24]. 무지방 우유는 지방과 칼로리의 양을 줄이면서 영양소의 질은 손상시키지 않는 이점이 있으므로 섭취를 권장한다. 단순 당질의 섭취는 제한한다. 고기나 고지방 유제품과 같이 포화지방이 많은 음식은 제한하고 과일, 채소 섭취를 권장하며 식물성 지방은 음식 내의 콜레스테롤의 신체흡수를 저해하므로 권장한다. 특히 식이섬유 섭취는 심장질환의 위험을 낮출 수 있으므로 적극 권장한다.
2. 생활습관 개선
한국 소아청소년 이상지질혈증 유병률의 증가는 서구화된 식습관과 신체활동 감소로 인한 것으로 여겨지고 있다. 하루에 60분 이상의 규칙적인 중등도 이상의 신체활동, 유산소 운동이 권장되며, TV 시청이나 인터넷 사용시간은 하루 2시간 이내로, 가능한 줄이는 것을 권장한다. 또한 체질량지수를 85백분위수 이하로 유지하고, 금연을 권고한다.
3. 약물요법
약물치료는 10세 이상의 소아청소년이 생활습관 및 식이 조절을 6-12개월 이상 했음에도 불구하고 효과가 좋지 않을 경우에 고려한다. 이상지질혈증을 보이는 소아는 이에 대한 가족력 및 위험인자에 대해 평가가 필요하다. 10세 이전에는 일반적으로 약물치료를 시작하지 않는다. 그러나 심하게 높은 LDL 콜레스테롤혈증을 보이는 경우, 위험인자에 따라 약물치료를 고려한다. 조기 심혈관계 질환의 가족력, 1개 이상의 높은 수준의 위험인자 또는 2개 이상의 중등도 위험인자를 갖는 8-9세의 소아에서 생활습관 변화 및 식이요법(CHILD-1 → CHILD-2-LDL)에도 LDL 콜레스테롤이 지속적으로 190 mg/dL 이상일 경우, 스타틴(statin) 치료를 고려할 수 있다[18,25]. 또한 심한 일차성 고지질혈증이나 심각한 의학적 합병증에 대한 위험요인(동형접합 고콜레스테롤혈증, LDL 콜레스테롤 ≥400 mg/dL, 일차성 고중성지방혈증 ≥500 mg/dL, 심혈관계질환, 심장이식)이 있는 경우에도 약물치료를 고려한다[26].
10-21세의 소아청소년은 평균 LDL 콜레스테롤 ≥250 mg/dL 또는 중성지방 ≥500 mg/dL일 경우 전문가에게 의뢰해야 한다[20]. LDL 콜레스테롤 <250 mg/dL 또는 중성지방 <500 mg/dL인 경우, 3-6개월간의 식사요법(CHILD-1 → CHILD-2-LDL 또는 CHILD-2-TG)을 시행해야 한다. 체질량지수가 85백분위수 이상일 경우 신체활동량을 증가시키고 좌식 생활 습관을 줄이며 칼로리를 감량한다. 이러한 생활습관 교정과 식이요법에도 지질농도가 목표치에 도달하지 않을 경우 약물치료를 고려한다[20]. 10세 이상의 소아에서 LDL 콜레스테롤이 목표치에 도달했으나 non-HDL 콜레스테롤 농도가 ≥145 mg/dL일 경우 스타틴 제제나 파이브레이트(fibrate) 또는 나이아신(niacin) 투여를 고려할 수 있으며, 전문가에게 의뢰한다. 생활 습관 개선 및 식이요법(CHILD 1→CHILD 2-TG)에도 공복 시 중성지방 200-499 mg/dL, non-HDL 콜레스테롤 농도 ≥145 mg/dL일 경우 오메가-3 지방산의 투여를 고려할 수 있지만 소아에서 그 연구가 충분하지 않다[18,27,28].
1) HMG-CoA 환원효소 억제제
스타틴 제제는 내인성 콜레스테롤 합성의 중요한 효소인 HMG CoA 환원효소(hydroxymethylglutaryl coenzyme A reductase)를 억제하여 세포 내 콜레스테롤을 감소시키고 LDL 수용체를 상향 조절하여 LDL 콜레스테롤을 감소시킨다[29,30]. 스타틴 제제는 10세 이상의 소아청소년에 대해 미국 식품의약국 허가를 받은 약품이며, LDL 콜레스테롤이나 non-HDL 콜레스테롤 상승시에 일차적 치료제로 사용할 수 있다. 콜레스테롤 수치를 20-50% 낮추는 효과가 있으며, 부작용이 적다. Lovastatin, simvastatin, pravastatin 20-80 mg으로, atorvastatin은 5-80 mg으로 투약 가능하며, 특정 스타틴 제제를 선택하여 가장 적은 용량으로 하루 한 번 투여하는 것으로 시작한다. 용량 증량에 대한 위험도와 효과에 대해 소아에서 별다른 문제점이 보고되지 않았고, 부작용과 효과는 성인에서와 비슷한 것으로 알려져 있다. 스타틴 제제의 부작용은 통상적인 용량에서는 드물게 발생하는데 근병증, 간 효소 수치 상승 등이 있을 수 있으므로, 간 효소 수치와 근육 독성에 대한 크레아틴인산화효소(creatine kinase) 수치를 모니터링 해야 한다. 공복 지단백 분포, 간 효소 수치 등을 치료 첫 해에 매 3-4개월마다 모니터링하고 2년째부터 6개월마다 검사한다. LDL 콜레스테롤의 목표 농도는 130 mg/dL 미만이며 이상적으로는 110 mg/dL 미만으로 LDL-C 유지하도록 한다[31].
2) 담즙산제거제
담즙산제거제(bile acid sequestrants)는 장내의 담즙산과 결합하여 말단 회장에서의 장간 재흡수를 억제하여 간에서 담즙의 결핍을 일으킨다. 담즙산은 간에서 세포 내 콜레스테롤로부터 합성되므로 세포 내 콜레스테롤이 결핍되면 LDL 수용체가 증가되고 세포 내 콜레스테롤의 회복을 위해 혈중 LDL 콜레스테롤의 배설이 증가된다. 비교적 안전하고 효과적이나 소화기계 부작용이 있을 수 있다[32].
3) 콜레스테롤 흡수억제제, 파이브레이트, 나이아신
성인에서는 LDL 콜레스테롤이 감소하지 않는 경우 콜레스테롤 흡수억제제(cholesterol absorption inhibitors)를 부가적으로 투여할 수 있으며, 효과는 스타틴 제제와 독립적으로 작용하여 도움이 될 수 있다. 콜레스테롤 흡수억제제 ezetimibe는 소아청소년에서 사용하였을 때에도 그 효과 및 안정성이 입증되어 미국 식품의약국에서 10세 이상의 소아청소년에서의 사용을 승인받았다. Ezetimibe는 음식으로 섭취한 콜레스테롤이 소장에서 체내로 재흡수되는 것을 막음으로써 LDL 수치를 낮춘다.
소아청소년에서 파이브레이트와 나이아신의 치료 경험은 제한적으로, 효과와 안전성에 대한 데이터가 부족하다. 따라서 콜레스테롤 흡수억제제, 파이브레이트, 나이아신을 사용할 경우 전문가와 상의하여야 한다[18]. 소아에서 병용할 경우에도 효과는 증가하지만 부작용 발생은 증가되지 않는 것으로 알려져 있다. 소아청소년에서 사용할 수 있는 약물은 Table 3과 같다[19].
결론
서구화된 식습관과 신체활동 감소로 한국 소아청소년의 이상지질혈증 유병률은 과거에 비해 증가하였다. 죽상동맥경화증은 소아청소년기부터 시작할 수 있으며, 성인기 심혈관질환으로 이어질 수 있다. 성인이 된 이후에는 생활습관 교정이 어렵고, 약물치료 후 심혈관계 건강의 완전한 회복이 불가능하므로 소아청소년 시기부터 이상지질혈증을 조기에 발견하고 적극적인 생활습관 교정, 식이요법, 필요 시 약물요법을 추가하여 적절한 심혈관계 건강을 유지하는 것이 성인기 심혈관질환을 예방하는데 매우 중요하다. 아직까지 이상지질혈증의 약물요법 중 스타틴 제제를 제외하고 소아청소년에서의 치료 경험, 효과, 안정성에 대한 연구가 제한적인 실정이다. 향후 다른 제제들에 대해서도 후속 연구가 활발히 이뤄지고, 긍정적인 결과로 소아청소년에서 임상적 적용이 가능해진다면, 소아청소년기 심혈관계 건강을 향상시키는 데 도움이 될 것이다.
Notes
Conflict of Interest
No potential conflict of interest relevant to this article was reported.
References
Peer Reviewers’ Commentary
이 논문은 최근 소아청소년의 비만율 증가와 더불어 급증하고 있는 이상지질혈증의 진단 및 치료에 관하여 최신문헌을 토대로 정리하여 설명해 주고 있다. 이상지질혈증은 대사증후군, 심근경색증, 뇌졸중 등과 같이 생명을 위협할 수 있는 심각한 만성 합병증을 초래할 수 있기 때문에 소아청소년 시기부터 예방하는 것이 매우 중요하다. 하지만, 성인에서와 달리 소아청소년 이상지질혈증 환자에서 사용할 수 있는 약제는 한정적이어서 치료에 어려움이 있다. 이 논문에서는 소아청소년의 이상지질혈증에서 사용할 수 있는 약제들의 특장점과 부작용 등을 잘 정리하여 알기 쉽게 설명하고 소아청소년 비만 또는 이상지질혈증 환자를 진료하는 임상 현장에 많은 도움이 될 것으로 판단된다.
[정리: 편집위원회]