만성 경막하혈종의 발병기전 및 역학
Pathogenesis and epidemiology of chronic subdural hematoma
Article information
Trans Abstract
Background
Chronic subdural hematoma (SDH) is a common condition encountered in neurosurgical practice; however, its pathogenesis remains controversial.
Current Concepts
SDH refers to blood accumulation inside the dura and is classified into acute, subacute, and chronic types. Histopathologically, acute SDH shows no neomembrane formation and the hematoma is a clot, in contrast to chronic SDH characterized by a neomembrane surrounding the liquefied hematoma. SDH is usually categorized into acute and chronic types, with subacute SDH being more similar to chronic SDH. Posttraumatic subdural lesions include acute and chronic SDH, subdural hygroma (SDG), or effusion. SDG is a blood-tinged fluid accompanied by neomembrane formation in some cases. These lesions are pathologically different from each other but may change depending on the situation.
Discussion and Conclusion
Chronic SDH mainly originates from an SDG and acute SDH. SDG is usually triggered by trauma but only occurs in patients in whom sufficient potential space is available and may occur spontaneously in such cases. Therefore, SDG frequently occurs in children and in elderly patients, in men with a larger skull size, and on the left side of the body, which usually shows a wider hemisphere. Separation of the dural border cell layer causes inflammation, indicated by fibroblast proliferation and neovascularization. Conversion of an SDG into a chronic SDH or enlargement of a chronic SDH is attributable to formation of neomembranes, neovascularization, and repeated microhemorrhages from fragile capillaries. Chronic SDH is treated with removal of the hematoma to relieve the mass effect and embolization of the feeding artery for the bleeder. Outcomes of chronic SDH depend on the absorptive-expansion capacity dynamics.
서론
만성 경막하혈종(chronic subdural hematoma)은 신경외과 분야에서는 흔히 보는 질병이지만, 병인을 두고 논란이 있었다[1]. 경막하혈종은 경막 안쪽에 피가 고인 것을 말하는데, 흔히 혈종 발생 시기에 따라 급성, 아급성, 그리고 만성으로 분류해 왔다[2]. 병리조직학적으로 급성과 만성 경막하혈종을 구분하자면 급성은 혈종을 싸고 있는 신생막(neomembrane)이 없고, 혈종이 굳은 피 덩이(clot) 상태인 반면에, 만성은 혈종을 싸고 있는 막이 있고, 혈종이 액화(liquefied)된 상태란 점이 두드러진 특징이다. 아급성은 급성과 만성의 특징이 섞인 과도적 상태지만 만성과 더 유사하기 때문에, 아급성을 만성에 포함하여 보통 급성과 만성으로만 구분하기도 한다.
다친 뒤 생기는 경막하 병터(lesion)는 급성과 만성 경막하혈종 이외에 경막하수종(subdural hygroma)이 있다[3-5]. 경막하수종은 내용물이 황변색(xanthochromic) 또는 핏물이 든 수액(blood-tinged fluid)이며, 시기에 따라 신생막이 있을 수 있다. 이 병터들은 병리학적으로는 서로 다르지만, 상황에 따라 서로 바뀌기도 한다[3-5]. 최근 진단기기의 발달과 함께 새로운 사실이 많이 밝혀졌다[5-12]. 새로 발표된 내용을 중심으로 병인과 병태생리, 그리고 역학을 기술 하고자 한다.
경막하수종
경막하수종은 충분한 잠재공간(potential space)과 경막경계세포층(dural border cell layer) 분리라는 두 조건이 충족되면 생기는데, 충분한 잠재공간이 더 중요하다[12]. 경막경계세포층의 분리는 경막하수종의 직접적인 발생 원인이지만[5], 이층의 분리는 반드시 외상으로만 생기는 것은 아니다. 탈수나 인위적 뇌 수축, 개두술, 또는 과다한 뇌척수액 배액으로도 경막경계세포층이 분리된다[13-16]. 경막하수종의 전제조건인 충분한 경막하강은 연령의 양 끝인 5세 이전과 50세 이후에 흔한데[2], 5세 이전의 소아 뇌는 성인에 비해 수분함량이 많아 쉽게 압박될 수 있으며, 50세 이후의 노인의 뇌는 뇌 위축으로 인해 잠재적 경막하강이 넓다[5,13,17]. 그리고 이 나이 분포는 만성 경막하혈종도 같다. 곧 두 병터의 발생조건이 서로 같음을 뜻한다.
경막경계세포층이 분리되면 이 공간에 주로 삼출에 의해 수액이 고인다[2,5]. 경막하수종의 수액은 뇌척수액이나 혈장(serum)에서 모두 생길 수 있지만, 혈액보다는 뇌척수액에서 주로 만들어진다[18]. 경막경계세포층이 분리되면 바로 경막경계세포층이 증식되기 시작한다[10,13,19]. 24시간 이내에 섬유아세포(fibroblast)가 경막 표피에서 자라 들어오며, 일주일이 지나면 눈으로도 볼 수 있는 외막(outer membrane)이 생긴다. 그리고 3주가 지나면 내막(inner membrane)이 생겨 혈종이 완전히 둘러싸인다. 이 혈종막중 혈관이 많은 외막은 경막의 풍부한 혈관을 통해 증식이 더 활발해서 일찍 두꺼워지는 반면, 무혈관조직인 거미막과 가까운 내막은 얇고 더 늦게 생긴다. 신생막이 생기면, 이곳에는 신생혈관증식이 뒤따르는데, 이 신생혈관들은 투과성이 높고 유약하여 출혈되기 쉽다[19]. 이 신생혈관에서 반복 미세출혈(repeated micro-hemorrhage)이 지속되면 경막하수종에 혈액이 섞이고, 출혈이 많아지면서 점차 혈종으로 바뀐다[3,4,6,12,19]. 경막하수종은 뇌 위축이나 과다한 탈수 또는 두개강내압 감소와 같은 뇌 수축(shrinkage)이 심해지면 더 커지는 반면에, 두개강내압 항진이나 수두증(hydrocephalus)처럼 뇌가 팽창을 하면 흡수되어 없어진다. 거의 대부분이 3개월 이내에 흡수되어 소실되지만, 흡수되지 않고 오래 잔존하는 경막하수종은 만성 경막하혈종으로 바뀌게 된다[13].
급성 경막하혈종
급성 경막하혈종은 중증 두부손상의 가장 중요한 사망원인으로 알려져 있는데, 환자의 2/3가 혼수상태일 정도로 뇌 손상의 정도가 심하다. 혈종이 뇌를 압박하기 때문에, 응급감압수술로 혈종을 제거해야 한다. 그러나 혈종이 크지 않거나 경막하강에 여유공간이 있는 일부 환자에서는 혈종이 서서히 용해되고 흡수되어 소멸되기도 한다[20]. 때로는 경막하수종처럼 신생막이 생기고, 뒤이어 신생혈관이 생겨나 반복적인 미세출혈을 통해 혈종이 점점 커져 만성 경막하혈종으로 바뀌기도 한다[4]. 경막하혈종이 경막과 거미막(arachnoid) 사이에 고이면 경막하수종과 마찬가지로 분리된 경막경계세포층의 증식에 의해 혈종을 둘러싸는 막이 생긴다. 또한 혈종막 안의 혈액은 처음에는 응고된 혈종이지만, 곧 섬유소분해력(activity of fibrinolysis)이 증가되면서 액화된다. 경막 쪽으로는 경막경계세포층이 두텁게 증식하여 외막을 만들고, 이 신생 외막에는 새로운 혈관이 만들어진다. 이렇게 새로 만들어진 혈관은 투과성은 높고 기계적으로는 약한 상태에서 혈종의 액화로 증가된 섬유소분해력이 작용하여 외막에서 쉽게 출혈이 생기고, 이러한 출혈이 반복되면서 혈종이 점점 커진다. 이러한 과정을 통해 만성 경막하혈종은 경막 안쪽에 주머니에 싸인 검은 액체, 곧 전형적인 윤활유(crankcase oil)와 같은 모습이 된다.
만성 경막하혈종의 발병기전
만성 경막하혈종은 경막하수종과 일부 급성 경막하혈종이 기원이다(Figure 1). 경막하수종은 대부분 다친 뒤 3일 이내에 발견된다[5]. 다친 뒤 거의 대부분의 환자들은 앙와 위(바로누운자세, supine position)로 드러눕는데, 이 때 뇌는 아래쪽으로, 뇌척수액은 위쪽에 옮겨 양쪽 앞머리에 경막하수종이생긴다. 특히 두개골이 대칭인 사람은 양측 전두부에 생기는 반면, 비대칭인 경우 머리가 기울면서 경막하수종이 반대쪽 앞머리 한쪽에 자리잡는 경우가 많다. 물론 뇌 위축이 심한 쪽이거나 다른 덩이 병터(mass lesion)가 있을 때에는 이러한 예측을 벗어나기도 하지만, 경막하수종이 공간점유 병터가 아니라 빈자리 병터(ex vacuo)라는 사실과는 부합한다. 이를 통해 경막하수종의 위치는 두개골의 모양과 중 력에 의해 결정되며, 두개강 내에서 가장 압력이 낮은 곳에 생긴다[21]. 또한 두개골이 대칭일 때 양쪽에 생기기 쉽고, 비대칭일 때에는 머리가 기운 쪽 반대편에 생기기 쉽다. 한편, 비대칭 두개골이어서 한쪽으로 머리가 기울면, 처음에 양쪽에 생겼던 경막하수종이 기운 쪽에서는 축소되는 반면, 반대쪽에서는 커지기 쉽다. 머리가 기운 쪽에서는 흡수 소실되고, 반대쪽에서는 점점 더 커져서, 양측성이었던 경막하수종이 일측성 만성 경막하혈종으로 바뀌게 된다. 이런 과정을 통해 경막하수종은 80% 정도가 양측성이지만, 만성 경막하혈종은 거꾸로 약 80%가 일측성이 된다. 급성 경막하혈종이 양쪽에 생기는 경우는 극히 드물다. 일측성이었던 급성 경막하혈종이 양측성 만성 경막하혈종으로 바뀔 가능성 역시 극히 희박하다. 반면에 경막하수종은 60-80%가 양측성으로 생긴다[21,22]. 따라서 양측성으로 생긴 만성 경막하혈종은 경막하수종에서 기원했을 가능성이 크다.
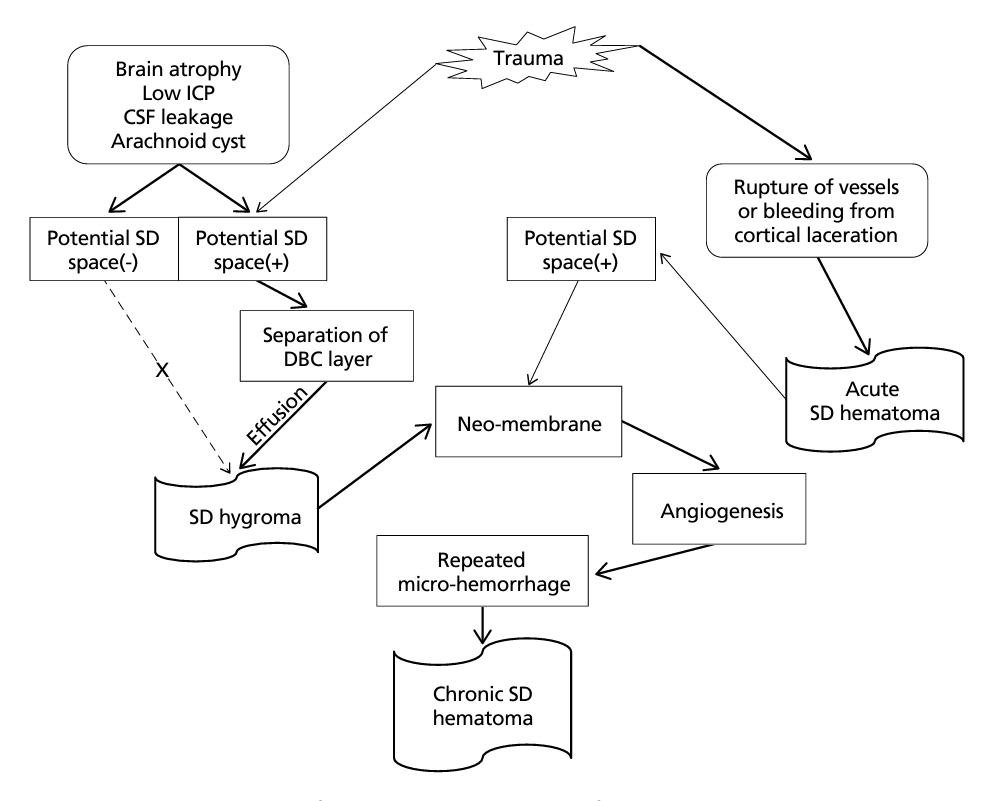
Schematic illustration of the origin and pathogenesis of chronic subdural hematoma. ICP, intracranial pressure; CSF, cerebrospinal fluid; SD, subdural; DBC, dural border cell. Illustrated by the author.
만성 경막하혈종이 생기기 위해서도 충분한 잠재적 경막하강과 경막경계세포층의 분리라는 두 가지 조건이 충족되어야 한다. 다쳐서 생긴 경우가 많지만, 두부외상이 없더라도 위 두 가지 조건이 충족되면 만성 경막하혈종이 생길 수 있다. 만성 경막하혈종이 잘 생기는 요인으로는 기계적 인자(mechanical factor)와 혈액인자(hematologic factor)가 있다.
기계적 인자로는 낮은 두개강내압(질병이나 손상, 요추천자나 뇌척수액 단락술, 탈수 등), 뇌 위축, 그리고 출생할 때 과다한 두개골 변형 등을 들 수 있다. 혈액인자로는 혈우병, 혈소판감소증, 간질환, 항응고제 투여 등의 응고장애를 들 수 있다. 실제로는 이러한 요인이 함께 존재하여 축적효과를 보인 경우가 많다. 즉 노년층에서는 생리적인 뇌 위축이 있고 잦은 음주로 간 기능이 나쁜데다 자주 머리를 다치거나 치료 또는 예방목적으로 항응고제를 사용하는 경우가 많기 때문이다.
어떤 형태의 혈액응고 장애든 모두 만성 경막하혈종이 쉽게 생길 수 있는 요인이 될 수 있지만[23], 실제로 혈액응고장애와 관련된 만성 경막하혈종의 빈도는 대상 환자의 특성에 따라 서로 다르다. 만성 경막하혈종의 8-41%가 항응고제의 사용과 관련이 있다고 하며, 최근 노인인구의 증가로 항응고제를 사용하는 사람들이 늘어나면서 항응고제가 만성 경막하혈종의 발생을 촉진하는 경우도 점점 늘고 있다고 한다[24,25]. 특히 와파린(warfarin)을 쓴 환자는 그렇지 않은 환자에 비해 무려 42.5배의 위험이 있다고 한다[26]. 혈액응고 이상이 있을 때에는 만성 경막하혈종이 더 잘 생기게 하는 조건이 되면서 다른 한편으로는 수술 후 재발할 위험을 더 높이기도 한다[27]. 한편 아스피린(aspirin)이나 클로피도그렐(clopidogrel) 같은 항혈소판제를 사용하다가 생긴, 증상이 심하지 않은 만성 경막하혈종은 항혈소판제 사용을 중지하기 만해도 혈종이 저절로 없어지기도 한다[28].
경막하혈종의 신생막은 경막경계세포층이 떨어지면서부터 생기기 시작하는데, 신생막이 처음 생길 때에는 미성숙 섬유아세포(immature fibroblasts)와 교질섬유(collagen fibers)가 듬성듬성 성기게 있고 가끔 신생 모세혈관이 보이는 정도의 얇은 비염증막(noninflammatory membrane, type I)의 형태지만, 시간이 지나면서 많은 세포들과 신생혈관들이 침투한 미성숙 결체조직(connective tissue)이 한 층을 이루는 염증막(inflammatory membrane, type II)으로 바뀐다. 이후 염증반응이 더 심해지면 두세 층의 결체조직 안에 더 많은 세포들이 침투되고, 큰 직경의 모세혈관과 함께 혈종 쪽에는 많은 얇은 신생혈관이 보이는 출혈성 염증막(hemorrhagic inflammatory membranes, type III)으로 바뀐다[10]. 이 때부터 막내 출혈(hemorrhage into the membrane)이 가끔 관찰되며 혈종이 커지기 시작한다. 하지만 뇌 위축이 심하여 두개강내압과 조금씩 커지는 혈종이 서로 균형을 이루게 되면 출혈성 염증막 상태가 반복적으로 지속되는 경우가 생길 수 있는데, 이렇게 염증막 안으로 출혈이 생기고, 출혈부위에 섬유세포층이 자라 들어간 다음, 새로운 혈관이 또 만들어지면서 여러 층의 섬유조직과 혈관과 출혈에 섞이면서 혈종이 기질화되면 내출혈 경막증(internal hemorrhagic pachymeningiosis), 또는 박리성 경막증(pachymeningiosis dissecans)이라고 하는 드문 병터가 생긴다[29]. 그러나 세월이 가면 취약했던 신생혈관이 성숙하면서 출혈이 줄어들고, 만성 염증과 흉터가 대부분을 차지하는 반흔성 염증막(scar inflammatory membrane, type IV)으로 바뀐다[10,30]. 신생막이 반흔성 염증막으로 성숙하면 신생혈관도 더 이상 취약하지 않게 되어 출혈은 줄고 흡수가 늘어나면서 결국 혈종은 흡수되어 소실된다. 출혈성 염증막의 비정상적 비후가 내출혈 경막증이라고 하는 드문 병터를 만드는 데 비해, 반흔성 염증막에 비정상적으로 석회가 침착하면 만성 경막하혈종의 석회화가 생기고, 더 드물게는 골화가 되기도 한다[31]. 석회화가 되기까지 걸리는 시간은 대부분 6개월 이상이라고 하고, 골화가 되기까지는 수년이 걸린다고 한다[31,32]. 한편, 내출혈 경막증은 경막이 출혈과 괴사가 섞인 여러 층의 섬유조직으로 두꺼워진 특발성 비후성경막염(idiopathic hypertrophic pachymeningitis)이라고 하는 만성 염증성 질환과 비슷한데, 특발성 비후성 경막염은 주로 대뇌겸(falx cerebri)과 천막(tentorium)에 잘 생기는 반면 내출혈 경막증은 대뇌 볼록면(convexity)에 잘 생긴다[33]. 염증막이나 석회화는 주로 바깥쪽, 그러니까 경막 쪽 신생막에서 더 일찍, 그리고 더 활발하게 진행되며, 두껍고 출혈이 잘 생기는 혈종 외막과 달리 혈종 내막은 투명한 황갈색 막으로 그 두께는 30-300 μm 정도로 얇다고 한다[34].
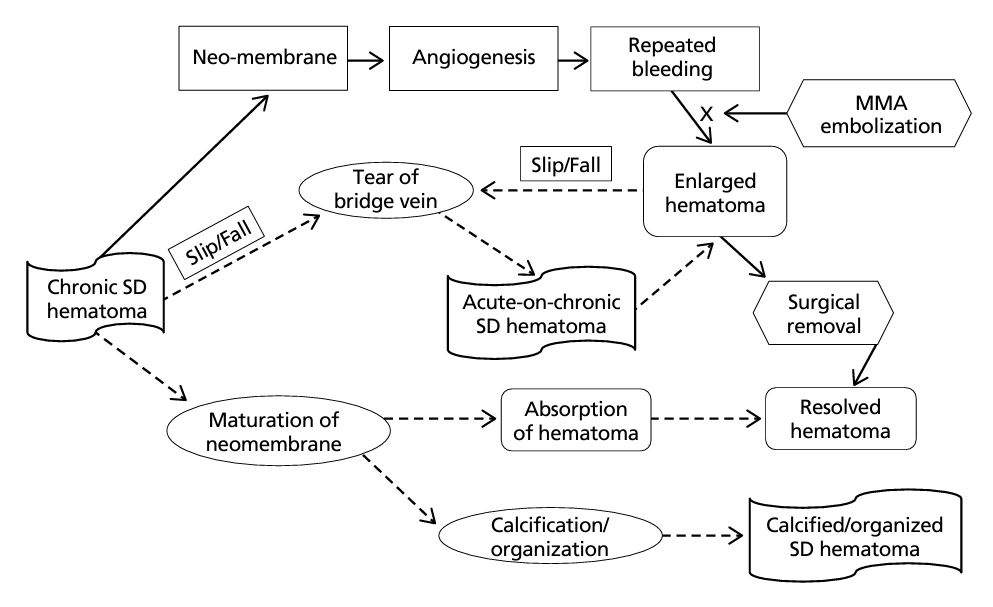
경막하수종이 만성 경막하혈종으로 전환되거나 만성 경막하혈종이 더 커지는 기전은 결국 신생혈관의 유약한 혈관과 국소 응고장애로 인한 반복적인 미세출혈 때문이다[35]. 그리고 중간수막동맥(middle meningeal artery)이 신생혈관의 주요 영양혈관(feeder)이 된다[36]. 만성 경막하혈종은 시간이 갈수록 계속 조금씩 바뀌는데, 크게 세 가지 과정을 따른다(Figure 2). 첫 번째는 신생막을 따라 생긴 새로운 혈관의 반복되는 미세출혈에 의해 혈종이 조금씩 점점 커지는 과정이다. 만성 경막하혈종이 점점 커져서 증상을 만들게 되면 그 증상 때문에 진단을 하고 치료를 하게 되어 만성 경막하혈종은 제거된다. 만성 경막하혈종의 증상 유발은 대부분 커진 혈종 때문이고, 혈종의 제거는 증상을 제거함과 같지만, 혈종 성장의 원인인 출혈혈관(bleeder)은 그대로 둔 상태이다. 반면 중간수막동맥의 색전술(embolization)은 혈종은 그대로 두고 출혈혈관을 제거하는 방법이다. 두 방법 모두 팽창역량(expansion capacity)보다는 흡수역량(absorption capacity)을 크게 하여 혈종소실로 이끌지만, 제거되지 않은 출혈혈관 때문에 재발되기도 한다. 두 번째는 만성 경막하혈종으로 인해 쉽게 넘어지면서 별로 심하지 않은 외상으로도 늘어진 교정맥이 쉽게 찢어져 만성 경막하 혈종에 새로 급성 경막하혈종이 중첩되는 과정이다[37]. 하지만 모든 만성 경막하혈종이 다 커지는 게 아니라 뇌가 위축되거나 뇌척수액이 두개강에서 다른 쪽으로 빠져나가면서 균형을 이루게 되면 아무런 증상이 없는 채로 지나기도 한다. 그리고 경막하혈종이 조금씩 저절로 흡수되어 없어지기도 하고, 드물게 혈종의 막이 비정상적으로 비후되거나 기질화(organization)되면서 특이한 형태의 변형된 만성 경막하혈종이나[29,38] 석회화(calcified) 또는 골화(ossified) 된 만성 경막하혈종을 만들기도 한다[31-33,39]. 또한 이처럼 만성 경막하혈종은 시간이 지남에 따라 계속 변하게 되며, 최종 운명은 혈종의 흡수역량과 팽창역량 간의 줄다리기에 의해 결정된다[40].
만성 경막하혈종의 역학
만성 경막하혈종의 빈도는 인구 10만 명당 1-2명에서부터 많게는 인구 10만 명당 약 7.4명 정도까지 다양하다[41,42]. 이는 인구의 구성비에 따라 노인인구가 많아질수록 빈도가 올라가는 경향이 있기 때문이다. 주로 노년층에서 호발하며 3/4 이상이 50대 이후에 발생하고, 평균연령은 63세라고 한다. 노인에 잘 생기는 이유는 노화에 따른 뇌 위축과 두개강내압 감소에 의해 교정맥(bridge vein)이 팽팽하게 늘어진 상태로 있기 때문이며, 나이가 들면 운동신경이 둔해져 다치기 쉽고, 고혈압이나 동맥경화 등으로 인해 항혈소판제나 항응고제를 복용하는 경우가 많은 것도 영향을 준다.
만성 경막하혈종은 외상에 의해 발생하는 경우가 가장 흔하다. 전체 만성 경막하혈종의 약 50-80% 정도가 외상에 의해 발생한다고 한다[43]. 바꾸어 말하면 20-50%의 환자가 뚜렷하게 외상을 받은 기억이 없다. 기억을 못하는 경우도 물론 있지만, 기억하지 못할 정도로 가벼운(trivial) 손상인 경우도 많다. 때로는 저절로 생기기도 하는데, 특히 상습적인 음주나 혈액응고 장애, 출혈성 질환, 항응고제 투여, 뇌전증, 두개강내압 저하, 뇌종양, 거미막 낭종(arachnoid cyst) 등이 있는 사람들은 기억할만한 외상이 없어도 만성 경막하 혈종이 생길 수 있다[43]. 일반적으로 나이가 아주 많은 사람들에 비해 젊은 나이에 생긴 만성 경막하혈종은 알코올중독이나 거미막 낭종, 또는 뇌전증과 같은 위험요소가 있는 경우가 더 많다고 한다. 알코올중독은 만성 경막하혈종 환자의 약 6-35% 정도에서 확인되는데, 잦은 음주로 인한 알코올성 뇌 위축과 함께, 알코올성 간 질환으로 인해 혈액응고 이상이 있을 위험이 큰 상태에서 술에 취해 머리를 다칠 가능성까지 높기 때문에, 만성 경막하혈종이 생길 위험이 아주 높다. 한편 뚜렷하게 다친 기억이 없거나 다치지 않은 상태에서도 만성 경막하혈종이 생길 수 있기 때문에, 때로는 그 원인을 두고 다툼이 생기는 경우도 있다. 이런 경우에는 외상이 영향을 준 정도를 정량적으로 추정하는 방법[44]을 이용할 수도 있겠다.
만성 경막하혈종은 여자보다는 남자에서 더 잘 생긴다. 성비는 저자에 따라 서로 다른데, 1.6-5.6:1이라고 한다. 이처럼 남자에서 더 잘 생기는 이유로 흔히 남자들이 더 잘 다치기 때문이라는 주장[43], 여성의 경우 에스트로젠이 모세혈관 보호 작용을 하기 때문이라는 주장[45], 그리고 뇌의 노화가 남녀가 서로 다르기 때문이라는 주장[46]도 있다. 하지만 두개골의 크기가 남자가 더 크고 왼쪽 대뇌반구가 더 큰 비대칭성 때문에, 남자에 많고 왼쪽에 더 잘 생긴다[47].
결론
만성 경막하혈종은 주로 경막하수종과 급성 경막하혈종에서 기원한다. 경막하수종은 주로 외상이 촉발하지만, 두개강 내 충분한 잠재공간이 있을 때에만 생긴다. 잠재공간이 충분할 때에는 저절로 생기기도 한다. 이런 이유로 소아와 노인에 잘 생긴다. 또한 두개골이 큰 남자에 더 잘 생기고, 왼쪽에 더 잘 생긴다.
경막하수종이든 급성 경막하혈종이든 경막경계세포층이 분리되면 섬유아세포 증식과 신생혈관생성 등 염증반응이 유발된다. 경막하수종이 만성 경막하혈종으로 전환되거나 만성 경막하혈종이 커지는 기전은 염증반응에 따른 신생막과 신생혈관의 생성, 그리고 유약한 혈관과 국소 혈액응고 장애로 인한 반복적인 미세출혈의 결과이다. 만성 경막하혈종의 제거는 덩이 효과에 대한 처치인 반면, 영양혈관인 중간수막동맥의 색전술은 출혈혈관에 대한 처치라고 볼 수 있다. 만성 경막하혈종의 운명은 흡수역량과 팽창역량 간의 줄다리기에 의해 결정된다.
Notes
Conflict of Interest
No potential conflict of interest relevant to this article was reported.
References
Peer Reviewers’ Commentary
이 논문은 만성 경막하혈종의 발병기전, 역학 및 치료에 대해서 최신문헌을 토대로 정리하여 상세하게 설명해 주고 있다. 만성 경막하혈종은 노년층에 많이 발생하는 신경외과 질환이다. 만성 경막하혈종은 비교적 흔한 질환이지만 어떤 기전으로 반복 출혈이 발생하여 확장되고 증상을 일으키게 되는지 밝혀진 것은 그리 오래되지 않다. 급격히 노령화가 진행되고 있는 점을 고려하면, 만성 경막하혈종 환자는 더 많이 증가하게 될 것이므로 일차의료기관에서도 드물지 않게 진료하게 될 것으로 예상된다. 이 논문은 임상 현장에서 만성 경막하혈종 환자를 진단하고 적절한 치료를 수행하는 데 많은 도움이 될 것으로 판단된다.
[정리: 편집위원회]