유방암 검진 권고안 개정안
The Korean guideline for breast cancer screening
Article information
Abstract
Breast cancer is the second most common malignancy among Korean women. The 2002 National Cancer Center screening guideline breast cancer was revised via an evidence-based approach to provide medical personnel with a standard protocol of screening breast cancer. There is moderate-level evidence that biennial screening mammography in asymptomatic women aged 40 to 69 reduces breast cancer mortality, while low-level evidence suggests that screening mammography in women 70 years or older does not reduce breast cancer mortality. The committee concluded that the current evidence is insufficient to assess the benefits and harms of either ultrasonography or clinical breast examination as screening modalities for breast cancer. Future researches about the benefits and harms of the National Breast Cancer Screening Program in Korea are strongly required because the characteristics of breast cancer in Korea are different from those in the West, especially regarding dense breast. In conclusion, the committee recommends biennial screening mammography in asymptomatic women aged 40 to 69 years (grade B recommendation). The committee recommends selective screening mammography in women 70 years or older according to individual risk and preference (grade C recommendation). The committee neither recommends nor opposes ultrasonography and clinical breast examination as screening modalities (grade I recommendation). Symptomatic and high-risk women, however, should be offered complementary measures including ultrasonography and clinical breast examination under clinical supervision.
검진 근거문과 근거수준
40-69세 여성을 대상으로 유방촬영술을 이용한 유방암 검진을 2년마다 시행하는 것은 유방암 사망률을 유의하게 감소시키며 근거수준은 중등도이다(moderate). 70세 이상 여성에서 유방촬영술을 이용한 유방암 검진이 유방암 사망률을 낮추는가에 대한 근거수준은 낮다(low). 유방암 검진에서 유방초음파검사 또는 임상유방진찰의 사망률 감소효과에 대한 근거는 불충분하며 근거수준은 매우 낮다(very low).
검진 권고안과 권고등급
40-69세 무증상 여성을 대상으로 유방촬영술을 이용한 유방암 검진을 2년마다 시행할 것을 권고한다(권고등급 B). 70세 이상에서 유방촬영술을 이용한 유방암 검진은 개인별 위험도에 대한 임상적 판단과 수검자의 선호도를 고려하여 선택적으로 시행할 것을 권고한다(권고등급 C). 유방초음파검사 단독 또는 유방촬영술과 병행하여 유방초음파검사를 유방암 검진으로 시행하는 것을 권고하거나 반대하지 않는다(권고등급 I). 임상유방진찰 단독 또는 유방촬영술과 병행하여 임상유방진찰을 유방암 검진으로 시행하는 것을 권고하거나 반대하지 않는다(권고등급 I).
검진의 이득과 위해
(1) 검진의 이득
무작위대조 비교임상시험 결과들을 메타분석했을 때 유방촬영술을 이용한 유방암 검진군은 대조군보다 유방암 사망률이 약 19% 낮았고 통계적으로 유의하였다.
(2) 검진의 위해
유방촬영술을 이용한 유방암 검진은 방사선 피폭, 과진단, 위양성으로 인한 불안감, 불필요한 생검과 수술, 중간암 발생 등의 위해가 있을 수 있다. 그러나 유방암 검진의 위해 보다는 이득이 중등도로 더 크다고 판단하였다.
임상에서의 고려사항
본 권고안은 무증상의 평균적인 위험을 가진 여성을 대상으로 한 것이다. 증상이 있거나 고위험군 여성은 임상의의 판단에 따라 임상유방진찰, 유방초음파검사 등의 추가적인 조치를 시행할 수 있다.
서론
유방암은 국내에서 갑상선암 다음으로 많이 발생하는 여성암으로서 1999년 국가암발생통계가 산출된 이래 2012년까지 매년 연평균 6.1%씩 증가하고 있으며 2012년 현재 유방암의 연령표준화 발생률은 인구 10만 명당 65.7명으로 여성암 발생자의 14.8%를 차지하고 있다[1]. 국내 유방암의 발생률은 연령에 따라 점점 증가하다가 45-49세 구간에서 가장 높고, 그 이후에는 감소하는 추세를 보이는데 이는 연령이 증가할수록 유방암 발생률이 증가하는 서구와는 다른 양상이다[1].
유방암 검진 및 관련 연구는 주로 서구에서 활발히 진행되었는데 최근에는 유방촬영술을 이용한 검진이 진행암의 발생을 효과적으로 감소시키지 못하므로 유방암 사망률 감소효과가 미약하다는 주장과, 수검 대상자에게 이득과 위해에 대한 정보를 충분히 제공하여 informed decision을 내릴 수 있도록 해야한다는 주장이 대두되고 있다[23].
1999년 국가암검진사업의 일환으로 유방암 검진이 시작된 이후 정확도에 대한 문제가 계속 제기되었으나 최근에는 질 관리 사업을 통해 유방암 검진의 정확도가 향상되었고(미발표 자료), 국가유방암검진 자료를 분석하여 유방암 검진의 효과에 대한 근거가 마련되었다[4]. 이에 따라 유방암 검진의 이득과 위해를 기반으로 유방암 검진 권고안을 개정하게 되었다.
국립암센터 주관으로 한국유방암학회, 대한영상의학회, 대한예방의학회, 대한가정의학회가 추천한 다학제적 전문가로 유방암 검진 권고안 개정위원회(이하 위원회)를 구성하였다. 위원회는 근거중심의 유방암 검진 권고안을 개발하여 의료인에게 유방암 검진의 표준지침을 제공하고, 유방암 검진의 효과와 위해에 대한 적절한 정보를 제공하고자 하였다.
개발방법
1. 유방암 검진 권고안 개발전략
위원회는 유방암 검진에 대한 핵심질문 6개를 도출하고(Figure 1), 관련 권고안 검토와 체계적 문헌 고찰을 통해 유방암 검진의 이득과 위해를 평가하였다. 먼저, 기존의 유방암 검진 권고안을 검색하여 근거에 기반하여 개발된 권고안이 있는 경우 그 근거를 수용하였다. 권고안 개발 이후에 발표된 최신 국내외 문헌을 추가로 검토하여 근거를 평가한 후 기존 권고안을 개작하는 방식으로 권고안을 개발하였다.

Framework of developing a guideline for breast cancer screening. Key question (KQ) 1, effectiveness of breast cancer screening using mammography (reduction of breast cancer mortality and all cause mortality, and stage shift); KQ 2, starting and ending age, and appropriate period of breast cancer screening using mammography; KQ 3, hazard of mammography screening; KQ 4, effectiveness of breast cancer screening using ultrasonogrphy; KQ 5, hazard and accuracy of breast cancer screening using ultrasonogrphy; KQ 6, effectiveness of breast cancer screening using clinical breast examination. CBE, clinical breast examination.
2. 검진 권고안 검색
무증상 여성을 대상으로 시행한 유방촬영술, 유방촬영술 + 유방초음파검사, 유방촬영술 + 임상유방진찰을 이용한 유방암 검진 지침을 검색하였다. 국외 검색원은 PubMed (http://www.ncbi.nlm.nih.gov/PubMed/), National Guideline Clearinghouse (NGC, http://www.guideline.gov), Guideline International Network (GIN, http://www.g-i-n.net), Cochrane Library (http://www.thecochranelibrary.com)였고, 국내 검색원은 Korean Guideline Clearinghouse (KGC, http://ncrc.cdc.go.kr/guideline), 진료지침(권고안) 정보센터 (KoMGI, http://www.guideline.or.kr/)였다. 검색어는 breast cancer screening guideline으로 하였고 검색기간은 2005년 이후로 제한하였다.
검색결과 10개를의 권고안을 선정하였으며 권고안 당 2인의 실무위원이 AGREE II 도구를 이용하여 독립적으로 질 평가를 시행하였다. 위원들 간의 의견이 일치하지 않는 경우에는 합의를 통해 최종적으로 결정하였다. 그 결과 2011년에 발표된 캐나다 권고안과 2013년에 발표된 일본 권고안 초안을 수용개작의 대상으로 선택하였다[56].
3. 문헌검색
두 권고안에 반영된 문헌의 검색기간을 고려하여 그 이후에 발표된 국내외문헌을 추가로 검색·선정하였고, 국내 연구결과도 검색·선정하였다. 국내외 문헌검색원은 Ovid-Medline, Ovid-Embase, Cochrane library (CENTRAL), 한국과학기술정보연구원, 한국의학논문데이터베이스, 과학기술정보통합서비스, 한국학술정보, KoreaMed였다. 검색어는 breast cancer screening, mammography + breast sono vs. mammography, ductal carcinoma in situ overdiagnosis, 위해였다. 핵심질문에 따라 검색전략을 달리하였는데 유방촬영술을 이용한 유방암 검진에 대한 문헌은 캐나다 권고안에 포함한 것을 일차적으로 선정하고, 2009년 이후에 발표된 무작위배정 비교임상시험으로 제한하여 추가검색을 실시하였다. 유방촬영술 + 유방초음파검사 vs. 유방촬영술의 효과와 정확도에 대한 문헌은 코크란 리뷰의 검색전략을 활용하였고 2011년 이후의 문헌을 추가로 검색하였으며 무작위대조 비교임상시험이나 관찰연구 등의 연구디자인은 제한하지 않았다. 과진단과 위해에 대한 문헌은 캐나다 권고안의 검색전략을 활용하였으며 2009년 이후에 발표된 추가문헌을 검색하였으나 연구디자인은 제한하지 않았다. 국내 문헌과 연구결과는 모든 핵심질문에 대해 검색기간과 연구디자인의 제한을 두지 않고 검색하였다.
검색된 문헌은 문헌당 2인의 실무위원이 독립적으로 문헌 선택/배제여부를 평가하였다. 먼저, 제목과 초록을 보고 선택/배제를 결정하였으며, 1명이라도 선택한 문헌은 원문을 검색하였다. 그 후에 원문을 보고 비뚤림 위험도(risk of bias)와 RoBANS (risk of bias assessment tool for nonrandomised study)를 이용하여 질 평가를 시행하였다. 위원들 간의 일치가 이루어지지 않은 경우 재평가 및 합의를 통해 최종적으로 결정하였다.
핵심질문 1의 사망률 감소효과에 대해서는 자체적으로 메타분석을 시행하였다. 메타분석시 변동효과모형(random-effect model)을 사용하였고, 통계 프로그램은 RevMan 5.2를 이용하였다. 핵심질문 2는 기존의 메타분석 결과를 차용하였다[67]. 메타분석 결과에 대한 근거수준 평가는 grading of recommendations assessment, development and evaluation (GRADE)를 이용하였다. 그 외의 핵심질문은 근거수준을 평가하지 않았다. 체계적 문헌검색과 문헌 질평가 및 근거수준 평가는 국립암센터가 개발한 '국가암검진 권고안 제개정 연구 방법론'에 따라 진행하였다. 유방암 검진에 대한 최종 권고등급은 GRADE로 평가한 근거수준과 위원회가 평가한 유방암 검진의 이득과 위해의 크기를 종합하여 결정하였다.
결과
1. 유방암 선별검사로서 유방촬영술은 효과적인가?
1) 유방암 사망률
수용개작 대상으로 선택한 캐나다와 일본 권고안에서 유방촬영술을 이용한 검진의 효과에 대해 평가의 근거로 삼은 무작위배정 비교임상시험은 총 8개였다. 그중 연구의 질이 낮았던 Edinburgh trial을 제외하고 UK Age Trial, Canadian National Breast Screening Study (CNBSS), Göteborg Trial, Health Insurance Plan (HIP) Trial, Malmö Mammographic Screening Trial (MMST), Stockholm Mammographic Screening Trial, Swedish Two-County Trial 등 7개의 연구를 이용하여 메타분석을 시행하였는데 CNBSS는 CNBSS-1과 CNBSS-2 대상자를 25년간 추적관찰한 결과를 이용하였다[891011121314]. 메타분석 결과 유방촬영술을 이용한 검진의 유방암 사망률에 대한 상대위험도는 0.81 (95% 신뢰구간, 0.73-0.91) 이었고, 검진군에서 유방암 사망률이 19% 감소하였으며 통계적으로 유의하였다(Figure 2) [891011121314]. 메타분석에 포함된 7개의 연구 중 UK Age Trial, CNBSS, MMST를 제외한 4개는 무작위배정에 문제가 있었으므로 메타분석 결과에 대한 근거수준은 moderate으로 평가하였다(Table 1).

Forest plot for breast cancer mortality (all age). Relative risk of breast cancer mortality in screening with mammography is 0.81 (95% confidence interval [CI], 0.73 to 0.91) on the meta-analysis using 7 randomized clinical trials.

Grading of Recommendations Assessment, Development and Evaluation evidence profile for breast cancer mortality (all age)
국내에서 시행된 무작위배정 비교임상시험은 없었다. 2002-2003년 국가유방암검진 대상자 중 유방암 사망자와 생존자를 1:4 매칭하여 과거 유방암 검진 수검 여부를 조사한 코호트내 환자대조군연구(nested case control study)에서 유방촬영술을 이용한 검진의 유방암 사망률에 대한 교차비(odds ratio)는 0.61 (95% 신뢰구간, 0.55-0.67) 이었으며, 검진군의 유방암 사망률이 대조군보다 유의하게 낮았다[4]. 그러므로 위원회는 유방촬영술을 이용한 검진이 유방암 사망률을 감소시킨다고 평가하였다.
2) 전체 사망률
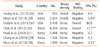
캐나다와 일본 권고안에 반영된 무작위배정 비교임상시험 8개 중 연구의 질이 낮았던 Edinburgh Trial을 제외하고 UK Age Trial, CNBSS, Göteborg Trial, HIP Trial, MMST, Stockholm Mammographic Screening Trial, Swedish Two-County Trial을 이용하여 메타분석을 시행하였는데 CNBSS는 CNBSS-1과 CNBSS-2 대상자를 25년간 추적관찰한 결과를 이용하였고, Swedish Two-County Trial은 W-county (Kopparberg)와 E-county (öster-götland) 각각의 전체 사망률 결과를 이용하였다[891011121314]. 메타분석 결과 유방촬영술을 이용한 검진의 전체 사망률에 대한 상대위험도는 0.99 (95% 신뢰구간, 0.98–1.01)이었으며 통계적으로 유의하지 않았다(Figure 3)[891011121314]. 메타분석에 포함된 8개의 연구 중 UK Age Trial, CNBSS, MMST를 제외한 5개의 연구는 무작위배정과 비일관성에 문제가 있었으므로 메타분석 결과에 대한 근거수준은 low로 평가하였다(Table 2).

Forest plot for breast cancer mortality (all age). Relative risk of breast cancer mortality in screening with mammography is 0.81 (95% confidence interval [CI], 0.73 to 0.91) on the meta-analysis using 7 randomized clinical trials.

GRADE (Grading of Recommendations Assessment, Development and Evaluation) evidence profile for all-cause mortality (all age)
국내의 국가유방암검진 대상자 자료를 이용한 코호트내 환자대조군연구에서 유방촬영술을 이용한 검진의 전체 사망률 감소효과에 대한 교차비는 40-69세에서 0.45-0.70이었고 통계적으로 유의하였으나, 70세 이상에서는 0.82-1.33이었고 통계적으로 유의하지 않았다[4]. 그러므로 위원회는 유방촬영술을 이용한 검진의 전체 사망률 감소에 대한 효과는 근거가 낮다고 평가하였다.
3) 병기이전
병기이전에 대하여 3개의 국내외 문헌이 검색/선택되었다. Kalager 등[15]은 50-69세 여성을 대상으로 1995년에서 2004년까지 시행한 노르웨이 국가유방암검진사업 결과를 이용한 후향적 코호트연구에서 그 전에 비해 검진사업 이후에 stage I, II가 증가하고 stage III, IV는 감소했다고 보고하였으며, 질 평가 결과 비뚤림 위험은 낮았다. Schonberg 등[16]은 80세 이상을 대상으로 1994년에서 2004년까지 미국에서 시행한 다기관 후향적 코호트연구에서 유방촬영술을 이용한 검진군과 대조군 간에 침윤성 유방암의 병기는 차이가 없었다고 보고하였으며, 비뚤림 위험은 낮았다. Kim 등[17]은 단일기관 후향적 코호트연구에서 검진에서 발견된 무증상 유방암은 외래에서 진단된 유증상 중간암보다 침윤암이 많고, 병기가 높다고 보고하였으나, 관찰연구였으므로 문헌의 질이 낮았다. 그러므로 위원회는 50-69세 여성에서 유방촬영술을 이용한 검진이 유방암의 병기이전에 효과가 있다고 평가하였으나 근거수준은 낮다.
2. 유방촬영술을 이용한 유방암 검진의 시작, 종결연령과 주기는?
1) 유방암 검진의 시작과 종결연령
30대 여성에서 유방촬영술을 이용한 검진이 유방암 사망률을 낮추는지에 대한 연구는 국내와 국외 모두 없었다.
40-49세 여성에서 유방촬영술을 이용한 검진의 유방암 사망률에 대한 상대위험도는 캐나다 권고안에서 0.85 (95% 신뢰구간, 0.75–0.96), 코크란 리뷰에서 0.84 (95% 신뢰구간, 0.73-0.96)였고 통계적으로 유의하였다[57]. 캐나다 권고안의 메타분석에 포함된 8개의 연구 중 5개(HIP Trial, Kopparberg Trial, Stockholm Trial, Ostergotland Trial, Goteborg Trial)에서 무작위배정에 문제가 있었으므로 근거수준은 moderate였다[5]. 코크란 리뷰의 메타분석에 포함된 8개 연구를 위원회가 검토한 결과 5개 연구(Kopparberg Trial, Stockholm Trial, Ostergotland Trial, Goteborg Trial, New York Trial)에서 무작위배정에 문제가 있었으므로 근거수준을 moderate로 평가하였다. 국내의 국가유방암검진 대상자 자료를 이용한 코호트내 환자대조군연구에서 유방촬영술을 이용한 검진의 유방암 사망률에 대한 교차비는 40-44세에서 0.55 (95% 신뢰구간, 0.44-0.68), 45-49세에서 0.58 (95% 신뢰구간, 0.46-0.74)이었으며 통계적으로 유의하였다[4]. 그러므로 위원회는 40대 여성에서 유방촬영술을 이용한 검진이 유방암 사망률을 감소시킨다고 평가하였다.
50-69세 여성에서 유방촬영술을 이용한 검진의 유방암 사망률에 대한 상대위험도는 캐나다 권고안에서 0.79 (95% 신뢰구간, 0.68–0.90), 코크란 리뷰에서 0.77 (95% 신뢰구간, 0.69-0.86) 이었으며 통계적으로 유의하였다[57]. 캐나다 권고안의 메타분석 결과에 대한 근거수준은 moderate이었으며, 코크란 리뷰의 메타분석에 포함된 연구를 위원회가 검토한 결과 근거수준을 moderate으로 평가하였다. 국내의 국가유방암검진 대상자 자료를 이용한 코호트내 환자대조군연구에서 유방촬영술을 이용한 검진의 유방암 사망률에 대한 교차비는 50-69세에서 0.34-0.75 (95% 신뢰구간, 0.21-0.93) 통계적으로 유의하였다[4]. 그러므로 위원회는 50-69세 여성에서 유방촬영술을 이용한 검진이 유방암 사망률을 감소시킨다고 평가하였다.
70세 이상 여성에서 유방촬영술을 이용한 검진의 유방암 사망률에 대한 상대위험도는 캐나다 권고안에서 0.68 (95% 신뢰구간, 0.45-1.01)이었으며 통계적으로 유의하지 않았다[5]. 메타분석에 포함된 연구는 2개였는데(Kopparberg Trial, Ostergotland Trial) 모두 무작위배정과 비정밀도에 문제가 있었으므로 근거수준은 low였다[14]. 국내의 국가유방암검진 대상자 자료를 이용한 코호트내 환자대조군연구에서 유방촬영술을 이용한 검진의 유방암 사망률에 대한 교차비는 0.70-0.84였으나 통계적으로 유의하지 않았다[4]. 그러므로 위원회는 70세 이상 여성에서 유방촬영술을 이용한 검진의 유방암 사망률 감소 효과는 유의하지 않다고 평가하였다.
2) 유방암 검진의 주기
캐나다 권고안의 메타분석 결과 전체 연령에서 유방촬영술을 이용한 검진의 유방암 사망률에 대한 상대위험도는 주기가 24개월 미만일 때는 0.83 (95% 신뢰구간, 0.76-0.92)으로 통계적으로 유의하였으나, 24개월 이상일 때는 0.77 (95% 신뢰구간, 0.57-1.03)로 유의한 효과가 없었다[5]. 연령별로 보았을 때 39-49세는 검진 주기가 24개월 미만인 경우에 유방암 사망률이 유의하게 감소하였으나(상대위험도, 0.82; 95% 신뢰구간, 0.82-0.94), 24개월 이상인 경우는 사망률 감소 효과가 없었다(상대위험도, 1.04; 95% 신뢰구간, 0.72-1.50) [5]. 50-69세는 주기가 24개월 미만과 이상일 때 모두 유방암 사망률이 감소하였다(24개월 미만 상대위험도, 0.67; 95% 신뢰구간, 0.51-0.88; 24개월 이상 상대위험도, 0.86; 95% 신뢰구간, 0.75-0.98) [5]. 70세 이상에서 주기가 24개월 이상일 때는 유방암 사망률 감소 효과가 없었고, 24개월 미만 주기에 대한 연구는 없었다[5]. 2011년 이후에 발표된 유방촬영술을 이용한 유방암 검진에 대한 코호트 연구에서 검사 주기는 대부분 2년이었으며, 2년과 3년 주기의 검진에서 유방암 사망률 감소 효과를 비교한 연구는 없었다. 캐나다 권고안의 메타분석 결과에 대한 근거수준은 주기별로, 연령별로 다양하였으나 위원회에서 검토한 결과 최종 근거수준을 moderate으로 평가하였다.
국내의 국가유방암검진 대상자 자료를 이용한 코호트내 환자대조군연구에서 40-49세는 35개월까지 유방암 사망률 감소효과가 있었으며, 50-59세는 23개월까지 유방암 사망률이 유의하게 감소하였다. 그러나, 70세 이상은 어떤 주기에서도 유방암 사망률 감소효과가 없었다[4]. 그러므로 위원회는 40-69세 여성에서 2년 주기의 유방촬영술을 이용한 검진이 유방암 사망률 감소시킨다고 평가하였다.
3. 유방촬영술의 위해는?
유방촬영술을 이용한 검진 후 심리적 스트레스에 대한 문헌은 6개였다. 그러나 대상 연령, 추적기간, 대상 집단의 구분 등의 기준이 문헌마다 다양하였고, 비교군이 없는 문헌도 있어서 결과를 비교하는데 제한점이 있었다[1819].
방사선 피폭에 대한 문헌은 5개였다. 유방촬영술을 이용한 검진을 이른 연령에서 시작할수록, 검진 간격이 짧을수록, 생애 누적 피폭선량이 증가할수록 방사선에 의해 발생한 유방암의 사망자 수와 사망에 대한 이익 대비 위험이 증가한다[202122]. 20-30대는 유방촬영술을 이용한 검진을 매년 시행하는 경우 이익보다 위해가 더 클 가능성이 있으나, 40세 이상에서는 방사선 피폭의 위해보다 검진의 이득이 더 큰 것으로 추정된다[2123].
유방촬영술로 인한 과진단은에 대한 문헌은 8개였으나 정의와 측정방법이 다양하였다. 캐나다와 일본 권고안에서 보고된 과진단률도 0-54%로 범위가 매우 넓기 때문에 결론을 내리기 어렵다[56]. 위양성률에 대한 문헌은 10개였는데 유방암 검진 개시 연령이 젊을수록 위양성률이 높지만 3.4-61.3%로 범위가 다양하기 때문에 결론을 내리기 어렵다[242526]. 유방촬영술 후 불필요한 생검에 대한 문헌은 3개였고 불필요한 생검률은 3.8-31%였으며 [2627], 중간암 발생에 대한 문헌은 5개였고 중간암 발생률은 0.01-3.7%로 다양하기 때문에 역시 결론을 내리기 어렵다[272829].
이와 같이 유방촬영술을 이용한 검진의 위해에 대한 결과가 매우 다양하므로 위원회에서 위해와 이득을 종합한 결과 검진으로 인한 위해보다 이득이 중등도(moderate)로 크다고 판단하였다.
4. 유방암 선별검사로서 유방초음파검사는 효과적인가?
유방초음파검사 단독 또는 유방촬영술과 병행한 유방초음파검사의 유방암 사망률 감소 효과를 평가한 무작위배정 비교임상시험이나 코호트연구가 없었으므로 유방초음파검사의 유방암 사망률 감소효과는 평가할 수 없었다.
암 발견율과 진단정확도를 주요 내용으로 하는 관찰연구 문헌은 15개였다. 암 발견율은 Tohno 등[30]의 연구에서 유방촬영술과 유방초음파검사 병용검진군이 0.31%, 유방촬영술군이 0.22%였으나 통계적으로 유의한 차이는 없었다. Chae 등[31]은 치밀유방을 가진 여성의 암 발견율이 유방촬영술과 유방초음파검사 병용검진군은 2.87%, 유방촬영술군은 0.48%라고 보고하였다. 유방촬영술이 음성일 때 유방밀도에 상관없이 유방초음파검사를 시행한 연구에서는 1,000명 당 1.9-3.3명의 유방암을 추가로 발견하였고, 유방촬영술이 음성이고 치밀유방일 때 유방초음파검사를 시행한 연구에서는 1,000명당 0.3-5.1명의 유방암을 추가로 발견하였다[3233343536373839] (Table 3). 이처럼 유방초음파검사의 암 발견율이 매우 다양하고 연구마다 디자인이 다르기 때문에 결론을 내리기 어렵다.
5. 유방초음파검사의 위해와 진단정확도는?
유방초음파검사를 이용한 검진의 위해에 대한 문헌은 6개였으며 유방초음파검사의 위해로는 과진단, 위양성, 불필요한 조직검사나 수술 및 이로 인한 정신적 스트레스 등을 들 수 있다. 치밀유방을 가진 여성에서 보조적으로 시행한 유방초음파검사의 위양성률은 0.9-19.3%였는데 범위가 넓고 연구마다 디자인이 다르기 때문에 결론을 내리기 어렵다[313940] (Table 4).
유방초음파검사를 이용한 검진의 진단정확도를 평가하는 지표로 양성예측도(positive predictive value)를 이용할 수 있다. 유방초음파검사의 양성예측도는 0.5-80.8%로 매우 다양하고 연구마다 유방촬영술의 이상소견이나 치밀유방 여부, 조직검사 시행기준, 양성예측도의 정의 등이 다르기 때문에 결론을 내리기 어렵다[313234353740] (Table 5).
6. 유방암 선별검사로서 임상유방진찰은 효과적인가?
임상유방진찰 단독검진의 사망률 감소에 대한 연구는 필리핀, 인도, 이집트에서 진행되고 있으나 진행 중이거나 이미 중단된 상태이므로 사망률 감소 효과를 평가할 수 없었다[41424344]. 임상유방진찰과 유방촬영술 병용검진의 유방암 사망률 감소에 대한 상대위험도는 40-49세에서 0.78 (95% 신뢰구간, 0.56-1.08), 50-59세에서 0.79 (95% 신뢰구간, 0.59-1.07)이었으며 유의하지 않았다[45].
임상유방진찰 단독검진의 민감도는 51.7-62.4%, 양성예측도는 1.0-3.4%로 보고되었으나 연령이나 유방밀도에 따라 차이가 있었다[4346] (Table 6). 임상유방진찰과 유방촬영술 병용검진을 시행할 경우 민감도는 높아지나, 특이도가 감소하였다[474849] (Table 6). 임상유방진찰의 예측 가능한 위해로는 위양성으로 인한 추가검사와 위음성으로 인한 진단 지연이 있을 수 있다.
고찰
유방암 검진의 효과에 대한 무작위대조 비교임상시험 결과들을 메타분석하였을 때 유방촬영술을 이용한 검진은 유방암 사망률을 약 19% 감소시켰으며 이는 기존의 캐나다 권고안과 코크란리뷰의 메타분석 결과와 큰 차이가 없었다[57]. 유방촬영술을 이용한 검진의 전체 사망률 감소에 대한 상대위험도는 0.99 였으며 통계적으로 유의하지 않았고 기존의 메타분석 결과와 큰 차이가 없었다[57]. 연령군별 메타분석에서는 40대와 50-69세만 유의한 유방암 사망률 감소가 있었고, 70세 이상 여성에서는 유방암 사망률 감소에 대한 효과와 근거가 부족하였다. 검진 주기별 메타분석에서는 24개월 미만에서만 유의한 유방암 사망률 감소가 있었다[5]. 그러므로 40-69세 여성에서 2년 주기로 유방촬영술을 이용한 검진을 시행하는 것은 유방암 사망률 감소에 대한 유의한 효과와 충분한 근거가 있다.
유방촬영술을 이용한 검진의 위해 중 가장 중요하다고 생각되는 방사선 피폭은 40세 이상인 경우 위해보다 이득이 더 큰 것으로 추정되며, 40-69세에서 2년 주기로 검진하는 경우 이익 대비 위해의 크기는 111:1 이었다[21]. 그러므로 위원회는 유방촬영술을 이용한 검진의 이득이 위해보다 크다고 판단하였다.
2002년에 발표된 기존 권고안은 30세 이상에서 매월 유방자가촉진, 35-40세에서 2년마다 의사에 의한 임상유방진찰, 40세 이상에서 2년마다 유방촬영술과 임상유방진찰을 시행하도록 권고하였으나 본 개정안은 검진의 효과가 증명된 40-69세 여성에 대해서만 유방촬영술을 이용한 검진을 권고한다. 70세 이상은 유방암 사망률 감소에 대한 효과가 유의하지 않았으므로 개인별 위험도에 대한 임상적 판단과 수검자의 선호도를 고려하여 선택적으로 시행하는 것이 바람직하다.
실제 임상 현장에서는 유방촬영술에서 치밀유방의 제한점을 보완할 목적으로 유방초음파검사를 널리 사용하고 있으나 유방초음파검사의 유방암 사망률 감소효과에 대한 연구가 없었기 때문에 유방초음파검사 단독 또는 유방촬영술과 병행한 유방초음파검사를 유방암 검진으로 시행하는 것은 근거가 불충분하였다. 또한, 유방암 검진 목적으로 임상유방진찰을 단독으로 시행하거나, 유방촬영술과 병행하여 시행하는 것도 근거가 불충분하였다. 그러므로 위원회는 유방초음파검사나 임상유방진찰에 대하여 단독 또는 유방촬영술과 병행하여 유방암 검진으로 시행하는 것을 권고하거나 반대하지 않는다. 그러나 본 개정안은 무증상 여성이 대상이므로 증상이 있는 여성은 임상유방진찰과 유방초음파검사 등의 추가적인 조치가 필요하다. 또한, 고위험군 여성도 임상의의 판단에 따라 추가적인 검사를 시행할 수 있다.
본 권고안은 유방촬영술의 질 관리를 다루지 않았으나, 효과적인 유방암 검진을 위해서는 질 관리가 매우 중요하다. 그러므로 유방촬영장비, 촬영자(방사선사), 판독자(영상의학과 전문의) 등의 영역에서 질 관리가 지속적으로 이루어져야 하며 특히 방사선사들을 위한 자세잡기 교육과 영상의학과 의사를 위한 검진 유방촬영 판독법에 대한 교육이 필요하다.
이번 개정작업의 제한점은 다음과 같다. 첫째, 개정작업을 위하여 국외의 무작위배정 비교임상시험 결과를 이용하였는데 그 당시에 비해 현재는 진단과 치료수준이 많이 발전하였으므로 결과에 차이가 있을 수 있다. 그러므로 이를 보완하기 위하여 최신 문헌을 최대한 포함하였다. 둘째, 개정된 권고안에 반영된 국외 문헌은 국내와 유방암 역학이 상이한 서구의 연구결과이므로 이를 보완하기 위하여 국내 문헌을 최대한 포함하고자 노력했지만 국내 문헌 자체가 매우 부족하였다. 그러나 국가유방암검진 자료를 이용한 연구에서 유방촬영술을 이용한 검진의 유방암 사망률 감소효과가 유의하게 나타났기 때문에 국내 문헌의 질적인 면에서는 충분한 근거가 될 수 있다.
국가유방암검진사업을 효과적으로 시행하기 위해서 앞으로 해결할 문제점이 몇 가지 있다. 첫째, 국내 유방암의 역학이 서구와 다르기 때문에 국내 여성을 대상으로 하는 연구가 필요하다. 특히 국내 여성의 치밀유방 비율이 높은 점을 고려하여 유방암 검진의 효과와 검진의 질 향상을 위한 연구가 필요하다. 둘째, 본 개정안에서 검진 연령을 40-69세로 제한하였으나 국내 여성의 평균수명이 84세인 점을 감안할 때 검진 상한연령에 대한 추가연구가 필요하다.
결론
40-69세의 여성에서 2년마다 유방촬영술을 이용한 검진을 시행하는 것은 유방암 사망률 감소효과가 있고 중등도의 근거수준이 있으며, 위해보다 이득이 중등도로 크다고 판단되므로 40-69세의 무증상 여성에서 유방촬영술을 이용한 검진을 2년 주기로 시행하는 것을 권고한다. 검진 목적으로 유방초음파검사나 임상유방진찰을 시행하는 것은 근거가 불충분하므로을 권고하거나 반대하지 않는다. 그러나 증상이 있거나 고위험군 여성은 임상의의 판단 하에 추가적인 조치가 필요하다.
Peer Reviewers' Commentary
본 논문은 다학제적 전문가로 구성된 국가암 검진 권고안 개정위원회의의 유방암 검진 권고 개정안이다. 위원회는 근거중심의 유방암 검진 권고안을 개발하여 의료인에게 유방암 검진의 표준지침을 제공하고, 유방암 검진의 효과와 위해에 대한 적절한 정보를 제공하고자 국내외의 연구논문을 분석하였다. 2002년에 발표된 기존 권고안은 30세 이상에서 매월 유방자가촉진, 35-40세에서 2년마다 의사에 의한 임상유방진찰, 40세 이상에서 2년마다 유방촬영술과 임상유방진찰을 시행하도록 권고하였으나 본 개정안은 검진의 효과가 증명된 40-69세 여성에 대해서만 유방촬영술을 이용한 검진을 권고했다. 개정안의 가장 큰 변화는 국가암 검진대상에서 70세 이상 여성을 제외한 것이며 검진 목적으로 유방초음파검사나 임상유방진찰을 시행하는 것을 권고하지 않았다. 다만 개인별 위험도에 대한 임상적 판단과 수검자의 선호도를 고려하여 선택적으로 시행토록 했다. 본 개정안은 우리나라 여성의 유방암 검진 권고의 기준을 마련했다는 점에서 의의가 있다고 판단된다.
[정리: 편집위원회]