|
 |
- Search
| J Korean Med Assoc > Volume 58(5); 2015 > Article |
Abstract
Hepatocellular carcinoma (HCC) is one of the major cancers with a high incidence and mortality in Korea. A Korean multidisciplinary collaborative committee consisting of hepatologists, radiologists, epidemiologists and family medicine doctors systematically reviewed clinical practice guidelines in the world and literatures. The level of evidence for each recommendation was assessed and discussed to reach a consensus. Meta-analysis was also conducted to evaluate the grade of recommendation for the five key questions. Several randomized controlled studies and cohort studies showed a survival gain associated with surveillance for those at risk of developing HCC. The target populations for HCC surveillance were identified as hepatitis B virus or hepatitis C virus carriers and cirrhotic patients, since numerous studies revealed that these patients have significantly higher risk of HCC compared with non-infected or non-cirrhotic controls. Individual surveillance strategy according to treatment history or degree of fibrosis in patients with viral hepatitis remains to be settled. Based on several cohort and randomized studies, a surveillance interval of six months was recommend. The starting age of surveillance was determined as 40 years from the epidemiologic data. Although ultrasonography (US) is the mainstay for detection of HCC, its sensitivity is not fully accepted. Measurement of serum alpha-fetoprotein can complement US examination, increasing the sensitivity of HCC detection. The recommendation for HCC surveillance is that those with hepatitis B virus (or hepatitis C virus) infection or cirrhosis should have liver US and serum alpha-fetoprotein measurement every six months from 40 years of age or at the time of diagnosis of cirrhosis.
간암 고위험군(B형, C형 간염 바이러스 보유자, 간경변증)을 대상으로 한 간암 검진의 이득은 위해에 비해 충분히 높으며, 중등도(mode-rate)의 근거수준을 가지고 있다.
간암 고위험군(B형, C형 간염 바이러스 보유자, 간경변증)을 대상으로 매 6개월 간격으로 간 초음파 검사와 혈청 알파태아단백(alpha-fetoprotein) 검사를 검진 검사로 시행할 것을 권고한다(권고 등급 A). 검진의 시작 연령은 B형 또는 C형 간염 바이러스 보유자에서는 40세부터, 간경변증에서는 진단 시점부터 권고한다.
우리나라의 간암으로 인한 사망은 2012년 현재 인구 10만 명당 11,355명(15.4%)으로 암 사망률 2위이다. 특히, 연령대별로 간암 사망률을 비교해 보면 40대와 50대에서 각각 12.1명, 36.2명으로 간암으로 인한 암 사망률이 가장 높다. 암 사망 분율을 성별에 따라 살펴보면, 남자의 경우 간암이 전체 암 사망의 18.3%로 폐암 다음으로 높은 사망을 차지하였으며, 여자의 경우 암 사망의 10.4%로 폐암, 대장암, 위암 다음으로 높은 사망 분율을 차지하고 있다.
한국중앙암등록본부의 2012년 암발생통계에 의하면 2012년 남성에서 간암의 조발생률은 인구 10만 명당 48.2명, 여성에서 16.3명으로 남성에서 네 번째, 여성에서 여섯 번째로 많이 발생하고 있다. 1999-2012년 간암의 연령표준화 발생률(인구 10만 명당) 추이를 보면 남성의 경우 1999년 48.5명에서 2012년 35.2명으로 매년 2.2%씩 감소하고 있으며, 여성의 경우 1999년 12.6명에서 2012년 9.7명으로 1.6%씩 감소하고 있다. 이처럼 우리나라의 간암 발생률이 매년 감소하고 있으나 외국과 비교하면 여전히 높은 수준으로 전세계 평균(남성 15.3명, 여성 5.4명)보다 약 2배 정도 높고, 중국과 비슷한 수준의 발생률을 보이고 있다. 2012년 전세계적으로 78만 명의 간암 환자가 새롭게 발생하였는데 암 발생자의 80% 이상이 중국, 일본, 한국 등을 포함한 아시아와 아프리카 거주자였다.
우리나라 간암의 5년 생존율은 30.1%로 미국(16.6%)이나 캐나다(20.0%), 일본(27.9%)과 비교하면 상대적으로 높은 생존율을 보이지만 전체 암종 중에서는 폐암(21.9%) 다음으로 생존율이 저조한 암이다. 병기에 따른 간암의 5년 상대생존율을 보면, 국한(localized) 병기의 생존율은 49.4%에 이르지만 원격 전이가 있는 경우에는 약 1/10 이하인 2.8%까지 감소한다.
간암 검진 권고안은 2002년 국립암센터와 대한간학회가 공동으로 개발하였으며, 이를 토대로 2003년 국가암검진사업의 일환으로 간암검진사업이 시작되었다. 현재 국가암검진사업에서 간암 검진은 만 40세 이상 남녀로 간경변증이나 B형 간염 바이러스 항원 또는 C형 간염 바이러스 항체 양성으로 확인된 자를 대상으로 6개월 간격의 간 초음파와 혈청 알파태아단백검사를 병행해서 시행할 것을 권고하고 있으나, 2012년부터는 1년에 한번씩 시행하고 있다. 처음 제정된 간암 검진 권고안은 전문가들의 의견을 바탕으로 한 것이지만, 근거중심의 권고안 개정을 위해 다학제 위원회가 구성되어 문헌을 검색하고 각 문헌의 근거수준을 평가한 후 메타분석을 통해 권고문의 권고등급을 추가한 것이 달라진 점이다.
간암 검진 권고안 개정위원회에서는 핵심질문에 따라 기존 간암의 임상진료지침을 검색하여, 간암 고위험군의 감시검사 지침의 질과 근거를 평가하고 수용 개작한 후에, 최신 문헌과 국내 문헌을 추가적으로 검토하여 필요한 사항에 대해서 신규개발 방식으로 개정하기로 결정하였다.
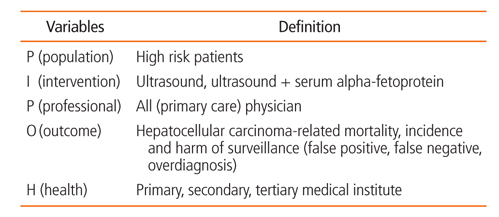
고위험군을 대상으로 간암 검진을 시행하였을 때 검진의 효과와 위해를 평가하기 위하여 핵심질문을 도출하였다. 핵심질문 1은 간암 검진으로 과연 고위험군에서의 간암 사망위험이 낮아질 것인가의 질문으로 간암 사망률과 전체 사망률의 감소를 확인하는 것이다. 핵심질문 2는 적절한 간암 검진 대상자는 누구인가라는 질문으로 간암 검진 대상자 선정을 위해 간암 발생률이 유의하게 높은 위험요인을 찾기 위한 것이다. 여기에는 고위험군의 정의와 검진의 시작, 종료 연령 등이 포함된다. 핵심질문 3은 효과적인 간암 검진 주기는 무엇인가라는 질문으로 통상적인 6개월과 1년을 비교하기로 하였다. 핵심질문 4는 효과적인 검사방법은 무엇인가라는 질문으로 초음파와 초음파-혈청 알파태아단백검사를 비교하기로 하였다. 마지막으로, 핵심질문 5는 간암 검진과 관련된 위해는 무엇인가라는 질문으로 과진단이나 위양성, 위음성 등으로 인한 검진과 관련된 위해를 논의하기로 하였다. 간암 검진 권고안의 개발 범위와 분석의 틀은 각각 Table 1, Figure 1과 같이 설정하였다.
고위험군을 대상으로 하는 간암 검진과 관련되어 개발되어 있는 임상진료지침을 문헌검색 데이터베이스를 이용하여 검색하였다. 임상진료지침의 검색은 일반 검색원인 Medical Literature Analysis and Retrieval System Online (Medline), Excerpta Medica database (Embase)와 지침특성화 검색원인 National Guideline Clearinghouse (NGC), US Preventive Service Task Force (USPSTF), National Institute for Health and Care Excellence (NICE), Guideline International Network (GIN)에서 검색하였다. 검색기간을 보면 일반 검색원은 2009년 이후부터, 지침특성화 검색원은 연도 제한 없이 검색하였고 B형 간염, C형 간염, 간경변증 등 간암 관련 검색어도 포함하였다. 검색된 임상진료지침은 2인의 평가자가 독립적으로 평가하였고, 평가결과가 다른 경우에는 재평가 및 합의를 통해 수용할 임상진료지침을 선정하였다. 간암 감시검사와 관련된 임상진료지침 검색 결과 국내, 국외 데이터베이스를 통틀어 29개의 진료지침이 검색되었다. 이 중에서 근거 기반이 아닌 합의 기반에 의해 개발된 진료지침, 개발 주체가 동일한 중복된 진료지침, 대상검사가 포함되지 않았거나 대상 환자군이 아닌 경우 또는 다른 지침과 중복 사항이 있는 임상진료지침 9개를 1차 배제하였다. 또한, 국가별로 대표성을 띠는 지침을 선택하는 과정에서 9개의 지침이 배제되어, 총 11개의 임상진료지침에 대한 질 평가를 시행하였다. 캐나다 간학회(Canadian Association for the Study of the Liver Consensus Guidelines)와 SIGN (Scottish Intercollegiate Guidelines Networks)의 지침은 대상 집단이 B형 바이러스 또는 C형 바이러스 보유자로 국한되어 있으며, 내용도 검진보다는 관리 및 진료지침의 목적으로 개발되어 참고 지침에서 제외하였다. 국내 데이터베이스에 대한 검색 결과 간암 관련 지침으로 대한간학회의 '만성 B형 간염 진료 가이드라인'과 대한간암연구회의 '2009 간세포암종 진료 가이드라인'이 검색되었으며, 최종적으로 대한간암연구회의 것을 참고 지침으로 선정하였다.
근거 문헌은 선정된 임상진료지침의 근거 문헌 중에서 제목 및 초록을 평가하여 핵심질문에 적절한 것으로 2011년 이후 출판된 문헌에서 선정하기로 하였다. 또한 최신 문헌을 반영하기 위해 Medline (via PubMed)과 Embase (via Emabse.com)를 이용하여 2011년 이후 발간된 논문으로 hepatocellular carcinoma, liver neoplasms을 기반으로 epide-miology, pathology, diagnosis 등을 포함하여 연구 참가자의 수, 연구 디자인에 제한을 두지 않고 검색하였다. 또한, 국내에서 출판된 관련 문헌을 추가적으로 검색하여, 국내 연구결과를 지침에 반영할 수 있도록 하였다. 국내 및 국외 검색 데이터베이스에서 검색된 문헌은 핵심질문별 선택·배제기준에 따라 문헌 당 2인의 검토자가 독립적으로 문헌 선택, 배제를 진행하였다. 1차로 제목과 초록을 보고 선택, 배제를 하였으며 1인이라도 선택한 문헌은 원문을 검색하였다. 2차로 원문을 보고 개정위원회의 실무위원들이 선택, 배제를 하였으며, 실무위원들 사이에 일치가 이루어지지 않은 경우 합의를 통해 최종 선택, 배제를 결정하였다.
AGREE 평가를 통해 최종 선정된 검진지침의 근거 문헌을 검토한 결과, 검진의 임상적 이득 관련문헌 13개, 고위험군 관련으로 B형 간염 41개, C형 간염 23개, 간경변증 5개가 검색되었다. 연령 관련 문헌으로 5개, 혈청 알파태아단백검사 관련 28개, 초음파 21개, 초음파와 알파태아단백검사 두 검사 모두를 시행한 문헌 5개, 검진 기간 관련 18개로 총 159편 논문이 검색되었다. 또한 2011년 이후 문헌을 검색한 결과 데이터베이스 별로 Medline 189개, Embase 299개, Cochrane 11개가 검색되었으며, 중복된 문헌 제거 이후 총 395개의 문헌이 선정되었다. 국내 문헌 데이터베이스의 경우 검색 기간을 최근 10년으로 제한하여 검색한 결과, 국내문헌 총 1,083개가 검색되었다. 따라서 기존 임상진료지침 근거 문헌 159편, 최근 근거 문헌 395편, 국내 문헌 1,083편의 제목 및 초록을 보고 3명의 개정위원회 위원과 3명의 실무위원이 독립적으로 평가하였다.
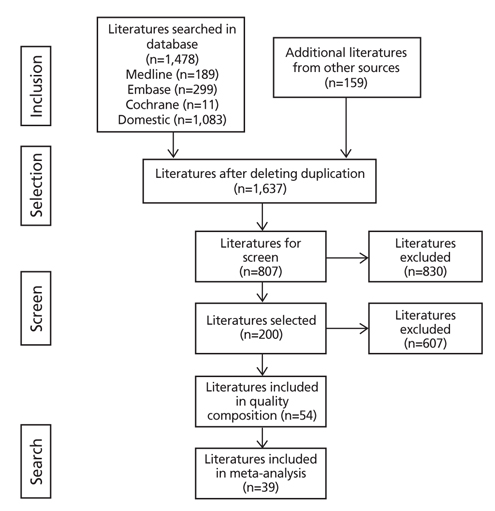
임상진료지침에 포함되어 있는 근거문헌 159편 중에서 1차로 85편이 배제되었으며, 남은 74편 중 49편의 문헌이 2차 선정되었다. 2011년 이후 발간된 논문 395개 가운데 1차 배제작업으로 206편이 배제되었으며, 1차 배제되고 남은 189개 논문 가운데 56편이 배제되어 최종 131편이 선정되었다(중복 제거). 마지막으로 국내 문헌 총 1,083개 문헌 가운데 539편이 1차 배제되었으며 524편이 2차 배제되어 최종 20편이 선정되었다. 또한 간암 검진의 검사방법과 관련하여 2008년 이후 '민감도,' '특이도'를 포함하여 검색한 결과 총 282개 문헌이 검색되었으나, 초음파 단독 결과 혹은 초음파와 혈청 알파태아단백검사 결과를 모두 제시한 문헌은 없었다. 다만 초음파와 혈청 알파태아단백검사로 감시검사를 한다고 제시하는 총 16개 문헌을 최종 선정하기로 하였다. 이로써 핵심질문 1에 해당하는 문헌 7편, 핵심질문 2에 해당하는 문헌 33편, 핵심질문 3 해당하는 문헌 7편, 핵심질문 4에 해당하는 문헌 16편, 핵심질문 5에 해당하는 문헌 2편을 포함하여 총 65편을 최종 선정하였다(Figure 2).
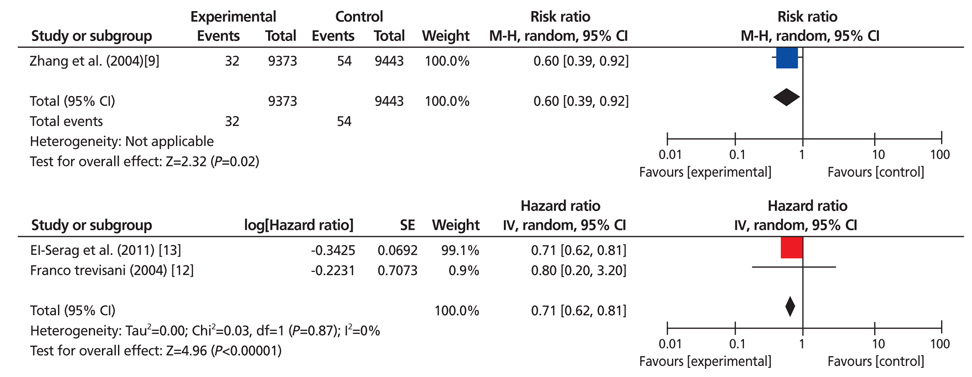
개정위원회의 평가 및 합의를 통해 선택된 총 8개의 진료지침(Asia-Pacific Association for the Study of Liver [APASL], 싱가폴 보건국, 뉴질랜드, NICE, Japan Society of Hepatology [JSH], European Association for the Study of the Liver [EASL]-European Organisation for Research and Treatment of Cancer [EORTC], American Association for the Study of Liver Diseases [AASLD], 대한간암연구회)에서 고위험군에 대한 간암 검진은 간암 사망위험률을 낮추는 효과가 있어서 권고된다는 일치된 의견을 확인할 수 있었다[1,2,3,4,5,6,7,8]. 또한 중등도의 근거 수준을 갖는 1편의 무작위배정 비교임상연구(randomized controlled trial, RCT) 결과를 보면 간암 고위험군인 만성 B형 간암 환자를 대상으로 6개월마다 혈청 알파태아단백검사 및 간 초음파검사를 시행한 군에서 검진을 시행하지 않은 군에 비해 유의한 임상적 이득이 있음을 보고한 바 있다[9]. 또한 여러 코호트 연구와 환자대조군 연구들이 고위험군을 대상으로 한 간암 검진검사의 유용성을 보고하였고, 국내의 연구결과도 이러한 결과를 뒷받침하고 있다. 이상의 결과로 간암 고위험군에 대한 감시검사를 통한 검진은 간암 사망률을 낮출 수 있다고 판단한다.
간암 검진과 사망률에 대한 RCT는 총 2개의 논문이 검토되었다[9,10]. 이 중 Chen 등[10]이 2003년에 중국인을 대상으로 수행한 연구는 혈청 알파태아단백을 이용한 간암 감시검사가 간암의 조기 발견과 5년 생존율 향상에는 도움을 주지만 lead time bias로 간암의 사망률을 감소시키지 못하기 때문에 다른 간암 검진방법이 요구된다고 보고하였다. 그러나 위 연구는 개정위원회에서 평가하고자 했던 간암의 주된 검진방법인 초음파검사를 이용한 연구가 아니어서 최종 문헌분석에서 제외하였다. 따라서 본 개정위원회는 고위험군을 대상으로 간암 검진에 대한 의미 있는 RCT 연구로 Zhang 등[9]이 2004년에 중국인을 대상으로 발표한 문헌만을 의미 있는 것으로 판단하여 분석하였다. Zhang 등[9]은 35세에서 59세 사이 18,816명의 만성 B형 간염 환자를 대상으로 전향적으로 무작위 배정하여, 6개월마다 혈청 알파태아단백검사 및 복부 초음파검사를 시행한 군이 검진을 받지 않은 군에 비해 5 cm 이하의 소간세포암종 발견의 빈도가 높았고(45.3% 대 0%), 5년 생존율도 뚜렷이 높았으며(46.4% 대 0%), 간암으로 인한 사망률을 37% 감소시켰다고 기술하였다. 따라서, 이 연구에서는 고위험군을 대상으로 주기적인 간암 검진이 이루어진다면 간암에 의한 사망률을 낮출 수 있다고 주장하였다. 그러나, 2012년 코크란 리뷰에서는 Zhang 등[9]의 논문의 결과에 대해 비뚤림이 있어 연구결과에 대한 신뢰성이 떨어진다고 기술하였는데, 그 이유로는 동일 연구진이 동일한 연구에 대해 발표한 다른 논문에서 기존 연구와는 다른 대상자 수를 제시하고 있으며, 무작위 배정에 대해서도 기술이 같지 않음을 지적하였다[11]. 또한 연구 대상자의 참여율이 초기(2차 검진) 58.2%에 지나지 않았고, 8번의 간암 추적 검진 기간 동안 참여율이 30%로 감소되었음을 문제로 지적하였다. 연구대상 역시 만성 B형 간염 환자로 한정하였기 때문에 만성 C형 간염이 간암의 주된 원인이 되는 서양인에 적용시키는데 한계가 있음을 지적하였다. 이에 코크란 리뷰에서는 Zhang 등[9]의 연구결과에 대하여 비뚤림이 높음으로 평가하고 논문의 근거 수준이 낮다고 판단하였다.
본 개정위원회는 Zhang 등[9]의 연구가 우리나라 간암 발생의 주된 원인인 만성 B형 간염 환자를 대상으로 하였으며, 우리와 인종적으로 유사한 동양인에서 시행되었기에 환자군 선택에 따른 비뚤림은 적다고 판단하였다. 또한 국가암검진사업은 질환의 조기발견 뿐 아니라 적절한 치료를 통한 사망률의 감소를 목적으로 기획되어야 된다는 원칙을 생각한다면 이 연구의 임상적 의미는 더욱 강조될 수 있다. 추적 검사된 환자가 58.2%에 지나지 않았음에도 간암 검진으로 고위험군의 사망률을 낮출 수 있다는 이 연구의 결과 또한 적극적인 추적검사가 이루어진다면 보다 의미 있는 간암 사망률 감소를 기대할 수 있다. Zhang 등[9]의 연구에서 검진결과에 따라 치료 효과가 좋을 것으로 예상되는 무증상 병기(subclinical stage)의 간암 환자 중 단지 75%에서 수술적 절제, 간동맥화학색전술, 알코올 소작술 등이 시행되었다. 연구가 시행되었던 90년도 말에 비해 현재 초음파기기의 발전으로 소간암의 발견이 보다 용이해진 점과 수술적 절제나 국소 치료법의 성적이 향상된 점, 간 이식이 활발하게 시행되 는 점 등은 간암 치료에 있어서 조기진단의 중요성이 더욱 강조되는 이유이다. 따라서, 본 개정위원회는 코크란 리뷰와는 다르게 Zhang 등[9]의 논문을 중등도의 근거 수준을 가지는 의미 있는 논문으로 판단하였다.
현재 동서양을 막론하고 간암 조기진단을 위한 감시검사는 이미 표준 진료행위에 속하는 것으로 받아들여져 고위험군의 간암 검진과 관련된 추가적인 RCT 연구는 윤리적 문제와 직결되어 있어 수행되기 어려운 측면이 있다. 실제 미국에서 2005년 RCT를 계획하였으나 단 한 명의 환자도 연구에 동의하지 않아 연구를 진행할 수 없었으며, 향후 RCT 연구는 더 이상 불가능할 것으로 보인다. 본 개정위원회는 Zhang 등[9]의 RCT 연구 외에도 간암 검진의 이득을 평가한 관찰연구를 검색하였으며, 그 중 선택기준에 부합하는 1편의 코호트 연구와 1편의 환자-대조군 연구를 선정하여 메타분석을 실시하였다[12,13] (Figure 3). 분석결과, 고위험군을 대상으로 하는 간암 검진이 간암 사망률을 약 29% 감소시켰고 이것은 통계적으로 유의하였다(hazard ration, 0.71; 95% confidence interval [CI], 0.62-0.81). 비록 코호트 연구와 환자 대조군 연구가 RCT 연구에 비해 여러 가지 비뚤림(lead time bias, length-time bias, self-selection bias 등)에 취약한 연구설계이기는 하지만 간암 검진의 유용성을 일관되게 제시하고 있었다[12,13]. 이상의 결과로 간암 고위험군을 대상으로 한 주기적인 간암 검진은 간암 사망위험을 낮추는데 효과적인 것으로 평가되었다.
다른 암종과 달리 간암의 위험군은 비교적 명확히 정의할 수 있으며, 간암의 약 90%가 이미 잘 알려진 위험인자와 연관이 되어 있다. 지금까지 국내외 연구 결과를 보면 대표적인 위험군으로 B형 간염 바이러스 보유자, C형 간염 바이러스 보유자, 간경변증(어떤 원인이든)을 들 수 있다. 전 세계적으로 약 54%의 간암이 B형 간염과 연관이 되어 있으며, 31%의 간암이 C형 간염과 관련되어있는 것으로 보고되고 있다. 여러 환자-대조군 또는 코호트 연구[14]에서 B형 간염 표면항원 양성인 환자의 간암 발생 상대 위험도가 9 이상으로 유의하게 높은 것으로 잘 알려져 있고, 이같은 결과는 만성 B형 간염이 만연한 동북아시아 지역의 간암 환자수가 전 세계의 2/3를 차지하는 현상과 맥락을 같이 한다. 만성 C형 간염은, 특히 간경변증으로까지 진행한 경우 만성 B형 간염보다 간암 위험도가 더 높은 질환으로 환자-대조군 연구[15,16,17,18]와 코호트 연구[19,20,21]의 메타분석에서 만성 C형 간염의 상대 위험도는 각각 5.95와 23.92였다. B형 간염의 경우 유행지역인 대만과 국내 보고에 따르면, 국가차원의 범국민예방접종사업과 주산기 감염 예방사업에 따라서 급격히 B형 간염의 발병률이 감소하고 있으며 이에 따라서 대만에서는 소아 간암의 발생이 현저히 줄었다. 또한, 만성 B형 간염에서 인터페론과 라미부딘과 같은 항바이러스 약제 치료에 반응을 보이는 경우 무반응군과 비교하여 의미 있게 간암 발생률을 줄였으며[22], 만성 C형 간염도 항바이러스 치료에 성공하면 간암의 발생률이 현저하게 감소되므로[23], 이런 연구 결과들은 B형 간염과 C형 간염이 간암의 고위험군인 것을 뒷받침해주는 근거라고 할 수 있다. 특히, 만성 C형 간염 환자에서는 진행된 간 섬유화(METAVIR 3기 이상)일 때 간암 발생의 위험도가 높아지는 것으로 알려져 있고[23], 덜 진행된 간 섬유화에서는 상대적으로 간암의 위험도가 낮다. 그러나, 실제 진료에서 간조직 생검을 거의 시행하지 않기 때문에 환자의 간 섬유화 정도를 파악할 수 없다. 즉, 임상적 기준으로 환자의 간암 발생 위험도를 평가할 수 없으므로 만성 C형 간염 환자에서 간 섬유화에 따른 차별화된 검진전략은 현재로는 근거가 불충분하다. 따라서, 간 섬유화의 정도에 무관하게 만성 C형 간염을 간암의 고위험군으로 설정하는 것이 바람직하겠다. 다만, 조직학적으로 또는 임상적으로 섬유화가 없거나 경미하다고 판단한 경우 간암 검진의 효과는 크지 않다고 볼 수 있겠다[24]. 간경변은 간암의 중요한 위험인자로 간경변의 원인으로는 만성 바이러스 간염(B형, C형), 음주, 유전성 대사질환(혈철색소증, alph-1 antitrypsin deficiency 등), 비알콜성 지방간질환 등이 알려져 있다[7]. 간암환자의 약 80%가 간경변을 동반하고 있고, 통상적으로 간경변증 환자는 잔여 여명동안 약 1/3에서 간암이 발병하며, 장기간 추적연구에 의하면 매년 약 1-8% 에서 간암이 발생한다고 보고되고 있다. 이 중 B형 간염 간경변의 경우 매년 2%, C형 간염에 의한 간경증에서는 매년 3-8%의 간암 발생률을 보인다[25]. 또한, 간경변증은 간암 발생의 가장 강력한 위험 인자로서 국내외의 여러 연구결과를 종합할 때 상대 위험도가 5 이상인 것으로 분석되었다[26,27].
전 세계적으로 간암 발생의 위험 인자(B 또는 C형 간염, 간경변증)를 가진 환자에서 간암 검진의 시작과 종결 연령에 관한 일치된 의견은 없다. 간경변증은 간암 발생의 가장 강력한 위험 인자이기 때문에 간경변증 환자는 연령과 무관하게 진단 시점부터 간암 검진을 받는 것이 바람직하다. 간경변증이 없는 만성 B형 또는 C형 간염 환자의 경우, 국내 간암 역학자료를 볼 때 40세 이상부터 발생률이 증가하는 것을 볼 수 있으므로 40세 이상부터 검진을 시작하는 것이 필요하다. 고령화 시대로 접어듦에 따라 80세 이상의 고령이라도 신체 연령은 적은 경우가 많으며 검진 대상군이 이미 간암의 고위험군 환자임을 고려할 때 나이만으로 간암 검진을 제외하기는 어렵다.
간암 발생의 고위험군에서 적절한 검진 주기를 결정하기 위해 본 개정위원회에서는 검진주기에 따른 간암 발생률 및 생존율을 비교하기 위한 문헌검색을 실시하였다. 간암 발생의 검진주기를 비교한 연구들 중 원문검색이 가능한 국내연구 1편[28]과 해외연구 2편[29,30]이 있었으며 이 중 간암의 검진주기를 6개월과 12개월로 나누어 비교한 연구는 이탈리아에서 시행한 후향적 관찰연구 하나였다[29]. 연구결과에서 12개월 간격으로 추적 관찰한 환자군은 나이, 혈소판 수, 혈청 알파태아단백 수치, Child-Pugh 등급, 그리고 식도정맥류 등 간암 환자의 예후와 연관된 변수들을 보정한 후에도 사망위험률이 39% 높았다. 다른 연구는 검진주기를 4개월과 12개월 간격으로 비교한 무작위배정 비교임상연구로[31], 역시 4개월마다 추적 관찰한 환자군에서 BCLC (Barcelona Clinic Liver Cancer) 병기를 기준으로 조기 간암의 발생률이 높았다. 그러나 두 환자군을 4년 동안 추적 관찰한 결과 전체생존율의 통계적인 차이는 없었다. 국내 연구는 간암 발생 고위험군을 대상으로 검진주기를 6개월 이내와 6개월 이상으로 나누어 비교한 후향적 관찰연구로[28], 6개월 이내에 검진을 시행한 군에서 5년 생존율의 중간 값이 33개월로 6개월 이상인 군에서의 24개월에 비하여 높았다. 또한, 세계보건기구의 권고에 따르면 간암환자의 5년 생존율은 25-60%로 다양하며 이러한 생존율의 차이는 종양의 크기, 신체증상, 종양의 절제가능성, 그리고 혈청 알파태아단백 수치에 따라 다르기 때문에 간암 발생률이 높아지는 연령의 고위험군 환자에서 6개월 간격으로 간 초음파와 혈청 알파태아단백을 주기적으로 검사하는 것을 권고하고 있다. AASLD에서도 간암의 고위험군에서 추적관찰기간을 6개월 간격으로 할 것을 권고하고 있다[1]. EASL 가이드라인 역시 간암 발생의 고위험군에서 6개월 간격으로 복부 초음파를 권고하고 있다[6]. 간암의 이상적인 검진주기는 암 발견이 가능한 최소한의 성장속도와 대상인구의 암 발생률을 모두 고려하여야 한다. EASL 가이드라인에서는 간암의 배가 시간(doubling time)을 고려할 때 6개월 간격의 추적관찰이 합리적인 것으로 기술하고 있다[6]. 또한, 후향적 분석에서 생존기간 향상에 유의하고 치료 가능한 간암의 병기 이동을 고려할 때 6개월 간격의 검사주기가 합당한 것으로 보고되었다. 뿐만 아니라, 메타분석에서 초음파 기반의 민감도는 6개월 추적관찰 군에서 70%인 반면 12개월 추적 관찰군에서는 50%로 감소하는 것으로 보고되었다[32]. 따라서, 국내외의 연구결과들과 국외 가이드라인을 근거로 할 때 간암 발생 고위험군에서 검진주기를 6개월로 권고한다.
간암의 조기진단을 위하여 초음파 검사와 혈청 알파태아단백 수치를 동시에 검사하는 방법이 널리 사용되고 있다. 여러 나라의 실정에 맞게 다양한 프로토콜의 간암 검진 프로그램이 실시되고 있지만 전향적으로 이러한 검진 프로그램의 유용성을 검증하는 임상연구가 거의 없고 임상연구 결과와 실제 검진 프로그램 적용 시에 진단 능력에 차이가 있으며, 무엇보다도 국가 간 질병의 유병률이나 비용효과의 차이로 인해 권고하는 검사방법에서의 차이가 존재한다. 유병률이 상대적으로 낮은 미국과 유럽의 여러 나라에서는 간 초음파만을 검사방법으로 권고하고 있으며[6,7] 상대적으로 유병률이 높은 우리나라와 일본에서는 간 초음파와 혈청 알파태아단백검사를 함께 하도록 권고하고 있다[33,34].
간 초음파 검사의 민감도와 특이도는 각각 65-80%와 90% 이상으로 이는 알파태아단백 등 혈청학적 검사보다 간암의 발견에 있어 그 민감도가 높은 것으로 보고되어 있다[11]. 개정위원회에서 선택한 16개 기존 연구들의 메타분석에서는 간 초음파 검사와 혈청 알파태아단백 측정을 함께 시행하는 경우 추정값이 0.79 (95% CI, 0.57-0.91)로 간 초음파만 시행하였을 때와 비교하여 약간 높았지만(0.69; 95% CI, 0.46-0.85) 통계적으로 유의한 차이를 보이지는 않았다[26,27,29,35,36,37,38]. Singal 등[32]이 수행한 연구결과에서도 조기 간암의 민감도가 0.69와 0.63으로 통계적 차이를 보이지 않는다고 보고한 바 있다.
따라서 간 초음파 단독검사보다 간 초음파와 혈청 알파태아단백검사를 병행하여 실시하는 경우 민감도가 통계적으로 유의하게 높다는 근거는 부족하다. 하지만, 각 연구에서 혈청 알파태아단백검사의 기준치가 다르며, 따라서 이들 연구에서 나온 결과로 민감도를 비교, 분석하는 것은 불가능하다. 최근에는 항바이러스 치료를 많이 하고 있고, 특히 치료에 좋은 반응을 보이는 만성 B형 간염환자에서 혈청 알파태아단백 검사는 간암 발견에 유용하다는 보고들이 있어 고위험군을 대상으로 하는 간암 검진에서 혈청 알파태아단백 검사의 유용성은 더욱 강조되고 있다[39]. 따라서, 간암 검진 권고안 개정위원회는 국외의 연구결과들과 국내외 가이드라인 그리고 국내 간암 유병률을 근거로 간암 발생 고위험군에서의 검진방법은 간 초음파검사와 혈청 알파태아단백검사 검사를 병행하는 것으로 권고한다.
영상 소견과 임상기준을 통하여 간암을 진단하지 못하는 경우 조직검사를 통한 확진을 시도하게 되는데, 합병증으로는 통증, 출혈, 사망 등이 있다[40]. 통증은 흔하며 약 84%의 환자가 호소한다는 보고가 있다. 수혈이 필요하거나 지혈을 위한 시술이 필요한 출혈 등 중등도 이상 중증 합병증의 빈도가 0-0.75% (2000년 이후), 사망률이 0-0.4%로 보고되고 있다. 간 초음파 유도하 조직생검을 시행하면서 합병증의 빈도가 감소하는 경향이며, 출혈 소인이 있는 환자에서는 간정맥을 통한 조직검사를 시행하기도 한다. 합병증을 막기 위해 협조가 되지 않는 환자에서는 시행해서는 안되고, 초음파 유도 시 굵은 간 내 혈관을 피하여 조직검사를 시행하여야 하며 경피적 시술 시에도 늑간동맥을 피하여 시술하여야 한다. 혈소판 수치가 낮은 경우(<50,000-60,000/mL)에는 혈소판 수혈을 고려해야 한다.
간암 진단을 위한 검사 중 컴퓨터단층촬영(computed tomography, CT)는 방사선 피폭의 위험이 있는 검사방법이다. 한차례의 복부 CT 검사를 통한 방사선 피폭량은 약 8 mSv 정도이고 간암 진단을 위한 CT 검사인 경우 간 부위의 반복 스캔을 시행하므로 약 15 mSv 정도로 보고되고 있다. 방사선 피폭으로 인한 피해는 탈모나 피부괴사와 같은 확정적 영향, 그리고 발암과 같은 확률적 영향으로 구분할 수 있으며 CT 검사와 같은 저선량 방사선의 경우, 대부분 확정적 영향은 무시될 수 있다. 확률적 영향의 경우에도 100 mSv 이하의 저선량 방사선의 경우에는 고형암의 발생과 방사선 피폭간의 상관관계가 정확히 밝혀져 있지 않았으며, 다만 문턱값 없는 선형관계(linear no threshold)로 정의하기로 하였다[41].
간암 검진 권고안 개정위원회는 근거중심의 적절한 간암 검진안을 개발하기 위하여 국내외의 기존의 간암 검진지침을 검토하고, 간암 검진에 따른 사망률 감소를 중심으로 체계적인 문헌고찰을 통해 검진의 효과에 대한 의학적 근거를 평가하였다. 국내에서 만든 지침을 포함하여 총 8개의 임상 진료지침(APASL, 싱가폴 보건국, 뉴질랜드, NICE, JSH, EASL-EORTC, AASLD, 대한간암연구회)를 검토한 결과 고위험군에 대한 정의와 검진 방법, 검진 주기에 관해 약간의 차이가 있었지만 간암 검진은 고위험군에서 간암 사망위험률을 낮추는 효과가 있어서 권고된다는 일치된 의견을 확인할 수 있었다[1,2,3,4,5,6,7,8].
선택된 지침에서 근거 자료와 추가 검색 및 국내 자료를 검토한 결과 중등도의 근거 수준을 가지는 의미 있는 논문으로 판단한 1편의 RCT에서 고위험군인 만성 B형 간염 환자에서 초음파검사와 혈청 알파태아단백 검사를 6개월 간격으로 시행하면 간암에 의한 사망률을 37% 줄일 수 있다는 연구 결과와 많은 코호트 연구, 환자대조군 연구들에서 간암 검진이 유용하다는 동일한 보고를 하였고, 국내의 모든 연구결과도 이러한 결과를 뒷받침하고 있다.
간암 검진의 대상인 고위험군이 누구인가에 대해서는 문헌 검색을 통한 근거 평가와 세계적으로 가장 많이 활용되고 있는 AASLD와 EASL의 가이드라인을 참고하여 근거수준을 결정하였다[6,7]. 본 개정위원회에서는 간암 발생에 영향을 주는 간암의 가족력이나 알코올 섭취력 여부에 따른 간암 검진에 대한 연구가 근거를 평가하기에는 아직 불충분한 점을 고려하여 문헌검색에서 제외하였다. 간암 발생의 가장 강력한 위험 인자로 알려진 간경변증 환자를 간암 검진의 대상으로 정하는 것에는 이견이 없으며 우리나라에서 간암의 주요 원인이 되는 만성 B형 간염 역시 앞서 논의된 1편의 RCT와 문헌검색을 이용한 근거 평가를 통해 검진의 대상이 된다는 것이 확인되었다. 만성 C형 간염의 경우, 섬유화 정도를 알 수 없을 때 간암 검진으로 인한 명확한 이득이 있다는 보고나 임상지침은 없지만 서양이나 일본에서 간암의 주요 원인으로 알려져 있고 특히, 섬유화가 진행되어 있거나 간경변증이 있는 경우 간암 발생 확률이 높다. 다만, 만성 B형 간염 환자에서는 간경변증이 동반되지 않더라도 바이러스의 발암 기전에 따라 간암이 발생할 수 있지만, C형 간염의 경우는 진행된 간섬유화(F3 이상)에서 대부분 간암이 생기기 때문에 섬유화가 없거나 경미한 경우는 간암 검진의 이득이 상대적으로 덜 하다고 볼 수 있다[24]. 그러나, 간조직 생검을 하지 않고 임상적 소견으로 간 섬유화의 정도를 판단하는 것이 현실적으로 어렵기 때문에 만성 C형 간염에서 섬유화의 정도에 따라서 검진의 필요 유무를 결정하는 것은 추후 개정에서 다루기로 하였다.
만성 바이러스성 간염에서 최근 강력한 항바이러스제 치료가 과거보다 확대됨에 따라 항바이러스 치료를 받는 환자들의 간암 발생이 현저히 줄어든다는 보고가 늘고 있다. 특히, 만성 C형 간염은 일정 기간의 항바이러스 치료로 바이러스가 체내에서 완전히 소멸되는 일종의 '완치' 개념에 가깝기 때문에 치료 성공한 만성 C형 간염 환자에서 검진이 필요한지에 대해서는 아직까지 논란의 여지가 있다. 그러나 분명한 것은 간경변증이 있는 만성 C형 간염 환자에서 항바이러스 치료에 성공하더라도 여전히 간암 발생의 가능성이 있다는 사실이다[42]. 향후 검진지침에서는 이와 같이 바이러스성 간염으로 항바이러스 치료를 받는 환자들의 개별 위험도에 따라서 검진의 유무를 더 세밀하게 결정하는 것이 필요하다. 따라서 본 개정위원회에서는 현재의 근거평가를 통해 간암의 위험인자로 알려진 만성 B형 간염, 만성 C형 간염, 간경변증을 간암 검진의 대상으로 결정하였으며 진행된 섬유화를 동반하지 않는 만성 C형 간염환자의 경우 간암 발생의 위험이 낮아 검진 대상에서 제외할 수 있다는 임상적 고려사항을 추가하였다.
검진의 시작 연령과 종결 연령에 대해서는 세계적으로도 연구된 바가 없으나, B형과 C형 간염 환자의 40세 이상에서 간암 발생이 상승하기 시작한다는 국내 역학 결과를 근거로 하여 시작 연령을 40세로 결정하였고, 고령화 시대로 접어듦에 따라 80세 이상의 고령이라도 신체연령은 적은 경우가 많고 검진 대상군 자체가 간암의 고위험군 환자임을 고려할 때 나이만으로 간암 검진을 제외하기는 어렵다고 판단하였다.
간암 고위험군의 검진주기에 대한 연구는 3개월에서 12개월까지 다양하게 시행되었으며 대부분의 진료지침에서 6개월 간격의 검진주기를 권고하고 있다[6,7,30,43]. EASL, AASLD, 국내 간세포암종 진료가이드라인의 경우 6개월 간격의 추적관찰을 권고하고 있으나 근거수준은 낮다. 초음파를 이용하여 조기 간암을 발견하는 경우 6개월 간격으로 추적 관찰했을 때 조기 간암 진단의 민감도를 제한적으로 향상시킬 수 있는 것으로 보고되었다[32]. 따라서, 향후 6개월 간격의 검진주기에 대한 근거 높은 연구가 필요할 것으로 생각된다.
간암의 조기발견을 위한 검사 방법은 각 나라마다 차이를 보이는데 미국이나 유럽에서는 알파태아단백검사의 민감도가 낮으므로 이를 감시검사의 방법에서 제외하고 초음파 검사만을 권고하지만, 일본에서는 두 검사의 병행을 권고하고 있다. 이러한 간암 검진방법의 차이는 인종에 따라 간암 발생률의 차이가 있고 주된 간암의 원인질환이 다르기 때문이다. 개정위원회의 문헌 검색 결과 초음파 단독검사보다 초음파와 혈청 알파태아단백검사를 같이 하는 경우 민감도가 통계적으로 유의하게 높다는 근거가 부족하다. 그러나 각 문헌마다 알파태아단백의 절단값에 차이가 있고 항바이러스 치료를 받고 있는 경우, 알파태아단백이 간암 감시에 높은 민감도를 보이므로 본 개정위원회는 간암의 조기발견을 위한 검사방법으로 초음파검사와 혈청 알파태아단백 검사의 병행을 권고하였다. 고위험군에서 정기적으로 초음파와 혈청 알파태아단백 검사를 받더라도 검사 자체의 한계로 인해 진행된 병기의 간암으로 진단되는 경우가 있는 바, 간암의 조기 진단을 향상시키기 위한 새로운 영상 또는 혈청학적 검사의 개발이 반드시 필요하겠다.
간암 검진의 위해는 높은 위음성률로 이로 인해 약 20%의 간암 환자에서 진단이 지연될 수 있다. 특히, 간 초음파 검사는 검사 결과가 검사자의 능력에 지나치게 의존적이며 간경변으로 인해 결절화가 심하게 진행된 간에서는 검사가 매우 제한적일 수 있는 점, 비만인 수검자나 간 초음파로 검사가 어려운 위치에 있는 병변은 발견하기 어려운 점 등의 단점과 한계점들이 많이 지적되고 있다.
간 초음파 검사의 민감도와 정확도는 숙달된 검사자에 의한 결과이므로, 적절한 교육을 받지 않은 검사자에 의한 검사의 경우는 민감도가 더 낮을 수 있다. 그러므로 우리나라 국가 간암 검진의 경우 적극적인 검사의 질 관리가 필요하다.
알파 태아단백 검사도 관리가 되지 않을 경우 그 결과의 신뢰성을 얻을 수 없고 기준값에 대해서도 충분히 고려되어야 한다. 현재 혈청 알파태아단백 검사가 정량적인 검사 뿐 아니라 정성적인 검사도 간암검진 검사에서 인정하고 있으므로 향후 정부 차원에서 검사 방법의 질 관리 등 관련 정책을 수립하고 연구가 진행되어야 한다.
또한 위험군을 대상으로 함으로써 개인정보 관리의 문제가 발생할 수 있는데, 국가에서 주도하는 간암 검진 프로그램으로 인해 의도하지 않게 환자의 신체, 건강상의 비밀이 노출될 위험이 있으며, 특히 B형, C형 간염 환자의 경우 만성 전염성 질병으로 사회적 불이익을 받을 위험의 소지가 있다. 이와 더불어 건강보험청구 자료에 근거하여 국가가 간암 고위험군을 선정하는 방식 역시 개인정보보호 위배의 소지가 있다. 따라서 간암 검진 프로그램 개발 시 환자의 개인정보를 보호하기 위한 방안이 우선적으로 고려되어야 한다.
본 개정위원회는 국가간암검진사업으로 고위험군 군에 있어 6개월 간격으로 초음파와 혈청 태아단백검사를 권유하고 있다. 이러한 권고안은 과거의 국가간암검진과 거의 동일하다. 간암의 영상학적 진단 방법의 비약적인 발전과 새로운 간염, 간암 치료법의 등장 그리고 만성 B형 간염의 유병률의 감소 등의 변화로 간암 검진방법의 변화가 요구되지만 문헌검색 결과 변화를 수용할 만한 근거가 부족했다. 간암 검진의 효율성을 높이기 위해서는 고위험군의 다양한 요인에 따른 간암 발생률의 차이를 고려하고, 검진 대상자 선정의 정확성과 검진의 수검율도 증가시켜야 한다. 이를 위해서는 고위험군을 대상으로 한 현재의 국가 간암검진 프로그램을 진료 영역으로 전환시켜 고위험군에 대한 간 초음파의 보험 급여화와 바우처 제도 및 고위험군에 대한 주치의 제도 등을 고려해야 한다. 앞으로 국가 간암검진에 대해 10년간의 빅데이터 분석과 국가차원의 체계적인 연구를 통해 사업의 유용성에 대한 평가와 향후의 발전방안에 대한 논의를 하는 것이 필요하다.
간암의 고위험군인 B형 간염 표면항원 양성자, C형 간염 항체 양성자, 또는 간경변증 환자는 40세 이상부터(또는 간경변증 진단 시점부터) 매 6개월 간격으로 간 초음파 검사와 혈청 알파태아단백검사를 받는 것이 폐암 사망률과 전체 사망률을 감소시킬 수 있다는 중등도 수준의 근거가 있고, 검진으로 인한 위해보다는 얻게 되는 이득이 크므로 검진을 권고한다.
본 논문은 근거중심의 유용한 간암(간세포암종) 검진 권고안을 개발하기 위하여 국립암센터 주도로 구성된 다학제위원회의 광범위한 문헌검색 결과를 서술하고 있으며, 최종 권고안과 함께 권고사항의 근거 수준과 권고 등급을 기술하고, 간암 검진의 이득과 위해에 대해 논하고 있다. 특히 국내에서 간암이 차지하는 의료학적 경제적 파급효과가 매우 큰 질환중 하나로서 간암의 조기진단과 이로인한 근치적 시술은 매우 의미가 있다고 생각된다. 본 논문은 간암 검진의 핵심 질문을 중심으로 방대한 논문을 검색하였으며 국내와 국외의 원인 질환과 상황을 고려하여 권고안을 만들었으먀 최신 지식을 기반으로하여 근거중심의 내용을 중심으로 만들었다는데 의미가 있다. 따라서 이러한 권고안은 간암의 조기진단과 치료에 매우 의미 있는 권고안이라 할 수 있다.
[정리: 편집위원회]
References
1. Omata M, Lesmana LA, Tateishi R, Chen PJ, Lin SM, Yoshida H, Kudo M, Lee JM, Choi BI, Poon RT, Shiina S, Cheng AL, Jia JD, Obi S, Han KH, Jafri W, Chow P, Lim SG, Chawla YK, Budihusodo U, Gani RA, Lesmana CR, Putranto TA, Liaw YF, Sarin SK. Asian Pacific Association for the Study of the Liver consensus recommendations on hepatocellular carcinoma. Hepatol Int 2010;4:439-474.




2. Singapore Ministry of Health. Cancer screening: clinical practice guidelines. Singapore: Ministry of Health; 2010.
3. New Zealand Ministry of Health; New Zealand Guidelines Group. Suspected cancer in primary care: guidelines for investigation, referral and reducing ethnic disparities. Wellington: New Zealand Guidelines Group; 2009.
4. National Institute for Health and Care Excellence. Hepatitis B (chronic): diagnosis and management of chronic hepatitis B in children, young people and adults [Internet] London: National Institute for Health and Care Excellence. 2013;cited 2015 Apr 27. Available from: https://www.nice.org.uk/guidance/cg165
5. Kokudo N, Makuuchi M. Evidence-based clinical practice guidelines for hepatocellular carcinoma in Japan: the J-HCC guidelines. J Gastroenterol 2009;44:Suppl 19. 119-121.



6. Blachier M, Leleu H, Peck-Radosavljevic M, Valla DC, Roudot-Thoraval F. The burden of liver disease in Europe: a review of available epidemiological data. J Hepatol 2013;58:593-608.


7. Bruix J, Sherman M; American Association for the Study of Liver Diseases. Management of hepatocellular carcinoma: an update. Hepatology 2011;53:1020-1022.


8. Korean Liver Cancer Study Group and National Cancer Center, Korea. Practice guidelines for management of hepatocellular carcinoma 2009. Korean J Hepatol 2009;15:391-423.


9. Zhang BH, Yang BH, Tang ZY. Randomized controlled trial of screening for hepatocellular carcinoma. J Cancer Res Clin Oncol 2004;130:417-422.



10. Chen JG, Parkin DM, Chen QG, Lu JH, Shen QJ, Zhang BC, Zhu YR. Screening for liver cancer: results of a randomised controlled trial in Qidong, China. J Med Screen 2003;10:204-209.



11. Aghoram R, Cai P, Dickinson JA. Alpha-foetoprotein and/or liver ultrasonography for screening of hepatocellular carcinoma in patients with chronic hepatitis B. Cochrane Database Syst Rev 2012;9:CD002799.

12. Trevisani F, Cantarini MC, Labate AM, De Notariis S, Rapaccini G, Farinati F, Del Poggio P, Di Nolfo MA, Benvegnu L, Zoli M, Borzio F, Bernardi M; Italian Liver Cancer (ITALICA) group. Surveillance for hepatocellular carcinoma in elderly Italian patients with cirrhosis: effects on cancer staging and patient survival. Am J Gastroenterol 2004;99:1470-1476.


13. Yoo KY, Heon-Kim , Lee MS, Park BJ, Ahn YO, Lee HS, Kim CY, Park TS. A reconstructed cohort study on the hepatitis B virus infection as a risk factor of liver cancer in Korea. J Korean Med Sci 1991;6:319-324.



14. El-Serag HB, Kramer JR, Chen GJ, Duan Z, Richardson PA, Davila JA. Effectiveness of AFP and ultrasound tests on hepatocellular carcinoma mortality in HCV-infected patients in the USA. Gut 2011;60:992-997.


15. Huh K, Lee JK, Choi SY, Hong SI, Lee DS. A study on the prevalence of HBsAg and Anti-HCV in patients with hepatocellular carcinoma: comparative study with healthy blood donors. Korean J Clin Pathol 1998;18:458-463.
16. Tsai JF, Jeng JE, Ho MS, Chang WY, Hsieh MY, Lin ZY, Tsai JH. Additive effect modification of hepatitis B surface antigen and e antigen on the development of hepatocellular carcinoma. Br J Cancer 1996;73:1498-1502.




17. Lee HS, Lee JH, Choi MS, Kim CY. Comparison of the incidence of hepatocellular carcinoma in HBV-and HCV-associated liver cirrhosis: a prospective study. Korean J Hepatol 1996;2:21-28.
18. Jee SH, Ohrr H, Sull JW, Samet JM. Cigarette smoking, alcohol drinking, hepatitis B, and risk for hepatocellular carcinoma in Korea. J Natl Cancer Inst 2004;96:1851-1856.


19. Evans AA, Chen G, Ross EA, Shen FM, Lin WY, London WT. Eight-year follow-up of the 90,000-person Haimen City cohort. I. Hepatocellular carcinoma mortality, risk factors, and gender differences. Cancer Epidemiol Biomarkers Prev 2002;11:369-376.

20. Sun CA, Wu DM, Lin CC, Lu SN, You SL, Wang LY, Wu MH, Chen CJ. Incidence and cofactors of hepatitis C virus-related hepatocellular carcinoma: a prospective study of 12,008 men in Taiwan. Am J Epidemiol 2003;157:674-682.


21. Tsukuma H, Hiyama T, Tanaka S, Nakao M, Yabuuchi T, Kitamura T, Nakanishi K, Fujimoto I, Inoue A, Yamazaki H. Risk factors for hepatocellular carcinoma among patients with chronic liver disease. N Engl J Med 1993;328:1797-1801.


22. Liaw YF, Sung JJ, Chow WC, Farrell G, Lee CZ, Yuen H, Tanwandee T, Tao QM, Shue K, Keene ON, Dixon JS, Gray DF, Sabbat J; Cirrhosis Asian Lamivudine Multicentre Study Group. Lamivudine for patients with chronic hepatitis B and advanced liver disease. N Engl J Med 2004;351:1521-1531.


23. Moon C, Jung KS, Kim do Y, Baatarkhuu O, Park JY, Kim BK, Kim SU, Ahn SH, Han KH. Lower incidence of hepatocellular carcinoma and cirrhosis in hepatitis C patients with sustained virological response by pegylated interferon and ribavirin. Dig Dis Sci 2015;60:573-581.



24. Yoshida H, Shiratori Y, Moriyama M, Arakawa Y, Ide T, Sata M, Inoue O, Yano M, Tanaka M, Fujiyama S, Nishiguchi S, Kuroki T, Imazeki F, Yokosuka O, Kinoyama S, Yamada G, Omata M. Interferon therapy reduces the risk for hepato-cellular carcinoma: national surveillance program of cirrhotic and noncirrhotic patients with chronic hepatitis C in Japan. IHIT Study Group. Inhibition of Hepatocarcinogenesis by Interferon Therapy. Ann Intern Med 1999;131:174-181.


25. Chiaramonte M, Stroffolini T, Vian A, Stazi MA, Floreani A, Lorenzoni U, Lobello S, Farinati F, Naccarato R. Rate of incidence of hepatocellular carcinoma in patients with compensated viral cirrhosis. Cancer 1999;85:2132-2137.


26. Bolondi L, Sofia S, Siringo S, Gaiani S, Casali A, Zironi G, Pis-caglia F, Gramantieri L, Zanetti M, Sherman M. Surveillance programme of cirrhotic patients for early diagnosis and treatment of hepatocellular carcinoma: a cost effectiveness analysis. Gut 2001;48:251-259.



27. Pateron D, Ganne N, Trinchet JC, Aurousseau MH, Mal F, Meicler C, Coderc E, Reboullet P, Beaugrand M. Prospective study of screening for hepatocellular carcinoma in Caucasian patients with cirrhosis. J Hepatol 1994;20:65-71.


28. Han KH, Kim do Y, Park JY, Ahn SH, Kim J, Kim SU, Kim JK, Lee KS, Chon CY. Survival of hepatocellular carcinoma patients may be improved in surveillance interval not more than 6 months compared with more than 6 months: a 15-year prospective study. J Clin Gastroenterol 2013;47:538-544.

29. Santagostino E, Colombo M, Rivi M, Rumi MG, Rocino A, Linari S, Mannucci PM; Study Group of the Association of Italian Hemophilia Centers. A 6-month versus a 12-month surveillance for hepatocellular carcinoma in 559 hemophiliacs infected with the hepatitis C virus. Blood 2003;102:78-82.



30. Santi V, Trevisani F, Gramenzi A, Grignaschi A, Mirici-Cappa F, Del Poggio P, Di Nolfo MA, Benvegnu L, Farinati F, Zoli M, Giannini EG, Borzio F, Caturelli E, Chiaramonte M, Bernardi M; Italian Liver Cancer (ITA.LI.CA) Group. Semiannual surveillance is superior to annual surveillance for the detection of early hepatocellular carcinoma and patient survival. J Hepatol 2010;53:291-297.


31. Wang JH, Chang KC, Kee KM, Chen PF, Yen YH, Tseng PL, Kuo YH, Tsai MC, Hung CH, Chen CH, Tai WC, Tsai LS, Chen SC, Lin SC, Lu SN. Hepatocellular carcinoma surveillance at 4- vs. 12-month intervals for patients with chronic viral hepatitis: a randomized study in community. Am J Gastroenterol 2013;108:416-424.



32. Singal A, Volk ML, Waljee A, Salgia R, Higgins P, Rogers MA, Marrero JA. Meta-analysis: surveillance with ultrasound for early-stage hepatocellular carcinoma in patients with cirrhosis. Aliment Pharmacol Ther 2009;30:37-47.



33. National Cancer Center. Korean Liver Cancer Study Group. 2014 Practice guidelines for the management of hepatocellular carcinoma. Goyang: National Cancer Center; 2014.
34. Kudo M. Real practice of hepatocellular carcinoma in Japan: conclusions of the Japan Society of Hepatology 2009 Kobe Congress. Oncology 2010;78:Suppl 1. 180-188.



35. Cottone M, Turri M, Caltagirone M, Parisi P, Orlando A, Fiorentino G, Virdone R, Fusco G, Grasso R, Simonetti RG. Screening for hepatocellular carcinoma in patients with child's A cirrhosis: an 8-year prospective study by ultrasound and alphafetoprotein. J Hepatol 1994;21:1029-1034.


36. Sangiovanni A, Del Ninno E, Fasani P, De Fazio C, Ronchi G, Romeo R, Morabito A, De Franchis R, Colombo M. Increased survival of cirrhotic patients with a hepatocellular carcinoma detected during surveillance. Gastroenterology 2004;126:1005-1014.


37. Sangiovanni A, Prati GM, Fasani P, Ronchi G, Romeo R, Manini M, Del Ninno E, Morabito A, Colombo M. The natural history of compensated cirrhosis due to hepatitis C virus: a 17-year cohort study of 214 patients. Hepatology 2006;43:1303-1310.


38. Tradati F, Colombo M, Mannucci PM, Rumi MG, De Fazio C, Gamba G, Ciavarella N, Rocino A, Morfini M, Scaraggi A, Taioli E. A prospective multicenter study of hepatocellular carcinoma in italian hemophiliacs with chronic hepatitis C. The Study Group of the Association of Italian Hemophilia Centers. Blood 1998;91:1173-1177.

39. Wong GL, Chan HL, Tse YK, Chan HY, Tse CH, Lo AO, Wong VW. On-treatment alpha-fetoprotein is a specific tumor marker for hepatocellular carcinoma in patients with chronic hepatitis B receiving entecavir. Hepatology 2014;59:986-995.


40. Rockey DC, Caldwell SH, Goodman ZD, Nelson RC, Smith AD; American Association for the Study of Liver Diseases. Liver biopsy. Hepatology 2009;49:1017-1044.


41. Committee to assess health risks from exposure to low levels of ionizing radiation, national research council. Health risks from exposure to low levels of ionizing radiation: BEIR VII-Phase 2. The national academies press; 2006.
42. Aleman S, Rahbin N, Weiland O, Davidsdottir L, Hedenstierna M, Rose N, Verbaan H, Stal P, Carlsson T, Norrgren H, Ekbom A, Granath F, Hultcrantz R. A risk for hepatocellular carcinoma persists long-term after sustained virologic response in patients with hepatitis C-associated liver cirrhosis. Clin Infect Dis 2013;57:230-236.


Figure 1
Concept of analysis frame. Key question (KQ) 1, does surveillance of hepatocellular carcinoma (HCC) for high-risk patients reduce HCC-related mortality?; KQ2, Who are the target population for HCC surveillance? (definition of high risk patients, starting and ending ages for surveillance); KQ3, What is the optimal interval of HCC surveillance?; KQ4, What is the appropriate surveillance tool?; KQ5, Is there any potential harm associated with HCC surveillance?
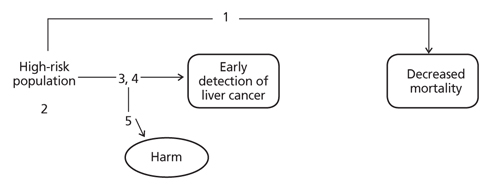
Figure 2
Flow of searching literatures for evidence of hepatocellular carcinoma surveillance guidelines.
- TOOLS
-
METRICS

-
Related articles in
J Korean Med Assoc -
Update on the Treatment of Hepatocelluar Carcinoma1997 February;40(2)
Treatment Guidelines for Gallbladder Polyps2006 May;49(5)
Up-to-date Information for Hepatocellular Carcinoma Treatment2008 May;51(5)
Recent advances in the management of hepatocellular carcinoma2013 November;56(11)
Recent development of diagnostic imaging of hepatocellular carcinoma2013 November;56(11)