|
 |
- Search
| J Korean Med Assoc > Volume 57(11); 2014 > Article |
Abstract
Health technology assessment was first introduced to the Republic of Korea in 2006 by amending the Medical Services Act. The Committee of New Health Technology Assessment (CNHTA) is the ministerial committee that has the responsibility of reviewing the safety and effectiveness of new health technology. CNHTA review plays a gatekeeping role for new health technology in Korea, which can increase the burden on patients in Korea, either by out-of pocket payments or co-pays for National Health Insurance covered service. This kind of gatekeeping is a function of the healthcare system in many countries where no financial cap such as a fixed budget or diagnosis-related group payment is applied. However, it has been argued that gatekeeping works against industrial promotion policy. The one-stop service introduced in 2014 is a system similar to US parallel review between the US Food and Drug Administration and Centers for Medicare and Medicaid Services. This service provides a simultaneous process of regulatory review by the Ministry of Food and Drug Safety, identification of existing technology by the Health Insurance Review and Assessment Services, and new health technology assessment by the National Evidence-based Healthcare Collaborating Agency and the Ministry of Health and Welfare. This service is expected to reduce the total review process by 3 to12 months. A limited health technology appointment service was introduced in April 2014. This service designates orphan health technologies and health technologies for rare and incurable diseases and supports evidence development at designated hospitals. Several countries have similar systems: US Coverage with Evidence Development, Canadian Conditionally Funded Field Evaluation, UK Only in Research, and many others. The future direction of Health technology assessment should focus on the life cycle management of health technology. A consistent, continuous, and transformative mechanism to manage from the research and development of health technology to delisting obsolete technology to make room for new innovative technology is warranted.
신의료기술평가제도가 도입되기 전 의료기술의 안전성·유효성은 2000년 7월 제정·고시된 미결정행위등의결정및조정기준에 의해 의료기관 관련단체나 중앙의료심사조정위원회의 의견으로 확인하였다. 당시에는 의료기술을 과학적으로 평가하겠다는 의미보다는 기존에 누적되었던 미결정행위의 건강보험 등재여부를 결정하기 위해 법적인 근거를 마련하였고, 이에 사용되는 명칭도 신의료기술이 아닌 미결정행위로 명명하였다[1].
미결정행위결정신청은 제도 도입초기에 만여 건이 넘는 기술이 폭발적으로 신청되었으나 2002년 이후 점차 안정화됨에 따라 현존하는 의료기술보다는 새로운 의료기술의 신청이 증가하였다. 이에 따라 2002년 8월 '미결정행위결정행위등의결정및조정기준'도 '신의료기술등의결정및조정기준 (제2002호-60호, 2002년 8월 21일)'으로 전문 개정되었다[1]. 개정 당시 의료기술의 안전성·유효성에 대한 검증을 각 전문위원회의 '실무검토'에서 건강보험심사평가원장이 '확인'하는 것으로 변경되었고, 확인 방법도 의료법 제3조 및 제26조의 규정에 의해 설립된 의료기관 관련단체나 의료법 제54조의2 규정에 의한 중앙의료심사조정위원회가 추가되었다. 문제는 안전성·유효성을 인정하는 주체가 다수이고 각기 상이한 의견이 제출되었을 때 이를 객관적으로 확인할 근거가 부족함에 따라 결국 결정신청 등이 지연처리되는 문제가 발생하였다[1].
또한, 의료기술의 공적 특성 때문에 특허 등의 개인적 이점이 없어 이를 의료인 혹은 관련단체가 과학적이고 객관적 판단이 가능한 안전성·유효성에 대한 근거를 제시하는데 대한 제도적 유인동기가 부족하여 건강보험심사평가원장이 이를 확인하는데 어려움이 있었다. 이러한 문제점으로 인해 보건복지부에서는 2003년 7월 건강보험심사평가원에 의료기술평가사업단을 구성하게 하고, 선험국들의 의료기술평가 관련 법적 제도나 기구 및 평가방법론 등에 대해 검토하도록 하였다. 건강보험심사평가원 의료기술평가개발단에서는 2004년 6월부터 12월까지 '간암에 실시하는 고주파 열치료술'에 대해서 1차 시범평가를 시행하였으며, 2004년 12월부터 2005년 8월까지 '실시간 정량적 중합효소연쇄반응'에 대해 2차 시범평가를 수행하였다. 또한 2004년 12월에는 신의료기술평가제도 도입을 위한 공개 심포지엄을 개최하여 대한의사협회, 대한한의사협회, 대한치과의사협회, 한국의료법학회의 참석 하에 제도 도입에 대한 의견수렴을 진행하여 모든 단체에서 찬성함에 따라 의료법 개정 발의를 진행하게 되었다[1]. 이러한 과정을 거쳐 의료법 개정을 통해 2006년 6월에 신의료기술평가 법적 근거가 마련되었으며, 2007년 4월 28일 신의료기술평가제도가 시행되었다.
신의료기술 안전성·유효성 평가는 개정된 의료법에 따라 보건복지부 산하 위원회인 신의료기술평가위원회에서 수행하고 있다. 위원회는 20명의 위원으로 구성되어 있으며, 대한의사협회, 대한치과의사협회, 대한한의사협회, 소비자단체, 대한변호사협회에서 추천하는 위원과 공익 위원으로 구성되어 있다. 위원회는 현재 신의료기술평가 대상이 되는지 여부와 신의료기술의 안전성·유효성 여부를 최종심의 하는 권한을 가지고 있으며, 위원회에서 안전성·유효성이 있는 기술이라고 심의된 경우에는 보건복지부 장관이 고시함으로 임상현장에서 사용할 수 있도록 최종 승인을 받게 된다. 신의료기술평가는 다양한 분야의 여러 기술을 평가해야하다 보니 20명의 위원으로는 전문적인 평가가 어려운 부분이 있다. 따라서, 초기부터 분야별 전문평가위원회를 구성하여 운영되어 왔는데 초창기에는 248인의 분야별 전문평가위원회 위원을 운영하다가 최근에는 새로운 신청 분야의 위원을 증원하여 548명으로 위원풀을 확대하였다.
신의료기술평가제도가 시행된 2007년 5월부터 2014년 9월 30일 현재까지 1,609건의 기술이 신청되었으며, 이는 연간 평균 약 220건의 기술이 신의료기술평가 신청되었다. 신청되는 기술들 중 완전히 새로운 개념의 기술이 신청되는 경우는 거의 없으며, 신청되고 있는 대부분의 기술은 기존기술을 개선한 기술들이다. 신의료기술평가위원회의 중요한 업무 중의 하나가 신청기술이 기존에 이미 임상현장에서 사용되는 기술에 포함되는 기술인지 여부를 결정하는 것이며, 안전성·유효성이 변경될 개연성이 크지 않은 경우 기존기술 범주에 포함되는 기술로 판단하고 있다. 2014년 9월 30일 현재까지 신청된 기술 1,609건 중 약 14.6%(242건)가 기존기술로 평가되었으며, 신청취하 및 반려된 기술 10.4%(167건)을 제외하면 약 71.7%(1,154건)가 기존기술이 아닌 신의료기술로 평가되었다. 기존기술이 아닌 신의료기술로 심의되어 평가된 안건들 중 아직 임상현장에 도입하기에는 근거가 부족하다고 판단되는 기술(조기기술 혹은 연구단계기술)이 전체 신청 건 중 약 3분의 1(32.6%)이며, 안전성·유효성이 확인되어 임상현장 도입이 가능하겠다고 심의된 기술이 조금 높은 35.1%(565건)로 유사한 비율을 보이고 있다.
신청기술 분야별로 분석해 보면, 의과가 95.9%, 한의과가 2.3%, 치과가 1.5%로 의과 기술의 신청비율이 압도적이었으며, 이는 건강보험 등재 현황과 무관하지 않을 것으로 판단된다. 의과 기술의 경우 사용대상·목적·방법 등이 세분화되어 등재되어 있는 반면, 치과·한의과 기술의 경우 적응증 등이 의과 기술보다 상대적으로 광범위하게 등재되어 있어 기존기술에 해당되는 범주가 넓어 신의료기술에 해당되는 기술이 많지가 않아 신청비율 또한 낮은 것으로 판단된다.
기술별로 보면, 처치 및 시술의 신청비율이 35.4%, 진단검사 43.5%, 유전자검사가 20.7%로 진단검사 분야가 가장 높은 신청 비중을 차지하고 있으며, 유전자검사 또한 진단검사 영역에 포함시켜야 하나, 신청비율이 증가하면서 별도로 통계를 산출하고 있다. 이는 진단검사 분야의 신의료기술 개발이 처치·시술에 비해 용이하며, 체외진단검사 분야가 세분화되어 등재되어 있어 신청비율이 높은 것으로 판단된다.
기관별 신청현황을 분석해보면, 상급종합병원이 39.9%, 종합병원이 8.8%, 병의원이 7.3%, 치과 병의원 0.5%, 한방 병의원 0.9%이었으며, 비의료기관(의료기기 제조·수입업체, 검사기관 등)이 42.6%로 나타났다. 신의료기술평가 신청은 현재 요양급여행위결정신청과 달리 누구나 신청가능하여 현재 의료기기 제조 및 수입업체의 신청 비율이 높게 나타나고 있으며, 또한 신의료기술의 경우 상급종합병원에서 가장 도입을 빠르게 시행하는 경우가 많아 신청 비율이 높은 것으로 판단된다.
신의료기술평가 후 요양급여결정신청을 하여 급여, 선별급여 혹은 비급여로 결정된 비율을 보면, 2014년 9월 30일 현재 기준으로 총 290개 기술이 결정되었으며, 급여비율이 26.6%(77개), 선별급여 0.14%(4개), 비급여 72.1%(209개)로 나타났다. 인정된 대부분의 기술이 새로운 의료기술이다 보니 급여로 지급하기에는 기존기술보다 경제적이라는 자료가 미흡할 것으로 판단되며, 또한 비급여로 결정된 절반 이상이 유전자검사(109개, 52.2%)로 비급여로 결정된 비율의 많은 비중을 차지하고 있다.
외국에서는 의료기술평가를 급여권에 진입하기 위한 사전절차로 시행을 하고 있다. 그래서 사회보장제도가 확립된 유럽국가에서 주로 의료기술평가제도가 발달하였으며, 안전성·유효성·경제성 평가를 함께 시행하여 급여여부를 결정하고 있다. 우리나라는 이와 달리 급여·비급여 여부를 결정하기 전에 신의료기술평가를 시행하고 있으며, 신의료기술평가를 받아 안전성·유효성이 인정되지 않을 경우 사실상 환자에게 비용을 지불하도록 할 수 없어 시장진입이 어려운 실정이다. 외국에서는 각국의 식약처 허가를 득한 이후에는 환자에게 비용부담을 시키는 것이 가능하나, 우리나라의 경우 식약처 허가 후 판매는 가능하지만 국민건강보험법에 의해 등재되어 있지 않은 행위에 대해서는 환자에게 비용 부담을 시킬 수가 없다. 이는 비급여까지 시장 진입에 대해 관리하고 있는 우리나라의 독특한 보험제도에서 기인한 현상이다. 이는 신의료기술평가제도 도입 전에도 새로운 의료기술에 대하여 안전성·유효성을 전문학회 의견으로 확인하였으며, 학회의견에서 안전성·유효성이 미확립되었다고 판단되는 기술에 대해서는 식약처 허가를 득한 경우에도 승인되지 않았던 절차를 계승하였기 때문이다.
이러한 제도가 정착하게 된 계기는 우리나라 비급여 관리문제와 연관되어 있다고 판단된다. 대부분의 유럽 국가에서는 급여로 등재되지 않은 기술에 대해서는 의료기관에서 사용하기 어려운 구조를 가지고 있다. 의료기관에서 비급여 의료행위를 시행하기를 원하는 경우, 의사가 환자에게 기존에 급여에 등재된 기존기술들에 대해 설명을 한 후 새로운 비급여 기술을 이용한 진료를 받을지 여부에 대해 사전 환자 동의를 얻어야 한다. 또한, 비급여 기술의 경우 급여로 지원되지 않아 가격 부담이 크기에 특별한 경우가 아니면 비급여 행위가 시행되기 어려운 상황이다[2].
그러나, 우리나라의 경우 저수가 기조로 인해 오히려 급여행위보다 비급여 진료행위를 의료기관에서 선호하고 있는 구조적 모순을 가지고 있으며, 급여권에 진입하고자 하는 노력을 시행하지 않는 경우가 다수이다. 이러한 비급여 관리기전 부재로 인해 신의료기술평가가 시장 도입 전 선별 절차의 하나로 수행되고 있으며, 신의료기술평가가 외국과 달리 시장 진입의 큰 장벽으로 인식되고 있어 산업계로부터 규제 철폐에 대한 제도 개선 압박을 지속적으로 요청받고 있는 실정이다.
신의료기술평가 현황에서 밝힌 바와 같이 신청 건 중 약 33%는 안전성·유효성을 확인할 만한 근거가 부족한 기술로 결정되어 시장 도입을 허용하고 있지 않다. 그러나, 근거가 부족한 기술 중에서도 발전 가능성이 있으며, 잠재적으로 이익을 줄 수 있는 기술들이 있으나 이를 지원해줄 수 있는 제도적인 체계가 미흡한 실정이다.
현재 미국의 경우 2014년 보건의료 연구개발(research and development, R&D) 지출비용이 327억 달러(약 34조 9천억 원)이며, 영국은 2011-2012년에 20억 파운드(약 3조 4천억 원), 일본은 2013년 3,000억 엔(약 2조 9천억 원)에 이르나, 우리나라의 보건의료 R&D 비용은 2014년 13억 달러(약 1조 3천억 원)로 선진국에 절반에도 못미치는 수준의 R&D 비용이 투자되고 있다. 이는 선진국에 비하여 전체 R&D 비용 중 보건의료 R&D 분야에 투여되는 자원 비중도 미흡한 실정이다(전체 R&D 비용 중 보건의료 R&D에 투여되는 비용은 미국 22.3%, 영국 18.2%, 일본 8.4%, 한국 6.6%) [3].
잠재적 이익이 있다고 하여 근거가 부족한 기술을 환자에게 비용을 지불하게 하여 직접 사용하게 하는 것은 윤리적·경제적으로 문제를 야기할 수 있으므로 근거를 창출할 수 있는 국가적인 임상 R&D 지원 확대가 필요할 것으로 판단된다. 또한 국내개발 기술에 대해서도 외국 글로벌기업과의 경쟁력을 갖추게 하기 위한 제도적인 보완장치가 필요할 것으로 생각된다.
신의료기술평가제도는 의료법에 명시된 것처럼 국민건강을 보호하고, 의료기술의 발전을 촉진하기 위하여 시행되고 있다. 국민건강을 보호하면서 안전성·유효성이 확보된 기술이 시장진입을 신속하게 할 수 있도록 시행된 제도가 신의료기술평가 원스탑서비스제도이다. 신의료기술평가 원스탑서비스제도는 의료기기 허가(식품의약품안전처), 기존기술여부 확인(건강보험심사평가원), 신의료기술평가(보건복지부·한국보건의료연구원)를 동시에 시행하는 제도이다.
미국에서도 'parallel review'라는 이름으로 식약처(Food and Drug Administration)의 의료기기 인허가를 진행하면서 공보험 관리기관인 Centers for Medicare & Medicaid Services가 동시에 보험급여등재여부를 검토하고 있는 유사사례가 보고되고 있다. 현재 연간 3-5건 정도를 시범사업으로 시행하고 있으며, 임상시험 검토 건에 한하여 실시하고 있다[4]. 호주에서도 유사제도가 시행되고 있으며, 호주 식약처인 Therapeutic Goods Adminisration (TGA)에서 의료기기 허가에 관한 '자동 이메일 알림서비스' 제도를 도입하여 TGA로 접수된 서류들이 호주의 의료기술평가기구인 Medical Services Advisory Committee에 동시에 전송되는 시스템으로 TGA 허가와 의료기술평가를 동시에 진행하고 있다. 이러한 동시 검토제도는 새로운 의료기술에 대해 검증은 충분히 시행하면서 행정적인 기간을 단축하여 환자에게 필요한 기술들이 신속하게 임상현장에 도입할 수 있도록 시행되는 제도이다.
신의료기술평가 원스탑서비스제도는 2013년 12월부터 시범사업을 실시하여 2014년 8월 전면 시행되었으며, 최소 3개월에서 최대 12개월까지 시장진입 기간이 단축될 것으로 예상된다. 또한, 검사 전문 소위원회, 유전자 전문 소위원회를 구성하여 신속평가를 수행한 것과 같이 단계적으로 평가기간을 단축할 수 있는 다양한 방안 모색이 필요할 것으로 판단된다. 추후에도 검증은 충분히 시행하면서 행정적인 기간 및 평가기간을 단축할 수 있는 방향으로 제도개선이 이루어져야 할 것이다.
안전성·유효성을 판단할 만한 근거는 부족하나 대체기술이 없거나 혹은 희귀난치성 질환 치료(혹은 검사)에 사용되는 기술로 임상도입이 시급한 기술을 선정하여 일부 의료기관에서만 시행하는 제한적 의료기술제도를 2014년 4월 도입하였다. 이러한 제도는 대부분의 선진국에서 고민하고 있는 부분으로 기존에 사용되고 있는 기술에 비해 새로운 기술이 얼마만큼의 안전성·유효성·경제성에 대한 이득을 줄 것인지에 대한 근거 마련을 위해 제도를 운영하고 있다.
미국에서는 이러한 안전성·유효성·경제성의 근거가 부족한 약물, 바이오 의약품, 의료기기, 진단법 및 시술의 보험급여에 대한 공식적인 허가제도 마련을 위해 Coverage with Evidence Development라는 제도를 운영하고 있다[5]. 캐나다에서는 Conditionally Funded Field Evaluation라는 제도로 시행되고 있으며, 마찬가지로 잠재성은 있으나 현재 유효성 관련 근거가 미약한 기술을 선정하여 정부가 연구지원을 시행하는 제도이다[6]. 영국은 Only in Research), 일본은 선진의료기술지원제도가 유사제도로 시행되고 있다[7]. 이러한 노력을 선진국에서 기울이는 이유는 국민들에게 시행되는 의료기술의 안전성 확보 및 한정된 자원을 효율적으로 사용하고자 시행하고 있다.
우리나라에서도 발전 가능성이 있는 기술에 대해서 근거창출마련 기회와 환자에게 치료 받을 권리를 보장할 수 있는 제도적인 보완장치가 지속적으로 확대될 수 있도록 노력해야 할 것이다.
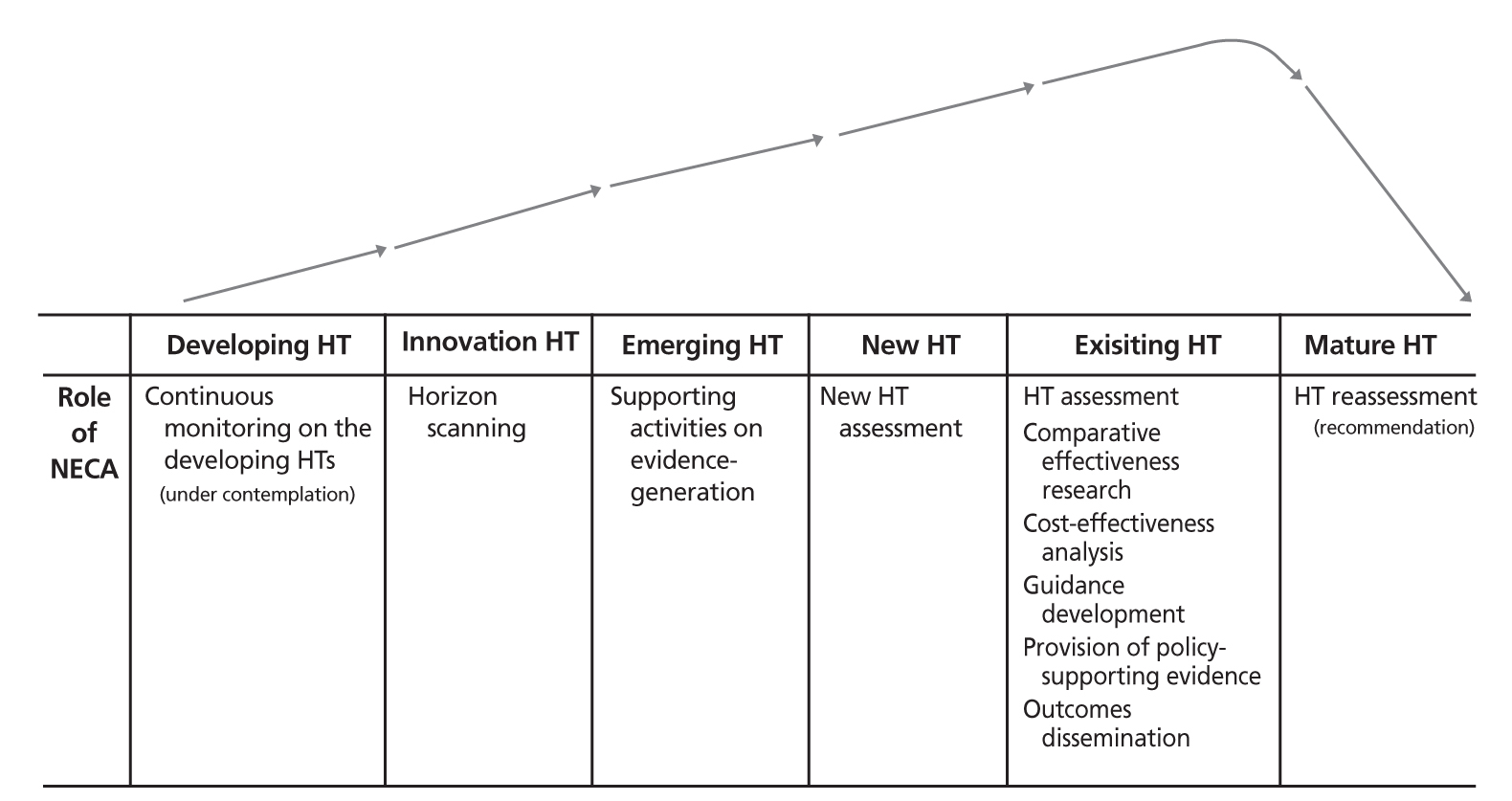
위에서 언급한 바와 같이 선순환 구조를 유지하기 위해서는 의료기술의 전 주기적 평가관리 체계를 확립해야 할 필요가 있다. 전주기적 의료기술 평가관리란 Figure 1과 같이 유망 의료기술의 발굴·분석, 개발단계 의료기술의 체계적 연구지원·관리, 신의료기술평가 기획 및 연구와 기존 의료기술의 최적 사용을 위한 재평가까지 일관성 있고, 연속적이며, 발전성 있게 수행하는 관리체계를 말한다. 이러한 체계가 구축될 때 효율적으로 보건의료 분야의 R&D 투자비용을 활용하여 의료기술 발전에 선순환 구조를 구축하고, 적절한 의료기술이 국민들에게 사용될 수 있도록 지원할 수 있을 것으로 생각된다.
의료기기나 의약품의 품목허가와 의료기술평가를 혼돈하고 있다. 전자는 효능 및 부작용자료를 검토하여 인체에 사용할 수 있는가를 관리하는 제도로 식품의약품안전처에서 담당하고 있는 반면, 후자는 해당 의료기술이 진료현장에서 사용할만한 가치가 있는지를 평가하는 제도로 한국보건의료연구원에서 수행하고 있다. 선진국과 비교하여 한국은 의료기술평가분야에서 많이 낙후된 상태로, 본 논문은 의료기술평가의 현재 상황과 문제점 및 개선책을 정리하고 있다. 근거중심의 의료제도 확립을 위한 전제조건인 의료기술평가가 활성화되기 위해서는 저자들이 제시하는 방안에 의료인, 관련 산업 종사자, 정책당국자 들의 적극적인 협조가 필요하다.
[정리: 편집위원회]
References
1. Lee SM. A study on the system and management plan for health technology assessment. Seoul: Health Insurance Review Agency; 2005.
2. Choi YS. Uninsured medical fee status and management plan. Seoul: National Health Insurance Corporation; 2007.
3. Kim JY. Health technology promotion government R&D plan. Seoul: Korea Health Industry Development Institute; 2014.
4. US Food and Drug Administration. FDA-CMS parallel review [Internet] New Hampshire: US Food and Drug Administration. 2014;cited 2014 Nov 3. Available from: http://www.fda.gov/MedicalDevices/DeviceRegulationandGuidance/HowtoMarketYourDevice/PremarketSubmissions/ucm255678.htm
5. Trueman P, Grainger DL, Downs KE. Coverage with Evidence Development: applications and issues. Int J Technol Assess Health Care 2010;26:79-85.


6. Goeree R, Chandra K, Tarride JE, O'Reilly D, Xie F, Bowen J, Blackhouse G, Hopkins R. Conditionally funded field evaluations: PATHs coverage with evidence development program for Ontario. Value Health 2010;13:Suppl 1. S8-S11.


7. Shin CM. The development of clinical management guide for temporary approval of new health technology. Seoul: National Evidenced-based Healthcare Collaborating Agency; 2013.
- TOOLS
-
METRICS

-
Related articles in
J Korean Med Assoc -
The current state and outlook of HIV infection and AIDS in South Korea2024 March;67(3)
Current status and direction of welfare policy for people with disabilities2010 December;53(12)
Current situation of national health screening systems in Korea2011 July;54(7)
Systematic review for new health technology assessment2012 March;55(3)