천공지피판 개념과 미세수술을 이용한 조직재건
Concept of perforator flap and reconstruction using microsurgery
Article information
Abstract
Free tissue transfer has revolutionized tissue reconstruction. Microvascular operation techniques using free tissue transfer make it possible to precisely restore various defects and deformities. There are various surgical flaps available for this surgery, such as muscle flaps, musculocutaneous flaps, or fasciocutaneous flaps. The development of perforator flaps enables multi-component reconstruction with reduced donor site morbidity. Successful reconstruction must be approached with the goals of not only providing stable coverage, but most importantly, of restoring function. Therefore, the selection of flaps is dependent on the recipient site characteristics and the functional and aesthetic results at both the recipient and donor sites. With the high success rate of free flaps and the popularization of the perforator flap, microvascular surgery has played a major role in various reconstructive fields.
서론
미세수술의 발전은 과거 여러 단계의 수술로 이루기 힘들던 재건을 한 단계의 유리피판술로 가능하게 하여 재건 수술 영역에서 큰 혁신을 일으켰다. 1897년 Murphy [1]가 첫 번째 혈관문합을 시행하였으며, 1902년 Carrel은 동맥과 정맥의 혈관문합을 이용한 혈관의 삼각망(triangulation) 방법을 기술하여 1912년 노벨상을 수상하였다[2]. 1960년대에 이르러 Jacobson과 Suarez [3]가 현미경을 이용하여 1.4 mm 정도의 가는 혈관문합에 성공하였으며 미세혈관 수술(microvascular surgery) 개념을 정립하였다. 1973년 Daniel과 Taylor [4]가 "유리피판(free flap)"이란 단어를 사용하고, 유리 서혜부 피판(free groin flap)이 발표되면서 재건미세수술이 시작되었다[5]. 한국에서도 세계적인 미세수술 분야의 발전에 편승하여 1970년대에 이르러 미세수술이 행해지기 시작하였으며, 1974년 최초의 피판 관련 논문이 [6], 그리고 1978년 유리피판 관련 논문이 국내 학회지에 게재되었다[7].
피판의 개념이 점차 발전하기 시작하면서, 동맥을 기저로 하는 피판에서, 동맥의 분지를 기저로 하는 피판, 최근에는 이 분지의 천공지(perforator)를 이용하는 천공지피판(perforator flap)에 대한 개념이 도입되었다. 즉 과거에는 동맥을 기저로 하고 근육을 포함하는 근피판(musculocutaneous flap)이 유용하게 사용되었으나[8] 부피가 크고 공여부 근육의 손실로 인한 공여부 이환율 문제가 대두되었다. 이후에 동맥의 분지를 기저로 한 근막피부판(fasciocutaneous flap)이 도입되어 근육을 보존하고 근막만을 포함한 얇은 피판이 가능하게 되었다[9]. 최근에는 1989년 Koshima와 Soeda [10]에 의해 천공지 개념이 도입되어, 근육을 관통하여 피부 및 피하지방에 안정적으로 혈류를 공급하는 말초 분지 혈관경인 천공지를 기저로 하는 피판을 천공지피판으로 명하게 되었다. 이후 혈관 분지와 혈관 분포영역(angiosome)에 대한 광범위한 연구가 진행되면서 다양한 공여부에서 천공지피판의 가능성이 보고되고 있다. 결과적으로 재건에 필요한 조직만을 선택적으로 거상함으로써 공여부의 희생을 최소화할 수 있세 되었으며, 두께를 자유롭게 조절하거나 결손부에 맞추어 조직을 재단사처럼 재단할 수도 있으므로 인해 피판의 선택이 보다 자유로워지게 되었다. 현재 이 천공지피판은 유방재건, 상하지재건, 두경부재건 등 다양한 분야에서 기존의 피판을 대체할 수 있는 또 다른 유용한 피판으로 생각되어 많은 적용이 이루어지고 있다[1112].
현재 재건 분야에서 가장 대표적인 수술방법으로 기능적, 미용적으로 만족스러운 재건을 위해 널리 이용되고 있는 미세수술을 이용한 유리피판술을 살펴보고, 여러 분야에 걸쳐 다양하게 사용되고 있는 천공지피판의 적용에 대해 소개하고자 한다.
미세수술의 장점
재건이 필요한 결손이 있을 때 전통적인 재건 사다리(reconstructive ladder)의 개념은 비교적 쉽고 간단한 피부이식부터 시작하여 국소피판, 유리피판 등 점차 어렵고 복잡한 수술을 통한 재건을 고려하는 개념이다[13]. 그러나 미세수술의 발전에 따라 재건미세수술의 결과가 더욱 향상되었으며 국내 학회지에 보고된 유리피판의 성공률은 97.3–100%로 매우 높아져 국재에서는 이제 모든 재건법을 고려하여 술자의 경험과 선호도, 환자의 상태에 따라 자유롭게 재건방법을 선택할 수 있는 세계적 수준의 단계에 이르렀다.
미세혈관수술을 이용한 유리피판전이술(free flap trans-fer)은 과거 수 차례의 수술 과정으로 이루어진 원거리 조직 이동을 단 한번의 수술로 옮길 수 있게 되었다. 또한 손상부위와 멀리 떨어져 있는 공여부를 선택할 수 있으므로 흉터가 쉽게 가려질 수 있는 부위에서, 재건에 필요한 적절한 조직을 거상할 수 있다. 특히 외상이나 방사선 조사를 받은 창상의 경우, 조직의 손상이 광범위하여 주변 조직을 이용한 재건이 어려운데, 다른 혈관분포를 기저로 하는 멀리 떨어져 있는 부위의 조직을 이용하여 상처치유를 도울 수도 있다[13]. 뿐만 아니라, 근육, 뼈, 소화기관가 같은 특수한 조직의 이식이 필요한 경우에도 미세수술을 이용하면 기능적 재건도 가능하다.
유리피판술의 적응증
유리피판술은 상처피복과 복합조직이식을 위해 안전하고 믿을 수 있는 재건방법으로 정립되었다. 95% 이상의 성공률과 다양한 공여부를 활용하여 복합조직이식이 가능하게 되었다. 연부조직재건의 중요한 요건으로는 안정적인 지지 구조, 손상 받지 않은 수용부 혈관(recipient vessel), 주변 조직으로부터 적절한 혈액공급, 안정된 환자 상태, 그리고 미세수술에 숙달된 의사가 필요하다[14]. 유리피판술이 요구되는 경우는 주변 조직손상으로 국소피판술이 불가능할 때 또는 연부조직 손상이 광범위하고 중요구조물인 뼈, 인대, 신경, 혈관 등이 노출되어 피부이식과 같은 수술이 어려울 때이다[14]. 또한 유리피판술은 국소피판술이나 줄기피판술(pedicled flap)과 비교하여 여러 가지 장점이 있다[15]. 이미 손상 받은 부위에서 또 다른 공여부의 거상에 따른 이환율 또는 수술적인 부담을 줄일 수 있고, 주요 혈관들을 보존할 수 있으며, 혈관분포가 풍부한 조직을 이식함으로써 상처치유를 돕고 감염률을 감소시키며, 또한 더 큰 결손부위의 피복이 가능해졌다[16]. 뼈, 인대, 신경 등을 포함한 복합조직재건 또한 자유롭게 작도할 수 있다. 따라서 기능적으로 미용적으로 최적의 결과를 얻기 위해 유리피판술이 여러 재건방법 중 우선적으로 고려해야 한다는 개념에 이르게 된다. 술기의 어려움과 복잡성, 긴 수술 시간에도 불구하고 유리피판술을 이용한 조직재건은 향상된 결과가 나오고 수술 후 합병증이 적으므로 빠른 재활 및 보조치료가 가능하게 한다[15]. 다만, 심각한 질환을 동반하고 있는 환자에게 사용을 제한하여야 하고, 당뇨가 있거나, 흡연자, 스테로이드, 면역억제제(immucosuppressants) 등을 사용하는 환자는 상처치유가 지연될 수 있고 합병증이 발생할 수 있다[17]. 심한 손상으로 혈관손상이 의심되거나, 당뇨로 인한 혈행부전이 있는 경우, 방사선조사를 받은 부위 등에서는 수술 전 컴퓨터단층혈관조영술(computed tomography angiography)를 시행하면 혈관의 주행경로, 문합을 위해 필요한 주변 혈관의 주행과 굵기 등 구제적인 수술계획에 도움을 준다[18].
재건의 시기
유리피판을 이용한 재건에 앞서 괴사조직과 생존 불가능한 조직의 죽은조직제거술(debridement)는 필수적이다. 오염된 상처를 깨끗한 상처로 전환하여 감염의 위험성을 낮추고 손상의 정도를 평가하여 재건의 필요성을 예측하는데 도움을 준다. 초기에 공격적인 죽은조직제거술을 시행하는 것이 고식적인 단계적인 죽은조직제거술보다 빠른 재건을 가능하게 하며 따라서 빠른 기능회복을 가능하게 한다[19]. 조직의 재건은 적절한 죽은조직제거술 또는 종양절제 후 가능하면 빠른 시기에 시행해야 한다. 빠른 조직재건은 일차 상처봉합을 가능하게 하고 중요 구조물이나 인공삽입물재료를 덮을 수 있으며 입원기간을 줄이고 빠른 재활치료를 할 수 있다[14,20]. 그러나 전신적으로 안정되지 못하여 긴 수술을 견딜 수 없는 상태의 환자나 절단이 고려되는 환자는 재건을 지연하는 편이 좋다. 또한 부위에 따라서, 하지의 경우 감염이 조절되고 손상의 정도가 파악될 때까지 음압상처치료(negative pressure wound therapy)를 병행하며 재건을 지연하는 경우가 흔한 반면에[1519], 상지의 경우 고정상태로 지속될 경우 관절의 구축과 인대의 협착, 섬유화 과정이 진행되므로 조기에 수술적 치료를 시행하는 경우가 많다(Figures 1,2) [20].
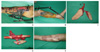
(A) A 49-year-old male patient who was involved in a traffic accident, resulting in large skin defect in the lower leg with uncovered tibia and fibula fracture sites. (B) The infected lower leg was radically debrided and a negative pressure dressing was applied for 2 weeks. (C) A latissimus dorsi chimeric flap was harvested to reconstruct both medial and lateral defects of lower leg. (D) As the second stage operation, fibular flap was harvested for the reconstruction of tibia. (E) Six months after the operation, the extensive lower leg defect was successfully reconstructed.
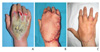
(A) A 48-year-old male had crushing injury of hand, resulting third degree burn involving skin and soft tissue of hand dorsum. (B) Emergent surgery was performed. After radical debridement, anterolateral thigh perforator flap was harvested to reconstruct the defect. (C) Six month after the surgery. Division procedure of fingers was performed.
유리피판의 선택
유리피판의 종류는 그 공여부에 따라 다양하며 유리피판의 선택은 결손의 크기와 필요한 조직의 정도, 기능적 또는 미용적으로 용인될 수 있는 공여부와 수혜부 여건에 따라 선택하게 된다. 성공적인 재건을 위해 재건수술 전 조직결손 부위에서 평가할 사항은 결손의 크기, 주변 조직의 색과 질감, 재건이 필요한 구조물, 가능한 수혜부 혈관, 그리고 감염 여부 등이다[1415]. 이상적인 유리피판은 크고 안정적인 조직 외에도 충분이 크고 긴 혈관경이 필요하다. 이는 손상 범위 밖에서 혈관문합이 가능하도록 하며 혈관문합 중 발생할 수 있는 혈관연축(vascular spasm)이나 혈전 등의 위험성을 최소화할 수 있다. 필요에 따라 정맥 이식편(vein grafts)이나 단측혈관문합술(end-to-side anastomosis) 등을 활용할 수 있다[1921].
근피판(musculocutaneous flap)과 근막피부판(fasciocutaneous flap)은 각각 적응증과 한계점이 있으며 성공적인 재건을 위해 둘 다 활용할 수 있어야 한다. 근피판은 복잡한 삼차원적 결손부위에 사강(dead space)을 채워야 할 경우 이상적이다. 혈행이 풍부한 근육을 이용하여 세균 증식을 조절할 수 있어 오염된 상처나 만성감염 상처(chronic infected wound)에 유용하다[16]. 근막피부판은 얇은 피복이 필요한 경우, 미용적인 윤곽 성형이 필요한 경우 사용되며 인대의 활주면(tendon gliding surface)이나 사지의 관절피복 등에 사용된다.
최근에 소개되어 각광 받고 있는 천공지피판의 경우, 근육을 포함하지 않고 공여부의 희생을 최소화할 수 있으며, 재피복 시 두께를 자유롭게 조절할 수 있고, 감각피판이 가능하고, 결손부에 맞추어 재단할 수 있는 작도의 자유로움이 있으며, 근위혈관(source artery)을 보존할 수 있으며 혈관경 길이를 길게 확보할 수도 있고 피판의 선택이 자유롭다는 장점이 있다[1112]. 과거에는 식도재건에는 유리공장피판술(free jejuna flap)이 가장 적합하며, 혀의 재건에는 전완부 요골동맥피판(radial forearm flap)이 적합하다고 생각하는 등 결손부에 따른 특정한 피판이 우선시 되는 소위 "우선적 선택 피판(flap of choice)"이라는 개념이 존재하였다. 하지만 천공지의 개념이 도입됨에 따라 이런 개념이 점차 변하게 되어 교과서적으로 사용되어 오던 피판이 천공지피판에 의해 많이 대체되고 있다(Figure 3). 대표적인 천공지피판으로 외측 대퇴 회선 동맥(lateral circumflex femoral artery)의 분지를 혈관경으로 하는 전외측 대퇴 천공지피판(anterolateral thigh perforator flap) [2122], 흉배동맥(thoracodorsal artery)을 혈관경으로 하는 흉배동맥 천공지피판(thoracodorsal artery perforator flap) 혹은 광배근 천공지피판(latissimus dorsi perforator flap) [111223], 심하복벽 동맥(deep inferior epigastric artery)을 혈관경으로 하는 심하복벽 천공지동맥피판(deep inferior epigastric artery perforator flap) 등이 있다[2425].

(A) A 73-year-old male patient had suffered hypopharyngeal cancer. (B,C) A 16×8 cm and 7×4 cm lateral thoracic perforator flap was harvested in chimeric pattern for cervical esophageal reconstruction. (D) Customized insetting of tubed lateral thoracic perforator flap and latissimus dorsi skin flap for simultaneous esophageal reconstruction and monitoring flap. (E) Esophagogram showed a good passage in a new conduit of tubed flap after the reconstruction. (F) Postoperative endoscopic view shows successful reconstruction of esophagus. (G) Postoperative view shows successful reconstruction of esophagus and outer resurfacing.
피판의 적용
1. 두경부 재건에의 적용
두경부의 광범위한 결손 또는 복잡한 결손을 재건할 경우, 사용할 수 있는 주변 조직이 부족하므로 유리피판술이 흔히 사용되는 부위이다[16]. 결손이 발생하는 원인으로는 흔히 악성종양 등의 광범위 절제술 후 발생한 결손, 또는 외상이나 화상 반흔 등이 발생한 경우가 있다. 두경부의 경우 매우 얇은 피판에서부터 어느 정도의 두께를 필요로 하는 두피 재건에 이르기까지 다양한 두께를 필요로 한다. 특히 설기저(tongue base), 편도암(tonsil), 인두벽(pharyngeal wall)이나 연구개(soft palate)등의 종양 적출 후에 얇은 두께의 피판으로 재건이 필요한데, 피판이 두꺼운 경우 음식물을 삼키기가 곤란하고, 발음에 있어서도 문제가 될 수 있다. 특히 설암(tong cancer)으로 혀 재건이 필요한 경우는 부위별로 어느 정도의 부피조절이 필요한데, 천공지피판의 경우 결손부에 맞게 부피 및 두께가 자유로이 조절이 된다[11]. 또 두피재건의 경우 기존의 피판들은 너무 두꺼워 외형적으로 좋은 결과를 얻지 못해서 이차적 수술이 필요한 경우가 많으나, 천공지피판을 이용할 경우 주변의 두께에 맞게 자유스럽게 두께를 조절할 수 있으므로, 미적으로 만족할 만한 결과를 얻을 수 있다[21]. 특히 뇌경막(dura)의 결손이 있는 경우 전외측 대퇴부 천공지피판 거상 시 근막을 함께 포함하여 두피의 재피복과 함께 경막의 재건에도 유용하게 이용할 수 있다. 경부의 재피복의 경우에도 적절하게 두께를 조절함으로써 구축 없이 기능적으로, 미용적으로 만족할 만한 결과를 얻을 수 있다[11]. 이처럼 천공지피판은 필요한 부위에 얇은 두께의 피판에서부터 결손부위의 두께에 맞게 부피를 자유롭게 조절하면서 재피복이 가능하다[2122].
악성종양 절제 후 발생한 중안면과 상악의 결손을 재건하는 것은 가장 어렵고 복잡한 재건으로 꼽힌다. 이는 여러 중요 구조물이 인접해 있으며 미용적으로도 만족스러워야 하고, 기능적으로도 우수한 삼차원적 재건이 요구되기 때문이다. 기존 피판의 경우 근육 및 피하조직, 피부판들이 하나로 연결되어 있어, 결손부에 맞게 배치시키는데 어려움이 많다. 하지만, 천공지피판의 경우 천공지를 기저로 근육 및 피하조직 및 피판을 각각 분리시킬 수 있어 조작이 매우 용이하며, 결손부의 접근이나 배치 또한 기존의 피판들보다 유리하다[23]. 상악골 재건(maxilla reconstruction)의 경우 3차원적인 재건을 필요로 하는데, 피부 바깥쪽의 결손 재건, 비내벽의 재건(nasal lining), 구강내벽의 재건(oral lining)과 함께 골재건(bony reconstruction)을 함께 필요로 하는 경우에도 각각의 천공지에 따라 피판을 한 혈관경으로부터 각각 분리하며, 입체적으로 재건이 가능한 장점이 있다. 또한 갈비뼈나 전거근(serratus anterior muscle) 및 피하 지방조직과 같은 다양한 구성요소를 포함시켜서, 마치 재단하듯이 원하는 대로 피판 제작이 가능하다(Figure 4) [222326]. 전외측 대퇴 천공지피판의 경우에서도 근육을 포함하여 사강 충전에 사용이 가능하며, 근피천공지와 격막천공지를 각각 분리하여 두개의 피판을 통해 인두암(pharyngeal cancer)환자의 재건에 사용할 수 있다.
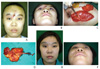
(A,B) A 22-year-old female with depressive deformity of forehead due to frontal sinusitis after traffic accident. (C,D) Intraoperative view of thoracodorsal perforator flap of adipomyofascial component. (E,F) Two years after the surgery. Depressive deformity was successfully reconstructed and the patient was satisfied with aesthetic result. Informed consent was received from the patient.
미세수술을 이용하여 양성 또는 악성 종양 제거 후 발생한 하인두-식도의 결손에서도 천공지피판을 성공적으로 이용할 수 있다. 그 동안 유리 공장 이식술(free jejunal flap)과 전완부 요골동맥피판이 유용하게 이용되어 왔다. 유리 공장 이식술은 점막과 같은 성상으로 자연스러운 재건이 가능하다는 점등의 장점을 지녔지만, 개복수술로 인한 탈장이나 장유착, 분비물로 인해 음성의 질이 떨어지거나 방사선 치료 후 누공이나 협착 등 다른 문제점들이 제기되었다[27]. 이에 반해 전완부 요골동맥피판은 근막피판이 가진 장점 즉, 음성의 질이 우수하며 감각회복이 좋다는 점을 지니고 있다. 하지만 공여부의 이환율이 높아 사용에 제한이 있고 경부식도재건에 부족한 점이 있다[28]. 최근 들어 전외측 천공지피판 또는 흉배동맥 혹은 광배근 천공지피판을 관상 형태로 말아서 하인두 및 식도재건에 적용하여 좋은 결과를 얻었으며, 기존의 유리공장이식술이 가진 낮은 누공율과 전완부 요골동맥피판이 가진 음성의 질이 우수한 장점을 천공지피판을 통해 얻을 수 있었다(Figure 3).
2. 체간 및 유방재건에의 적용
악성종양 제거 후나 외상 등으로 인한 흉벽 또는 복벽의 결손을 재건하기 위하여 국소피판 또는 유리피판이 사용될 수 있다. 복벽결손의 경우 다양한 국소피판술로 대부분의 재건이 가능하며 다양한 근피판을 활용할 수 있다[29]. 그러나 복벽과 흉벽에 걸친 광범위한 결손이나 방사선 조사로 생긴 손상의 경우, 유리피판을 이용하여 넓은 면적과 충분한 연부조직을 제공할 필요가 있다[30]. 흉벽결손 재건을 위해 대흉근피부피판(pectoralis major musculocutaneous flap), 광배근피부피판(latissimusdorsi musculocutaneous flap), 또는 심하복벽천공지 유리피판(deep inferior epigastirc artery perforator flap) 등이 사용될 수 있다[30].
유방암의 재건은 보형물을 이용하는 방법과 자가조직을 이용하는 방법으로 나누어 볼 수 있다. 자가조직을 이용한 유방재건은 자연스러운 모양, 부드러움 및 구축 변형이 없는 장점으로 인해 최근 보형물을 이용한 유방재건에 비해 훨씬 각광받고 있으며, 특히 하복벽의 풍부한 지방조직을 포함하는 횡복직근 피부피판(transverse rectus abdominis muscle flap), 심하복벽 천공지피판(deep inferior epigastric perforator flap)이 대표적인 것으로, 유방 재건과 동시에 늘어진 하복벽의 체형교정을 동시에 할 수 있어 널리 이용되고 있다(Figure 5) [25]. 횡복직근 피부피판의 경우 복직근을 포함하여 피판을 거상하게 되는데, 복직근의 소실로 인해, 술 후 복벽의 약화로 탈장 등의 합병증이 발생할 수 있으며, 근육의 손상으로 수술 후 통증 또한 상당하다. 이런 공여부의 이환을 줄이기 위해 천공지피판의 개념을 이용하여 배꼽 주변의 천공지에 의해 횡복직근을 포함하지 않는 피판으로 유방재건이 시도되었으며, 이는 심하복벽 동맥을 혈관경으로 하며 혈류 역시 기존의 횡복직근 피부피판과 같이 안정적인 것으로 보고되었다. 심하복벽 천공지피판은 유방재건에 있어 좋은 방법이라 할 수 있으며, 특히 공여부의 근육과 신경 희생을 줄일 수 있어, 수술 후 통증이 덜하며, 복벽봉합 또한 용이하고 공여부의 문제를 최소화할 수 있는 장점을 지녔다[25]. 하지만 횡복직근 피판술에 비해 지방괴사의 위험이 다소 높으므로, 술 중에 적어도 2-3개의 믿을만한 천공지를 확보하여 피판을 거상하는 것이 필요하다[24].
3. 사지재건에의 적용
하지의 연부조직 결손을 재건하는 방법은 과거에는 피부이식, 국소피판술, 교차지 피판술 등을 사용하였으나 뼈, 인대 등이 노출되거나 주변 조직손상이 심한 경우, 감염이 심한 경우에는 유리피판술을 사용하게 되고 또한 유리피판술은 한번의 수술로 복합 조직이식이 가능하고 미용적으로도 만족할 만한 결과를 얻을 수 있다는 장점이 있다[1519]. 대부분 하지손상은 외상으로 인한 경우가 많으며 그 외에도 당뇨성궤양, 만성창상, 종양절제 후 결손, 또는 말초혈관병으로 인한 결손이 있다. 대부분 하지손상은 개방성 골절, 뼈와 인대 등 주요 구조물의 노출, 넓은 연부조직 결손 등 광범위한 손상을 초래하는 경우가 많고 이차적 감염 등 상처 관리가 어려워 넓은 피복이 가능한 전외측 대퇴 천공지피판 혹은 광배근 천공지피판 등이 재건에 고려될 수 있다[1519].
족부의 경우 기능적인 면과 미용적인 면의 평가가 이루어져야 한다. 피판의 선택은 체중부하 여부와 연부조직 두께에 따라 결정된다. 체중부하를 받지 않는 족배부는 얇은 피복이 가능한 천공지피판술이 적절하며 체중을 받는 족장부 및 발꿈치는 피판이 내성이 있으며 감각이 있고 피판이 넓어야 하며 혈관이 길어야 한다. 또한 신발 신기에 적당하게 두께도 두껍지 않아야 한다(Figure 6). 과거에는 근육피부피한, 근육피판에 더한 피부이식 등의 방법이 사용되었고, 역시 천공지피판의 도입으로 전외측 대퇴 천공지피판 혹은 광배근 천공지피판 등이 활용되고 있다[1113].

(A) A 27-year-old female had a traffic accident. The car ran over the foot, resulting in skin defect. (B) The pattern of the defect was copied. (C,D) Thin thoracodorsal perforator flap was elevated according to the pattern of the defect for tailored reconstruction. (E,F) Two years after the surgery, the patient was able to wear same size shoes and walk normally.
상지에 발생할 수 있는 손상은 주로 외상으로 인한 것이다[20]. 뼈, 인대, 근육, 연부조직 등이 노출되며 감염되기 쉽고, 기능적 뿐만 아니라 구조적인 재건이 필요하다. 내구성이 있는 연부조직 피복이 필수적이며 피판의 선택은 결손의 크기, 상지에서 위치, 기능 여부에 따라 결정된다. 주요 근육손상이 있는 경우 근전이술이 필요하며 얇은 재피복을 위해서는 천공지피판이 이용될 수 있다[13].
수술 후 관리
미세수술을 이용한 재건 후, 환자는 따뜻한 온도를 유지하고, 충분한 수액을 공급하며, 통증을 조절한다. 항응고제가 주로 사용되며 헤파린(heparin), 아스피린(aspirin), 저분자 헤파린(low-molecular-weight heparin), 혈소판 당단백 IIb/IIIa 억제제(platelet glycoprotein IIb/IIIa inhibitor), 덱스트란(dextran) 등이 의사의 선호도에 따라 사용된다[14].
유리피판술의 가장 중요한 합병증은 혈전(thrombosis)이며 주로 수술 후 3일 내 발생한다. 동맥 또는 정맥의 혈전으로 인해 피판술이 실패하게 되며 완전 피판 손실을 초래할 수 있다. 이러한 혈전을 발견하기 위해 피판의 상태를 평가하기 위한 방법이 연구되어 왔고 임상적으로 많이 사용되고 있다. 대부분의 의사는 아직도 전통적인 임상양상(피판의 온도, 색, 출혈 여부, 울혈)에 의존하고 있다. 그러나 이러한 임상양상은 다소 늦게 나타나는 경향이 있고 피부피판이 포함된 피판에서만 사용할 수 있다[13]. 가장 흔히 사용되는 것은 휴대용 도플러(audible Doppler)가 있으나 정맥혈전을 발견하기에는 부족함이 있다. 매몰식 도플러(implantable Doppler)는 피판경 혈류상태를 정확하게 평가할 수 있으며 파묻힌 피판을 평가하는데 유용하다[1314]. 그럼에도 불구하고 수술 전후 모니터링으로 혈전을 조기에 발견하여 성공률을 높일 수 있다.
결론
미세수술을 이용한 성공적인 연부조직 재건은 단순한 피복뿐 아니라 결손 부위를 기능적, 미용적으로 재건하고 공여부의 결손을 최소화하는 것이라고 할 수 있다. 지속적인 미세수술 분야의 발전과 천공지피판의 도입 등으로 높은 성공률과 세련된 재건이 가능하게 되었다. 다양한 피판의 성격을 이해하고 목적에 따라 자유롭게 재건방법을 선택해서 사용할 수 있다면, 적절한 공여부를 선택하여, 결손 부위에 맞게, 다양한 성분을 포함하여, 작도하듯이 맞춤형 재건이 가능하다. 유리피판술은 재건 분야에 있어 가장 중요한 역할을 할 것이며, 많은 분야에서 있어 더욱 다양하게 적용될 것으로 생각되며, 특히 최근에 성행하는 천공지피판 개념으로 인해 환자에게 더욱 만족스러운 수술 결과를 제공할 수 있게 될 것이다.
Peer Reviewers' Commentary
본 논문은 미세수술을 이용한 재건분야의 최신지견인 천공지 피판에 대한 논문으로서, 미세재건 분야에 많이 이용되어져왔던 근피판, 근막피판 등, 여러피판의 역사적 배경 및 천공지 피판의 탄생까지를 자세하게 기술함으로서 천공지피판에 대한 전반적인 이해에 도움을 주는 논문이다. 더욱이 천공지 피판의 장단점을 기술하고 있고, 피판의 적응증, 재건시기, 피판의 선택, 수술 후 관리에 대해 자세히 기술함으로서 천공지 피판의 전반적인 사항을 다루는 논문이다. 또한, 두경부, 체간 및 유방재건, 사지재건 등의 신체부위별로 피판 적용에 대한 특이점을 기술하여, 재건분야에서 이용되어지는 전반적인 피판에 대해 체계적으로 기술함으로서 피판을 이용한 재건분야의 전반적인 이해를 제시했다는 점에서 의의가 있는 논문이라 판단된다.
[정리: 편집위원회]

