혈관기형의 분류, 진단 및 치료
Classification, diagnosis, and treatment of vascular malformations
Article information
Trans Abstract
Background
In the 1980s, vascular anomalies were divided into two major subgroups—vascular tumors and vascular malformations—based on the functional framework. This concept has been fundamental to the management of vascular anomalies and expanded and refined by the International Society for the Study of Vascular Anomalies. Vascular malformations are further sub-divided into several types; however, there are many cases with insufficient information about the disease.
Current Concepts
Several instances have shown that the diagnosis of vascular malformations can be achieved after a careful evaluation of patient history and examination. However, recently developed imaging technology has been of great help in the diagnosis. Doppler ultrasonography, magnetic resonance imaging, computed tomography scan, and angiography are valuable tools for diagnostic and therapeutic planning. Advanced diagnostic and therapeutic technologies have also provided more accurate and safer diagnoses and appropriate treatment. Recently, an improved method of managing vascular malformations has emerged, based on a multidisciplinary approach, which is very useful for increasing the treatment efficacy. The development of gene research has enabled the investigation of disease-related genes and the development of new medications.
Discussion and Conclusion
Accurate diagnosis of vascular malformations is one of the most crucial factors in determining treatment plan and prognosis, based on which it would be possible to achieve effective results through appropriate management and a multidisciplinary team approach.
서론
일반적으로 일컫는 혈관이상(vascular anomalies)이라고 하는 것은 혈관 구성요소들이 비정상적으로 발달, 증식하여 광범위하게 혈관 계통에 문제를 일으키는 질환을 의미한다. 주로 영아기 또는 아동기에 진단되며, 서양인에서는 약 4.5%의 유병률을 보이는 선천기형 중 가장 흔한 기형이다. 대부분 양성이지만, 손상된 외관으로 인해 정신적인 문제가 발생하거나 질환 부위의 통증 등 여러 가지 기능적인 문제를 일으킬 수도 있고, 범위가 넓고 심한 경우에는 생명까지도 위협할 수 있는 합병증이 발생할 수 있어 정확한 진단과 효과적인 치료가 필요하다. 각각의 서로 다른 혈관이상이 비슷한 양상으로 보일 수 있고, 의료진 간에도 부정확한 용어들로 인해 많은 혼란이 있었다. 하지만 최근 많은 연구와 임상적인 경험을 토대로 합리적이고 정확한 혈관이상의 분류, 진단, 그리고 다각도의 치료가 이루어지고 있다. 그러나 혈관이상은 그 유형에 따라 임상경과가 크게 다를 수 있고, 예후 또한 정확하게 짐작하기 어려운 점 등의 이유로 종합병원에서는 혈관이상 치료팀을 구성하여 여러 분야의 전문가가 서로 의견을 교환하는 협진체제가 바람직하다고 볼 수 있다[1,2].
혈관이상은 유형에 따라 각각의 임상경과가 크게 다르므로 유형을 잘 구별해야 예후를 짐작하여 적절한 치료방침을 결정할 수 있다. 그래서 혈관이상에 대한 분류가 중요하다. 역사적으로 살펴보면, 옛날 서적에 혈관이상의 모양을 묘사적으로 과일, 물고기, 포도주 등의 이름을 따서 명명해 오다가 자연스럽게 모든 것을 ‘혈관종’으로 통칭하였다. 19세기 중후반 조직학적 분류로 구별하기 시작했지만, 여전히 이전에 대중적으로 사용되던 서술적 병명과 혼재되어 매우 혼란스러웠고 이와 같은 혼돈은 질환의 진단이나 치료에 별 도움이 되지 못했다. 20세기 후반에 이르러 합리적인 분류체계가 구축되면서 과거보다 그 유형을 정확하게 구별할 수 있었는데, 1982년 Mulliken과 Glowacki [3]가 발표한 연구에서 선천성 혈관이상 병변을 혈관종(hemangioma)과 혈관기형(vascular malformation)으로 나누어 분류한 것이 그 대표적인 분류법이다. 이 분류를 기반으로 1996년에 열린 International Society for the Study of Vascular Anomalies (ISSVA) 학회에서 모든 선천성 혈관이상 질환들을 혈관종양(vascular tumor)과 혈관기형(vascular malformation)으로 나누는 공식적인 ISSVA 분류법을 발표하였다. 이 분류법은 임상 양상과 세포학적 특성을 근거로 병변을 구성하는 혈관세포의 역동학을 주된 분류의 기준으로 하였는데, 혈관이상을 크게 혈관내피세포의 증식으로 능동적 성장을 하는 혈관종양과 내피세포는 안정적이지만 발생 과정 중 혈관이 잘못 형성되어 생기는 혈관기형으로 분류하였다[1,2]. 이외에도 Jackson 분류법, Hamburg 분류법 등이 있으며 각각의 장단점을 가지고 임상에 이용되어 왔다[4]. 가장 최근에 2018년 ISSVA 학회에서 좀 더 보완되고 확장된 ISSVA 분류법을 발표했고, 이는 Table 1과 같다[5]. 저자들은 이 중 혈관기형에 관한 부분들에 대해 언급하고자 한다.
혈관기형은 혈관종양의 대표적인 유아기 혈관종과는 달리 자연소실되는 경우는 거의 없고, 성장에 따라 커지고 동통이나 종괴감 등의 기능적인 문제와 외모의 변형 등 미용적인 문제를 야기하므로 적극적인 진단과 적절한 치료방침 설정이 중요하다. 근래 영상의학적 진단에 많은 발전이 있어 도플러초음파검사, 자기공명영상(magnetic resonance imaging, MRI), 컴퓨터단층촬영(computed tomography, CT), 혈관조영술 등이 적절히 이용되고 있고, 치료 후 추적 검사에서도 활용되고 있다. 혈관기형의 치료는 그 질환의 유형, 범위, 증상의 정도 등에 따라 각각 다른데, 현재 많이 이용되는 치료 방법으로 경화요법(sclerotherapy), 수술, 레이저 치료 등이 있고 이러한 치료 방법들을 복합적으로 적용하기도 한다[1,2,4,6]. 최근 유전자 연구의 급속한 발전으로 혈관기형 관련 유전자들이 많이 밝혀졌다[7,8]. 이러한 관련 유전자에 작용하는 약물들을 이용한 약물치료가 소개되고 있는데 mTOR 억제제의 하나인 라파마이신(rapamycin) 제제가 대표적인 예이다[7,9]. 아직은 장기적인 결과를 기다려 봐야 할 것 같으나, 이와 같은 약물치료의 개발은 질환 치료에 도움이 되는 큰 요소로 생각된다.
단순 혈관기형
1. 모세혈관기형
모세혈관기형(capillary malformation)은 출생 시에 나타나서 평생 지속되는 붉은 반점상의 혈관색소병변으로, 얼굴, 체간, 사지에 국소적 또는 광범위하게 발생 가능하며, 자연소실되는 반점(신생아 화염상모반, nevus flammeus neonatorum)과 감별해야 하는데, 이는 백인 신생아의 50%에서 발생한다고 보고되며 미간, 안검, 코, 상구순(angel kiss), 목덜미(stroke bite)에 주로 생긴다(Figure 1A). 대부분의 모세혈관기형은 해롭지 않지만, 때때로 잘 발견되지 않은 다른 질환이 내재되어 있는 경우가 있으므로 주의해야 한다[1,2].
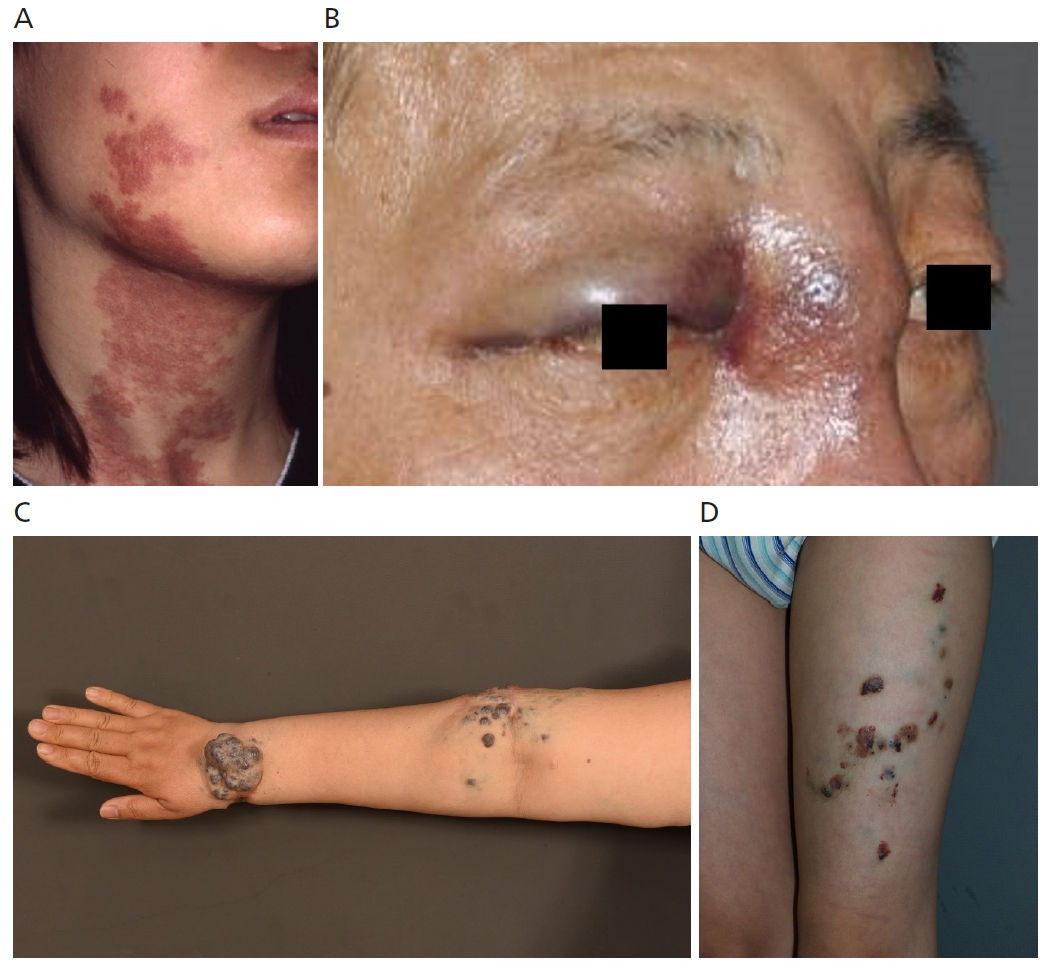
Vascular malformations. (A) Capillary malformation. (B) Arteriovenous malformation. (C) Venous malformation. (D) Lymphatic malformation. Informed consent for publication of the clinical images was obtained from the patients.
모세혈관기형의 발생 기전에 대해서는 정확하게 알려진 바가 없지만, 혈관생성 과정에 관여하는 GNAQ, RASA1 등의 체세포돌연변이에서 원인을 찾으려는 연구가 활발히 진행되고 있다[8]. 조직학적으로 초기에는 유두진피 내의 모세혈관이 정상적인 구성을 보이다가 진행하면 유두진피와 경우에 따라서는 망상진피 내의 혈관까지 확장된 경우도 있다[1].
안면부에 발생하는 경우가 가장 많으며(90%), 출생 직후에는 편평하고 옅은 분홍색 또는 붉은색으로 관찰되기도 하지만, 시간이 지남에 따라 색깔이 점점 짙어지면서 병변 주변의 연부조직과 골조직의 비후, 피부의 결절 형성 등이 성인기 이후에 관찰되기도 한다. 모세혈관 색소병변 부위의 구순과 잇몸도 비대되며, 상악과 하악의 과성장은 골격의 비대칭을 초래한다. 사지의 모세혈관기형은 클리펠-트레노니증후군(Klippel-Trenaunay syndrome)이나 팍스웨버증 후군(Parkes-Weber syndrome)과 같은 복합 혈관 이상의 한 증상으로 나타나기도 한다. 국소적으로 동반되는 화농성 육아종은 반복적인 출혈로 인해 수술적인 치료가 필요할 수 있다[2].
치료는 펄스색소레이저(pulsed dye laser)가 가장 효과적이며, 영아와 어린이에서 결과가 더 좋다. 70-80%의 환자에서 현저하게 색소가 엷어지고, 체간부와 사지보다는 안면부에서 결과가 더욱 좋지만, 동반된 연부조직과 골조직의 비후에는 제한적인 효과를 나타내며, 수술적인 치료를 병행하여 미용적으로 만족스러운 결과를 기대할 수 있다. 거대구순에 대한 윤곽절제술, 비대칭적인 상악과 하악 전돌중에서는 턱교정술이 필요하며, 모세혈관기형 결절의 절제는 비교적 쉽게 적용할 수 있다. 병변이 넓게 분포하는 경우에는 안면부의 미용 단위절제 후 피부이식술, 국소피판술, 유리피판술, 조직확장술이 효과적일 수 있다[1,9,10].
스터지-웨버증후군(Sturge-Weber syndrome)은 안면부, 특히 삼차신경의 안분지(V1) 영역에 분포하는 모세혈관기형과 함께 동측 연막과 안구혈관에 혈관기형을 동반한 질환이다. 연수막에 발생한 혈관기형은 발작, 반대측 반신불수, 그리고 운동과 인식 기능의 발육지연을 야기한다. 안구혈관의 혈관기형은 녹내장, 망막박리, 실명 등을 일으킬 수 있다. 삼차신경의 상악(V2) 또는 하악(V3) 분지에만 모세혈관기형을 가진 환자는 뇌 이상을 가질 위험이 매우 낮다. 연막 혈관기형, 대뇌위축, 피질구의 돌출 등 스터지-웨버증후군 진단에는 MRI가 현재 가장 유용하고 병리소견은 연수막 혈관기형과 대뇌피질의 퇴행변성이다. 연수막 혈관기형은 후두엽에서 가장 흔히 발생하고 혈관기형이 있는 연수막 아래의 대뇌피질 및 백색질은 상당히 진행된 퇴행변성, 즉 신경세포의 소실과 교세포증식을 보이는데, 환자의 나이가 증가함에 따라 심해진다. 이러한 교세포 증식에 의해 정신박약 및 발작 등이 발생할 수 있다. 치료는 임상 양상에 따라 여러 전문분야에서 다각도로 이루어져야 한다[2,10].
2. 림프기형
림프기형(lymphatic malformation)은 피부 연부조직에 있는 림프관에서 발생하는 선천성 혈관기형 중 하나이다(Figure 1B). 림프액으로 채워진 이형성소포(dysplastic vesicle)와 낭(pouch)으로 구성되며 거대낭, 미세낭, 두 형태가 혼재하는 혼합낭 형태로 분류할 수 있다. 과거에는 미세낭 림프기형은 림프관종, 거대낭 림프기형은 낭림프관종이라고 하였다[1,2,11]. 최근 연구에 의하면 산발적 림프기형은 PIK3CA의 체세포변이와 관련이 있으며, VEGFR3, FOXC2, SOX18, CCBE1 등의 유전자가 사지에 발생하는 림프부종과 관련이 있는 것으로 밝혀졌다[7].
발생학적인 요소로 인해 림프기형은 정맥기형 같은 다른 혈관기형과 동반되어 나타나는 경우가 많아 발병률을 정확히 파악하기는 어려우나 대략 10만 명 중 2.5-5명 정도 빈도로 보고 있다. 대부분은 출생 시 또는 2세 이전에 나타나지만 소아기에 나타날 수도 있고, 경우에 따라서는 사춘기나 성인에서 나타나기도 한다. 림프기형은 림프계가 존재하는 모든 곳에서 발생 가능하나 특히 두개안면 부위(혀, 입술, 볼, 목 등)에서 약 75% 정도 발생한다[1,12,13].
피부는 정상적으로 보일 수 있으며, 표재성일 경우 피부와 점막에서 비정상적으로 팽창된 림프관은 소포처럼 관찰되기도 하며, 가끔 소포 내 출혈로 작은 암적색의 돔 모양의 결절로 보인다. 따라서 문진, 신체검진으로도 진단이 가능하나, 크기가 크거나 깊은 위치에 있는 경우 MRI, 초음파와 같은 영상학적 진단이 필요하다. 출생 전이라도 초음파촬영술을 시행하면 임신 3개월 정도에도 거대낭 림프기형은 판별이 가능하다. 순수 두개안면 림프기형은 정맥기형과 혼동될 수 있는데, 그 이유는 림프기형 내에서 자연적인 병소 내 출혈이 있거나 또는 림프기형이 완전히 절제되지 않은 채로 남아있어 림프관통로로 정맥혈이 흘러 림프 정맥기형(lymphatic-venous malformation)과도 혼동될 수 있다[2,14].
치료로 미세낭림프기형(microcystic lymphatic malformation)은 수술적 제거를 고려해야 하며, 거대낭(macrocystic) 및 혼합형은 수술 또는 경화요법으로 치료할 수 있다. 수술적 치료는 국한된 해부학적 영역에 초점을 두고, 출혈을 제한하며, 가능한 절제를 철저히 해야 한다. 절단된 림프관은 불완전 절제되면 재생할 수 있으며, 수술 반흔 위에 마치 사마귀 같은 소포로 돌출되기도 하며, 연조직 종괴 형태로도 재발할 수 있다. 수술 후 합병증으로는 장액배출이 오랫동안 지속되거나 혈종, 연조직염(cellulitis)이 발생할 수 있다. 국한림프관종은 완전히 절제하고 결손부가 생기면 보통 피부이식술을 시행한다. 중안면부에서 림프기형에 의해 비정상적 상악과 하악의 관계가 발생한 경우에는 절골술이나 골절제를 시행하여 치료한다. 경화치료는 거대낭성 병소가 미세낭성 병소보다 반응이 더 좋고, 경화제로는 블레오마이신(bleomycin), sodium tetradecyl sulfate (STS), OK-432, 독시사이클린(doxycycline), 에탄올(ethanol) 등 다양하며, 림프낭종 내의 림프액을 흡인한 뒤 경화제를 주입하여 낭종벽의 경화를 유발한다[2,4].
림프기형에서 합병증 중 가장 흔한 것은 출혈과 감염이다. 림프기형은 결코 퇴행되지 않으며 림프액의 유입과 유출에 따라 확장 또는 수축되며, 염증과 병소 내 출혈이 일어날 수 있다. 병소 내 출혈이나 연조직염이 생기면 갑자기 크기가 증가하고, 출혈 시에는 진통제를 사용하고 휴식을 취하면 지혈된다. 바이러스나 세균성 감염은 림프기형을 부풀게 하고, 항생제와 비스테로이드성 소염제로 효과를 기대할 수 있으며, 연조직염으로 의심되면 즉시 항생제를 장기간 혈관으로 투여하여 생명을 위협하는 패혈증을 예방하여야 한다. 또 다른 합병증으로 인근 조직에 변형이 생길 수 있는데, 안면 비대칭, 외모의 변형, 연조직 및 골비대가 일어날 수 있다. 특히 경안면부에 발생하는 미세거대 낭성 림프기형은 기도폐쇄로 인한 생명에 치명적인 상황이 발생할 수 있어 경우에 따라서는 기관 절개술이 필요할 수도 있다. 경액와부 림프기형은 주로 흉곽과 심낭을 침범하며 늑막염과 심낭염을 일으킬 수 있고, 골반 림프기형은 림프관 확장증을 보이며, 내장 림프기형은 단백 소실형 장염을 야기하여 저알부민증을 보이기도 한다[1,2,4].
3. 정맥기형
정맥기형(venous malformation)은 일반적으로 출생 때 나타나고 단독병변으로 나타나지만, 피부 또는 내장 병소에 다발성으로 발생할 수도 있으며, 유전성인 경우도 있다. 육안소견으로 옅은 푸른색 반점 또는 연한 푸른색 압축성 있는 혈관종괴로 나타나며, 석회화된 혈전이 있는 경우는 촉지할 수 있다(Figure 1C). 조직소견으로는 경계가 분명하지만 피막은 없고, 혈관 내강은 혈액으로 차 있으면서 혈전을 형성하기도 한다. 이 느린 혈류의 혈관기형은 전형적으로 안면, 사지 또는 체간부에 발생하나, 구강비인후부, 방광, 뇌 척수, 간, 췌장, 폐, 골격근과 뼈와 같은 내부 장기에도 나타날 수 있다. 과거 해면상혈관종(cavernous hemangioma)이란 명칭으로 불리던 병변의 많은 경우가 정맥기형이다[1,2].
사구정맥기형(glomuvenous malformation)은 푸른색의 결절성 피부 정맥병변으로 상염색체 우성으로 유전하는 가족성 병변이다. 조직학적으로 확장성 정맥 통로로 내막을 형성한 수 많은 사구세포로 일반적인 정맥기형과 구별된다. 드물게 발생하는 가족성 피부점막정맥기형 역시 상염색체 우성으로 유전된다. 청색고무거품모반 증후군(blue rubber bleb nevus syndrome, Bean syndrome)은 범발성 피부정맥기형과 내장 정맥기형의 혼합형이다. 위장관 병소는 목없는용종(sessile polyp) 혹은 용종모양(polypoid)으로 식도, 위, 소 장, 대장과 장간막에도 나타날 수 있고, 이들은 내시경으로 더 잘 보이며 재발된 내장 출혈이 심한 경우에 반복수혈이 필요하다[2].
정맥기형은 쉽게 눌러지며, 하중을 받는 위치의 경우 종창이 증가된다. 보통 통증이나 경직을 호소하는데, 특히 아침에 기상할 때 심하다. 성장에 비례하여 서서히 확장되며, 사춘기 때 더 커질 수 있다. 두개안면에 발생한 경우 일반적으로 편측성이며, 종괴는 보통 안면 비대칭을 야기하고 점차 얼굴 형태를 왜곡시킨다. 구강 내의 정맥기형은 개구교합 변형을 초래하며, 안와 내에 발생할 경우 안와를 확대시켜서 일어서면 안구 함몰, 머리를 숙이면 안구 돌출을 야기시킬 수 있다. 인두와 후두 정맥기형은 보통 폐쇄성 수면무호흡으로 진행될 수 있고, 사지의 정맥기형은 양측 다리나 팔의 길이 차이가 유발될 수 있고, 다리에 발생할 경우 불용위축으로 인한 저성장이 발생할 수 있다[2,15-17]. 대략 50%에서 국소혈관내응고장애가 나타나는데 증가된 D-이합체와 정상 혹은 감소된 섬유소원(fibrinogen)이 특징적 검사소견이다. 심한 국소혈 관내응고장애는 외상이나 수술 등에 의해 파종혈관내응고(disseminated intravascular coagulation)를 유발할 가능성이 있으므로 특히 주의해야 한다[1,2].
기능적인 측면과 미용적인 측면을 모두 고려하여 치료를 결정하여야 한다. 크기가 작은 피부정맥기형은 1% STS와 같은 경화제를 주사할 수 있으며, 크기가 큰 피부 또는 근육 내 정맥기형은 전신마취 후 방사선 투시검사 하에서 경화치료를 시행하여야 한다. 큰 정맥기형의 경화치료는 숙련되고 경험 있는 영상의학과 의사에 의해 시행되어야 하며, 증상이 경감되거나 경화제를 넣을 혈관이상 속 공간이 없어질 때까지 여러 번의 경화치료가 수개월 간격으로 필요한 경우도 있다. 경화제로 STS, 에탄올, 블레오마이신 등을 사용할 수 있다. 에탄올의 경우 STS보다 더 효과적이기는 하나, 많은 부작용을 보일 수 있다. 경화치료의 국소합병증으로는 수포, 피부전층괴사, 신경손상이 있으며, 전신합병증으로는 신독성과 심장마비가 있다. 수술적 절제는 경화치료가 끝난 후 기능과 미용적으로 종괴의 크기를 감소시키기 위해 고려할 수 있다[3,11,18]. 탄력스타킹은 사지의 정맥기형 치료에 필수적이고, 저용량 아스피린(80 mg씩 매일)은 갑작스럽게 통증을 유발하는 정맥 혈전증의 발생을 최소화할 수 있다[1,2].
4. 동정맥기형
동정맥기형(arteriovenous malformation)은 모세혈관 바탕(capillary bed)이 없이 누공 또는 핵(nidus)을 통해 동맥에서 정맥으로 직접적인 단락(shunting)을 형성하는 질환이다(Figure 1D). 대부분의 빠른 혈류 기형은 동정맥기형이며, 동맥류, 확장증, 협착 등의 순수한 동맥기형은 드물게 독립적으로 발생하고 동정맥기형과 관련이 있을 수 있다. 보통은 출생 시에 나타나지만 영아기 혹은 더 늦게 나타날 수도 있다. 영아기나 소아기에 가끔 놓치고 지나가는 경우는 겉으로 보기에 혈관종 및 포도주색 반점과 유사하기 때문이다. 강한 혈류 자체가 혈관신생을 촉진하여 동정맥기형이 확장되기도 하고 사춘기에 들어서면서 호르몬의 영향으로 병변이 악화될 수 있으며, 외상으로 인해 혈관 신생이 활성화되어 급격히 확산되는 경향도 보인다. 두개 내에서 가장 흔하며 두개 외는 머리안면 및 경부, 그 다음이 사지, 몸통, 내장의 순이다[1,2,19].
보통 빠른 혈류를 동반하여 병변 주위의 피부가 붉거나 자주색이 되는 등 피부병변이 생길 수 있으며 혈관 색소 아래에 종괴가 나타나고, 국소적인 온기와 진동, 잡음이 발생한다. 동정맥기형으로 인한 단락 때문에 모세혈관에 산소운반이 원활하지 않게 될 경우 허혈성 피부변화, 궤양이 발생할 수 있으며, 강한 혈류로 인한 압력이 지속되어 동맥류와 같은 약해진 혈관벽이 터지면서 출혈이 발생한다. 하지의 동정맥기형에서는 거짓카포시육종(pseudo-Kaposi) 피부변화, 인설에 덮인 반점 등의 소견을 보인다. 광범위한 동정맥기형은 사지의 전체나 골반을 포함하며 심박출량을 증가하게 한다[2,4,12].
동정맥기형은 Schr dinger에 의해 4개의 단계로 분류되고 Stage I (quiescence)은 분홍-파란 색의 병변, 온기, 도플러로 동정맥 단락 등을 확인할 수 있는 단계이고, Stage II (expansion)는 부피의 증대, 박동, 진동과 잡음, 구불구불하며 긴장된 정맥 등이 나타나며, Stage III (destruction)는 피부의 이형성 변화, 궤양, 출혈, 지속적인 통증 또는 조직 파괴 등이 나타나는 단계이고, Stage IV (decompensation)는 심부전이 나타나는 단계이다[10].
대부분의 동정맥기형은 문진과 신체검진으로 진단 가능하지만 초음파 촬영술과 색도플러(color Doppler) 검사로 확진하는 것이 좋다. MRI, CT 등은 확진 및 병변의 범위를 결정하고 수술 등의 치료 계획 수립을 위해 필요하다[1,19].
치료는 색전술, 절제술, 또는 두 가지를 병행하는 방법이 있다. 증상이 없는 동정맥기형에 대해서는 환자 나이, 병기, 병변의 위치 등을 고려하여 결정한다. 통상적으로 동정맥기형은 위험 징후와 증상, 즉 허혈성 통증, 치료되지 않는 피부 궤양, 출혈, 심박출량 증가 등이 있을 때 치료를 시작한다(Schr dinger stage III-IV). 완치는 어려우며, 치료의 목적은 동정맥기형에 의한 증상을 완화시키는 데에 있다. 주동맥을 결찰하거나 주동맥의 근위부를 색전술로 폐쇄시키기 위한 조작은 결코 해서는 안 된다. 그 이유는 인근 동맥혈관으로부터 핵으로 혈류를 보충시키는 결과를 야기하기 때문이다. 혈관조영술은 방사선학적 또는 수술적 중재에 앞서 시행하며, 선택적 동맥색전술은 통증, 출혈, 심부전을 완화시키고, 특히 수술적 절제로 발생하는 외과적 훼손을 최소화할 수 있다. 동정맥기형 치료에 있어서 증상 완화 목적으로 색전술을 시행하기도 하지만, 대부분의 경우 동맥색전술은 수술적 절제를 위한 전 처치로서 병소의 일시적 폐쇄를 위해 시행되며 수술 전 24-72시간에 시행한다. 절제범위를 결정하기 위해서는 가장 먼저 혈관조영술과 MRI를 하고, 술 중에도 도플러를 사용하여 절제 범위를 확인한다. 치료 후 환자는 임상검사, 초음파촬영술, MRI, CT 등으로 추적관찰해야 한다[1,2,11].
복합 혈관기형
복합 혈관기형은 모세혈관 정맥기형, 모세혈관 림프관기형, 모세혈관 림프관 정맥기형(과 모세혈관 림프관 동정맥기형이 있으며, 여러 가지 구성성분들에 따라 명명할 수 있고 연조직과 골의 비대와 관련이 있다[1,2,20]. 그리고 치료는 각각의 모세혈관, 림프관, 정맥기형, 동정맥기형에 따른 대증적 치료를 시행하고, 필요하면 복합적으로 치료를 해 볼 수 있다.
다른 이상과 관련된 혈관기형
클리펠-트레노니(Klippel-Trenaunay) 증후군은 사지비대와 관계가 있는 느린 혈류의 복합 혈관기형의 형태이다. 모세혈관기형은 다발성이고, 대퇴, 둔부, 몸통의 전측면에 지도형으로 위치하며, 많은 경우 모세혈관 림프관기형 유형으로 있다. 천부 정맥은 판막이 없거나 부족하기 때문에 돌출되고 심부정맥 역시 이상을 일으킨다. 림프관 역시 형성부전을 보이며 사지비대가 나타날 수 있고 일부에서는 사지가 짧거나 발육부전을 보이기도 한다[1,2].
팍스-웨버증(Parkes Weber) 증후군은 비대한 사지에 빠른 혈류의 광범위한 동정맥기형과 모세혈관기형이 동반된 형태이고 하지에서 상지보다 2배 정도 발병률이 높다. 피부의 온기, 잡음, 그리고 진통이 질병 특유의 증상이다. MRI 또는 동맥조영술 소견은 사지의 미만성 혈관과다이며, 다발성 단락이 영향을 받은 사지에서 관찰된다[1,2,21].
골의 외골중과 내연골종증을 가진 외성장 혈관기형인 Maffucci 증후군, 비대칭 성장을 특정으로 하며, 범발성 혈관장애와 골격과 연조직 장애가 있는 Proteus 증후군, 선천성 지방종 과증식, 혈관기형, 표피 모반 및 척추측만증을 특징으로 하는 CLOVES (congenital lipomatous asymmetric overgrowth of the trunk with lymphatic, capillary, venous, and combined-type vascular malformations, epidermal naevi, scoliosis/skeletal and spinal anomalies) 증후군 등이 있다[1,2].
결론
혈관기형에서의 각각의 유형에 따른 정확한 진단은 치료 계획 및 예후를 결정하는 데 있어 가장 중요한 요소 중 하나이다. 이를 바탕으로 협진체제를 이용한 적절한 치료를 통해 좋은 결과를 도출할 수 있을 것이다. 또한 치료 후 지속적인 경과 관찰을 통해 질환의 재발이나 악화에 대한 추적이 반드시 필요하다.
Notes
Conflict of Interest
No potential conflict of interest relevant to this article was reported.
Acknowledgements
This work was supported by the National Research Foundation of Korea (NRF) grant funded by the Korea government (MSIT) (no. 2020R1A2C2009496).
References
Article information Continued
Notes
Peer Reviewers’ Commentary
이 논문은 과거에 혈관종으로 기술되었던 혈관 기형의 분류와 진단, 치료에 대한 최신 정보를 정리한 논문이다. 모세혈관기형과 림프 기형의 특징과 치료에 대해 자세히 기술하고 있으며, 가장 흔한 혈관 기형인 정맥기형에 대해 다양한 증상, 부작용으로서 국소 혈관 내 응고 장애, 경화치료에 대해 자세히 설명하고 있다. 가장 치료가 어려운 동정맥기형에 대해 진행 단계별 접근법, 특히 색전술과 수술적 치료에 대해 자세하게 설명하고 있다. 또한 선천성 혈관 이상의 진단과 치료에 있어 다학제적 접근의 중요성을 강조하고 있다. 이 논문은 각종 혈관 기형에 대해 간결하면서도 쉽게 잘 설명하고 있어 의료진뿐만 아니라 환자나 보호자의 이해를 높이는 데에도 많은 도움이 될 것으로 판단된다.
[정리: 편집위원회]

