신경병증성 통증 환자의 관리
Management of patients with neuropathic pain
Article information
Trans Abstract
Background
Neuropathic pain diseases commonly treated with pain medicine are postherpetic neuralgia (PHN), diabetic peripheral neuropathy (DPNP), complex regional pain syndrome (CRPS), and chronic pain after spinal surgery. Diagnosis and treatment of these neuropathic pain diseases is an arduous task, and there is a need to improve the understanding of these entities.
Current Concepts
PHN is diagnosed when pain persists for more than 3 months after the healing of herpes zoster rashes, and this disease is commonly encountered in the elderly population. The pathophysiology of DPNP is ischemia of nerve tissue due to microvascular damage. In addition to sensory nerves, DPNP can also result in changes in motor and autonomic nerves. CRPS is a chronic intractable pain disorder, and is classified into types 1 and 2. Type 1 CRPS is diagnosed when there is no evidence of nerve damage while type 2 CRPS shows evidence of nerve damage. However, the signs and symptoms do not differ depending on the type. Chronic pain after spinal surgery is characterized by persistent back pain even after one or more spinal surgeries. This neuropathic pain occurs in the lower back or leg region.
Discussion and Conclusion
The most crucial step in the management of patients with neuropathic pain is to suspect and diagnose if the pain has the characteristics of any pain-related disease. Although the etiology and pathophysiology may differ, the treatment of neuropathic pain remains the same and includes both conservative and interventional approaches. Neuropathic pain diseases often become chronic in nature, and thus, it is important to establish a treatment plan which aims at decreasing pain, improving patient’s functionality and attaining an acceptable quality of life.
서론
신경병증성 통증(neuropathic pain)은 세계통증학회(International Association for the Study of Pain)에 의해 체성감각계(somatosensory system)를 침범하는 병변이나 질환의 직접적인 결과로 발생하는 통증으로 정의된다. 전 세계적으로 6.9-10%의 유병률을 보이는데[1], 이는 일반 인구에서의 유병률이며 질병에 따라 신경병증성 통증은 다양하게 나타나는 것으로 알려져 있다. 암성통증을 호소하는 환자 중에 31.2-43% 정도가 신경병증성 통증을 동반하며[2], 만성 요통 환자 중 33.5% 이상의 환자가 신경병증성 통증의 징후를 보인다고 한다[3]. 같은 질환을 가졌지만 환자들의 통증 양상이 다른 것은 다양한 통증의 형태가 공존하기 때문이며 병태생리에 따라 통증을 침해성 통증(nociceptive pain), 신경병증성 통증으로 나누지만, 한 환자의 통증을 하나의 병태생리만으로 정확하게 정의하는 것은 불가능하다. 특히, 신경병증성 통증은 침해성 통증과 달리 자발통증, 무해자극통증, 통각과민, 감각이상, 불쾌감각 등 통증 양상이 다양하고 같은 원인에 의해 발생할지라도 기전이 다양하여 진단 자체가 어려운 경우가 많다. 신경병증성 통증으로 진단이 되었더라도 통증의 기전이 연구된 만큼 비례하여 치료 방법이 다양하거나 치료 성공률이 높지 않기 때문에 만성적인 통증을 겪을 확률이 높아 임상의에게도, 환자에게도 분명 어려움을 주는 질환이다.
통증의학 분야에서 많이 만나게 되는 대표적인 신경병증성 통증은 말초신경병성 통증에 속하는 대상포진후신경통(postherpetic neuralgia), 당뇨병성 말초신경병증(diabetic peripheral neuropathy)이 있고, 복합부위통증증후군(complex regional pain syndrome)과 척추수술후만성통증 (chronic pain after spinal surgery)은 신경병증성 통증만으로 정의되는 것은 아니지만 신경병증성 통증 질환으로 분류될 수 있다. 각 질환에 대한 이해를 통해 신경병증성 통증 환자의 접근에 대해 논해보고자 한다.
대상포진후신경통
대상포진(herpes zoster)은 수두 바이러스(varicellazoster virus)의 최초 감염 이후 바이러스가 척수후근신경 절이나 삼차신경절에 잠복해 있다가 재활성화되면서 신경 분포를 따라 신체의 편측으로 피부 발진과 함께 통증을 수반하면서 발생하는 질환이다[4]. 대상포진은 적절한 치료를 받을 경우, 일정기간이 경과하면 수포가 치유되면서 피부병변이 사라지고 통증이 감소하게 된다. 그러나 대상포진후신경통(postherpetic neuralgia)은 대상포진에 이환된 후에 발생하는 만성통증으로 정의되고, 수포가 치유되는 30일 이내의 대상포진을 급성 대상포진, 수포 시작 30일부터 90일까지의 통증을 아급성 대상포진 연관통, 수포 시작 후 90일이 경과하여도 통증이 지속되면 대상포진후신경통으로 분류하게 된다. 그러나 아급성 대상포진 연관통 시기부터 신경병증성 통증으로 진단하여, 수포 발생 후 1개월 이상 지속되는 통증을 대상포진후신경통으로 정의하는 것이 일반적이다[5].
기존 연구에 의하면 대략 치료받지 않은 대상포진 환자 4명 중 한 명에서 피부병변이 치유된 이후에도 통증이 지속된다고 보고되고 있다. 그런데 이 비율은 나이가 증가하면서 급격히 증가하여, 40대에서는 약 10%만이 대상포진후신경통으로 발전하는 데 비해, 70대 이상에서는 50% 이상으로 발전한다고 알려져 있다. 이러한 사실로 볼 때 대상포진후신경통으로의 발전과 연관된 요인으로는 고령이 가장 중요한 요인임을 알 수 있다[6]. 고령 이외에도 급성기 통증/발진이 심했던 경우, 안면부에 발생한 경우, 항바이러스제 투여가 72시간 내에 이루어지지 않은 경우가 대상포진후신경통으로 발전될 가능성이 높은 것으로 알려져 있다. 대상포진 발생시 피부 발진 시작 후 72시간 이내에 항바이러스제를 투여하는 것이 중요하며, 이는 바이러스 개체 수를 직접적으로 감소시켜주어 추가적인 신경 파괴를 막을 수 있다는 데 중요성이 있다. 약제 부작용과 대상포진후신경통이라는 난치성 질환의 중요성을 비교해 볼 때, 72시간 이후라도 항바이러스제 제를 투여하는 것이 이점이 있을 것으로 생각된다[7].
대상포진후신경통의 치료는 통증을 경감시키고 이환 부위의 감각을 정상화시켜 일상 생활이 가능하도록 하는 것이 가장 큰 목표이다. 많은 경우에 있어, 우울증이나 불면증 등이 동반되므로 이에 대한 치료를 함께해 주는 것이 필요하다. 대상포진후신경통 치료에 있어 현재 가장 널리 사용하는 경구 약제로는 pregabalin이나 gabapentin 등의 항경련제와 삼환계 항우울제이며, 이들 약제는 신경병증성 통증 질환에 가장 많이 사용된다[8]. 신경병증성 통증의 경우 단순 진통제로는 만족스러운 진통 효과를 기대할 수 없는 경우가 많다. 이와 더불어 말초신경차단술이나 경막외신경차단술 등의 신경차단술을 적용할 경우 손상된 신경을 안정화시켜 통증을 감소시키는 작용을 하여 효과가 크다. 성상신경절 차단술이나 흉부/요부 교감신경차단술 또한 교감신경 매개성 통증에 효과가 좋은 것으로 되어 있으며, 고주파 열응고술 (pulsed/conventional radiofrequency ablation)도 대상포진후신경통에 효과적인 것으로 알려져 있다[9].
당뇨병성 말초신경병증
신경병증성 통증을 유발하는 대사성 원인의 질환 중에 말단에 대칭성 다발 신경병증을 보이는 당뇨병성 말초신경병증(diabetic peripheral neuropathy)이 대표적이다. 대한당뇨병학회에 따르면 입원 중인 제2형 당뇨 환자에서 당뇨병성 말초신경병증의 유병률은 33.5%이며, 당뇨병성 말초신 경병증 환자 중 43.1%가 48시간 이상 지속되는 시각통증등급 4점 이상의 통증성 당뇨병성 말초신경병증을 보이는 것으로 나타났다[10]. 특히 여성, 당뇨병의 이환기간이 길수록, 인슐린 치료를 받고 있는 환자, 미세혈관 합병증과 고혈압이 동반되어 있는 환자에게서 통증성 당뇨병성 말초신경병증 유병률이 높은 것으로 알려져 있다[11].
당뇨병성 말초신경병증의 원인은 당뇨병이 미세혈관 손상을 야기하고 이들 혈관에 의해 혈액 공급을 받는 신경 조직이 손상을 받게 되어 신경 조직의 허혈이 진행되는 것으로 알려져 있다. 혈당조절을 적절히 시행하는 것이 당뇨병성 말초신경병증의 발생을 줄일 수 있다는 것은 일부 맞지만 당뇨병성 말초신경병증의 발생을 완전히 예방할 수는 없다고 알려져 있다. 당뇨병성 말초신경병증은 신경전도이상을 흔하게 보이며 심호흡이나 발살바 요법(Valsalva)에 의한 심박동 저하를 보일 수 있다. 통증은 대개 서서히 시작되고 특히 밤에 심해지며 쑤시거나 화끈거리는 증상과 찌르는 통증을 호소한다. 이는 신경병증성 통증의 양상이며 감각신경 외에도 운동신경과 자율신경의 변화도 초래할 수 있다. 치료는 혈당조절과 영양불량의 해결이 우선적이며, 신경병증성 통증 원칙에 따라 삼환계 항우울제, 항경련제, 세로토닌-에피네프린 재흡수 억제제(serotonin-epinephrine reuptake inhibitor) 등의 적용이 가능하다. 중재적 신경차단술에 대한 의학적 근거는 명확하지 않다[12].
복합부위통증증후군
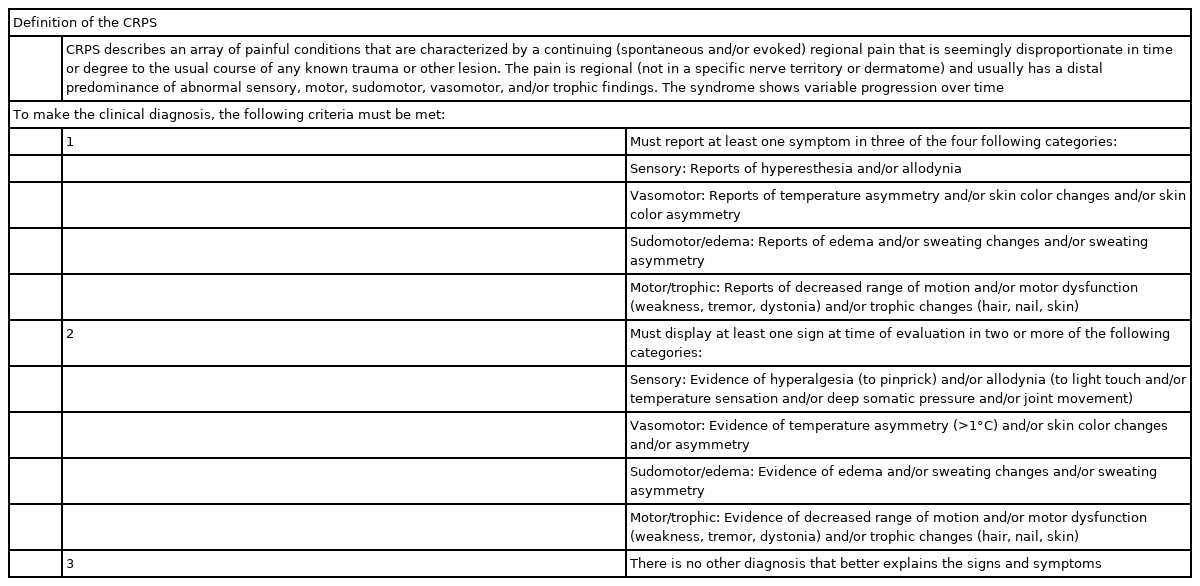
복합부위통증증후군(complex regional pain syndrome, CRPS)은 예전에 반사교감신경이상증(reflex sympathetic dystrophy) 또는 작열통이라고 불리던 질환으로, 1994년 세계통증학회에서 용어를 통일한 이후 현재는 복합부위통증 증후군으로 지칭한다. 우리나라에서는 국가 지정 희귀 난치성 질환으로 분류되어 국가 차원에서 치료를 지원해 주고 있다. 일반적으로 가벼운 외상, 수술, 인대 손상, 부목 고정 이후 발생한다고 알려져 있으나, 약 10% 정도에서는 원인 없이 발생하기도 한다[13]. 주로 사지 원위부에서 발생하는 경우가 많으나 몸의 여러 부위에서도 발생하는 경우가 있고, 환자들은 주로 불에 타는 듯한 통증이나 전기충격과 같은 느낌 등 신경병증성 통증의 양성 증상을 호소하기도 하며, 차가운 느낌이나 먹먹한 느낌과 같이 음성 증상을 경험할 수도 있다. 복합부위통증증후군은 제1형과 2형으로 나뉘며 1형은 신경손상의 증거가 없을 때, 2형은 신경손상의 증거가 있을 때이며, 증상과 징후의 양상은 다르지 않다(Table 1) [14].
크게 네 가지 범주의 증상 및 징후가 나타나게 되는데, (1) 이질통, 통각과민 등의 감각 이상, (2) 부종, 피부 색깔 변화, 피부 온도 변화 등의 혈관 운동 이상, (3) 조갑 및 털의 변화, (4) 운동 범위 감소, 마비 및 진전 등 운동 이상이 바로 그것이다. 진단에 도움이 되는 검사실검사는 단순방사선검사, 적외선 체열 촬영, 핵의학검사(3-phasic bone scan), 근전도 및 신경전도검사(1형과 2형의 구분), 교감신경기능검사 등이 있다[14,15].
복합부위통증증후군의 치료는 통증을 경감시키고 이환 부위의 기능을 정상화시켜 일상 생활이 가능하도록 하는 것이 가장 큰 목표이다. 많은 경우에 있어, 우울증이나 불면증 등이 동반되므로 이에 대한 치료를 함께 해 주는 것이 필요하다. 아직까지 이 질환에 대한 확실한 치료 방법이 정립되어 있지 않으나, (1) 항경련제, 항우울제, 국소 도포제, 아편양 제제, bisphosphonate 등의 약물치료, (2) 경막외차단술이나 교감신경차단술 등의 신경차단술, (3) 물리치료, (4) 척수 자극술 등의 여러 가지 치료를 동시에 시도하는 것이 추천된다. 이 질환의 예후는 진단이 늦어지고 치료가 잘 이루어지지 않을 경우 만성적인 장애로 이어질 수 있어 조기 진단 및 치료가 반드시 필요하다[9,16].
척추수술후만성통증
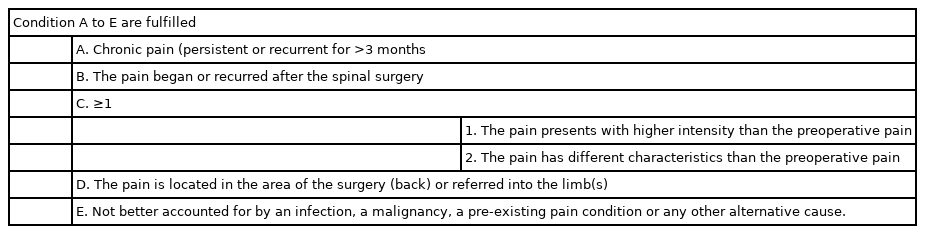
척추수술후만성통증(chronic pain after spinal surgery)의 정의는 1회 이상의 척추수술 이후에도 요통이 지속되고 하지 방사통은 존재하거나 그렇지 않은 상태로 정의된다. 이전에 척추수술실패증후군(failed back surgery syndrome)이라 통용되었는데 질환명에서 드러나는 부정적인 암시로 인해 명칭에 대한 논란이 있어 동시에 여러 명칭을 가진 질환이기도 하다[17]. 수술 실패라는 의미를 암시하지 않는 척추후궁절제술후증후군(post laminectomy syndrome), 척추수술후통증증후군(post spinal surgery syndrome), 요추수술후증후군(post lumbar surgery syndrome) 등의 명칭이 있지만 세계보건기구에서 2018년 6월에 발표한 국제질병분 류(International Classification of Diseases, ICD-11)에 따르면 척추수술후만성통증으로 명명된 것을 알 수 있다. 정의는 수술 후 발생한 만성 요통이나 하지 통증이 3개월 이상 지속되거나 재발한 경우이다. 5가지 진단기준도 함께 제시 하였는데(Table 2) [18], 만성통증이 지속되거나 재발한 경우 3개월 이상일 것, 통증이 척추수술 후 시작하거나 재발한 경우, 수술 전보다 더 높은 강도로 통증이 발생하거나 혹은 수술 전과 다른 양상의 통증이 있을 때, 통증이 수술 부위에 해당하는 등에 있거나 하지 방사통일 때, 감염, 악성 질환, 이전 존재하던 통증, 어떤 다른 원인으로 설명되지 않는 통증이 그것이다[18]. 척추수술후만성통증으로 인해 척추 재수술을 거듭할수록 수술 성공률은 감소하게 된다는 보고는 익히 알려져 있다. Nachemson [19]은 첫 번째 수술 시행 시 50%, 두 번째 수술 시행 시 30%, 세 번째 수술 시행 시 15%, 네 번째 수술 시행 시 5%의 성공률을 보고하였다. 또한, 치료 과정 중에 척추수술이 좀 더 일찍 논의될수록 척추수술후만성통증의 환자수는 증가하였다는 보고들도 있었다[20-22]. 건강보험공단에서 2016년 발표한 주요 수술 통계 연보에 따르면 주요 33개 수술 중, 일반 척추수술 건수는 4 위를 기록하였다. 2016년에 대한민국 인구 10만 명당, 323 명이 일반 척추수술을 시행 받았고, 이는 2011년과 비교 시연평균 1.2% 정도 증가하였다. 또한 총 수술비용이 5,807억 원으로 진료비 상위 7개 수술 중 1위를 차지하였다. 현재 국내 척추수술후요통증후군의 발생률은 정확히 알려진 바 없으나, 이와 같은 일반 척추수술 건수를 감안할 때, 적지 않은 환자가 존재함을 짐작해 볼 수 있다. 또한 척추수술 건수가 증가할수록 척추수술후만성통증의 발생률은 높아질 것으로 예상할 수 있다. 반면에 척추수술의 술기와 장비가 발전하여도 수십 년 전에 비해 척추수술후만성통증의 발생률은 크게 변하지 않았다는 보고도 있는데 결국, 다른 종류의 수술, 각 척추 외과의의 술기, 환자의 소인과 처해있는 임상 상황 등이 이 질환의 발생에 영향을 미친다고 생각된다. 추후 이러한 인자를 포함한 국내 척추수술후만성통증의 발생률에 대한 조사가 필요하다.
척추수술후만성통증의 원인은 단 한 가지로 정의하기 어려우나, 통증 발생의 원인은 여러 가지 요인이 복합적으로 관여한다고 알려져 있다. 척추수술후만성통증의 흔한 원인으로는 경추간공협착(25-29%), 디스크성통증(20-22%), 추간판탈출증의 재발(7-12%), 신경병증성 통증(10%), 후관절증(3%), 천장관절통(2%)이 보고된다[23]. 경추간공협착이나 추간판탈출증의 재발은 기존 질환의 악화나 불완전한 수술의 결과 혹은 수술 주변 구조물의 변화가 원인일 수 있다. 수술 위, 아래의 인접 부위의 역동성 증가로 척추전위증 (spondylolisthesis), 척추협착증 자체가 빠르게 진행되는 경우도 있고[24,25] 이는 척추의 불안정성으로 이어지기도 한다. 수술 후 인접 부위의 질환은 6-27%의 빈도로 발생하며 재수술로 이어지는 흔한 원인이기도 하다[26]. 척추수술후만성통증의 원인 중 하나인 경막외유착(epidural fibrosis)은 경막외 공간에서 척추수술을 시행하게 되면 일어나는 섬유화에서 기인한다. 경막외유착으로 인해 척추수술 후 통증이 발생하는 빈도는 전체 환자 중 20-36%라는 보고가 있다 [27]. 그러나 척추수술 시 불가피하게 거의 모든 환자에게 섬유화가 일어나는데 이 현상이 반드시 통증과 연결되는지, 환자마다 다른 예후를 보이는 이유에 대한 논란이 지속적으로 있어 왔다. 경막외유착 자체가 원인이 되는 것이 아닌, 유착으로 인한 척추 신경의 당김, 허혈, 신경 주변의 영양을 공급해주는 뇌척수액 흐름의 방해가 신경병증성 통증 양상의 직, 간접적인 원인이 된다고 볼 수 있다[27].
증상은 요통 혹은 하지 방사통을 동반하는데 양측 혹은 편측일 수 있으며, 척추 신경의 감각 신경 분절을 따르지 않는 경우가 많다. 척추수술후만성통증의 신경병증성 통증 양상은 영상이나 신경학적 검사에서 그 원인이 발견되지 않는 경우도 매우 흔하다. 또한 신경병증성 통증의 양성 및 음성 증상을 모두 보일 수 있다. 척추수술후만성통증 환자는 하지 방사통만을 혹은 축성통증과 하지 방사통을 함께 호소하는 등 증상이 전형적이지 않고 한 환자에게서 변화하기도 한다. 하지 방사통의 원인은 이학적 검사와 자기공명영 상을 통해 척추 신경이 압박되는 부위를 확인하는 것이 중요하며 추간공 경막외강 신경차단술(transforaminal epidural nerve block)이 진단 및 치료에 도움을 줄 수 있다. 이는 추궁간(interlaminar) 혹은 미추(caudal) 경막외강 신경차단술에 비해 특정 척추 신경에 집중적으로 국소마취제 및 스테로이드 주입을 시행하여 증상 완화 여부를 통해 진단에 도움을 줄 수 있다고 알려져 있다[28,29].
약물치료는 비스테로이드성 항염증제, 삼환계 항우울제, 항경련제 등 신경병증성 통증에 준하는 약물치료를 시도해 볼 수 있으며, 마약성 진통제는 통증과 기능을 개선시키며 소염진통제의 원치 않는 부작용을 줄여준다고 알려져 있으나 추가적인 연구가 필요하고 처방에 주의해야 한다[30]. 중재적 시술법으로 경막외신경차단술, 후지내측지 신경차단술 및 교감신경차단, 경피적 신경성형술 및 유착박리술이 있다. 보존적 요법이나 시술에 효과가 적은 경우 척수자극술을 시도할 수 있다.
결론
신경병증성 통증은 여러 질환에서 비롯되며, 원인이 되는 질환이 다를지라도 같은 기전이나 같은 증상을 보이기도 한다. 이에 신경병증성 통증 환자의 접근에서 가장 중요한 첫 단계는 어떠한 통증 질환이더라도 환자가 보이는 특성 중에 신경병증성 통증이 존재하는지 의심해보는 것이다. 이후, 객관적 검사에서 그 원인이 모두 나타나는 것은 아니지만 진단을 위한 적절한 검사를 시행하고 통증의 원인을 찾아보려는 노력을 기울여야 한다. 원인은 다르더라도 신경병증성 통증의 치료는 가이드 라인에 기반한 약물치료 및 물리치료와 같은 보존적 치료와 중재적 시술이 동시에 이루어지는 경우가 많다. 치료 성공률이 높지 않고 만성화되는 경우가 흔하므로 환자의 통증 감소와 기능 개선을 목표로 구체적인 치료 계획을 세우는 일 역시 중요하다.
Notes
Conflict of Interest
No potential conflict of interest relevant to this article was reported.
References
Peer Reviewers’ Commentary
이 논문은 고령화하고 있는 한국 사회에서 점점 유병률이 높아지고 있는 신경병증성 통증의 기본적인 개념과 대표적인 원인 질환에 관하여 최신 문헌을 정리하여 설명하고 있다. 임상 현장에서 흔히 볼 수 있는 통증 질환의 증상 중에서 신경병증성 통증과 관련된 증상이 무엇이며, 이를 어떻게 진단하고 치료할 수 있는지에 대해 일목요연하게 정리되어 있다. 신경병증성 통증 질환은 다른 통증 질환과는 치료 방법이나 예후에 있어서 차이가 있다. 많은 경우에서는 단순히 진통제만 장기간 사용하여 적절한 치료 시기를 놓치거나, 약제에 의한 이차적인 부작용에 노출되고, 지연된 치료로 인해 경제적 사회적 비용이 예상외로 소모되는 경우가 많다. 따라서, 진료 초기부터 신경병증성 통증에 대한 개념을 갖고 환자에 접근하는 것이 중요하다. 이 논문에서는 임상에서 흔히 볼 수 있는 신경병증성 통증 질환에 관하여 핵심적인 내용을 알기 쉽게 설명하고 있어 통증 환자를 진료하는 임상 현장에 많은 도움이 될 것으로 판단된다.
[정리: 편집위원회]