표적항암치료의 부작용 관리
Management of the adverse effects of targeted therapy for cancer
Article information
Trans Abstract
Background
Advances in genomics and molecular biology over the past 20 years have resulted in numerous approved molecular targeted cancer therapies. The two main approaches for targeted cancer therapy are monoclonal antibodies and small molecules. Targeted therapy is expected to exert few side effects, but a new class of toxicities has been reported. Thus, the classical chemotherapy-induced toxicities of alopecia, myelosuppression, mucositis, nausea, and vomiting have been replaced in patients receiving targeted therapies by dermatologic, cardiovascular, gastrointestinal, endocrine, ocular, and pulmonary toxicities, and infusion reactions.
Current Concepts
Targeted therapy toxicities vary, but common side effects include skin rash, diarrhea, and stomatitis. Most of these side effects are mild and can be prevented and treated. Rare and dangerous side effects, including pneumonitis, cardiotoxicities, and infusion reactions, can also be induced by targeted therapies. In most cases, toxicities are low grade (grade ≤2) and can be treated effectively, but in some cases, they can be fatal without appropriate intervention. Symptoms can be nonspecific, rendering identification of early symptoms challenging. Physicians should thus be aware of these side effects and manage toxicities appropriately.
Discussion and Conclusion
The side effects of targeted therapy exert a critical impact on survival and quality of life. Most patients receiving targeted therapy need help to prevent and relieve toxicities. Management of the toxicities of targeted therapy involves patient monitoring, adjusting therapeutic dose or frequency, and providing supportive care. Serious side effects require early detection and prompt intervention, including discontinuation of targeted therapy and the use of corticosteroids.
서론
2000년대 이후 항암치료에서 많은 종류의 표적치료제(targeted therapy)가 개발되어 사용되고 있다. 표적치료제는 암세포의 성장과 전이에 관여하는 특정 단백질, 혹은 특정 유전자변이를 선택적으로 억제함으로써 치료 효과를 나타낸다. 크게 저분자 인산화효소 저해제(small molecule kinase inhibitor), 단클론항체(monoclonal antibody), 항체약물결합체(antibody-drug conjugate)로 분류할 수 있다.현재 70여 가지가 넘는 저분자 인산화효소 저해제와 10여 가지의 단클론항체가 항암치료에 허가되어 사용되고 있으며, 다양한 표적치료제 지속적으로 개발 중이다[1,2]. 표적치료제는 기존 세포독성 화학요법(cytotoxic chemotherapy)에 비해 구토, 탈모, 호중구감소증 등의 비특이적 독성은 적다. 하지만 암과 정상 조직 간에 신호 전달 경로를 공유하기 때문에 다양한 형태의 특징적인 부작용이 보고된다(Figure 1). 이러한 부작용을 예방 및 완화하면서 치료 효과를 높일 수 있도록 관리법에 대해 알아보고자 한다.
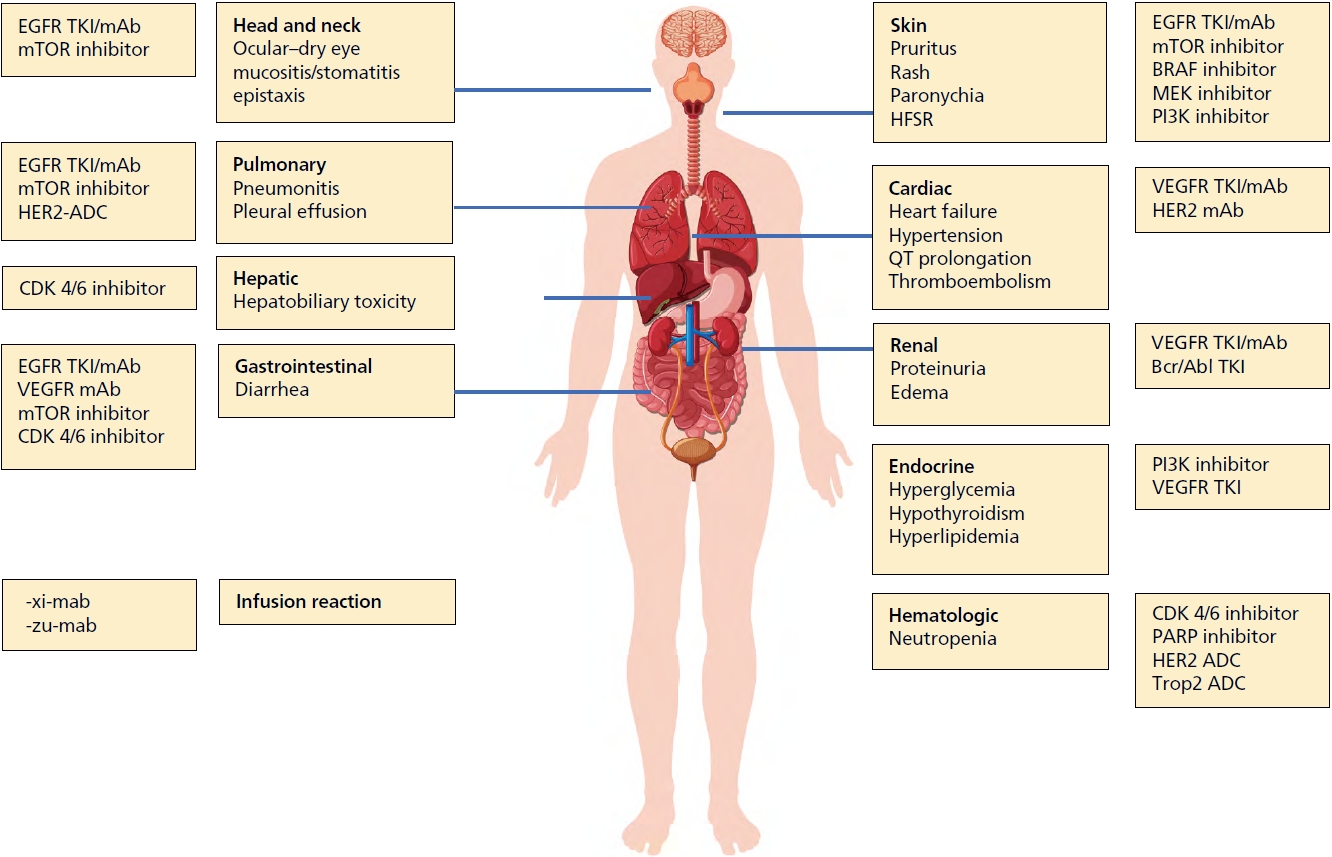
The spectrum of toxicity of targeted therapy by organ. EGFR TKI, epidermal growth factor receptor tyrosine kinase inhibitor; mAb, monoclonal antibody; mTOR, mammalian target of rapamycin; HER2, human epidermal growth factor receptor 2; ADC, antibody-drug conjugate; CDK, cell cycle dependent kinase; VEGFR, vascular endothelial growth factor receptor; PI3K, phosphoinositol 3-kinase; HFSR, had-foot skin reactions; PARP, poly(ADP-ribose) polymerase. Designed by Freepik. 106
피부 부작용
대부분의 피부 부작용은 경증(1등급과 2등급)이지만 외모와 직결되기 때문에 경증이더라도 환자가 느끼는 불편은 상당하다. 피부 부작용은 환자의 75-90%에서 보고되며 대표적인 피부 부작용으로는 구진농포성 발진(60-80%), 가려움증(pruritus), 건조증(xerosis, 4-35%), 손발톱주위염(paronychia)(6-12%), 탈모(5-6%), 수족피부반응(hand foot skin reaction), 구내염 등이 있다[3].
1. 구진농포성 발진(Papulopustular exanthema), 여드름성 발진(Acneiform rash)
Epidermal growth factor receptor (EGFR) 억제제의 흔한 피부 부작용으로 EGFR 단클론항체(예: cetuximab, panitumumab)와 소분자 티로신키나아제 억제제(예: gefitinib, erlotinib, afatinib, dacomitinib, osimertinib, lasertinib, lapatinib)로 치료받은 환자에서 흔히 발생한다[4,5]. EGFR은 악성 세포의 성장, 증식에 관여하며 수많은 고형암에서 과발현되거나 비정상적으로 활성화된다. 하지만 표피, 모낭, 피지선, 손발주위 조직, 결막 상피, 각막 상피, 눈꺼풀 및 눈꺼풀 모낭 등의 정상세포에서도 과발현되기 때문에 피부 부작용은 매우 빈번하게 나타난다[6,7]. 가장 흔하고 특징적인 피부 독성은 구진농포성 발진(여드름형 발진)으로, 치료 시작 후 첫 수일에서 수주 이내에 환자의 75-90% (모든 등급)에서 발생하며 이중 10-20%는 3등급 이상의 발진이 나타난다[6]. 구진농포성 발진은 구진과 농포로 구성된 발진이 치료 시작 1주일 후 얼굴, 두피, 상부 가슴 및 등에서 나타나며 일반적으로 피지선의 밀도가 높은 부위, 주로 얼굴(이마, 코, 뺨)에서 발생하고 가슴과 등 상부로 진행하고 발진의 존재 및 중증도는 치료 반응과 비례한다[5,6,8,9]. 빈도는 덜하지만, EGFR 계열 항-HER2 제제로 치료받은 유방암 환자에서도 이 특유의 구진농포성 발진이 발생한다[10]. 미토겐 활성화 단백질 키나아제 억제제(mitogen activated protein kinase inhibitors (trametinib, binimetinib, cobimetinib)도 환자의 74-85% (모든 등급)에서 구진농포성 발진이 발생하며 5-10%에서 3등급 이상의 발진이 발생한다[11,12]. 예방을 위해서 무알코올성 피부 보습제, 요소함유 보습제(5-10%), 자외선 차단제 사용이 권고된다. 경구용 tetracycline (doxycycline 100 mg 하루 2회 또는 minocycline 100 mg 하루 1회)을 6-8주간 사용하면 2등급 이상의 발진을 낮출 수 있다. 예방적으로 국소 코티코스테로이드(corticosteroid; 예: 하이드로코르티손 2.5% 또는 알클로메타손 0.05%와 같은 낮은 효능의 코티코스테로이드)를 얼굴이나 가슴에 사용해 볼 수 있다[13]. 1등급 및 2등급 구진농포성 발진(여드름양 발진)이 발생한 경우에는 국소 코티코스테로이드를 사용하고, 이미 사용하고 있는 경우에는 역가가 높은 국소 스테로이드를 변경하여 사용한다. 3등급 발진이 발생하면 전신 코티코스테로이드(예: prednisone 0.5-1mg/kg 5-7일)를 투여하고 1등급이 될 때까지 표적치료제의 사용을 중단하고 추후 재투여 시 용량 감량이 필요하다[14]. 감염이 의심되는 경우, 세균 배양을 채취하고 항생제를 투여해야 한다[12]. 추가 치료로 경구 retinoid (즉, acitretin, isotretinoin 20-30 mg/일)를 사용해 볼 수 있다.
2. 건조증, 균열, 가려움증
건조증은 EGFR 억제제를 사용하는 환자의 최대 50%에서 용량 의존적으로 발생한다[15]. 건조함과 피부 취약성은 사지에서 가장 두드러지며 말단 균열(fissure) 및 건성 습진으로 진행될 수 있다[4]. 부드러운 피부 관리와 국소 연화제의 사용이 필요하고 증상이 심한 경우 국소 코티코스테로이드를 사용해 볼 수 있다[4]. EGFR 억제제, vascular endothelial growth factor receptor (VEGFR) 억제제, mTOR, BRAF, c-MET, c-MEK 같은 티로신키나아제 억제제뿐 아니라 rituximab 및 tositumomab 등의 단클론항체가 모두 약물 유발 소양증을 유발할 수 있다[16]. 중증 소양증 발생률 범위는 0.5-1.8% EGFR 억제제로 치료받은 군에서 빈도가 높았다[16,17]. 보습제의 사용, 항히스타민, 항경련제, 삼환계 항우울제의 사용이 가려움증 완화를 유도할 수 있고 심한 경우 전신스테로이드를 일시적으로 고려할 수 있다.
3. 모발 변화
멀티키나아제 억제제를 사용하면 치료 2개월 즈음 모발의 질감, 밀도, 색상 및 성장 패턴 등 다양한 모발 상태의 변화가 시작된다. 모발은 곱슬거리고 끊어지기 쉽고 천천히 자란다. Sorafenib을 사용한 경우 반흥성 탈모 및 비 반흥성 탈모를 유할 수 있고, 국소 minoxidil과 국소 코티코스테로이드로 각각 치료해 볼 수 있다[18]. 속눈썹의 비대 및 컬링이 나타날 수 있으며 안쪽 속눈썹 컬링(eyelash trichomegaly)은 각막염의 위험이 있으므로 속눈썹 트리밍이 권장된다. 이러한 변화는 일시적으로 치료가 종료되면 돌아온다.
4. 점막 합병증
점막염, 구내염, 구강 및 생식기 점막의 아프타 유사 궤양, 외음질염, 귀두염 및 결막염이 발생할 수 있다. 대부분의 점막 증상은 자발적으로 호전된다. mTOR 억제제를 사용하는 경우 구내염(stomatitis)의 발생 빈도가 44%로, 매우 높은 편인데 전통적인 점막염과 달리 각질화되지 않은 상피에 별개의 아프타성 궤양을 형성한다[19]. 구강 통증, 삼킴통, 삼킴 곤란이 발생하여 탈수와 영양실조를 초래할 수 있으므로 덱사메타손 가글, 리도카인 가글을 사용하여 조절해야 한다[20].
5. 손(발)톱 변화
EGFR 저해제를 사용한 경우 손발톱분리증(onycholysis), 손발톱주위염, 화농성 육아종 유사 병변, 색소침착(Beaus’ lines) 등이 관찰된다[21-23]. EGFR 저해제로 치료받은 환자의 17.2%에서 치료 2개월째 손발톱주위염이 발생하고 <2% 정도는 중증으로 진행한다[24]. 미토겐 활성화 단백질 키나아제 억제제(selumetinib, cobimetinib, trametinib) 및 mTOR 억제제(everolimus, temsirolimus)에서도 유사한 손발톱주위염이 나타날 수 있다. 손톱을 너무 짧게 자르지 않고, 국소 피부 연화제를 매일 도포하고, 장갑을 착용하여 반복되는 마찰, 외상, 압력을 피하는 예방적 조치가 필요하다. 손발톱주위염이 발생한 경우 소독 및 항생제 사용이 필요하고 중복 감염을 유의하고 심한 경우 손(발)톱을 제거할 수 있다.
6. 손발피부반응(수족피부반응, 손발바닥각질피부증)
손발피부반응은 치료 시작 후 수일에서 수주 내에 발생하며, 발뒤꿈치나 관절과 같이 압력을 받는 부위에 특징적으로 나타난다. 굳은살 모양의 과다각화증이 나타나고 이후 물집이 발생하게 되면서 악화된다. VEGFR 멀티키나아제 억제제로 치료받은 환자의 35%에서 발생하며, 5-20%에서 3등급 이상의 손발피부반응이 보고된다. Sorafenib (10-62%), cabozantinib (40-60%), sunitinib (10-50%) 또는 regorafenib (47%)으로 치료받은 환자에서 흔히 발생한다[5,8,25]. 손발피부반응의 발생 및 중증도는 치료 반응과 밀접한 관련이 있다[8,10,15]. BRAF 억제제(vemurafenib, dabrafenib, encorafenib)도 손발피부반응이 나타날 수 있으며, 드물게 압박 부위에 수포가 나타난다[4]. 심한 경우 통증을 일으키고 일상적인 기능을 심각하게 저해한다[26]. 완화제, 각질용해제, 국소 코티코스테로이드, 국소마취제, 소독액을 사용하는 것이 권장되며, 중증인 경우 용량을 줄이거나 치료를 중단한다[27]. 예방을 위해서 무알코올 피부 보습제(요소 10%)의 사용과 기계적 스트레스(장갑, 양말/쿠션 신발 없이 긴 산책 또는 무거운 물건 운반) 및 화학적 스트레스(피부 자극제, 용제 또는 소독제)를 피하는 것이 좋다. 요소연화제(요소 10% 크림)는 모든 등급의 수족피부반응 발생률을 유의하게 감소시켰고, 첫 발생까지의 시간을 연장했으며, sorafenib으로 치료받은 환자의 삶의 질을 개선했기 때문에 권장된다[28].
심혈관 부작용
1. 좌심실 기능장애
Trastuzumab은 좌심실 박출률 감소 및 울혈성 심부전 발생의 위험을 각각 7.5%와 1.9% 높인다. Anthracycline을 병용한 경우 그 위험이 증가하여 27%까지 보고된다. Pertuzumab의 병용은 trastuzumab 단독에 비해 심혈관 부작용을 증가시키지 않는다. 심장독성을 예방하는 데 입증된 조치는 없으며 조기 유방암 환자는 3개월마다, 진행성 유방암 환자는 증상이 있는 경우 심장 초음파 혹은 multigated acquisition scan으로 추적이 필요하다.
2. 고혈압
VEGF pathway의 억제제를 사용하는 환자에게 흔히 고혈압이 발생한다[4,29]. 따라서 혈압을 주기적으로 추적하고 고혈압 발생 시 dihydropyridine 계열의 칼슘채널차단제, 안지오텐신전환효소억제제 또는 안지오텐신수용체차단제 등 의 항고혈압제 투여가 권장된다.
3. 출혈
Bevacizumab, sorafenib, sunitinib 등의 VEGF pathway 억제제를 사용하면 최대 16.7% 정도에서 출혈이 발생할 수 있다[30,31]. 대부분 비출혈로 나타나는 점막피부출혈이 빈번하게 나타지만, 중증 출혈이 2.8%에서 발생할 수 있다.
4. 전도이상
Sunitinib, pazopanib, sorafenib, pazopanib, lapatinib nilotinib, dasatinib, vemurafenib, crizotinib, ribociclib 등은 심전도 상 QT prolongation을 유발할 수 있어서 임상의들의 주의를 요한다[32].
5. 혈전색전증
Bevacizumab으로 치료받은 환자의 19%에서 혈전색전증이 발생한다[33].
간질성 폐렴
간질성 폐렴(interstitial pneumonia)은 치료 첫 6개월에 발생하며 빠르면 2개월 이내에 발생하고, 0.1-15%에서 보고된다. mTOR 억제제로 치료받는 환자에서 45%로 빈번하게 보고된다[34]. 최근 허가된 trastuzumab deruxtecan(T-DXd)을 사용한 경우 10-15%에서 간질성 폐렴이 발생하였고 그중 2-5%는 사망에 이를 수 있어 주의를 요한다[35]. 컴퓨터단층촬영 소견은 부분적으로 확산된 간질 유리 혼탁부터 급성 간질성 폐렴(acute interstitial pneumonitis) 및 급성호흡곤란증후군(acute respiratory distress syndrome)과 유사한 간질성 폐질환(interstitial lung disease) 패턴에 이르기까지 다양하다[34,36]. 중증 또는 생명을 위협하는 증상이 있는 환자에서 약물 중단이 필요하고, 코티코스테로이드 사용이 권고된다[36]. 기침과 호흡곤란 등 비특이적 증상이 발생하면, 이러한 부작용이 발생할 수 있음을 인지하고 적절한 조치가 필요하다.
부종
Imatinib, dasatinib으로 치료받는 환자의 16-54%에서 흉막삼출, 부종이 관찰된다[37]. 증상이 심한 경우 용량을 감량하고 부종이 있는 경우 저염식을 권장할 수 있으며, 이뇨제 스테로이드를 사용해 볼 수 있다.
대사/내분비
PI3K inhibitor인 alpelisib을 사용하면 고혈당(모든 등급: 63.7%/3등급 이상: 36.6%)의 발생을 높인다. 따라서 혈당과 당화혈색소를 모니터링 하고 metformin의 투약을 예방적으로 고려해 볼 수 있다. imatinib, sorafenib, sunitinib 사용 시 갑상선기능저하증이 발생할 수 있다[29]. ALK 저해제인 loratinib 사용 시 고콜레스테롤혈증(82.4%), 고중성 지방혈증(60.7%)이 나타날 수 있어 지질 모니터링이 필요하다[38].
설사
CDK 4/6 억제제인 abemaciclib, VEGFR inhibitor인 aflibercept, EGFR tyrosine kinase inhibitor인 afatinib은 각각 86-90%, 58-69%, 87-95%에서 설사가 발생하며, 이중 13-20%, 13-19%, 14-22%는 3등급 이상의 설사를 유발한다[39]. 적절히 조절하지 않으면 생명을 위협하는 탈수를 일으킬 수 있어 수분섭취를 격려하고 loperamide의 사용이 추천된다.
주입반응
Rituximab, Cetuximab, trastuzumab, pertuzumab 심각한 주입반응과 관련이 있다[40]. 첫 투약 시 rituximab의 경우 77%, trastuzuamb의 40%, cetuximab의 경우 15%에서 주입관련반응이 발생한다[41]. 단클론항체 중 -xi-mab은 50% 이상의 인간 서열과 쥐의 서열을 공유하는 키메라단클론항체를 의미하며 따라서 주입반응이 높은 빈도로 나타난다. 또한 -zu-mab은 인간화 항체를 의미하며, 95% 이상이 인간서열로 구성되고 주입반응이 나타날 수 있다. 반면 -u-mab은 100% 인간 서열로 만들어진 항체로 주입반응이 드물게 보고된다. 주입반응을 예방하기 위해 아세트아미노펜과 항히스타민제를 사용한 전처치를 시행한다. 심한 경우 약제 투여를 중단하고 epinephrine (아나필락시스의 경우), 항히스타민제 및 코티코스테로이드를 사용해야 한다[42].
결론
지난 20년간 많은 표적치료제가 개발되어 환자의 생존기간이 혁신적으로 증가하였다. 환자의 삶의 질을 유지하면서 항암치료의 효과를 극대화 하기 위해서는 각각의 고유한 부작용을 이해하고, 부작용의 발생을 감시하며 예방하고 조기 대처하는 것이 매우 중요하다.
Notes
Conflict of Interest
No potential conflict of interest relevant to this article was reported.
Acknowledgements
This work was supported by Chungnam National University Hospital Research Fund, 2018.
References
Peer Reviewers’ Commentary
이 논문은 암 환자의 항암치료에서 항암화학요법으로 대표되던 항암치료의 개념을 뛰어넘어 2000년 이후 본격적으로 상용화된 표적치료제의 독성 및 부작용에 관해 최신문헌을 정리하여 자세히 설명해 주고 있다. 진료를 담당하는 의사나 치료받는 환자의 입장에서는 약제의 효과에 관한 부분에 집중하는 경향이 있어 새로운 약제, 그리고 이름에서 주는 선입견, 자료의 부족 등으로 독성 및 부작용의 측면을 소홀히 하는 경우가 있다. 항암화학요법과는 완전히 다른 형태의 표적치료제의 독성은 약제마다의 다른 작용 원리에 따라 각각 다르게 나타나고 있으며 이에 관한 관리는 환자의 안전뿐 아니라 표적치료제의 효과적인 치료 유지에도 도움을 주어 환자의 생존과도 관련이 있다. 이 논문은 부작용 측면에서 세포독성 화학요법제와 큰 차이를 보이는 표적항암제의 부작용을 설명하고 실질적인 관리 방법을 제시해 주고 있어, 암 환자를 진료하는 임상 현장에 많은 도움이 될 것으로 판단된다.
[정리: 편집위원회]
