비결핵마이코박테리아 폐질환의 진단과 평가
Diagnosis and evaluation of nontuberculous mycobacterial pulmonary disease
Article information
Trans Abstract
Background
Nontuberculous mycobacteria (NTM) represent a broad spectrum of acid-fast bacilli, excluding the pathogens responsible for tuberculosis and leprosy. Over 200 species have been identified and classified as NTM, based on shared phenotypic characteristics. These bacteria are prevalent in diverse environments and are implicated in NTM pulmonary disease (NTM-PD), resulting from interactions between the host, the environment, and the microorganism.
Current Concepts
Diagnosing NTM-PD necessitates a comprehensive approach. It is essential to identify the risk factors, including underlying lung conditions, compromised immune responses, and other host-specific factors. The clinical diagnosis considers pulmonary or systemic symptoms aligned with the disease and the exclusion of alternative pulmonary disorders. Radiological evaluations, such as chest X-rays and computed tomography scans reveal patterns indicative of the disease, including fibrocavitary and nodular bronchiectatic forms. Microbiological criteria are fundamental to the diagnostic process and require a minimum of two positive cultures from separate sputum samples or a single positive result from invasive techniques, such as bronchoscopy or biopsies.
Discussion and Conclusion
As there are multiple phenotypes of NTM-PD, it is necessary to assess the likelihood of the disease in individuals with increased risk factors. A combination of the clinical, radiological, and microbiological criteria is essential for the accurate diagnosis of NTM-PD. Once diagnosed, a thorough assessment is necessary to guide appropriate management decisions.
서론
항산균(acid-fast bacilli)인 마이코박테리아(mycobacteria) 중에서 결핵균 및 나병균을 제외한 모든 균들은 비결핵마이코박테리아(nontuberculous mycobacteria)로 분류된다[1,2]. 200여 종(species) 이상이 확인되었음에도 특정한 표현형(phenotype)을 가지기 때문에 동일한 범주로 분류된다. 비결핵마이코박테리아는 다양한 주변 환경에서 발견되며, 숙주와 환경, 그리고 미생물의 상호작용을 통해 비결핵마이코박테리아 폐질환(nontuberculous mycobacterial pulmonary disease)을 유발할 수 있다[3]. 비결핵마이코박테리아 폐질환은 독특한 임상 및 영상의학적 특징을 보이지만, 질병의 경과 및 예후는 미생물과 숙주 요인에 따라 다르게 나타난다. 이 논문은 비결핵마이코박테리아 폐질환의 위험인자과 진단기준을 중점적으로 검토하며, 진단 후 주요 평가 항목에 대해서도 논하고자 한다.
비결핵마이코박테리아 폐질환의 발병 기전 및 위험인자
비결핵마이코박테리아 폐질환의 발병 위험인자를 파악하려면 비결핵마이코박테리아 폐질환의 발병 기전에 대한 이해가 선행되어야 한다. 이 질환은 미생물, 숙주, 그리고 환경과의 복잡한 상호작용에 기반하여 발생한다[4,5]. 비록 비결핵마이코박테리아라는 카테고리 내에 포함되더라도, 각 균종마다의 발병력(virulence, pathogenicity)이 다르게 나타난다. 예컨대, Mycobacterium kansasii는 높은 발병력을 지닌 균종으로 알려져 있는 반면, Mycobacterium gordonae는 대체로 오염균으로 분류된다[6-8]. 심지어 같은 균종 내에서도 발병력의 차이가 관찰될 수 있다[9,10]. 생물에만 감염되는 결핵균과는 달리 비결핵마이코박테리아는 토양과 자연수와 같은 주위 환경에 광범위하게 분포하고 있는데 이러한 분포 특성은 비결핵마이코박테리아의 독특한 생물학적 특성 때문이다[11]. 균의 표면은 지방이 풍부하여 소수성(hydrophobic)을 띠며, 다양한 표면에 잘 부착하고 바이오필름을 형성한다. 바이오필름은 균으로 하여금 소독제, 항생제, 및 아메바에 대한 저항성을 띠도록 한다. 낮은 산소포화도와 탄소 농도에서도 성장이 가능하며 열 내성이 있어 온수기 및 순환 온수 시스템에서도 생존할 수 있다.
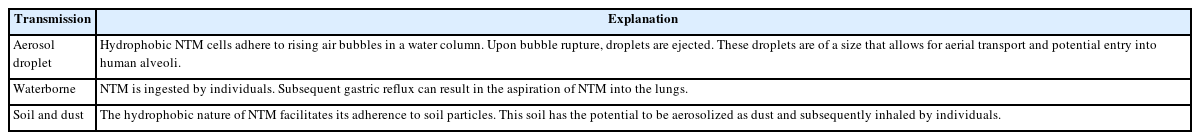
비결핵마이코박테리아는 에어로졸 형태로 폐에 흡입될 수 있다. 미국 메디케어 수혜자를 대상으로 한 과거 연구에서는 높은 일일 증발산과 넓은 표면수 면적을 지닌 지역에서 비결핵마이코박테리아 폐질환의 유병률이 상승하는 경향이 있음을 보고하였다[12]. 에어로졸 형태 외에도, 비결핵마이코박테리아는 액체 내에서 존재하여 섭취 후 위에서 기도로 역류하여 폐로 진입할 수 있다. Mycobacterium avium은 산성 환경에 대한 저항성을 지니며, 최근의 국내 연구에 따르면 위식도역류증을 가진 환자에서 비결핵마이코박테리아 폐질환의 발병률이 상승하는 것으로 나타났다(Table 1) [13].
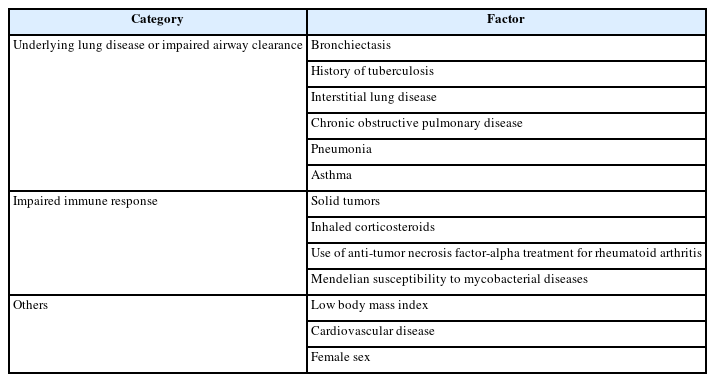
환경적 요인 외에도, 숙주의 특정 요인이 비결핵마이코박테리아 폐질환의 발병에 영향을 미칠 수 있다. 만성 폐쇄성 폐질환, 기관지확장증, 과거 결핵 병력 등의 기저 폐질환을 가진 환자, 특히 기도 청결이 불량한 환자에서 위험도가 상승한다[14]. 기도 청결이 원활하더라도 면역 체계에 이상이 있는 사람의 경우 비결핵마이코박테리아 폐질환 발병 위험이 높다. 특히 체내 인터페론 감마(interferon gamma) 공급의 이상이 있는 mendelian susceptibility to mycobacterial diseases가 있는 경우 파종성 비결핵마이코박테리아 질환을 일으키기도 한다[15]. 이외에도 체질량지수가 낮은 환자에서는 비결핵마이코박테리아 폐질환의 발병률이 상승하는 경향이 있다[16]. 이렇듯 비결핵마이코박테리아 폐질환은 단순히 하나의 요인에 의한 발병이 아닌, 미생물, 환경, 그리고 숙주 간의 복잡한 상호작용에 기반한 질환으로 이해되어야 한다(Table 2).
진단기준
비결핵마이코박테리아 폐질환의 진단은 단일 조건에 의존하는 것이 아닌, 임상적 특징, 영상학적 소견, 그리고 미생물학적 기준의 종합적인 고려를 필요로 한다. 2007년에 미국흉부학회(American Thoracic Society)와 미국감염병학회(Infectious Diseases Society of America)에 의해 확립된 진단기준은 지난 15년 동안 크게 변경되지 않았으며, 현재까지도 광범위하게 적용되고 있다(Table 3) [1,2].
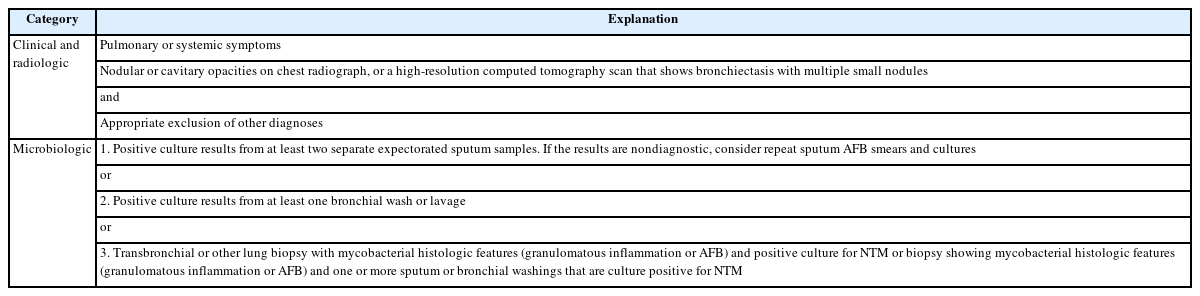
Clinical and microbiologic criteria for the diagnosis of nontuberculous mycobacterial pulmonary disease
1. 임상적 기준
비결핵마이코박테리아 폐질환의 진단을 위해 적합한 임상적 증상의 확인이 필요하며 다른 폐질환의 가능성을 배제해야 한다. 비결핵마이코박테리아 폐질환의 증상은 호흡기 및 전신 증상을 포함하며 대부분 비특이적이다[1]. 특히 만성폐쇄성 폐질환이나 기관지확장증과 같은 기저 폐질환을 가진 환자의 경우, 증상의 원인이 비결핵마이코박테리아 폐질환인지 기저 폐질환에 기인한 것인지 구분하기 어렵다. 기침, 가래, 호흡곤란, 흉통, 객혈 등의 호흡기 증상과, 전신 위약감, 피로감, 체중 감소 등의 전신 증상이 대표적이다. 갈수록 증가하는 비결핵마이코박테리아 폐질환의 유병률을 고려할 때[17], 위와 같은 증상을 호소하는 환자의 경우 비결핵마이코박테리아 폐질환의 가능성을 고려해야 한다.
신체 검진에서도 비결핵마이코박테리아 폐질환에 특이적인 소견을 찾기는 어렵다. 그러나 흉곽의 구조적 이상, 예를 들면 척추측만증이나 오목가슴 같은 소견은 육안으로 확인될 수 있으며, 환자의 체형을 평가하기 위해 체질량지수를 계산해볼 수 있다. 청진음은 기저 폐질환의 종류에 따라 다양한 소견을 보일 수 있다.
2. 영상의학적 기준
비결핵마이코박테리아 폐질환의 진단에서 영상의학적 소견은 중요한 역할을 한다. 하지만 다양한 영상의학 소견을 보이며 다른 폐질환과 공존하는 경우가 많아 초기 진단이 어려울 수 있다[1]. 이러한 경우, 정기적인 추적관찰이 필요하다.
비결핵마이코박테리아 폐질환의 영상의학적 특징은 크게 섬유공동형(fibrocavitary)과 결절 기관지확장증형(nodular bronchiectatic) 두 가지로 구분된다. 일반적인 흉부 X-ray로도 이 질환을 확인할 수 있지만, 섬유공동형이 아닌 경우, 초기 병변은 정상으로 나타날 수 있어 자세한 평가가 어려울 수 있다. 이를 위해 고해상도 흉부 전산화단층촬영(computed tomography, CT)이 필요하다[1,18].
섬유공동형의 주요 특징은 상엽에 위치한 공동과 그 주변의 흉막 비후가 동반되는 것이다. 심한 섬유화가 있는 경우 상엽의 용적 감소와 기관의 전위가 발생하며 흉부 X-ray에서도 확인이 가능하다(Figure 1) [19]. 반면, 결절 기관지확장증형의 경우 흉부 X-ray에서 폐 중하부의 병변이 관찰되며 초기 병변의 경우 확인이 어려운 경우가 많다. 추가로 흉부 CT를 촬영해야 하는 경우가 많으며, 이때는 다병소의 원통형 기관지확장증과 함께 5 mm 이하의 소결절, 소엽중심부 결절(centrilobular nodule), 그리고 나뭇가지발아 모양(tree-inbuds pattern)이 특징적으로 나타난다(Figure 2) [19]. 때로는 섬유공동형과 결절 기관지확장증형이 혼합되어 나타나기도 하며 명확한 구분이 어려운 경우도 있다.
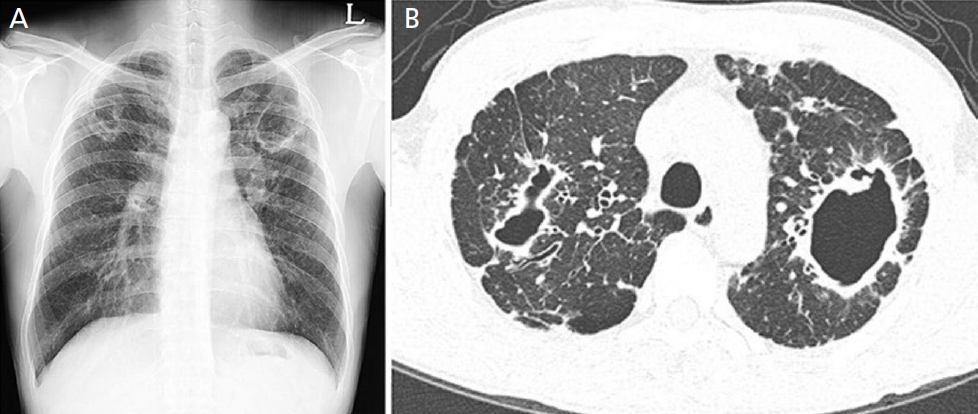
Fibrocavitary form of Mycobacterium kansasii pulmonary disease in a 39-year-old male. (A) Chest radiograph shows thin-walled cavitary lesions in both upper lungs. (B) Chest computed tomography image shows cavitary lesions associated with irregular linear and nodular densities and multifocal low attenuation areas in adjacent areas of the cavitary lesions in both upper lobes. Adapted from Kang EY et al. J Korean Soc Radiol 2021;82:838-850, with permission of Korean Society of Radiology [19].
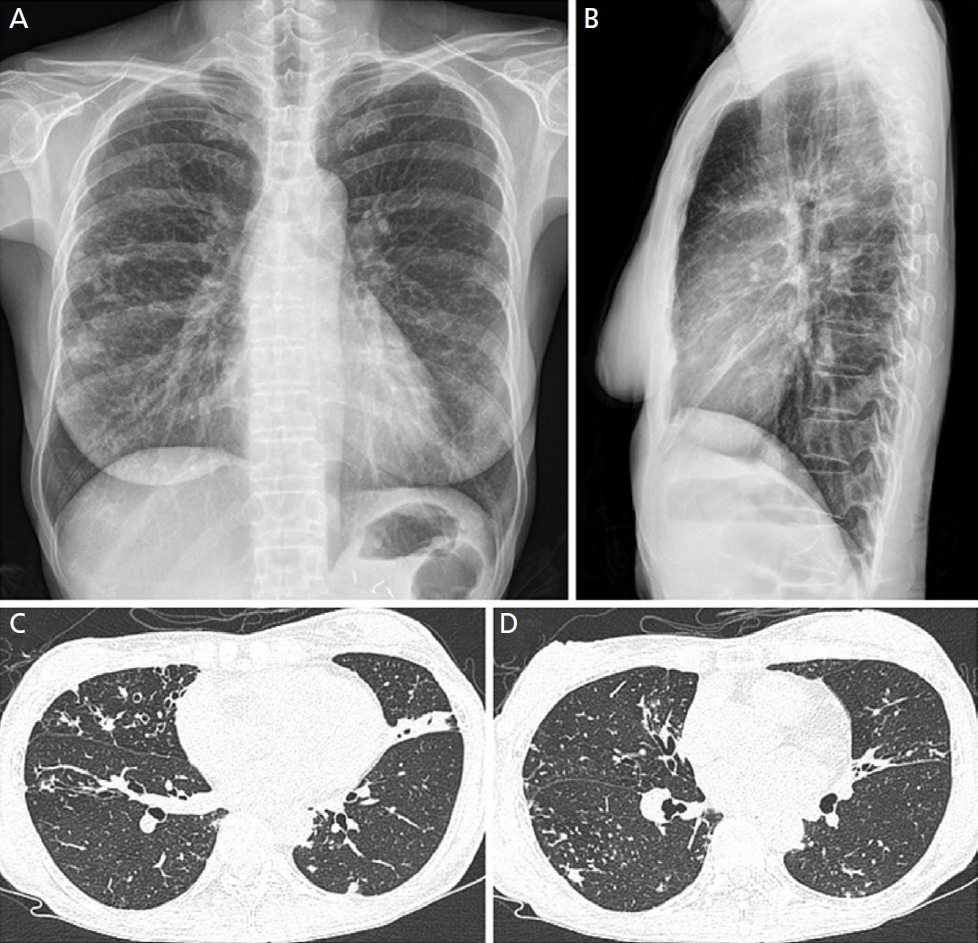
Nodular bronchiectatic form of Mycobacterium avium pulmonary disease in a 58-year-old female. (A, B) Chest posteroanterior and lateral views show small patchy and nodular opacities in the mid to lower lungs, with anterior lung zone dominancy. (C, D) Chest computed tomography images reveal the nodular bronchiectatic form characterized by mild bronchiectasis, small nodules, centrilobular nodules, and branching densities in both lungs, predominantly in the right middle lobe and the lingular segments of the left upper lobe. Adapted from Kang EY et al. J Korean Soc Radiol 2021;82:838-850, with permission of Korean Society of Radiology [19].
처음에는 공동이 없던 환자도 추적관찰을 하면 공동이 발생할 수 있으며[20], 공동의 직경이 클수록 추가 공동이 발생하거나 크기가 더 커질 가능성이 있다[21]. 공동의 부피가 클 경우 객담에서 마이코박테리아 도말 양성이 나오거나 치료가 필요한 경우가 더 많은 반면[22], 직경 2 cm 이하의 공동은 치료 효과나 사망에 영향을 미치지 않는다는 선행 연구들이 있다[23]. 공동 내부를 살펴보면 비결핵마이코박테리아가 바이오필름을 형성하고 있는데[24], 이 바이오필름은 체내의 면역 반응을 방해하고, 항생제의 작용을 어렵게 만든다[25,26]. 따라서, 비결핵마이코박테리아 폐질환 환자의 영상 소견에서 공동의 유무와 크기는 중요한 예후인자로 판단되며, 지속적인 추적관찰이 필요하다.
비록 영상의학적으로 특징적인 소견이 있으나 영상 소견만으로 비결핵마이코박테리아 폐질환을 확진하기엔 그 정확도가 부족하다[27]. 따라서 항상 임상적 및 미생물학적 진단기준을 함께 고려해야 한다.
3. 미생물학적 기준
미생물학적 기준은 비결핵마이코박테리아 폐질환 진단의 필수적인 요소이다. 비결핵마이코박테리아는 주변 환경과 구강 내에서도 발견될 수 있어, 가래 검체에서 최소한 두 번 이상 배양되어야 하고, 두 검체의 원인균이 동일해야 한다[1,2,28]. 이상적으로 1주 간격으로 3회의 독립된 아침 객담 채취가 권장된다[29].
기관지내시경 시행의 적응증은 아직 명확하게 정립되지 않았다. 전문가들은 일반적으로 기관지내시경 검체가 객담 검체보다 균을 민감하게 검출할 수 있고, 주변 환경으로 인한 오염 가능성이 낮다는 공통된 의견을 가지고 있다. 이전 일본에서 2,657명의 환자를 대상으로 한 후향적 연구를 살펴보면, 객담 검사가 음성이더라도 기관지내시경 검사를 통하여 비결핵마이코박테리아 폐질환을 진단한 경우가 199명 중 105명(52.8%)이었다[30]. 그러나 국내 연구에서는 침습적인 방법으로 진단된 환자가 객담으로 진단된 환자에 비해 질병의 진행 위험이 낮거나 비슷하다고 보고되었다[31,32]. 기관지내시경 검사는 검사 자체에 의한 잠재적인 위험과 오염균에 의한 가성 유행의 가능성을 포함하므로[33,34], 장단점을 충분히 고려하여 각 환자에 대한 적절한 판단이 필요하다. 만약 균이 검출되지 않는다면 적절한 진단이 이루어질 때까지 반복적인 미생물 검사와 추적관찰이 필요하다.
배양에서 비결핵마이코박테리아가 동정된 경우, 균 동정 검사 및 약제 감수성 검사를 반드시 시행해야 한다. 균종에 따라 발병력이 다르며, 약제 감수성 결과에 따라 치료 성공률 및 초기 약제 구성이 달라질 수 있기 때문이다. 특히나 M. avium complex나 Mycobacterium abscessus species의 경우에는 clarithromycin과 amikacin에 대한 약제 감수성 검사 결과를, M. kansasii의 경우에는 rifampicin과 clarithromycin에 대한 약제 감수성 결과를 파악해 두어야 한다[35]. 드문 균종이 동정될 경우에는 전문가에게 진료를 의뢰하는 것이 바람직하다.
진단 후 평가 및 추적관찰
진단 후 치료가 권장되지만[2], 일부 환자들에서는 치료 없이도 균의 음전화가 관찰된다[36-38]. 최근의 국내 연구에서는 진단 후 치료 시작 시점과 환자의 사망률과의 관련성이 없다는 결과도 보고되었다[39]. 약물 부작용의 가능성을 고려할 때, 원인이 되는 균종의 발병력, 항생제의 감수성, 예상되는 치료 반응, 환자의 순응도 등을 종합적으로 고려하여 개별적인 치료 접근이 중요하다[40].
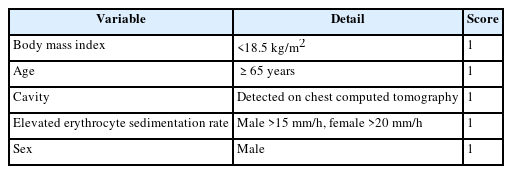
비결핵마이코박테리아 폐질환의 예후와 관련된 여러 인자들이 알려져 있다. 이러한 인자로는 공동의 존재, 남성, 염증 표지자의 상승, 도말 양성, 체질량지수의 저하, 저알부민혈증, 배양 양성까지의 시간, 다른 미생물과의 동시 감염, 기저 질환 등이 포함된다[41-46]. 국내 연구자들이 개발한 Body mass index, Age, Cavity, elevated Erythrocyte sedimentation rate, male Sex (BACES) 점수는 비결핵마이코박테리아 폐질환 환자의 예후를 평가하는 데 유용하고 간단한 도구로 간주되며, 점수에 따라 5년 사망률은 1.2%에서 82.9%까지 다양하게 나타날 수 있다(Table 4) [47-50]. 치료를 즉시 시작하지 않는 경우에도, 환자의 상태 변화를 지속적으로 모니터링하고, 질병의 악화가 예상될 때 적절한 치료를 시작하는 것이 중요하다.
결론
비결핵마이코박테리아 폐질환은 다양한 주변 환경에서 발견되는 미생물로 인한 질환으로, 숙주와 환경, 미생물 간의 상호작용에 의해 발병한다. 이 질환의 진단은 단일 기준에 의존하는 것이 아니라 임상적, 영상의학적, 그리고 미생물학적 기준을 종합적으로 고려하여 이루어진다. 특히, 원인 미생물의 종류를 파악하고 약물에 대한 감수성을 검사하는 것은 진단과 치료과정에서 매우 중요하다. 비결핵마이코박테리아 폐질환은 다양한 임상상과 예후를 보이므로, 초기 평가를 통해 환자의 상태를 정확히 파악하고 개별 환자에 맞는 적절한 대응 방안을 선정하는 것이 필요하다.
Notes
Conflict of Interest
No potential conflict of interest relevant to this article was reported.
References
Peer Reviewers’ Commentary
이 논문은 비결핵마이코박테리아 폐질환의 발병 기전, 위험인자, 진단 기준, 진단 후 평가에 대해 최신문헌을 토대로 체계적으로 정리한 논문이다. 비결핵마이코박테리아는 토양, 자연수 등 주위 환경에 분포하며 증상이 대부분 비특이적이므로 진단 기준과 발병 위험인자에 대한 이해가 중요하다. 이를 위해 바이오필름 형성, 산성 환경에 대한 저항성 등의 미생물 요인으로 인해 기저 폐질환 등의 숙주 요인이 중요하며 에어로졸이나 역류된 위액 흡인 등으로 발병할 수 있다는 기전에 대한 이해가 선행되어야 한다. 또한 진단 후 균 동정 검사, 약제 감수성 검사의 필요성, 예후 평가 항목에 대한 파악도 중요하다. 이 논문은 난해한 비결핵마이코박테리아 폐질환 환자를 진료하는 임상 현장에 많은 도움이 될 것으로 판단된다.
[정리: 편집위원회]