|
 |
- Search
| J Korean Med Assoc > Volume 63(6); 2020 > Article |
|
Abstract
Carotid stenosis is an important etiology of ischemic stroke. Most of the strokes associated with carotid stenosis are caused by artery-to-artery embolism. The risk of embolism highly depends on the stenosis degree and the vulnerability of the carotid plaque. Carotid ultrasonography is useful for evaluating the characteristics of carotid plaque. This review aims to provide information on performing and interpreting the result of carotid ultrasonography and the treatment of carotid artery disease based on the current guidelines. The degree of stenosis can be measured by the diameter reduction and flow velocity criteria. The risk of embolism is highest when the stenosis degree is around 70% to 80%. A heterogeneous echolucent plaque with an irregular surface or an ulcer shows a high risk of embolism. Appropriate treatment is important for the patients with carotid stenosis. In symptomatic patients, a potent antiplatelet treatment, especially during the acute stage, is beneficial. Patients with asymptomatic stenosis over 50% can also be considered for antiplatelet treatments. The associated risk factors should be managed according to the targets. Medically intractable cases or patients with high risk of embolism may receive carotid endarterectomy or carotid artery stenting depending on the concomitant disease and the degree of carotid stenosis. Considering the safety of ultrasound imaging, treatment may be followed-up by carotid ultrasonography.
뇌졸중의 종류에는 뇌혈관이 막히는 허혈뇌졸중과 뇌혈관이 터지는 출혈뇌졸중이 있다. 허혈뇌졸중은 원인에 따라 치료가 달라지는데, 전체 허혈뇌졸중의 40%는 큰 혈관의 죽상동맥경화에 의해 발생하며, 이중 경동맥 협착은 허혈뇌졸중 발생의 주요 원인 중 하나이다[1]. 경동맥 협착으로 인한 대부분의 허혈뇌졸중은 동맥-동맥 간 혈전증에 의해 발생하며 적절한 치료를 통하여 이차 예방이 가능하다. 일부는 혈관 내부에 혈전증을 일으켜 혈관폐색이 일어나기도 하고 협착으로 인한 혈류저하로 뇌졸중이 유발되기도 한다. 최근 건강검진이 늘면서 경동맥 협착이 우연히 발견되는 경우가 늘어나고 있으며, 5-10% 정도의 환자에서 뇌허혈 증상이 없는 무증상 경동맥 협착이 발견된다. 무증상 협착의 경우 뇌허혈 증상을 일으킨 증후성 경동맥 협착과 치료 방침이 다르므로 증상에 대한 주의 깊은 확인이 필요하다. 또한 경동맥 협착은 뇌졸중뿐 아니라, 뇌로 가는 혈류를 만성적으로 감소시켜 뇌 용적을 감소시키고 인지기능 장애를 일으켜 장기적으로는 치매의 위험도 증가시키는 알려져 있다[2].
경동맥질환은 경동맥 초음파를 이용하여 진단할 수 있다. 경동맥 초음파검사는 상대적으로 안전하고 간편하여 협착의 원인을 찾아 치료의 방향을 결정하는 데에 적합하다. 자기공명영상 혈관조영술이나, 전산단층 혈관조영술의 경우 혈관 내강의 협착을 보여주지만, 혈관 벽 자체를 검사하는 데에 한계가 있다. 반면, 초음파의 경우 혈관 벽 자체의 병리를 볼 수 있기 때문에 협착의 원인을 판별하는 데에도 도움을 준다. 뿐만 아니라, 반복적인 검사가 가능하여 경동맥질환의 치료 후 추적검사를 위해 사용할 수 있다. 그러나, 초음파검사의 특성상 검사자에 따라 결과가 달라질 수 있어 정확한 검사법을 숙지하고 이를 바탕으로 올바르게 해석하는 것이 매우 중요하다.
본 종설에서는 경동맥 초음파검사 방법에 대해 알아보고, 내중막두께와 죽상경화반을 정확하게 측정하고 해석하여 임상적으로 적용하는 방법에 대해 알아보고자 한다. 또한 발견된 경동맥질환의 항혈전제 치료, 위험인자 관리 및 시술이나 수술적 치료의 결정에 대해 알아보고자 한다.
경동맥 초음파검사의 통일된 방법은 없으나, 일반적으로 총경동맥, 목동맥갈림, 내경동맥, 외경동맥에서 B-모드(brightness mode)를 이용하여 세로영상, 및 가로영상을 획득한다. 또한 이를 통해 1) 죽상경화반, 2) 잔여내강의 측정과 3) 도플러(Doppler)를 통한 혈류 속도의 측정, 그리고 4) 척추동맥의 B-모드 및 도플러검사를 포함하여 시행한다. 이외에 필요에 따라 색조혈류영상과 파워도플러영상(power Doppler image)을 활용한다.
색조혈류영상의 경우 특히 1) 혈관이 매우 구불구불한 경우, 2) 혈관 내에 저강도에코(hypoechoic) 죽상경화반이 있어 B-모드에서 감별이 어려울 때, 3) 도플러의 입사각을 정확히 하려고 할 때, 그리고 4) 혈관 내에서 혈류속도가 높은 부위를 빨리 찾아내고자 하는 경우 등에 있어 유용하다. 파워도플러의 경우에는 아주 느린 혈류 또는 미약한 혈류를 검사하는데 장점이 있어 폐색 직전의 혈관을 찾아내는데 유용하다[3,4].
경동맥 초음파는 환자와 검사자의 위치에 따라 두 가지 검사방법이 있다. 하나는 검사자가 검사테이블 끝에서 환자의 머리 너머로 앉아 초음파촬영에 양손을 사용하는 방법이다. 이 위치의 장점은 검사자가 양손을 사용하여 초음파 탐침 위치를 다양하게 잡을 수 있다는 것이다. 음파 창을 더 넓게 만들 수 있고, 후측면 투사에서 경동맥을 명확하게 볼 수 있다. 하지만 검사자가 양손 사용에 익숙해야 하므로 검사 숙련도가 요구되고, 더 많은 공간이 필요하다. 따라서, 다른 초음파 검사처럼 환자 옆에서 검사하는 경우가 더 많다. 이 경우 검사자는 양측 경동맥에 모두 오른손을 사용하고, 장비를 쉽게 제어할 수 있는 장점이 있다. 그러나 이 경우에는 환자의 우측 후측면 투사가 조금 어렵다.
경동맥 초음파검사에서 베개는 초음파 창을 나쁘게 만든다. 환자의 얼굴을 검사하는 경동맥 반대편으로 약 45° 돌리면 넓은 시야를 얻을 수 있고, 근육의 수축은 초음파 투과를 약화시키고 탐침 위치를 결정하기 어렵게 하므로 환자의 목은 편안하게 이완되도록 한다. 우선 경동맥을 가로영상으로 관찰하고, 다음으로 세로영상으로 전체적인 모양을 파악한다.
경동맥 초음파 시행 시 종종 문제가 되는 것은 외경동맥과 내경동맥의 구별이다. 내경동맥은 외경동맥에 비하여 직경이 더 크고, 더 깊은 곳에 있으며, 후측면에 위치한다. 또한 내경동맥은 뇌와 같은 저항이 적은 조직에 혈액을 공급하기 때문에 수축기 혈류 속도가 느리고 확장기말혈류속도가 빠른 저저항성 혈류를 보이고, 외경동맥은 이와 반대로 고저 항성 혈류를 보인다. 이외에도 혈관분지의 유무를 파악하고 측두부 얕은관자동맥을 두드려봄으로써 혈류 형태의 변화를 관찰하여 구분할 수 있다(Table 1).
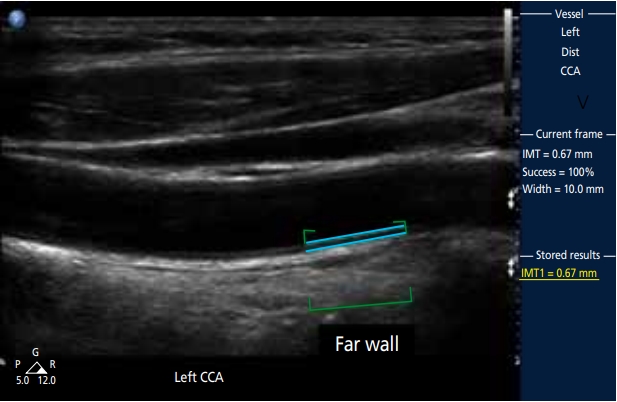
혈관벽은 내막, 중막, 외막의 세 층으로 구성되어 있다. 내중막두께는 B-모드에서 측정하는데, 경동맥의 세로 방향에서 혈관벽을 관찰하면, 동맥 벽을 따라 평행한 두 개의 밝은 경계면이 보인다. 멀리 있는 벽에서, 상부의 밝은 선은 혈액과 내막 사이의 경계이고, 하부의 밝은 선은 내막과 외막 사이의 경계이다. 이 두 선 사이의 거리가 내중막 두께이다. 초음파의 특성상 가까운 벽보다는 먼 벽이 더 선명하게 관찰된다(Figure 1).
내중막두께가 과대 평가되는 것을 최소화하기 위해서는 탐침을 경동맥과 평행하게 하는 것이 좋다. 내중막두께는 원위부 총경동맥에서 분지되기 직전 부위10 mm 길이에서 측정하는데, 총경동맥이 혈관이 크고 표면에 위치하고 있어 내경동맥보다 영상을 얻기 더 쉽고 변이가 많지 않으며 층류가 흘러 국소적 혈류의 영향을 덜 받기 때문이다. 내중막두께는 죽상경화반이 없는 부위에서 세로방향에서 조사하여야 한다. 최근에는 간편하고 정확도가 높은 경계선 추출법을 이용하여 자동 또는 반자동으로 내중막두께를 측정한다[4]. 내중막두께 정상치는 측정 방법과 연령, 인종, 성별에 따라 차이가 있지만 일반적으로 연령과는 관계없이 1.0 mm 이상이면 심근경색이나 뇌혈관질환의 위험이 뚜렷하게 증가된다고 볼 수 있다[5,6].
경동맥의 죽상경화반은 향후 뇌졸중의 발생과 깊은 상관을 가지고 있어 불안정성 죽상경화반을 진단하는 것은 경동맥 초음파 검사의 중요한 과제이다. 일반적으로 죽상경화반은 주위 내중막두께 기준 0.5 mm 또는 50% 이상 동맥내강에 국소적으로 돌출된 경우 또는 내중막두께가 1.5 mm를 넘는 경우로 정의한다[7]. 죽상경화반은 일반적으로 혈관 한쪽으로 치우친 모양이므로 다양한 각도에서 검사를 시행하여야 정확한 측정이 가능하다.
죽상경화반을 기술할 때는 죽상경화반의 위치와 분포, 에코밀도(echogenicity), 석회화와 그림자, 구조, 표면의 모양, 궤양의 존재, 협착의 유무 등을 기술해야 한다(Table 2). 에코밀도는 고강도(hyperechoic or echogenic), 중간 정도(isoechoic), 저강도 에코(hypoechoic or echolucent)로 기술한다. 구조는 에코의 균일성에 따라 균일한 경우와 균일하지 않은 경우로 기술한다. 고강도의 균일한 구조의 죽상경화반은 섬유 성분을 가지고 있어 안정적인 것으로 알려져있다. 반면, 무반향성 영역을 가진 죽상경화반은 조직학적으로 지방질이 풍부하고 괴사조직을 포함하여 불안정한 죽상경화반에 해당한다[8]. 특히 저음영의 균일하지 않은 죽상경화반은 더욱 불안정하여 허혈뇌졸중을 일으킬 위험이 크다고 알려져 있다[8]. 죽상경화반 내에 석회화 부분이 있는 경우, 칼슘이 조직 내의 초음파의 전파를 차단하기 때문에 고음영으로 나타나며, 석회화된 구조의 뒷면으로 에코가 나타나지 않는 음향 그림자가 관찰된다(Figure 2). 죽상경화반 표면은 매끄럽거나 불규칙하거나 궤양이 있는 것으로 설명 할 수 있는데, 궤양의 존재는 불안정한 죽상경화반을 의미하며, 뇌졸중 위험 증가와 연관된다[9]. 최근에는 삼차원 초음파 영상을 이용하여 죽상경화반 부피를 측정하기도 한다[10]. 죽상경화반 부피는 적절한 치료를 하지 않는 경우에는 증가하고 스타틴 등으로 적극적인 치료를 할 경우에는 감소한다[11]. 삼차원 초음파검사는 죽상경화반의 모니터링에 유용한 것으로 생각되며 치료의 평가에도 유용하게 사용할 수 있다[10].
색조혈류(color Doppler) 영상은 혈관의 혈류를 시각화하고 협착 부위를 찾는데 유용한 도구인데, 적절한 색조혈류영상을 얻으려면 적절한 음향 각도가 필수적이다. 선형 탐침을 사용할 경우, 일반적인 초음파 영상을 생성하려면 음파가 피부에 수직이어야 한다. 그러나 색조혈류 영상 초음파에서 적절한 속도 정보를 얻으려면 도플러 입사 각도가 30°-60°사이여야 한다. 60° 이상에서는 도플러가 갖고 있는 물리적 성질 때문에, 각도를 보정하더라도 혈류속도의 왜곡이 발생한다. 경동맥은 깊게 위치한 구조가 아니기 때문에 도플러 탐침의 적절한 각도를 확보하는 것은 쉽지 않다. 이런 경우 탐침의 머리 쪽 또는 발 쪽 모서리를 누르는 방법을 사용하면 탐침 표면과 혈관 사이에 약간의 각도가 생겨서 최적의 도플러 각도를 얻을 수 있다.
색조혈류 영상 초음파 촬영의 목적 중 하나는 혈관에서 협착 부위를 찾는 것인데, 혈관을 지나가는 혈류량은 일정하기때문에, 협착 부위에서 혈류 속도가 가장 빠르다. 혈류 속도눈금은 혈관의 속도에 적합해야 하며 너무 높으면 색조혈류영상의 색이 잘 나타나지 않고, 너무 낮으면 둘러겹침 허상이 발생한다. 정확한 혈류 속도를 측정하기 위해 간헐파 도플러가 필요하다. 간헐파 도플러는 혈관의 중앙 또는 협착부위의 속도를 확인하는데 사용된다. 이 중 최고 수축기 속도가 협착의 정도를 반영한다. 실제 혈류 속도를 측정하려면 각도 보정이 필수적이며 각도 보정은 혈관 벽이 아닌 혈류 방향을 따라야 한다. 혈류 방향은 일반적으로 혈관 방향과 다르지 않지만 한쪽에 치우쳐진 죽상경화반의 경우 혈류방향과 혈관 방향이 다를 수 있기 때문이다.
내경동맥의 유의미한 협착증을 탐지하기 위해 속도 기준이 사용된다(Table 3) [12]. 이 기준에서는 최고 수축기 속도가 중요한데, 내경동맥에서 125 cm/sec 이상의 최고 수축기 속도를 보이는 경우 내경동맥에 50% 이상의 협착증이 있다고 볼 수 있다. 최고 수축기 속도로만 판단이 어려운 경우에는 내경동맥/총경동맥 최고 수축기 속도와 내경동맥의 말기 확장기 속도를 같이 확인한다. 이 두 가지 변수를 추가로 사용하면 다발 병소, 내경동맥 최고 수축기 속도와 시각적 죽상경화반 판독 사이의 불일치, 반대측 총경동맥 혈류속도 상승, 과역동 심장병상태, 저심박출상태 등으로 인해 내경동맥 최고 수축기 속도만으로 협착 정도의 정확한 판단이 어려울때 매우 유용하다. 반대측에 경동맥 협착증이 있는 경우에는 정상 측의 혈류량이 증가로 인하여 심각한 협착증이 없는데도 불구하고 최고 수축기 속도가 상승할 수 있다. 또한 0.7mm 미만의 잔류 직경과 같이 내경동맥에 매우 심한 협착이 있는 경우에는 최고 수축기 속도가 정상 범주를 보이는 거짓정상화(pseudonormalization)될 수도 있다. 따라서 혈관의 협착 정도는 혈류 속도와 지름 감소 정도를 복합적으로 고려하여 판단한다.
경동맥 협착은 해당 경동맥의 혈관영역에서 허혈증상이 발생하였는지 여부에 따라 증후성 경동맥협착 또는 무증상경동맥협착으로 구분한다. 무증상 협착의 경우 증후성 협착에 비해 뇌졸중 발생 위험성은 낮으나 협착 정도에 비례하여 뇌졸중 발생위험도는 증가한다. 무증상 경동맥협착의 정도가 80% 이상으로 진행한 경우에는 그 이하보다 일과성허혈발작 또는 허혈뇌졸중 위험이 약 3배 정도 증가하는 것으로 알려져 있다[13]. 특히 무에코 또는 저에코 죽상경화반이 동반된 경우에는 뇌졸중 발생 위험성이 더욱 높으므로 경동맥내막절제술(carotid endarterectomy, CEA)이나 경동맥 스텐트삽입술(carotid artery stenting, CAS)을 고려할 때 경동맥 초음파가 유용하게 사용될 수 있다. 증후성 경동맥협착과 무증상 경동맥협착의 치료 방침은 다른데 이는 치료 부분에서 다루기로 한다.
경동맥 협착으로 인한 증상으로는 허혈뇌졸중, 일과성 허혈발작, 일과성흑암시, 망막동맥페색, 허혈시신경병증 등이 있다. 경동맥 협착의 정도를 고려할 때, 혈류량이 줄어드는 90% 이상의 심한 협착이나 폐색된 경우에 비해 70-80% 정도의 협착을 보일 때 가장 높은 뇌졸중의 위험을 보인다. 경동맥 초음파는 수술 및 시술결정에 필요한 혈관 협착 정도를 비침습적으로 검사할 수 있으며, 자기공명혈관조영술 및 컴퓨터단층혈관조영술와 비교하였을 때 비슷한 정도의 정확도와 함께 높은 특이도를 보였다[14]. 그러나, 음향 그림자나 거짓정상화 등의 제한점이 있으므로 불필요한 수술이나 시술을 시행할 오류를 최소화하기 위해서는 자기공명혈관조영술 및 컴퓨터단층혈관조영술을 같이 병행하여 시행하는 것이 필요하다[15]. 또한 CAS의 경우 죽상경화반을 제거하지 않고 혈관벽 측면으로 밀어내는 과정이므로 죽상경화반의 표면(매끄러운지, 불규칙한지)과 구조(균질한지, 비균질한지, 출혈동반 여부, 석회화 여부)에 대한 초음파정보를 통하여 시술의 위험성을 평가할 수 있다.
경부동맥박리는 전체 허혈뇌졸중 원인의 약 2%를 차지하지만, 젊은 연령에서는 상대적으로 흔하여 45세 이하에서 발생한 뇌졸중의 약 10-25%를 차지한다. 경부동맥박리는 다양한 원인에 의해서 혈관벽이 손상되고, 맥관벽 혈관이 파열되어 벽내혈종을 통해 협착이 발생하거나, 혈관벽이 약화되어 동맥류처럼 혈관확장이 발생하는 질환이다. 혈관이 자유로운 위치에서 주로 발생하므로 내경동맥박리는 경동맥망울의 2-3 cm 원위부에서 흔하게 발생하고, 척추동맥박리는 V2, V3 위치에서 주로 발생한다[17]. 따라서 대부분의 내경동맥박리와 척추동맥박리는 초음파에서 특징적인 소견을 관찰하기 힘든 위치에서 발생한다. 그러나 초음파에서 동맥박리의 특징적 소견이 관찰되었을 경우에는 진단적 특이도가 높으며, 비침습적으로 시행할 수 있다는 장점이 있다. 가장 흔한 초음파 소견은 해당부위의 혈관협착이며, 경도의 협착부터 완전폐색까지 다양한 정도의 협착을 동반한다. 죽상경화반이 거의 없는 저에코혈관벽이 원위부로 길게 가늘어지며 진행하는 협착 형태로 나타난다. 특징적인 소견인 벽내혈종, 거짓속공간, 내막편, 거짓동맥류가 관찰되면 동맥박리를 명확하게 진단할 수 있다(Figure 3).
타카야수동맥염(Takayasu arteritis)은 대동맥과 대동맥에서 갈라져 나온 주요 동맥을 침범하는 만성 염증성질환으로, 병리소견으로 유아종염증과 혈관내막의 섬유화로 인한 혈관벽 비후와 혈전생성이 특징이다. 초기에는 두통, 어지러움, 발열, 피로감, 체중감소 실신 등 비특이적인 증상이 나타날 수 있어 진단이 어렵다. 또한 초기에는 혈관벽의 변화를 관찰할 수 없어 자기공명혈관조영술이나 컴퓨터단층혈관조영술에서는 위음성이 보일 수 있으므로 경동맥 초음파가 더 민감도가 높다[18]. 특징적 소견인 마카로니 모양의 균질한 등에코성 혈관비후(macaroni sign, homogenous isoechoic circumferential intima-media thickening)를 보이면 진단할 수 있다(Figure 4).
경동맥 초음파를 통하여 내중막두께와 죽상경화반을 측정하는 것은 심뇌혈관질환 위험도를 평가하는 중요한 방법이다. 무증상 환자의 경동맥 내중막두께는 심근경색, 뇌졸중 및 심혈관질환에 의한 사망과 유의한 연관성을 보였으며, 이는 고혈압, 당뇨병과 같은 다른 위험인자와는 독립적인 연관관계이다[19]. 따라서 내중막두께는 심혈관질환의 표지자로 사용되고 있으며, 중등도의 심혈관질환 위험도를 가진 무증상 성인에서 심혈관질환 위험도를 평가할 때 관상동맥칼슘 지수(coronary calcium score)와 함께 경동맥 내중막두께를 평가하는 것이 권고된다[20]. 또한 내중막두께는 고령, 흡연, 고혈압, 당뇨병, 이상지질혈증이 있는 경우 점차 증가하고, 이러한 위험인자를 잘 조절할 경우 내중막두께의 진행을 억제할 수 있다. 다만, 뇌졸중 환자들을 제외한 일반인구집단에서는 내중막두께의 진행을 억제하는 것이 향후 발생하는 심뇌혈관질환을 줄일 수 있는지에 대해서는 불확실한 상태이다[21,22]. 이미 알려진 죽상경화성혈관질환이 있거나, 검사결과가 치료에 영향을 미치지 않을 때는 임상적으로 도움이 되지 않으며, 주기적인 추적관찰검사는 추천하지 않는다[4].
내중막두께뿐만 아니라 경동맥 죽상경화반도 심혈관질환의 예측, 예후인자임은 잘 알려져 있다. 여러 메타분석 결과 경동맥 죽상경화반은 내중막두께에 비해 향후 심근경색을 예측하는데 더 높은 진단 정확성을 보여주었다[23].
경동맥 동맥경화에 대한 치료는 크게 항혈소판 치료를 포함한 약물치료, 동반된 혈관위험인자의 관리, 그리고 CEA 혹은 CAS와 같은 혈관재건술이 있다. 경동맥 협착에 대한 치료방향을 결정할 때 여러 가지 고려해야 할 요소 중 가장 중요한 요소는 증상의 유무와 경동맥 협착의 정도이며, 대부분의 진료지침이 이 두 가지를 기본으로 치료방침을 결정하도록 권장하고 있다[24,25].
무증상 경동맥 협착의 경우 50% 이상의 경동맥 협착이 있는 경우 금기사항이 없는 한 항혈소판제 치료가 권장된다. 경동맥 협착이 50% 미만인 환자에서의 항혈소판제 치료는 동반된 위험인자와 출혈 부작용 위험을 고려하여 결정하는 것이 바람직하다. 가장 대표적인 항혈소판제인 아스피린은 심뇌혈관질환의 일차예방 약물로 잘 알려져 있다. 하지만, 최근 아스피린의 일차 예방 효과를 살펴본 연구들이 모두 실패함에 따라 일차 예방을 위한 일률적인 아스피린의 사용에는 주의할 필요가 있다. 따라서, 심뇌혈관질환 발생 고위험군으로 주요 출혈부작용 발생위험에 비해 아스피린 예방효과의 이득이 높을 것으로 판단하는 경우에 한해 항혈소판제 치료를 고려해야 한다. 이를 판단하기 위해 나이, 성별, 흡연, 고지혈증, 혈압 등의 요소를 고려한 10년 심뇌혈관질환 위험도를 계산해야 하며, 그 위험도가 20% 이상인 경우 심뇌혈관질환 발생 고위험군으로 고려할 수 있다. 또한 경동맥 초음파를 통해 죽상경화반의 형상을 보고 색전의 위험이 높은 경우 항혈소판제 사용으로 인한 출혈 위험이 높지 않다면 저용량 아스피린(100 mg, 1일 1회)의 사용을 고려할 수 있겠다.
증후성 경동맥 협착증 환자의 경우에는 50% 미만의 경도의 협착 환자에게도 내과적인 치료가 권장된다. 허혈뇌졸중 이차 예방을 위해 하루 100-300 mg 사이의 아스피린을 사용할 수 있다. 최근 POINT (Platelet-Oriented Inhibition in New TIA and Minor Ischemic Stroke) trial [26]과 CHANCE (Clopidogrel in High-Risk Patients with Acute Non-disabling Cerebrovascular Events) trial [27]의 연구결과들은 급성 허혈뇌졸중 환자들을 대상으로 허혈뇌졸중 발생 후 첫 90일동안 아스피린과 클로피도그렐 복합 사용시, 아스피린 단독에 비해 허혈뇌졸중 재발 위험이 낮아, 허혈뇌졸중 급성기의 경우 항혈소판제 복합 사용이 허혈뇌졸중 재발 예방에 더 효과적이다. 또한, 50% 이상의 증후성 경동맥 협착증 환자를 대상으로 초음파를 사용해 미세 색전 신호를 모니터링 한 CARESS (Clopidogrel and Aspirin for Reduction of Emboli in Symptomatic Carotid Stenosis)trial [28]에서 아스피린과 클로피도그렐 복합 투여는 아스피린 단독 투여에 비해 무증상 색전을 줄이는데 더 효과적이었다. 장기간의 항혈소판제 복합 사용에 대해서는 아직 논란이 있는데, 허혈뇌졸중 중 큰동맥 동맥경화로 인한 허혈뇌졸중은 장기간의 항혈소판제 복합 치료가 허혈뇌졸중 이차 예방에 더 효과적이었다는 연구도 있으나[29], 이는 출혈의 위험성을 고려하여 주의 깊게 결정해야 하며, 아직까지 모든 환자에서 권장되지 않는다.
경동맥 협착 환자는 뇌졸중의 치료 가능한 위험인자를 조사하여 동반된 위험인자를 집중적으로 치료해야 한다. 경동맥 협착 환자에게서 고혈압이 동반된 경우, 140/90 mmHg 미만으로 유지하는 것이 권고된다. 당뇨병이나 알부민뇨를 동반한 만성 콩팥병, 심뇌혈관 위험도가 고위험군인 환자에서 혈압 조절의 목표는 130/80 mmHg 미만으로 유지하는 것이 권고된다[30]. 뇌졸중 일차 예방을 위하여 특정한 종류의 항고혈압제를 선택하는 것보다는 적절하게 혈압을 떨어뜨리는 것이 가장 중요하다. 단 특별한 적응증이 없고, 동일한 혈압강하 조건에서는 베타차단제보다는 칼슘차단제나 레닌안지오텐신계 억제제가 추천된다. 경동맥 협착 환자에서 당뇨병이 동반된 경우, 식이요법, 운동요법, 약물요법 등을 통한 엄격한 혈당조절 및 고혈압, 이상지질혈증, 흡연 등의 동반된 위험인자에 대한 종합적이고 적극적인 평가 및 치료가 필요하다. 허혈뇌졸중 이차 예방의 경우 당화혈색소(HbA1c)의 목표 수치가 7% 미만이 되도록 혈당을 조절하는 것이 바람직하다[31].
저밀도콜레스테롤 치료 목표 수치는 일반적인 권고사항에 따른다. 특히 증후성 경동맥협착 환자의 경우 스타틴 사용을 적극적으로 고려해야 한다. 유의한 경동맥 협착이 있는 환자는 당뇨병, 복부동맥류 환자와 같은 고위험군으로 일차 예방을 위해 저밀도콜레스테롤 100 mg/dL 이하, 비고밀도지단백 콜레스테롤 130 mg/dL 이하를 치료목표로 삼는다. 증후성 경동맥 협착은 관상동맥질환, 말초 동맥질환과 함께 초고위험군으로 분류하며 저밀도콜레스테롤 70 mg/dL, 비고밀도지단백 콜레스테롤 100 mg/dL 이하를 목표로 조절한다. 최대 가용 용량의 스타틴을 투여해도 저밀도콜레스테롤 목표 수치 미만으로 감소하지 않으면 에제티미브를 병용할 수 있고, 최대가용 용량의 스타틴 단독 또는 에제티미브를 병용하여도 저밀도콜레스테롤 목표에 도달하지 않으면 PCSK9(proprotein convertase subtilisin/kexin type 9) 억제제를 병용하여 사용할 수 있다[32].
2006년에 발표된 SPARCL (Stroke Prevention byaggressive Reduction in Cholesterol Level) 연구에 따르면 최근 1-6개월 이내 뇌졸중이나 일과성 허혈발작이 생긴 환자들을 대상으로 고용량 스타틴(atorvastatin 80 mg/day)을 사용한 경우 위약사용군에 비해 뇌졸중과 심혈관질환의 위험이 낮았다[33]. 최근 발표된 TST (Treat Stroke to Target) trial에서는 최근 3개월 이내 허혈뇌졸중 또는 일과성 허혈발작이 발생한 환자들을 대상으로 저밀도콜레스테롤 조절 정도에 따른 심뇌혈관질환 예후를 분석하였는데, 저밀도콜레스테롤을 70 mg/dL 이하로 조절한 환자군에서 90-110 mg/dL 정도로 조절한 환자군에 비해 더 좋은 예후를 보였다[34]. 이러한 연구결과를 고려할 때 허혈뇌졸중 환자에서도 스타틴 투약을 통해 저밀도콜레스테롤을 70 mg/dL에 가깝게 낮추는 것이 도움이 될 것으로 생각된다.
CEA나 CAS의 경우에는 시술 전에 연령 및 환자의 요소, 증상 유무, 동맥경화반의 성상 등 여러 상황을 파악하여 치료의 방법을 선택하는데, 그 중 가장 중요한 요소는 증상의 유무와 경동맥 협착의 정도이다. 대한뇌졸중학회 및 미국심장/뇌졸중학회 지침을 포함한 대부분의 진료지침이 이 두 가지를 기본으로 치료방침을 결정하도록 권장하고 있으며 해당 지침에서 세부내용을 확인할 수 있다[35-37].
무증상경동맥협착에서의 CEA의 효과는 ACAS (Asymptomatic carotid atherosclerosis study)와 ACST (Asymptomatic Carotid Surgery Trial) 연구를 통해 검증되었다[38]. 현재 뇌졸중 진료지침에 따르면 60-99% 무증상 경동맥협착은 예방적 CEA 또는 CAS를 고려할 수 있다. CEA의 수술 위험성을 높이는 동반질환이 있는 경우 CAS를 고려할 수 있다. 다만 이러한 진료지침은 오래 전 연구를 기반으로 만들어진 것으로 최근 약물치료의 성적이 좋아진 것을 반영하지 못하므로, 경동맥 초음파 시행 후 죽상경화반의 형태가 색전증의 위험이 높은 경우에 수술 혹은 시술을 고려할 수 있다.
증후성 경동맥 협착 환자의 경우 70-99% 심한 협착에 대해 CEA 또는 CAS를 시행하는 것이 권장되며, 50-69%의 중등도 내경동맥 협착 환자의 환자의 연령, 성별, 동반된 질환, 처음 증상의 정도를 고려하여 CEA를 시행할 수 있다. CEA는 조기 수술의 금기사항이 없다면 허혈 증상이 발생한 뒤 2주 이내에 시술하는 경우 더 좋은 예후를 기대할 수 있다. 또한 후유증이 심하지 않은 작은 뇌경색의 경우에는 초기 재발율을 고려하여 48시간에서 7일 이내에 CEA또는 CAS를 시행해볼 수 있다. CAS 시기에 대한 근거자료는 아직 없으며, CAS 직전과 시술 후 최소 1개월 이상 클로피도그렐과 아스피린 병용 투여를 유지하는 것이 추천된다.
CEA와 CAS의 효과를 비교한 대표적인 연구들의 메타분석에서 시술 후 1개월 이내의 사망 혹은 뇌졸중의 발생이 CAS군에서 약 1.53배 정도 높은 것으로 보고하였다. CAS를 시행한 경우 7.3%에서, CEA를 시행한 경우 4.4%에서 허혈뇌졸중이 발생하여, CAS를 시행한 경우 시술 후 허혈뇌졸중 발생률이 높았다. 또한 연령에 따른 차이를 보였는데, 70세 이상에서는 CAS가 2배 가량 높은 합병증 발생률을 보여서 고령의 환자에서 CAS 시행에는 주의가 필요하다[39]. 최근에 발표된 CREST (the Carotid Revascularization Endarterectomy Versus Stenting Trial) 연구에서는 시술 후 1개월 이내에 뇌졸중은 CAS (4.1%)에서 CEA (1.1%)보다 흔하게 발생하여, 전체 합병증 발병률은 양군에 차이가 없었으나 뇌졸중 위험도는 여전히 CAS군에서 높았다[40]. 최근에는 CAS 시술 중 생길 수 있는 색전증을 예방할 수 있는 다양한 색전방어장치가 개발되고 있다. 이러한 개발을 통해 CAS가 더욱 일반화되고 있으며, CAS의 안정성과 효용성 및 장기적인 내구성에 대해서는 연구가 더 필요하다. 많은 연구에서 CAS와 CEA간 중장기적 예후는 큰 차이가 없는 것으로 보고되고 있다.
경동맥 협착 치료를 위해 CEA 또는 CAS를 선택할 때, 각각의 위험요소와 금기사항에 대한 고려가 필요하다. CEA를 시행하기 힘든 해부학적 요소로는 CEA 후 재협착, 경부 수술의 병력, 경부 방사선조사의 병력, 내경동맥 위치가 높은 경우, 총경동맥 위치가 낮은 경우, 기관절개술을 시행한 경우, 반대쪽 후두신경마비, 반대쪽 내경동맥폐색, 혈관 내 혈전, 매우 긴 불완전 내경동맥폐색을 보이는 경우가 있다. 특히, 경동맥 초음파를 시행하여 협착 원위부의 정상 혈관이 초음파상에서 관찰되지 않는 경우 CEA를 시행하기 어렵다. CEA는 동반된 내과 질환을 고려해야 하는데, 심부전 class III 또는 IV단계, 치료되지 않은 좌측 주심장동맥 혹은 다발성 심장동맥질환, 협심증 class III 또는 IV단계, 30일 이내의 급성 심근경색, 심한 신부전, 80세 이상 고령, 심한 폐질환, 동반된 심장수술 그리고 최근 약물 방출성 심장스텐트 삽입술 등의 기왕력을 갖는 환자는 CEA 시행의 고위험군으로CAS를 우선적으로 고려할 수 있다.
반면, CAS 시행 고위험군은 80세 이상 고령, 중증 신부전, 대동맥활에 심각한 질환이 동반되거나 휘어진 경우, 총경동맥에 심각한 질환이 동반되거나 만곡도가 높은 경우, 내경동맥에 혈관이 심각하게 구불구불한 경우, 거의 혈관이 막힌 경우, 대퇴동맥의 천자가 어려운 상황, 주요 뇌졸중 후 4-6주 이내, 광범위한 대뇌혈관질환이 동반된 경우이다. 아스피린과 클로피도그렐에 내성이 있거나, 내경동맥에 고리석회화, 혈관내 혈전, 만성 내경동맥 폐색, 동맥류나 혈관 기형으로 혈관 내 시술이 필요한 경우는 CEA를 우선적으로 고려할 수 있다(Table 4).
뇌졸중을 일으킬 수 있는 경동맥 협착증의 치료는 매우 다양하며 각 환자의 특성을 고려하여 치료 전략을 선택한다. 치료 결정에 있어 경동맥 초음파는 유용한 정보를 제공한다. 경동맥 초음파를 이용하여 지름감소 정도 및 혈류 속도를 측정하여 협착의 정도를 계산할 수 있고, 혈관 협착의 정도에 따라 뇌졸중 위험이 달라진다. 또한 죽상경화반의 모양에 따라 저-음영이거나 음영이 균일하지 않은 경우, 표면이 불규칙적이고 궤양을 동반한 경우 색전증의 위험이 높은 것으로 알려져 있다. 경동맥질환이 발견된 경우 증상 발생시기에 따라 적절한 항혈소판제가 필요하며, 무증상이더라도 뇌졸중 발생의 위험이 높거나 50% 이상의 협착인 경우 선택적으로 항혈소판제의 사용을 고려할 수 있다. 이외에도 고혈압, 이상지질혈증, 당뇨병의 위험인자를 목표에 맞게 조절해야 하며, 약물치료에도 불구하고 뇌졸중이 재발하거나, 뇌졸중의 발생위험이 높은 70% 이상의 협착에서는 CEA나 CAS를 고려할 수 있다.
따라서, 경동맥 초음파는 뇌졸중의 일차 및 이차 예방의 치료전략을 수립하기 위해 유용한 검사이며, 반복적으로 안전하게 검사할 수 있는 방법으로 환자들의 치료 후 추적검사에도 유용하게 사용할 수 있다.
Acknowledgement
This study was supported by a VHS Medical Center Research Grant, Republic of Korea (VHSMC 20003).
Figure 2.
Atherosclerotic plaques in distal common carotid artery. (a) Acoustic shadowing (arrow) caused by hyperechoic plaque with calcification. (b) Isoechoic plaque with smooth surface.

Figure 3.
Common carotid artery dissection. (A) Computed tomography angiography shows arterial dissection and intimal tear (arrow). (B) Ultrasound shows intimal flap (arrow) without evidence of atherosclerosis.
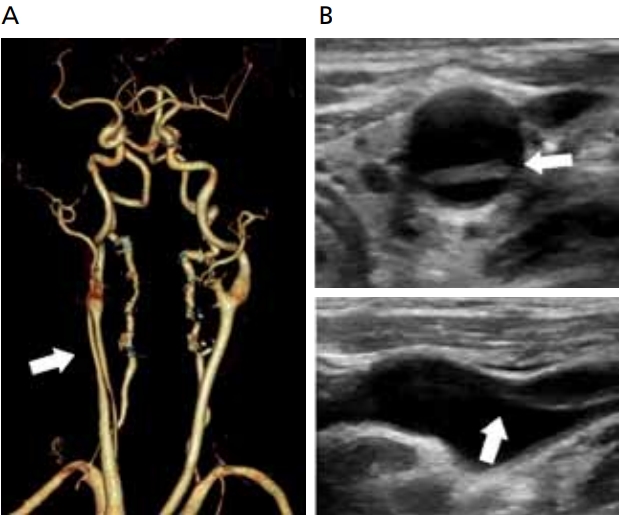
Figure 4.
Takayasu arteritis. Longitudinal scan of ultrasound shows the “macaroni sign” (homogeneous, iso-echoic, and concentric wall thickening) at the common carotid artery.
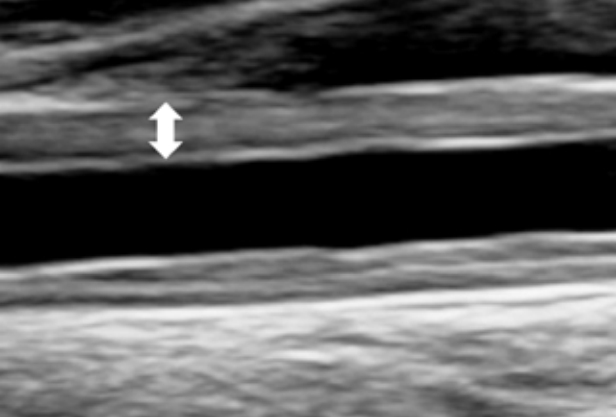
Table 1.
Differentiation between ICA and ECA
| ICA | ECA | |
|---|---|---|
| Size | Usually larger | Usually smaller |
| Location | Posterolateral | Anteromedial |
| Branches | Rarely | Yes |
| Pulsed Doppler | Low-resistance | High-resistance |
| Temporal tap | Usually negative | Usually positive |
Table 2.
Description of ultrasonographic findings of carotid plaque
Table 3.
Doppler criteria for the diagnosis of ICA stenosis
Table 4.
Considerations for CEA and CAS
References
1. White H, Boden-Albala B, Wang C, Elkind MS, Rundek T, Wright CB, Sacco RL. Ischemic stroke subtype incidence among whites, blacks, and hispanics: the Northern Manhattan Study. Circulation 2005;111:1327-1331.


2. Naylor AR. Why is the management of asymptomatic carotid disease so controversial? Surgeon 2015;13:34-43.


4. Lee JY, Choi HY, Lee SI, Hwang Y-H, Cho AH, Seo WK, Lee SJ, Yu S, Hong JM, Ahn SH, Jeong SK, Kim SB, Choi JC, Han SW, Koh IS, Hwang SH, Lee YS, Lee JH, Suk SH, Kim YJ, Song HJ, Kwon HM, Park JH. Extracranial carotid duplex ultrasonography. Part II - clinical utility of carotid duplex ultrasound. J Neurosonol Neuroimag 2018;10:61-79.


5. Bots ML, Hoes AW, Koudstaal PJ, Hofman A, Grobbee DE. Common carotid intima-media thickness and risk of stroke and myocardial infarction: the Rotterdam Study. Circulation 1997;96:1432-1437.


6. Lee JH. Cerebrovascular ultrasound in stroke diagnosis and its applications. J Korean Med Assoc 2004;47:620-630.

7. Touboul PJ, Hennerici MG, Meairs S, Adams H, Amarenco P, Bornstein N, Csiba L, Desvarieux M, Ebrahim S, Hernandez Hernandez R, Jaff M, Kownator S, Naqvi T, Prati P, Rundek T, Sitzer M, Schminke U, Tardif JC, Taylor A, Vicaut E, Woo KS. Mannheim carotid intima-media thickness and plaque consensus (2004-2006-2011). An update on behalf of the advisory board of the 3rd, 4th and 5th watching the risk symposia, at the 13th, 15th and 20th European Stroke Conferences, Mannheim, Germany, 2004, Brussels, Belgium, 2006, and Hamburg, Germany, 2011. Cerebrovasc Dis 2012;34:290-296.



8. Biasi GM, Froio A, Diethrich EB, Deleo G, Galimberti S, Mingazzini P, Nicolaides AN, Griffin M, Raithel D, Reid DB, Valsecchi MG. Carotid plaque echolucency increases the risk of stroke in carotid stenting: the Imaging in Carotid Angioplasty and Risk of Stroke (ICAROS) study. Circulation 2004;110:756-762.


9. Eliasziw M, Streifler JY, Fox AJ, Hachinski VC, Ferguson GG, Barnett HJ. Significance of plaque ulceration in symptomatic patients with high-grade carotid stenosis. North American Symptomatic Carotid Endarterectomy Trial. Stroke 1994;25:304-308.


10. Makris GC, Lavida A, Griffin M, Geroulakos G, Nicolaides AN. Three-dimensional ultrasound imaging for the evaluation of carotid atherosclerosis. Atherosclerosis 2011;219:377-383.


11. Pollex RL, Spence JD, House AA, Fenster A, Hanley AJ, Zinman B, Harris SB, Hegele RA. A comparison of ultrasound measurements to assess carotid atherosclerosis development in subjects with and without type 2 diabetes. Cardiovasc Ultrasound 2005;3:15.




12. Grant EG, Benson CB, Moneta GL, Alexandrov AV, Baker JD, Bluth EI, Carroll BA, Eliasziw M, Gocke J, Hertzberg BS, Katanick S, Needleman L, Pellerito J, Polak JF, Rholl KS, Wooster DL, Zierler RE. Carotid artery stenosis: grayscale and Doppler US diagnosis--Society of Radiologists in Ultrasound Consensus Conference. Radiology 2003;229:340-346.


13. Lewis RF, Abrahamowicz M, Cote R, Battista RN. Predictive power of duplex ultrasonography in asymptomatic carotid disease. Ann Intern Med 1997;127:13-20.


14. Wardlaw JM, Chappell FM, Stevenson M, De Nigris E, Thomas S, Gillard J, Berry E, Young G, Rothwell P, Roditi G, Gough M, Brennan A, Bamford J, Best J. Accurate, practical and cost-effective assessment of carotid stenosis in the UK. NIHR Health Technology Assessment programme: executive summaries. Southampton: NIHR Journals Library; 2006 [Epub]. Available from: https://www.ncbi.nlm.nih.gov/books/NBK62203/

15. Kim DI. Endovascular treatment of occlusive cerebrovascular diseases. J Korean Med Assoc 2004;47:636-644.

16. Bosch FT, Hendrikse J, Davagnanam I, Bonati LH, van der Lugt A, van der Worp HB, de Borst GJ, Mali W, Brown MM, Nederkoorn PJ. Optimal cut-off criteria for duplex ultrasound compared with computed tomography angiography for the diagnosis of restenosis in stented carotid arteries in the international carotid stenting study. Eur Stroke J 2017;2:37-45.


17. Kim SM, Ha SH, Noh SM, Heo SH, Kim BJ. Neurosonology and imaging in uncommon causes of stroke. J Neurosonol Neuroimag 2019;11:34-45.


18. Cantu C, Pineda C, Barinagarrementeria F, Salgado P, Gurza A, Paola de Pablo, Espinosa R, Martinez-Lavin M. Noninvasive cerebrovascular assessment of Takayasu arteritis. Stroke 2000;31:2197-2202.


19. Greenland P, Abrams J, Aurigemma GP, Bond MG, Clark LT, Criqui MH, Crouse JR 3rd, Friedman L, Fuster V, Herrington DM, Kuller LH, Ridker PM, Roberts WC, Stanford W, Stone N, Swan HJ, Taubert KA, Wexler L. Prevention conference V: beyond secondary prevention: identifying the high-risk patient for primary prevention: noninvasive tests of atherosclerotic burden: Writing Group III. Circulation 2000;101:E16-E22.


20. Greenland P, Alpert JS, Beller GA, Benjamin EJ, Budoff MJ, Fayad ZA, Foster E, Hlatky MA, Hodgson JM, Kushner FG, Lauer MS, Shaw LJ, Smith SC Jr, Taylor AJ, Weintraub WS, Wenger NK, Jacobs AK; American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. 2010 ACCF/AHA guideline for assessment of cardiovascular risk in asymptomatic adults: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. Circulation 2010;122:e584. e636.

21. Lorenz MW, Polak JF, Kavousi M, Mathiesen EB, Volzke H, Tuomainen TP, Sander D, Plichart M, Catapano AL, Robertson CM, Kiechl S, Rundek T, Desvarieux M, Lind L, Schmid C, DasMahapatra P, Gao L, Ziegelbauer K, Bots ML, Thompson SG; PROG-IMT Study Group. Carotid intimamedia thickness progression to predict cardiovascular events in the general population (the PROG-IMT collaborative project): a meta-analysis of individual participant data. Lancet 2012;379:2053-2062.



22. Baldassarre D, Veglia F, Hamsten A, Humphries SE, Rauramaa R, de Faire U, Smit AJ, Giral P, Kurl S, Mannarino E, Grossi E, Paoletti R, Tremoli E; IMPROVE Study Group. Progression of carotid intima-media thickness as predictor of vascular events: results from the IMPROVE study. Arterioscler Thromb Vasc Biol 2013;33:2273-2279.


23. Inaba Y, Chen JA, Bergmann SR. Carotid plaque, compared with carotid intima-media thickness, more accurately predicts coronary artery disease events: a meta-analysis. Atherosclerosis 2012;220:128-133.


24. Aboyans V, Ricco JB, Bartelink ME, Bjorck M, Brodmann M, Cohnert T, Collet JP, Czerny M, De Carlo M, Debus S, Espinola-Klein C, Kahan T, Kownator S, Mazzolai L, Naylor AR, Roffi M, Rother J, Sprynger M, Tendera M, Tepe G, Venermo M, Vlachopoulos C, Desormais I; ESC Scientific Document Group. 2017 ESC Guidelines on the Diagnosis and Treatment of Peripheral Arterial Diseases, in collaboration with the European Society for Vascular Surgery (ESVS): document covering atherosclerotic disease of extracranial carotid and vertebral, mesenteric, renal, upper and lower extremity arteries. Endorsed by: the European Stroke Organization (ESO). The Task Force for the Diagnosis and Treatment of Peri-pheral Arterial Diseases of the European Society of Cardiology (ESC) and of the European Society for Vascular Surgery (ESVS). Eur Heart J 2018;39:763-816.



25. Abbott AL, Paraskevas KI, Kakkos SK, Golledge J, Eckstein HH, Diaz-Sandoval LJ, Cao L, Fu Q, Wijeratne T, Leung TW, Montero-Baker M, Lee BC, Pircher S, Bosch M, Dennekamp M, Ringleb P. Systematic review of guidelines for the management of asymptomatic and symptomatic carotid stenosis. Stroke 2015;46:3288-3301.


26. Johnston SC, Easton JD, Farrant M, Barsan W, Conwit RA, Elm JJ, Kim AS, Lindblad AS, Palesch YY; Clinical Research Collaboration; Neurological Emergencies Treatment Trials Network; the POINT Investigators. Clopidogrel and aspirin in acute ischemic stroke and high-risk TIA. N Engl J Med 2018;379:215-225.



27. Wang Y, Wang Y, Zhao X, Liu L, Wang D, Wang C, Wang C, Li H, Meng X, Cui L, Jia J, Dong Q, Xu A, Zeng J, Li Y, Wang Z, Xia H, Johnston SC; CHANCE Investigators. Clopidogrel with aspirin in acute minor stroke or transient ischemic attack. N Engl J Med 2013;369:11-19.


28. Markus HS, Droste DW, Kaps M, Larrue V, Lees KR, Siebler M, Ringelstein EB. Dual antiplatelet therapy with clopidogrel and aspirin in symptomatic carotid stenosis evaluated using doppler embolic signal detection: the Clopidogrel and Aspirin for Reduction of Emboli in Symptomatic Carotid Stenosis (CARESS) trial. Circulation 2005;111:2233-2240.


29. Kim D, Lee SH, Joon Kim B, Jung KH, Yu KH, Lee BC, Roh JK; for Korean Stroke Registry investigators. Secondary prevention by stroke subtype: a nationwide follow-up study in 46 108 patients after acute ischaemic stroke. Eur Heart J 2013;34:2760-2767.



30. Lee HY, Shin J, Kim GH, Park S, Ihm SH, Kim HC, Kim KI, Kim JH, Lee JH, Park JM, Pyun WB, Chae SC. 2018 Korean Society of Hypertension Guidelines for the management of hypertension: part II-diagnosis and treatment of hypertension. Clin Hypertens 2019;25:20.




31. Kim MK, Ko SH, Kim BY, Kang ES, Noh J, Kim SK, Park SO, Hur KY, Chon S, Moon MK, Kim NH, Kim SY, Rhee SY, Lee KW, Kim JH, Rhee EJ, Chun S, Yu SH, Kim DJ, Kwon HS, Park KS; Committee of Clinical Practice Guidelines; Korean Diabetes Association. 2019 clinical practice guidelines for type 2 diabetes mellitus in Korea. Diabetes Metab J 2019;43:398-406.



32. Rhee EJ, Kim HC, Kim JH, Lee EY, Kim BJ, Kim EM, Song Y, Lim JH, Kim HJ, Choi S, Moon MK, Na JO, Park KY, Oh MS, Han SY, Noh J, Yi KH, Lee SH, Hong SC, Jeong IK. 2018 Guidelines for the management of dyslipidemia. Korean J Intern Med 2019;34:723-771.




33. Amarenco P, Bogousslavsky J, Callahan A 3rd, Goldstein LB, Hennerici M, Rudolph AE, Sillesen H, Simunovic L, Szarek M, Welch KM, Zivin JA; Stroke Prevention by Aggressive Reduction in Cholesterol Levels (SPARCL) Investigators. High-dose atorvastatin after stroke or transient ischemic attack. N Engl J Med 2006;355:549-559.


34. Amarenco P, Kim JS, Labreuche J, Charles H, Abtan J, Bejot Y, Cabrejo L, Cha JK, Ducrocq G, Giroud M, Guidoux C, Hobeanu C, Kim YJ, Lapergue B, Lavallee PC, Lee BC, Lee KB, Leys D, Mahagne MH, Meseguer E, Nighoghossian N, Pico F, Samson Y, Sibon I, Steg PG, Sung SM, Touboul PJ, Touze E, Varenne O, Vicaut E, Yelles N, Bruckert E; Treat Stroke to Target Investigators. A comparison of two LDL cholesterol targets after ischemic stroke. N Engl J Med 2020;382:9-19.


35. Korean Stroke Society. Clinical practice guidelines for stroke [Internet]. Seoul: Korean Stroke Society. [cited 2020 Jun 3]. Available from: https://www.stroke.or.kr:4454/guidelines/
36. Kernan WN, Ovbiagele B, Black HR, Bravata DM, Chimowitz MI, Ezekowitz MD, Fang MC, Fisher M, Furie KL, Heck DV, Johnston SC, Kasner SE, Kittner SJ, Mitchell PH, Rich MW, Richardson D, Schwamm LH, Wilson JA. Guidelines for the prevention of stroke in patients with stroke and transient ischemic attack: a guideline for healthcare professionals from the American Heart Association/American Stroke Association [published correction appears in Stroke. Stroke 2014;45:2160-2236.


37. Powers WJ, Rabinstein AA, Ackerson T, Adeoye OM, Bambakidis NC, Becker K, Biller J, Brown M, Demaerschalk BM, Hoh B, Jauch EC, Kidwell CS, Leslie-Mazwi TM, Ovbiagele B, Scott PA, Sheth KN, Southerland AM, Summers DV, Tirschwell DL. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke 2019;50:e344-e418.


38. Halliday A, Harrison M, Hayter E, Kong X, Mansfield A, Marro J, Pan H, Peto R, Potter J, Rahimi K, Rau A, Robertson S, Streifler J, Thomas D; Asymptomatic Carotid Surgery Trial (ACST) Collaborative Group. 10-year stroke prevention after successful carotid endarterectomy for asymptomatic stenosis (ACST-1): a multicentre randomised trial. Lancet 2010;376:1074-1084.



39. Bonati LH, Fraedrich G; Carotid Stenting Trialists’ Collaboration. Age modifies the relative risk of stenting versus endarterectomy for symptomatic carotid stenosis--a pooled analysis of EVA-3S, SPACE and ICSS. Eur J Vasc Endovasc Surg 2011;41:153-158.


40. Brott TG, Hobson RW 2nd, Howard G, Roubin GS, Clark WM, Brooks W, Mackey A, Hill MD, Leimgruber PP, Sheffet AJ, Howard VJ, Moore WS, Voeks JH, Hopkins LN, Cutlip DE, Cohen DJ, Popma JJ, Ferguson RD, Cohen SN, Blackshear JL, Silver FL, Mohr JP, Lal BK, Meschia JF; CREST Investigators. Stenting versus endarterectomy for treatment of carotid-artery stenosis. N Engl J Med 2010;363:11-23.



Peer Reviewers’ Commentary
이 논문은 경동맥 질환이 있는 환자들에서 초음파의 활용 가치 및 치료 방법에 대해 최근 지식을 정리하여 제시해 주고 있다. 경동맥 초음파 검사 방법에 대한 개략적인 설명과 함께 초음파 검사의 임상적 유용성과 경동맥 질환에 대한 내과적 및 외과적 치료 전략도 소개해 주고 있다. 뇌졸중은 단일 질환으로 국내 사망률 1위의 질환이며, 경동맥 질환은 뇌혈관이 막혀서 발생하는 허혈성 뇌졸중인 뇌경색을 유발하는 주요 원인 중 하나로 알려져 있다. 특히 최근 건강검진이 늘면서 뇌경색을 유발한 유증상 경동맥 질환뿐 아니라 무증상 경동맥 협착이 발견되는 경우 가 늘어나고 있어 경동맥 질환에 대한 관리 및 치료 전략에 대한 이해가 중요해지고 있다. 이 논문은 일반적인 경동맥 초음파 검사법과 임상적 유용성을 포함하여 경동맥 질환에 대한 치료를 이해하는 데 많은 도움이 될 것으로 판단된다.
[정리: 편집위원회]
-
METRICS

-
- 1 Crossref
- Scopus
- 13,275 View
- 888 Download
-
Related articles in
J Korean Med Assoc -
Guideline for the diagnosis and treatment of scabies2023 December;66(12)
The classification, diagnosis, and treatment of rhinosinusitis2022 May;65(5)
Classification, diagnosis, and treatment of vascular malformations2021 September;64(9)
Understanding and Management of Occupational Diseases1997 May;40(5)
The Etiology and Treatment of Paresthesia in Feet and Hands1997 May;40(5)