 |
 |
- Search
| J Korean Med Assoc > Volume 64(7); 2021 > Article |
|
Abstract
Current Concepts: Recent research progress now allows us to obtain a bird view of neuropathic pain pathophysiology: peripheral and central sensitization. For peripheral sensitization, a local inflammatory milieu of the injured nerve primarily drives sequential phenotypic changes, which are critical and shared by both neuropathic and inflammatory pain. Central sensitization is led either by the hyperexcitability of the second-order afferent neuron itself or loss of physiological inhibitory control of the transmission of pain signal to the higher nervous system. Peripheral and central sensitization work synergistically but can also introduce neuropathic pain alone.
Discussion and Conclusion: The cause of neuropathic pain is diverse, and understanding of its pathophysiology is still insufficient to realize a mechanism-based approach to clinical phenotypes or therapeutic applications. In dealing with chronic neuropathic pain, it is highly desirable to assess key aspects of a patient’s pain based on a plausible mechanism and select the best management method accordingly.
Figure 1.
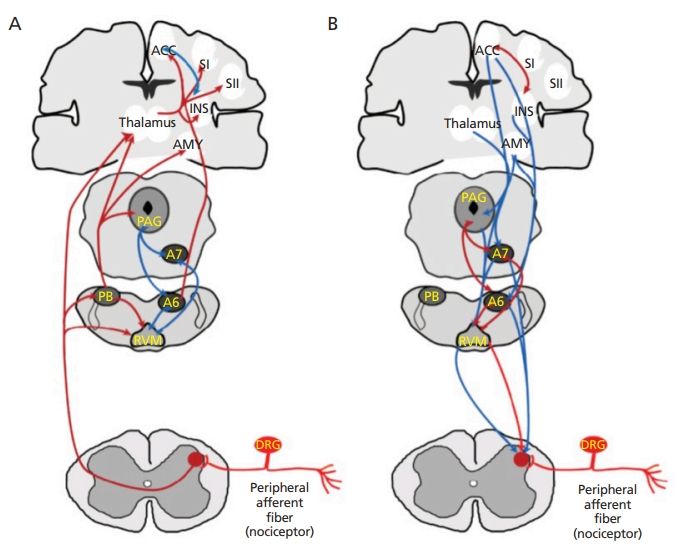
Table 1.
Adapted from Baron R. Handb Exp Pharmacol 2009;(194):3-30, with permission from Springer Nature [16].
DRG, dorsal root ganglion; SP, spontaneous pain; CBZ, carbamazepine; OCB, oxcarbazepine; TCA, tricyclic antidepressants; TNF-α, tumor necrotic factor- α; COX, cyclooxygenase; NSAIDs, non-steroidal anti-inflammatory drugs; TRPV1, transient receptor potential cation channel subfamily V member 1; TRPM8, transient receptor potential cation channel subfamily M member 8; ASIC, acid-sensing ion channel; TCA, tricyclic antidepressant; SMP, sympathetically maintained pain; NMDA, N-methyl-D-aspartate; NK1, neurokinin-1; GBP, gabapentin; PGB, pregabalin; CBZ, carbamazepine; MAPK, mitogen-activated protein kinase; TNF- α, tumor necrosis factor- α; GABA, g-aminobutyric acid; BDNF, brain-derived neurotrophic factor; NA, noradrenaline; 5-HT, 5-hydroxytryptamine (serotonin).
References
Peer Reviewers’ Commentary
-
METRICS

-
- 0 Crossref
- Scopus
- 5,699 View
- 349 Download
-
Related articles in
J Korean Med Assoc -
Management of patients with neuropathic pain2022 August;65(8)
Treatment of neuropathic pain2021 July;64(7)
Evaluation and diagnosis of neuropathic pain2021 July;64(7)
Etiology and epidemiology of neuropathic pain2021 July;64(7)
Importance and challenges of neuropathic pain2021 July;64(7)






