|
 |
- Search
| J Korean Med Assoc > Volume 65(9); 2022 > Article |
|
Abstract
Background: Robotic surgical systems were created partly to solve several constraints of laparoscopic surgery and to offer technical advantages. With a substantial body of evidence demonstrating its efficacy in rectal cancer treatment, robotic surgery will soon become another conventional treatment. However, further investigations and randomized trials focusing on primary endpoints are necessary to establish some advantages of robot-assisted colon surgery.
Current Concepts: Da Vinci Single-Site and SP platforms (Intuitive Surgical Inc.) were developed to overcome the shortcomings of single-port laparoscopic surgery. Despite the currently insufficient evidence, it seems that the SP platform addresses several limitations of single-port transabdominal or transanal surgery. Robotic transanal minimally invasive surgery and total mesorectal excision were developed to overcome conventional platforms’ limitations, using wristed instrumentation to enhance dexterity and ergonomics. Studies on the effectiveness and viability of this novel approach are ongoing. The near-infrared fluorescence technique, real-time stereotactic navigation technology, and other surgical data platforms based on artificial intelligence incorporated into the robotic system will play an important role in improving outcomes.
Discussion and Conclusion: Robotic systems for advanced colorectal cancer offer technical advantages for complex and precise surgeries. If robotic surgery costs are reduced by expanding its indications and enhancing competition among different robotic platforms, it will provide clinical benefits to more patients and reduce social healthcare costs.
Current Concepts: Da Vinci Single-Site and SP platforms (Intuitive Surgical Inc.) were developed to overcome the shortcomings of single-port laparoscopic surgery. Despite the currently insufficient evidence, it seems that the SP platform addresses several limitations of single-port transabdominal or transanal surgery. Robotic transanal minimally invasive surgery and total mesorectal excision were developed to overcome conventional platforms’ limitations, using wristed instrumentation to enhance dexterity and ergonomics. Studies on the effectiveness and viability of this novel approach are ongoing. The near-infrared fluorescence technique, real-time stereotactic navigation technology, and other surgical data platforms based on artificial intelligence incorporated into the robotic system will play an important role in improving outcomes.
Discussion and Conclusion: Robotic systems for advanced colorectal cancer offer technical advantages for complex and precise surgeries. If robotic surgery costs are reduced by expanding its indications and enhancing competition among different robotic platforms, it will provide clinical benefits to more patients and reduce social healthcare costs.
수술적 절제는 근치적 치료, 병기결정, 예후 및 기타 치료적 측면에서 대장암에 대한 가장 효과적인 치료이다[1,2]. 암 수술의 주요 목표는 부작용을 최소화하면서 생존율과 삶의 질을 향상시키는 것이다[3]. 종양학적, 기능적, 사회 의료비용 측면에서 대장암의 수술 술기 발전은 대장암 치료의 개선을 위해 필수적이다[3-7].
여러 무작위연구에서 복강경 수술이 개복 수술보다 더 우월하다는 것이 입증되었으며, 대장암의 치료를 위한 전통적인 방법이 되었다[8,9]. 왜냐하면 복강경 수술은 개복술에 비해 출혈이 적고, 장 운동성이 더 빨리 회복되며 종양학적 결과를 희생하지 않으면서, 입원기간을 단축하는 등 단기적으로 우수한 임상학적 결과를 보여주었기 때문이다. 그러나 복강경 수술은 본질적으로 수많은 기술적 한계를 가지고 있다. 특히 하부 직장암 절제술의 경우 제한된 골반강에서의 긴 직선 기구의 가동 범위 제한, 2차원적 시야, 촉각 감도의 상실 및 능숙도 저하 등의 기술적 어려움이 있다.
3차원 확대 영상, 외과의사가 제어하는 안정적인 카메라 시스템, 그리고 7° 자유도, 540° 회전이 가능한 손목관절, 생리적 떨림 필터링, 모션 스케일링 기능, 더 강력한 견인 및 안정적으로 고정된 세 번째 로봇 팔의 견인 등은 다빈치 로봇 시스템(Intuitive Surgical Inc., Mountain View, CA, USA)이 가진 기술적 장점들이다. 또한 로봇 대장암 수술은 최소 침습 치료를 시행하는 외과의사에게 복강경 수술에 비해 더 짧은 학습 곡선을 제공하는 것으로 보고되었다[10].
최첨단 기술을 활용한 로봇 수술은 대장암의 수술 치료에 혁신을 일으켰고, 대장암 수술 분야에서 대중화되고 있다. 그러나 대장암 수술에서 로봇 수술의 역할은 여전히 불확실하며 로봇 수술이 대장암 치료에 있어서 복강경 수술보다 더 중요한 임상적 장점이 있는지 명확하지 않다. 이 논문에서는 현재 특정 적응증에 대해 행해지는 로봇 대장암 수술의 현황을 살펴보고 향후 발전 방향을 제시하는 것을 목표로 한다.
대규모 다기관 무작위연구에서 장기적인 종양학적 안전성이 입증된 이후 복강경 절제술이 결장암에 있어서 표준치료가 되었다[11]. 하지만 아직까지 직장암에 대한 복강경 전직장간막절제술(total mesorectal excision)은 기술적으로 어려운 치료로 인식되고 있다. 왜냐하면 사용되는 복강경 기구가 일반적으로 직선이고 단단하며, 집도의가 한정된 골반 내에서 일련의 카메라에 의존한 복잡한 움직임을 수행해야 하기 때문이다. 직장암에 대한 복강경 전직장간막절제술의 종양학적 결과를 조사한 여러 무작위대조연구에서 복강경 수술 결과가 개복 수술에 비해 차이가 없었다[4,12].
로봇 수술은 직장 및 전립선 암 수술처럼 어려운 술기를 제한된 공간에서 시행되는 복강경 수술의 제약을 극복하 기 위해 개발되었다. 여러 연구에서 직장암에 대한 로봇 수술과 복강경 수술 사이에 장·단기적인 임상적 및 종양학적 결과가 큰 차이가 없는 것으로 보고되었다[13,14]. Lee 등[15]은 개방성 무작위통제연구에서 복강경과 로봇 직장암 수술 사이에 개복 수술로의 전환율에서 유의한 차이가 없음을 보고했다. 직장암에 대한 로봇 및 복강경 절제술에 대한 국제적 다기관 연구(Robotic Versus Laparoscopic Resection for Rectal Cancer, ROLARR)에서도 복강경 또는 로봇 수술 후 개복술로의 전환율에서 유의미한 차이가 없었다(12.2% 대 8.1%, P=0.16). 그러나 세부 분석에서 남성, 비만 환자 및 하부 직장암 환자에서 로봇 술기의 잠재적인 이점을 보였다[16]. Milone 등[17]은 직장암에서 로봇과 복강경의 전직장간막절제술의 완전성에 대한 메타 분석을 수행했으며, 로봇 수술이 복강경 수술에 비해 통계학적으로 유의하게 전직장간막절제술의 완전성이 우월함을 보여주 었다(교차비, 1.83; 95% 신뢰구간, 1.08-3.10; P=0.03). Kowalewski 등[18]의 메타 분석에서, 복강경 수술을 시행 받은 환자들에 비해 로봇 수술을 받은 환자들은 삶의 질이 더 좋았고, 요로 증상, 장폐색 및 요폐가 감소했지만 성기능에서는 눈에 띄는 장점이 관찰되지 않았다. 이전 연구에서 복강경과 로봇 직장암 수술 사이에 유사한 장기 종양학적 결과가 보고된 반면, 최근에는 로봇 수술이 다변량 분석 에서 전체 및 암 특이적 생존율에 대한 독립적으로 유의미한 예후 인자임이 보고되었다. 최근까지도 직장암 치료에서 로봇 수술의 유효성을 입증하기 위해 다양한 평가 변수들에 대한 수많은 연구가 진행 중이며 상당한 증거들이 축적되고 있다. 로봇 수술은 가까운 장래에 전립샘암과 마찬가지로, 직장암 수술에 대한 또 다른 표준 수술법이 될 수 있을 것으로 전망한다.
최근 결장암 치료를 위해 최근 전결장간막절제술(complete mesocolic excision)과 중심혈관결찰술(central vessel ligation)을 통합한 술식이 도입되었다. 우측 결장암에서 전결장간막절제술에 대한 복강경 수술과 개복술을 비교한 여러 연구에서 복강경하 전결장간막절제술의 시행 가능성과 안전성뿐만 아니라 만족스러운 종양학적 결과를 얻을 수 있음이 입증되었다[19]. 그러함에도 불구하고, 우측 결장암에서 최소 침습 수술을 통한 전결장간막절제술 및 중심혈관결 찰술은 도전적인 술기이다. 우측 결장암에 대해 로봇 결장절 제술은 다음과 같은 이점을 제공할 수 있다. 첫째, 상장간막간 혈관을 따라 안전하고 정밀한 림프절제술이 가능하다. 둘째, 향상된 수술 시야와 균일한 견인력으로 안정적인 전결장간막절제술이 가능하다. 셋째, 복강 내 체내 문합을 실용적이고 안전하게 한다. 그러나 로봇 전결장간막절제술 및 중심혈관결찰술이 임상 및 종양학적 결과에서 복강경 수술보다 우수하다는 증거는 아직 충분하지 않다. Park 등[20]은 전결장간막절제술 및 중심혈관결찰술의 원칙을 차용한 우측 대장절제술에서 로봇 수술과 표준 복강경 수술을 비교하는 무작위임상연구를 시행하여 양 군 간에 임상 및 장기 종양학적 결과가 유사하다고 보고했다. 그러나 로봇 결장절제술은 복강경 수술보다 유의하게 수술시간이 길고 고비용이었으며, 이런 고비용을 상회하기에는 이점이 충분하지 않다고 결론지었다. 한편 Tschann 등[21]이 최근 수행한 메타 분석에 따르면, 로봇군에서 개복술로의 전환율이 통계학적으로 유의하게 낮고 입원기간이 짧으며 혈액 손실이 적은 반면 장기 종양학적 결과는 두 군 간에 유사하였음을 보고하였다. Ferri 등[22]은 성향점수매치(propensity score match)를 이용한 전향적 비무작위연구에서 비용 효율성 분석을 수행했으며 로봇군과 복강경군 간에 총 비용 측면에서 유의한 차이가 없음을 기술하였다. 로봇 결장 수술의 장점을 확립하기 위해서는 전결장간막절제술 및 중심혈관결찰술, 체내 문합, 비용 효율성과 같은 특정 일차평가변수(primary end-point)에 초점을 맞춘 추가적인 연구들이 필요하다.
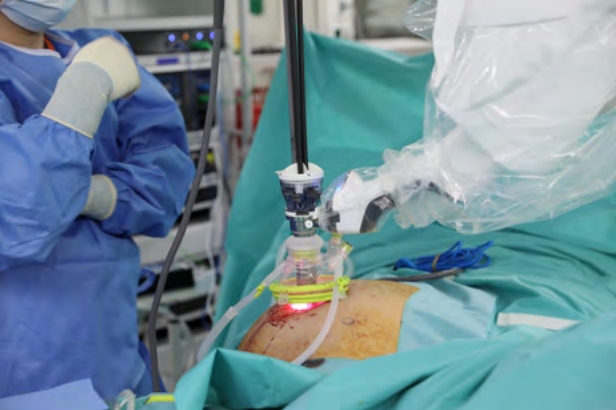
최근에 da Vinci Si 및 Xi 시스템과 호환되는 da Vinci Single-Site 플랫폼은 기존의 단일공 복강경 수술의 한계를 극복하기 위해 개발되었다. 혁신적인 Single-Site 플랫폼에 사용되는 소프트웨어는 복벽에서 엇갈린 두 개의 곡선 기구를 콘솔에서 외과의사의 손에 맞도록 재배치하여 단일공 복강경 수술과는 달리 오른손으로는 오른쪽의 기구를, 왼손으로는 왼쪽의 기구를 사용할 수 있도록 한다. 하지만 기존 로봇 시스템의 주요 장점 중 하나인 손목기구를 사용할 수 없고, 반강체 로봇 기구의 제한된 운동 범위, 카메라를 포함해 3개의 팔만을 사용함으로써 초래되는 조직 견인의 제한, Single-Site 시스템의 기구 가용성의 제한 등으로 인해 이플랫폼은 대장 수술에 널리 사용되지 않았다. 이런 면을 보완하기 위해 저자는 우측 및 좌측 결장암에 대해 Single-Site 이외에 하나의 추가적은 로봇 팔을 삽입한 축소공 로봇 수술법을 개발하여 이 술식의 안전성과 실행 가능성을 보고했다(Figure 1) [23,24]. 또한 12주간의 추적 방문에서 신체 이미지 인식 및 미용 만족도 평가에서 축소공 로봇 수술이 기존의 다중공 복강경 결장절제술에 비해 유의하게 우수한 결과를 보였음을 보고하였다[24]. 이 수술기법의 장점으로는 로봇 기구와 카메라 간의 충돌 감소, 삼각공간생성의 용이성, 미용적 이점, 로봇 관절손목기구를 통한 섬세한 절개, 인체 공학적 편안함 등이 있다. 또한 Single-Site 플랫폼은 da Vinci Si 또는 Xi가 설치된 대부분의 기관에서 사용할 수 있고 아래에 언급된 SP 플랫폼의 일부 단점을 해결할수 있기 때문에 선택적으로 대장암 환자에게 고려할 가치가 있다고 생각된다.
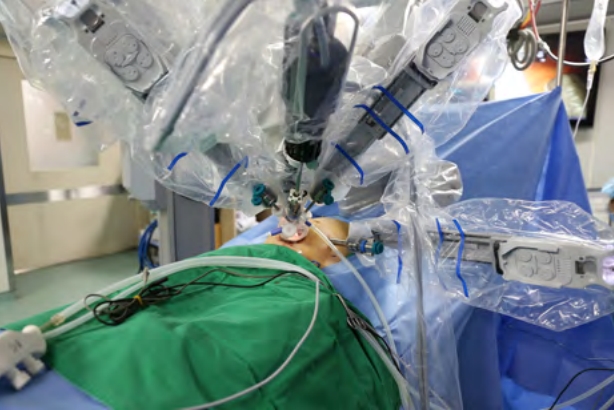
새로운 로봇 접근 방식인 SP da Vinci 로봇 플랫폼(Intuitive Surgical Inc., Sunnyvale, CA, USA)은 Single-Site 플랫폼의 단점을 보완하면서 단일공수술을 효과적으로 시행하기 위해 개발되었다. SP 시스템은 원래 전립샘, 인후 및 항문 직장과 같이 협소하고 접근하기 어려운 해부학적 부위에 접근하기에 용이하게 설계되었으나 장 수술을 비롯한 다양한 외과 분야에서도 활용되고 있다. SP 플랫폼의 장점은 홀로그램에 의한 기기 위치 표시, 로봇 손목관절 및 유연한 팔꿈치 사용, 콘솔 제어 카메라 및 3차원(3-dimensional, 3D) 광학 등이 있다. 또한 플랫폼의 붐(boom)은 포트의 원격 센터 안팎에서 360° 회전할 수 있어 로봇 시스템을 다시 도킹할 필요 없이 한 번의 도킹만으로 수술을 시행할 수 있도록 하는데 이는 대장암 수술과 같은 다중-사분면 수술에서 용이하다. Piozzi 등[25]은 SP 시스템의 효율성과 안전성을 평가하기 위해 괄약근간 절제술 7개 사례, 우측 결장절제술 5개 사례, 횡행 결장절제술 1개 사례의 수술 전후 단기 임상 결과를 보고했다. 저자들은 SP 적응증으로 우측 결장암, 괄약근 간 절제가 필요한 하부 직장암, 작은 종양이나 수술 전 화학방사선요법 후 축소되어 병기가 낮아진 종양 등으로 기술하였다. Kim 등[26]은 직장암 환자 5명에 대한 초기 경험에서 SP 플랫폼을 이용한 전직장간막절제술이 안전하고 실현 가능함을 보고했다. Marks 등[27]은 직장 병변에 대해 SP 경항문 최소 침습 수술(transanal minimally invasive surgery, TAMIS)을 받은 26명의 환자들과 경항문 전직장간막절제술(transanal total mesorectal excision, TaTME) 을 받은 2명의 환자들에 대한 초기 경험을 보고하여, 우수한 광학과 항문직장강에서 능숙도를 갖춘 SP 플랫폼의 안전성과 실행 가능성을 보여주었다. 저자의 연구팀은 S상 결장암에 대한 11개 사례의 전방 절제술, 직장암에 대한 2개 사례의 저위 전방 절제술, 신경내분비 종양에 대한 1개 사례의 TAMIS (미출판)를 시행했다(Figure 2). 최근 보고된 연구들과 우리의 경험들로 미루어 볼 때, SP 플랫폼이 기존 단일공 경복부 및 경항문 수술의 많은 제한 사항을 해결할 수 있다는 것은 분명하다. 그러나 SP 플랫폼 또한 몇 가지 단점이 있으며 추가 개선이 필요하다. 단극 곡선 가위 이외의 에너지 기구가 없고, 체내 봉합기가 개발되지 않았으며, 아직까지 근적외선 형광(near-infrared fluorescence, NIF) 기술은 SP 시스템에서 사용할 수 없다. 또한 SP 시스템에서는 세 번째 팔이 위쪽에 있고, 카메라가 아래쪽에 있어 기존의 수술 시야와 달라 수술자에게 불편할 수 있다. SP 시스템에서 사용할 수 있는 기구들이 추가적으로 개발되고 로봇의 움직임이 개선된다면 SP를 이용한 수술의 적응증이 확대되고 단일공수술을 위한 이상적인 플랫폼이 될 것으로 기대된다.
TAMIS는 직장의 양성 병변 및 저위험 T1 선암의 치료에 널리 사용되고 있다. 이 수술기법은 항문관에 설치된 다중 채널 단일공 장치를 사용하며, 표준 복강경 시스템과 직선형 기구를 사용하여 중부와 상부 직장까지도 접근이 가능하게 한다. 이전 연구에서 TAMIS의 이점이 입증되었지만, 시간이 지남에 따라 이 술식은 기술적으로 어렵고 학습 곡선이 가파르다는 것이 보고되었다[28]. TAMIS는 많은 장점이 있지만, 안정적인 플랫폼의 부재, 장치의 다리 사이에 수술자와 조수가 위치해야 하는 어려움, 제한된 직장 내강에서 직선 기구를 이용한 봉합 및 조작의 어려움, 기기 간의 충돌로 인한 절제 중 시야 훼손 등 제한점들이 여전히 존재한다. 로봇 TAMIS는 능숙도(dexterity)와 인체 공학(ergonomics)을 향상시키기 위해 로봇 손목기구를 사용하여 기존 TAMIS의 한계를 극복하기 위해 적용되었다(Figure 3). 여러 저자들이 로봇 TAMIS의 실현 가능성과 안전성에 대해 보고했으며, 최근에는 TaTME와 같이 보다 복잡한 술식에 적용하고 있다[29].
TaTME는 주로 좁은 골반에 하부 직장암이 있는 비만 또는 남성 환자에서 복강경 경복부 전직장간막절제술의 기술적 어려움을 극복하기 위해 개발되었으며 아래에서 위로 (bottom up) 접근하는 방식의 자연공 내시경 수술(natural orifice transluminal endoscopic surgery)을 기반으로 하는 새로운 기술이다. 이 술식은 특히 술기 시작 시 원위부 절제연을 확보할 수 있다는 장점이 있다. 그러나 TaTME는 직선형의 복강경 기구를 사용하는 단일공 복강경 기술을 기반으로 하기 때문에 학습 곡선이 가파른 어려운 술식으로 알려져 있다[30]. 로봇 TaTME는 복강경 TaTME와 비교하여 측면 박리 시 향상된 양손 능숙도(ambidexterity)와 골반 신경및 자율 기능의 보존 등에서 이점을 기대할 수 있다. 최초의 로봇 TaTME가 발표된 이후 최근 다른 연구들에서 이 새로운 접근 방식의 효율성과 실행 가능성에 대해 활발히 연구 중이다[29,31].
인도시아닌 그린(indocyanine green, ICG)을 이용한 NIF 기술은 감시 림프절 생검, 림프절 경로 매핑, 주요 혈관을 둘러싼 혈관계 식별, 대장 수술에서 의인성 요관 손상의 위험을 줄이기 위한 요관 감지 및 혈관, 혈류 및 조직 관류의 육안적 평가 등에 유용하다[32]. 최근 로봇 시스템에 설치된 수술 중 NIF 영상 시스템(Firefly; Intuitive Surgical Inc., Sunnyvale, CA, USA)은 실시간으로 혈관 내 NIF 신호를 식별하는 데 사용되고 있다. 근치적 수술을 위한 광범위한 림프절 절제술을 수행하기 위해 감시 림프절을 식별하고 절제 범위 외부에 추가 림프절을 매핑하기 위해 전이성 림프절을 감지하는 데 NIF 및 ICG 사용에 대한 많은 연구가 수행 되었다[33]. Kim 등[34]은 수술 전 의심되는 측방골반림프절을 찾고, 불완전한 박리를 피하기 위해 로봇 전직장간막절제술과 측방 골반 림프절 절제술을 시행하는 NIF의 사용 법을 보고하였다. Zhou 등[35]은 NIF 기술을 사용하여 전직장간막절제술 및 측방 골반 림프절 절제술을 받은 환자와 NIF 영상 없이 시행 받은 환자를 비교한 결과, NIF 그룹이 수술 중 출혈이 유의하게 낮고 채취된 골반 측방 림프절 수가 유의하게 더 많다는 것을 보고하였다. 또한 Park 등[36]과 Bae 등[37]은 결장암 수술에서 전결장간막절제술 및 D3 구역 림프절 절제술에 NIF 기술을 적용하였다. Park 등[36]은 종양 주위에 ICG를 주입하여 림프의 흐름과 림프절을 시각화한 결과, 선단(apical) 림프절의 수와 회수된 림프절의 총 수에서 NIF 그룹이 기존 그룹보다 유의하게 더 많다는 것을 보고하였다.
또한 NIF 기술을 이용하여 수술 중에 ICG를 경정맥으로 주입함으로써 육안으로 직접 수술 부위의 혈관 구조를 확인할 수 있다. Bae 등[38]은 직장암 환자에서 로봇 수술을 시행 받은 11명의 환자에서 하장간막동맥(inferior mesenteric artery)에서 분지하는 좌결장동맥의 위치를 NIF 영상을 이용하여 찾은 후 하장간막동맥의 하위 결찰을 시행하는 술식의 유용성을 보고하였다. 또한 NIF 영상을 이용하여 하장간막정맥 주변의 측부 혈관(Riolan 궁)을 식별하였다[39]. 좌결 장동맥은 주로 Griffith point에 있는데, 이는 비장 만곡부에 있으며 수술 중 손상이나 허혈에 취약하다. NIF를 사용하여 실시간으로 측부 혈관을 식별하면 하장간막정맥을 안전하게 결찰할 수 있고 측부 혈관의 손상을 방지하는 데 도움이 될수 있다. 아직까지 이에 대한 객관적인 근거가 부족하지만, NIF 방법을 이용한 로봇 수술이 임상 및 종양학적 결과의 향상에 도움이 될 것으로 기대한다.
실시간 정위 항법(stereotactic navigation)은 로봇 전직장간막절제술 동안 복잡한 해부학적 구조를 이해하고 정밀성을 향상시키는 데 유용할 수 있다[40]. Atallah 등[41]은 TilePro 인터페이스가 탑재되어 있는 da Vinci Xi 플랫폼을 사용하여 실시간 정위 항법의 유용성에 대해 보고하였고, TaTME를 시행하는 동안 로봇 시스템과 Stryker 탐색 시스템을 결합한 실시간 탐색에 대해 보고했다. 향후 인공지능 기반 로봇 시스템과 수술 데이터 플랫폼이 서로 보완해 외과의가 보다 최적화된 환자 진료를 제공하는 데 도움이 될 수 있을 것으로 기대한다.
일반적으로 지금까지 인접 구조물의 국소 침습, 장 폐쇄, 결장 천공 또는 심각한 출혈이 있는 환자는 전통적으로 개복 수술로 치료를 받았고, 이러한 상황은 복강경 수술에 대한 상대적 혹은 절대적 금기증으로 간주되었다. 국소 침습성 대장암에 대한 로봇 수술은 최적의 손목 움직임, 3D 시각화 및 떨림 안정화를 통해 적절한 노출과 박리의 가능하게 하고 인접 장기로의 직접 침범에 대한 통합절제술이나 광범위한 림프절 절제술과 같은 복잡한 수술에 기술적인 이점을 제공한다. 광범위 절제술은 대장암 치료에서 여전히 중요하며 최근 연구에서는 대동맥 주위나 측방골반 부위의 림프절 절제술 또는 골반 적출술과 같은 광범위하고 복잡한 술기에 대한 로봇 수술의 효과적인 적용을 보여주었다[42,43]. 괄약근 보존 수술의 장점은 로봇 수술과 병행할 경우 극대화될 수 있는데, 특히 선행 화학방사선요법을 시행한 경우 괄약근간 절제술, 동측 항문거근을 침범한 하부 직장암의 항문거근 부분 절제술, 전방에 위치한 직장암에 대한 부분 드농빌리에 (Denonvilliers)근막 절제 등 보다 정밀하고 선택적인 수술이 가능하다[1,2,44].
다빈치 로봇 시스템은 수년간 해당 분야의 유일한 리더였다. 그러나 현재 새로운 플랫폼들이 개발되고 있으며 일부는 단일공 및 자연공 수술에 중점을 두고 있다. 2017년 10 월, 미국식품의약국(Food and Drug Administration, FDA) 은 Senhance 수술 로봇 시스템(TransEnterix, Morrisville, NC, USA)을 허가했으며 최근 대장 질환에 대해 이 로봇 플랫폼을 적용한 여러 연구가 발표되었다. Samalavicius 등[45]은 암을 포함한 대장 질환에 대해 Senhance 시스템을 사용하여 로봇 수술을 받은 57명의 환자를 대상으로 연구를 수행하여 이 플랫폼의 안전성과 타당성을 확인했다. Flex Robotic System (MedRobotics Corp. Raynham, MA, USA)은 경항문 내시경 미세수술에 최적화된 소형의 연성 내시경 로봇이며, 2017년 미국 FDA 허가를 받았다. Morino 등[46]은 이 플랫폼을 이용하여 직장 종양이 있는 환자 14명에 대해 전층 절제술을, 12명에 대해 점막하 박리술을 시행한 결과, 15.4%의 수술 후 절제연 양성을 보였고, TEO (Karl Storz, Tuttlingen, Germany) 시스템을 사용한 기존 경항문 내시경 수술로의 전환율이 23.1%였음을 보고하였다. Single Port Orifice Robotic Technology-SPORT (Titan Medical Company, Toronto, ON, Canada), Versius (Cambridge Medical Robotics, Cambridge, UK), Revo-I (MSR-5000; Meerecompany Inc., Seongnam, Korea), MiroSurge (Medtronic, Minneapolis, MN, USA), Medicaroid (Kobe, Japan) 또한 임상에 적용하기 위해 다양한 연구 중에 있다. 이렇게 독점의 시대를 넘어 다양한 로봇 플랫폼들이 서로 경쟁하면서 로봇 수술 비용이 줄어든다면 대장암 로봇 수술이 더욱 발전할 것으로 기대된다.
로봇을 이용한 수술은 다양한 수술 과정에서 널리 활용되고 있지만 비싼 가격으로 인해 그 적용이 제한적이다. 비용 분석 연구들에 따르면 대장암 로봇 수술은 개복 수술과 복강경 수술에 비해 더 많은 비용이 드는 것으로 보고되었다. ROLARR 연구에 따르면 로봇군(11,853파운드 또는 13,668 달러)은 복강경군(10,874파운드 또는 12,556달러)보다 비용이 더 많이 들었다[16]. Kim 등[47]은 로봇 수술군과 복강경 수술군을 비교한 연구에서 단기 임상 결과는 비슷했지만 로봇 수술에서 병원비, 환자 부담금, 수술비, 마취비, 수술 후관리비 등 지출이 더 많았음을 보여주었다. 적응증의 확대와 다양한 로봇 플랫폼 간의 경쟁 심화로 로봇 수술 비용이 감소하면 더 많은 환자에게 혜택을 주고 사회의 의료비용을 줄일 수 있을 것으로 전망된다.
최소 침습 수술을 위한 로봇 시스템의 대안으로 여러 가지 복강경 관절 기구가 도입되었다[48]. 이러한 도구들은 관절이 있거나 곡선으로 구부러질 수 있게 하는 몇 가지 속성들을 가지고 있다. 그 중에서 ArtiSential (LIVSMED Inc., San Diego, CA, USA)은 사람의 손목과 같은 완전한 관절 기능과 직관적인 제어 기능을 갖춘 8 mm 직경의 손잡이 기구로 2019년 미국 FDA에 class I 의료기기로 등록되었다. 외과의는 로봇 플랫폼에 비해 훨씬 저렴한 비용으로 한 번에 두 개의 관절 장치를 사용하고 힘에 대한 피드백을 얻을 수 있다. 또한 콘솔이 아닌 환자 옆에서 직접 수술을 수행할 수 있다. 우리는 단일공 복강경 충수절제술 및 직장암에 대한 다중포트 복강경 저위 전방 절제술(미출간)을 일부 경험하였으며, 이 기구가 저렴한 가격으로 로봇 수술에서 볼 수 있었던 손목 관절 기능의 일부 이점을 제공할 것이라고 생각한다. 최근 로봇 수술의 발달과 함께, 복강경 수술 또한 예전에는 로봇 수술에서 주로 볼 수 있었던 3D 카메라 시스템, 손목관절 기구, 카메라 홀더 시스템, NIF 등의 요소들을 보완해 나가고 있다.
Figure 1.
Access port setup for single plus one-port right colectomy with intracorporeal anastomosis using the Single-Site platform.
References
1. Varela C, Kim NK. Surgical treatment of low-lying rectal cancer: updates. Ann Coloproctol 2021;37:395-424.




2. Piozzi GN, Kim SH. Robotic intersphincteric resection for low rectal cancer: technical controversies and a systematic review on the perioperative, oncological, and functional outcomes. Ann Coloproctol 2021;37:351-367.




3. Oh CK, Huh JW, Lee YJ, Choi MS, Pyo DH, Lee SC, Park SM, Shin JK, Park YA, Cho YB, Yun SH, Kim HC, Lee WY. Long-term oncologic outcome of postoperative complications after colorectal cancer surgery. Ann Coloproctol 2020;36:273-280.




4. Stevenson AR, Solomon MJ, Lumley JW, Hewett P, Clouston AD, Gebski VJ, Davies L, Wilson K, Hague W, Simes J; ALaCaRT Investigators. Effect of laparoscopic-assisted resection vs open resection on pathological outcomes in rectal cancer: the ALaCaRT randomized clinical trial. JAMA 2015;314:1356-1363.


5. De Robles MS, Young CJ. Triple-staple technique effectively reduces operating time for rectal anastomosis. Ann Coloproctol 2021;37:16-20.




6. Eldamshety O, Kotb S, Khater A, Roshdy S, Elashry M, Zahi MS, Elkalla HMHR, Elnahas W, Farouk O, Fathi A, Senbel A, Hamed EE, Abdelwahab K, Elzahby IA, Abdallah A, Abdelaziz M, Lezoche E. Early and late functional outcomes of anal sphincter-sparing procedures with total mesorectal excision for anorectal adenocarcinoma. Ann Coloproctol 2020;36:148-154.




7. Jaloun HE, Lee IK, Kim MK, Sung NY, Turkistani SAA, Park SM, Won DY, Hong SH, Kye BH, Lee YS, Jeon HM. Influence of the enhanced recovery after surgery protocol on postoperative inflammation and short-term postoperative surgical outcomes after colorectal cancer surgery. Ann Coloproctol 2020;36:264-272.




8. Clinical Outcomes of Surgical Therapy Study Group, Nelson H, Sargent DJ, Wieand HS, Fleshman J, Anvari M, Stryker SJ, Beart RW Jr, Hellinger M, Flanagan R Jr, Peters W, Ota D. A comparison of laparoscopically assisted and open colectomy for colon cancer. N Engl J Med 2004;350:2050-2059.


9. COLOR Study Group. COLOR: a randomized clinical trial comparing laparoscopic and open resection for colon cancer. Dig Surg 2000;17:617-622.



10. Kim HJ, Choi GS, Park JS, Park SY. Multidimensional analysis of the learning curve for robotic total mesorectal excision for rectal cancer: lessons from a single surgeon's experience. Dis Colon Rectum 2014;57:1066-1074.

11. Fleshman J, Sargent DJ, Green E, Anvari M, Stryker SJ, Beart RW Jr, Hellinger M, Flanagan R Jr, Peters W, Nelson H; Clinical Outcomes of Surgical Therapy Study Group. Laparoscopic colectomy for cancer is not inferior to open surgery based on 5-year data from the COST Study Group trial. Ann Surg 2007;246:655-662. discussion 662-654.


12. Jeong SY, Park JW, Nam BH, Kim S, Kang SB, Lim SB, Choi HS, Kim DW, Chang HJ, Kim DY, Jung KH, Kim TY, Kang GH, Chie EK, Kim SY, Sohn DK, Kim DH, Kim JS, Lee HS, Kim JH, Oh JH. Open versus laparoscopic surgery for mid-rectal or low-rectal cancer after neoadjuvant chemoradiotherapy (COREAN trial): survival outcomes of an open-label, non-inferiority, randomised controlled trial. Lancet Oncol 2014;15:767-774.


13. Cho MS, Baek SJ, Hur H, Min BS, Baik SH, Lee KY, Kim NK. Short and long-term outcomes of robotic versus laparoscopic total mesorectal excision for rectal cancer: a case-matched retrospective study. Medicine (Baltimore) 2015;94:e522.


14. Park CH, Bae SU, Jeong WK, Baek SK. Early and late clinicopathologic outcomes of minimally invasive total mesorectal excision for rectal cancer: a propensity score-matched comparison of robotic and laparoscopic approaches. Int J Med Robot 2021;17:e2324.



15. Lee D, Kim SK, Kim K, Lee JR, Suh CS, Kim SH. Advantages of single-port laparoscopic myomectomy compared with conventional laparoscopic myomectomy: a randomized controlled study. J Minim Invasive Gynecol 2018;25:124-132.


16. Jayne D, Pigazzi A, Marshall H, Croft J, Corrigan N, Copeland J, Quirke P, West N, Rautio T, Thomassen N, Tilney H, Gudgeon M, Bianchi PP, Edlin R, Hulme C, Brown J. Effect of robotic-assisted vs conventional laparoscopic surgery on risk of conversion to open laparotomy among patients undergoing resection for rectal cancer: the ROLARR randomized clinical trial. JAMA 2017;318:1569-1580.



17. Milone M, Manigrasso M, Velotti N, Torino S, Vozza A, Sarnelli G, Aprea G, Maione F, Gennarelli N, Musella M, De Palma GD. Completeness of total mesorectum excision of laparoscopic versus robotic surgery: a review with a meta-analysis. Int J Colorectal Dis 2019;34:983-991.



18. Kowalewski KF, Seifert L, Ali S, Schmidt MW, Seide S, Haney C, Tapking C, Shamiyeh A, Kulu Y, Hackert T, Muller-Stich BP, Nickel F. Functional outcomes after laparoscopic versus robotic-assisted rectal resection: a systematic review and meta-analysis. Surg Endosc 2021;35:81-95.




19. Bae SU, Saklani AP, Lim DR, Kim DW, Hur H, Min BS, Baik SH, Lee KY, Kim NK. Laparoscopic-assisted versus open complete mesocolic excision and central vascular ligation for right-sided colon cancer. Ann Surg Oncol 2014;21:2288-2294.



20. Park JS, Kang H, Park SY, Kim HJ, Woo IT, Park IK, Choi GS. Long-term oncologic after robotic versus laparoscopic right colectomy: a prospective randomized study. Surg Endosc 2019;33:2975-2981.



21. Tschann P, Szeverinski P, Weigl MP, Rauch S, Lechner D, Adler S, Girotti PNC, Clemens P, Tschann V, Presl J, Schredl P, Mittermair C, Jäger T, Emmanuel K, Konigsrainer I. Short- and long-term outcome of laparoscopic- versus robotic-assisted right colectomy: a systematic review and meta-analysis. J Clin Med 2022;11:2387.



22. Ferri V, Quijano Y, Nunez J, Caruso R, Duran H, Diaz E, Fabra I, Malave L, Isernia R, d'Ovidio A, Agresott R, Gomez P, Isojo R, Vicente E. Robotic-assisted right colectomy versus laparoscopic approach: case-matched study and cost-effectiveness analysis. J Robot Surg 2021;15:115-123.



23. Bae SU, Jeong WK, Baek SK. Reduced-port robotic right colectomy with intracorporeal anastomosis for right-sided colon cancer using the da Vinci Single-Site® platform: a pilot case series study. Ann Robot Innov Surg 2021;2:31-39.


24. Bae SU, Jegon WK, Baek SK. Single plus one-port robotic surgery using the da Vinci Single-Site Platform versus conventional multi-port laparoscopic surgery for left-sided colon cancer. Wideochir Inne Tech Maloinwazyjne 2022;17:179-187.



25. Piozzi GN, Kim JS, Choo JM, Shin SH, Kim JS, Lee TH, Baek SJ, Kwak JM, Kim J, Kim SH. Da Vinci SP robotic approach to colorectal surgery: two specific indications and short-term results. Tech Coloproctol 2022;26:461-470.



26. Kim HJ, Choi GS, Song SH, Park JS, Park SY, Lee SM, Choi JA. An initial experience with a novel technique of single-port robotic resection for rectal cancer. Tech Coloproctol 2021;25:857-864.



27. Marks JH, Kunkel E, Salem JF, Martin CT, Anderson B, Agarwal S. First clinical experience with single-port robotic transanal minimally invasive surgery: phase II trial of the initial 26 cases. Dis Colon Rectum 2021;64:1003-1013.


28. Lee L, Kelly J, Nassif GJ, Keller D, Debeche-Adams TC, Mancuso PA, Monson JR, Albert MR, Atallah SB. Establishing the learning curve of transanal minimally invasive surgery for local excision of rectal neoplasms. Surg Endosc 2018;32:1368-1376.



29. Atallah S, Nassif G, Polavarapu H, deBeche-Adams T, Ouyang J, Albert M, Larach S. Robotic-assisted transanal surgery for total mesorectal excision (RATS-TME): a description of a novel surgical approach with video demonstration. Tech Coloproctol 2013;17:441-447.



30. Persiani R, Agnes A, Belia F, D'Ugo D, Biondi A. The learning curve of TaTME for mid-low rectal cancer: a comprehensive analysis from a five-year institutional experience. Surg Endosc 2021;35:6190-6200.




31. Gomez Ruiz M, Parra IM, Palazuelos CM, Martín JA, Fernandez CC, Diego JC, Fleitas MG. Robotic-assisted laparoscopic transanal total mesorectal excision for rectal cancer: a prospective pilot study. Dis Colon Rectum 2015;58:145-153.

32. Son GM, Ahn HM, Lee IY, Ha GW. Multifunctional indocyanine green applications for fluorescence-guided laparoscopic colorectal surgery. Ann Coloproctol 2021;37:133-140.




33. Kusano M, Tajima Y, Yamazaki K, Kato M, Watanabe M, Miwa M. Sentinel node mapping guided by indocyanine green fluorescence imaging: a new method for sentinel node navigation surgery in gastrointestinal cancer. Dig Surg 2008;25:103-108.



34. Kim HJ, Park JS, Choi GS, Park SY, Lee HJ. Fluorescence-guided robotic total mesorectal excision with lateral pelvic lymph node dissection in locally advanced rectal cancer: a video presentation. Dis Colon Rectum 2017;60:1332-1333.


35. Zhou SC, Tian YT, Wang XW, Zhao CD, Ma S, Jiang J, Li EN, Zhou HT, Liu Q, Liang JW, Zhou ZX, Wang XS. Application of indocyanine green-enhanced near-infrared fluorescence-guided imaging in laparoscopic lateral pelvic lymph node dissection for middle-low rectal cancer. World J Gastroenterol 2019;25:4502-4511.



36. Park SY, Park JS, Kim HJ, Woo IT, Park IK, Choi GS. indocyanine green fluorescence imaging-guided laparoscopic surgery could achieve radical D3 dissection in patients with advanced right-sided colon cancer. Dis Colon Rectum 2020;63:441-449.


37. Bae SU, Jeong WK, Baek SK. Intra-operative near-infrared fluorescence imaging for robotic complete mesocolic excision and central vascular ligation in right-sided colon cancer-a video vignette. Colorectal Dis 2019;21:1459.


38. Bae SU, Saklani AP, Hur H, Min BS, Baik SH, Kim NK. Robotic interface for transabdominal division of the levators and pelvic floor reconstruction in abdominoperineal resection: a case report and technical description. Int J Med Robot 2015;11:296-301.


39. Bae SU, Min BS, Kim NK. Near infrared fluorescence imaging for real-time assessment of blood flow during totally robotic total mesorectal excision for rectal cancer--a video vignette. Colorectal Dis 2016;18:313.

40. Atallah S, Parra-Davila E, Melani AGF, Romagnolo LG, Larach SW, Marescaux J. Robotic-assisted stereotactic real-time navigation: initial clinical experience and feasibility for rectal cancer surgery. Tech Coloproctol 2019;23:53-63.



41. Atallah S, Zenoni S, Kelly J, Tilahun Y, Monson JR. A blueprint for robotic navigation: pre-clinical simulation for transanal total mesorectal excision (taTME). Tech Coloproctol 2016;20:653-654.



42. Bae SU, Jeong WK, Baek SK, Kim NK. Robotic complete mesocolic excision and para-aortic lymph node dissection for cecal cancer and paraganglioma. Dis Colon Rectum 2018;61:1235-1236.


43. Kim MC, Oh JH. Lateral pelvic lymph node dissection after neoadjuvant chemoradiotherapy in patients with rectal cancer: a single-center experience and literature review. Ann Coloproctol 2021;37:382-394.




44. Yang SY, Kim NK. Robotic partial excision of levator-ani muscle for locally advanced low rectal cancer invading ipsilateral pelvic floor. Ann Coloproctol 2020;36:415-416.




45. Samalavicius NE, Dulskas A, Janusonis V, Klimasauskiene V, Eismontas V, Deduchovas O, Janusonis T, Markelis R, Smolskas E. Robotic colorectal surgery using the Senhance® robotic system: a single center experience. Tech Coloproctol 2022;26:437-442.



46. Morino M, Forcignanò E, Arezzo A. Initial clinical experience with a novel flexible endoscopic robot for transanal surgery. Tech Coloproctol 2022;26:301-308.




Peer Reviewers’ Commentary
이 논문은 대장암 수술 중 최첨단 기술을 활용한 로봇 수술에 대해 최신 문헌을 정리하여 체계적으로 설명해 주고 있다. 대장암의 위치에 따른 로봇 수술의 임상적 의미, 다양한 로봇 플랫폼에 따른 최적의 적용 방법과 임상적 결과의 설명, 근적외선 형광, 실시간 정위항법 같은 최신 기술을 로봇 수술과 통합해서 적용할 수 있음을 제시하고 있다. 로봇 수술의 장점을 통해 기존의 개복 수술로만 가능했던 확대 절제술, 진행성 하부 직장암 환자를 더 정밀하게 수술할 수 있음을 설명하고 있다. 향후 비용적인 측면, 개발되고 있는 경쟁 로봇 플랫폼, 복강경 수술 시 사용할 수 있는 로봇 시스템의 대안 등에 대해서도 잘 설명하고 있다. 특히 저자의 경험을 바탕으로 한 수술 장면과 각 플랫폼에 대한 최적의 적응증, 장단점 등을 이해하기 쉽게 설명하고 있다. 이 논문은 가장 최신의 로봇 플랫폼 및 수술 기법을 체계적으로 기술하고 있어 로봇 수술을 이해하고 적용하는 데 많은 도움을 줄 것으로 판단된다.
[정리: 편집위원회]
-
METRICS

-
Related articles in
J Korean Med Assoc -
Endovascular surgery for chronic subdural hematoma2024 June;67(6)
Robot-assisted surgery in urology2024 March;67(3)
Endoscopic treatment of colorectal polyps and early colorectal cancer2023 November;66(11)
Molecular analyses of peritoneal metastasis from colorectal cancer2022 September;65(9)
Surgical treatment for metastatic colorectal cancer2022 September;65(9)