 |
 |
- Search
| J Korean Med Assoc > Volume 65(10); 2022 > Article |
|
Abstract
Background: Iron overload is frequently found in transfused patients with chronic anemia and congenital hemochromatosis. Iron toxicity adversely affects organs, including the heart, liver, and endocrine glands. Iron chelation helps patients with transfusion-related iron overload improve organ dysfunction and prolong survival.
Current Concepts: Iron overload is classified into primary and secondary causes. Acquired causes of secondary iron overload include ineffective erythropoiesis, chronic transfusion, and chronic liver diseases. The effectiveness of iron chelation therapy in reducing or maintaining body iron has been demonstrated in many studies of patients with transfusion-induced anemias. Deferasirox, a once-daily oral iron chelator for adult and pediatric patients with transfusion-induced iron overload, is available in Korea. The initial daily dose of deferasirox recommended by Korean guidelines is 20 mg/kg body weight, taken on an empty stomach at least 30 minutes before meals. Serum ferritin levels should be maintained below 1,000 ng/mL.
Discussion and Conclusion: Iron chelation therapy should be considered when a patient has undergone large red blood cell transfusions, and there is evidence of organ iron overload to improve organ dysfunction and survival.
Current Concepts: Iron overload is classified into primary and secondary causes. Acquired causes of secondary iron overload include ineffective erythropoiesis, chronic transfusion, and chronic liver diseases. The effectiveness of iron chelation therapy in reducing or maintaining body iron has been demonstrated in many studies of patients with transfusion-induced anemias. Deferasirox, a once-daily oral iron chelator for adult and pediatric patients with transfusion-induced iron overload, is available in Korea. The initial daily dose of deferasirox recommended by Korean guidelines is 20 mg/kg body weight, taken on an empty stomach at least 30 minutes before meals. Serum ferritin levels should be maintained below 1,000 ng/mL.
Discussion and Conclusion: Iron chelation therapy should be considered when a patient has undergone large red blood cell transfusions, and there is evidence of organ iron overload to improve organ dysfunction and survival.
철은 혈색소 생성에 중요한 물질로 주로 장내 흡수를 조절함으로써 철분의 체내 농도가 조절된다. 철을 배출하는 통로가 철이 포함된 장 상피 세포의 탈락이 유일하므로 철이 과도하게 체내에 축적되는 경우에는 과잉 철의 축적으로 인하여 장기 기능에 이상을 초래한다. 철과잉증(iron overload syndromes)은 여러 질환이나 조건에서 발생하며 궁극적으로는 장기 손상을 유발하게 된다. 여러 분류방법이 있으나 철 대사와 연관된 유전적 이상에 의한 1차성 철과잉증과 빈혈성 질환이나 수혈 등에 의해 발생하는 2차성 철과잉증으로 나눌 수 있다. 수혈성 철과잉증은 중증 빈혈 환자의 관리에서 중요한 관심 사항이다. 수혈이 지속적으로 반복될 때에는 여분의 철이 여러 장기에 축적이 되면서 장기 손상을 유발하게 된다. 따라서 적절한 철 킬레이트화 요법(iron chelation therapy)이 필요하게 된다.
인체에서 정상적인 철 공급의 유일한 통로는 식이성 철이다. 따라서 일반적으로 식이 철 부족이나 철 흡수 장애 등으로 철분이 부족하게 되는 경우가 흔하다. 체내 철은 3.5-4 g 정도이며, 체중 당 50-60 mg의 철 농도를 갖는다[1]. 적혈구 속의 혈색소에 약 2.3 g, 헤모글로빈을 제외한 철분 포함 단백질들(myoglobin, cytochrome, catalase 등)에 약 350 mg, 대식세포에 약 500 mg, 간에 ferritin 형태로 200-1,000 mg, 골수에서 발견되는 150 mg 정도 등으로 되어 있다[2]. 장세포와 피부상피 세포 탈락이나 출혈 또는 기생충 감염에 의해 약 1-2 mg의 철이 소실된다. 결과적으로 철 항상성 유지를 위해서는 하루 1-2 mg의 철이 장에서 흡수될 필요가 있다. 정상적인 상황에서 과잉의 철을 인체 외로 배출하는 생리적 기전은 존재하지 않는다. 인체 내 철분을 제거하는 것이 조절되지 않기 때문에 장세포에서 철이 흡수되는 과정이나 대식세포로부터 저장된 철의 방출 과정은 여러 전달 단백질 및 조절자에 의해 정밀하게 조절되고 있다. 유전 혈색소증(hereditary hemochromatosis)에서는 이러한 hepcidin이나 ferroportin과 같은 철 흡수 조절 물질의 유전자 변이(대표적으로 HFE 유전자에서 homozygous C282Y 돌연변이 또는 HJV, TFR2, HAMP, SCL40A1의 돌연변이)에 의해 장에서 철 흡수가 과도하게 일어나서 철과잉 상태가 된다[3]. 철과잉의 다른 원인으로는 지중해빈혈(thalassemia)과 같은 비효율적인 적혈구형성(ineffective erythropoiesis) 또는 출혈 이외의 원인(hemoglobinopathy나 악성 혈액질환 등)으로 많은 수혈을 시행한 경우 등이다.
철과잉증은 1차성 요인 및 2차성 요인 또는 선천적인 유전 요인 및 후천적인 요인으로 구분할 수 있다(Table 1). 선천적 유전 요인은 유전 혈색소증과 비효율적인 적혈구형성 유전 빈혈로 구분된다[3-5]. 1차성 원인은 철흡수와 연관된 유전자의 이상에 의해 철과잉이 발생하는 경우로 유전 혈색소증이 여기에 속한다. 유전 혈색소증은 대표적으로 HFE 유전자와 연관된 유전 혈색소증(C282Y/C282Y, C282Y/H63D, 다른 HFE 돌연변이 등), HFE와 연관 없는 유전 혈색소증, 청소년 혈색소증(juvenile hemochromatosis), transferrin receptor 2 혈색소증, ferroportin 질환이 있다.
2차성 원인은 다시 선천적 유전 이상에 의한 경우와 후천적 질환에 의한 경우로 나눌 수 있다. 2차성 원인 중 선천적 유전 이상에는 thalassemia, sickle-cell anemia, pyruvate kinase deficiency, the congenital dyserythropoietic anemia, hereditary spherocytosis, 그리고 X-linked sideroblastic anemia가 있다. 철과잉은 특히 homozygous β-thalassemia에서 심하다. 선천적 유전 이상에 의한 2차성 철과잉증은 dyserythropoiesis에 의한 철 대사이상에 의해 발생하는데 만성 수혈도 원인으로 작용한다. 후천적인 요인으로는 idiopathic sideroblastic anemia가 있는데 최신 세계보건기구(World Health Organization) 분류에 의해 골수형성이상증후군(myelodysplastic syndrome, MDS)에 속하며, myelodysplastic syndrome with ring sideroblast로 분류된다. 골수섬유화증(idiopathic myelofibrosis)과 재생불량빈혈(idiopathic aplastic anemia), 혈액암, 만성 신장 질환, 조혈세포이식 등 만성 빈혈이 또 다른 2차성 요인이며, 장에서 철의 흡수가 증가된 상태는 아니므로 만성 수혈이 철과잉의 원인이 된다. 이 외의 원인으로는 만성 간질환, aceruloplasminemia, Friedreich ataxia, congenital atransferrinemia 등이 있다. African iron overload은 철 성분이 과다한 맥주를 섭취함으로써 발생한다고 알려져 있다. 하지만 최근에는 ferroportin 유전자 SLC4OA1의 Q248H 돌연변이와 연관이 있다는 보고가 있다[6].
여분의 철은 transferrin과 결합하거나 그물내피계통(reticuloendothelial system)의 대식세포나 간세포에 ferritin 형태로 저장된다. 철 독성은 산소 분자와 반응하는 철의 능력에 기인한다. Transferrin은 주된 세포외 철 결합 단백질이다. 철은 transferrin과 결합하게 되면 분자의 구조적 변화를 일으켜서 철은 분자 내부에 격리되므로 독성 산화환원 반응이 일어나지 않게 된다[7]. 하지만 철이 더 축적되어 transferrin이 포화되면 혈청 내에 non-transferrin bound iron(NTBI)이 생성된다. NTBI의 산화환원 반응 부분은 labile plasma iron으로 알려져 있는데, 새포 내 섭취(endocytosis)에 의해 빠르게 세포 내로 들어간다. NTBI는 L-type calcium channels, ZIP14, and divalent metal transporter를 통하여 간, 심장, 뇌, 췌장과 같은 여러 장기에 축적된다[8,9]. 세포질 내의 과도한 철은 Fenton and Haber-Weiss 반응을 통하여 반응산소종(reactive oxygen species)을 생성한다. 반응산소종이 증가하면 사립체(mitochondria) 손상, 지질의 과산화(peroxidation), 세포막 손상, 전자 전달 체계의 중단을 초래한다. 시간이 지나면 해당 장기의 세포자멸사(apoptosis)를 유발한다[10]. 최근 연구에서 반응산소종은 산화질소(nitric oxide)의 생성을 저해하고 혈관벽의 손상을 일으킬 수도 있다는 것을 시사한다[11]. 결과적으로 만성 철과잉은 심근병증, 간경화, 내분비 병증, 관절염 등 다중 장기 손상을 초래한다.
심장 침범은 철과잉의 예후를 결정하는 데 중요한 인자이다[12]. 심장의 비대 및 확장이 흔하다. 분명한 심부전이 없더라도 비정상적인 심기능이 발생할 수 있다[13]. 수혈을 받으면서 철 킬레이트화 치료를 시행하지 않을 경우 심부전은 평균적으로 10년 정도 후에 발생한다[14]. 철 킬레이트화 치료는 심장 변화를 반전시켜서 기능을 향상시킨다[15]. β-thalassemia의 동물 모델에서 심근에 철 침착이 의미 있는 수준이 되기 이전에 이미 사이질 섬유화(interstitial fibrosis)와 재형성 등 심근 손상이 관찰된다. 이를 보면 심부전을 일으키는 추가적인 병리적 과정이 thalassemia에서 존재할 수 있다는 것을 의미한다[16].
수혈을 지속적으로 받아 저산소증이 교정되는 thalassemia major 환자보다는 수혈을 덜 받는 thalassemia intermedia 환자에서 폐고혈압이 더 흔하다[17-19]. 수혈 의존성 β-thalassemia major 환자의 3분의 1 이상에서 폐기능 이상이 나타나는데, 이는 철 킬레이트화 치료로 호전이 가능하다[20].
간 침범이 장기간 수혈을 받은 환자에서 흔하다. 초기 간경화 변화는 7세 thalassemia 환자에서도 발견된다[21]. NTBI 전달의 상향조절(upregulation)이 배양된 간세포에서 관찰되며, 체내에서도 유사할 것으로 보인다[22]. 일단 간경화가 발생하면 간세포암의 위험이 증가한다. C형 간염균이 장기간 수혈을 받는 환자에서 흔한데, 최근 연구에서 낫적혈구병(sickle-cell disease) 환자의 약 6%에서 HCV RNA가 확인되었다[23]. C형 간염과 함께 있는 경우에 수혈성 철과잉이 간경화로 진행하는 것을 촉진할 수 있다[24].
철 표지자는 3개 정도 고려할 수 있다; 혈청 철, transferrin saturation (TS), serum ferritin (SF)이 있다. 혈청 철은 그 자체로 철과잉증을 진단하는 데 유용하지 않다. 하지만 TS를 측정하는 데 필요하므로 필수 측정치이다. 철과잉증 진단 철 지표 중 몇몇은 철과잉이 아닌 경우에도 증가할 수 있으며, TS와 SF는 철과잉증이 발생하는 원리에 따라 서로 일치하지 않을 수 있다. Figure 1에서 보면 철과잉증에서 TS와 SF가 증가되는 서로 다른 기전을 표현하고 있다[33].
TS는 혈청 철과 총철결합능(total iron binding capacity)의 비율과 연관된다. 하지만 대부분의 검사실에서 총철결합능을 직접적으로 측정하는 것이 아니라 SF 농도로부터 일정한 값(transferrin 1 mg 당 1.24 또는 1.25배)을 교정한 값으로 구하게 된다[34,35]. 혈청 철의 일간 변화 또는 염증 등에 따라 변동되는 것에 의해 TS도 영향을 받게 되므로 임상적 유용성이 제한적이다[36]. 철과잉이 아닌 상황에서도 간 기능 이상이 있는 경우 간세포 괴사에 의한 혈정 철의 증가와 간 기능 부전에 의한 transferrin의 감소가 발생함에 따라 TS가 증가될 수 있다[36-38]. 하지만 시간이 지남에 따라 이러한 상황은 간경화에 의한 2차 혈철소증(hemosiderosis)의 원인이 될 수 있다[37,39]. 철과잉증에서 SF 증가 이전부터 TS는 일반적으로 증가되어(>50%) 있다. TS는 아스코브산결핍(ascorbic acid deficiency), 선천성 aceruloplasminemia에서 감소될 수 있고, dysmetabolic disorder와 연관된 철과잉증 및 Gaucher 병에서는 정상 수치를 보일 수 있다[40-42].
혈청 ferritin (SF) 수치는 대식세포의 저장철과 대응하여 인체 내 전체 철의 양을 확인하는 데 유용하므로 철과잉증을 확인하는 데 저렴하면서 널리 사용될 수 있는 검사다. 철과잉증에서는 혈청 철의 증가와 함께 TS도 대부분 증가한다. Thalassemia 환자에서 SF가 2,500 µg/L 초과한 경우에는 심장관련 사망률이 80% 이상 증가한다[43]. 유전성 혈색소증에서는 철과잉이 대식세포가 아닌 간세포에 영향을 주므로 SF 수치만으로는 간내 철 농도가 실제보다 낮게 예측될 가능성이 있다[44,45]. 그리고 SF가 급성기반응물질(acute phase reactant)이란 사실을 고려하면 SF가 상승할 수 있는 다른 원인(염증성 질환, 악성 종양, 대사 증후군, 신부전, 간 질환, 과도한 알콜 섭취 등)을 추가로 고려해야 한다[46]. 따라서 SF를 평가할 때에는 C-반응 단백질과 같은 염증 표지자를 함께 검사해야 한다. 또한 한 번의 검사 수치가 아닌 SF의 시간에 따른 경향을 보는 것이 중요하다[47,48]. SF는 일반적으로 체내 저장철의 양과 연관이 있으나 철과잉과 관련된 아스코브산결핍에서는 감소하거나, 간세포 괴사, 과음 또는 바이러스 감염 등에서는 체내 저장철의 양과 상관없이 증가하기도 한다[38,49]. 의미 있는 정도의 철과잉을 유발하는 정확한 수혈 횟수는 환자의 기저 질환 및 수혈 의존성의 기간에 따라 달라진다. 장기적인 수혈이 필요한 MDS 환자에서 21 단위의 적혈구 수혈 후에는 SF 중위 수치가 1,000 µg/L에 이른다[50]. 유전성 혈색소증에서 SF가 1,000 µg/L을 넘게 되면 간 손상(섬유화 또는 경화)의 가능성이 있고, thalassemia major에서는 SF가 1,000 µg/L을 넘게 되면 철과잉 합병증이 발생할 위험이 높아진다[51,52]. 철과잉증 진단을 위한 알고리즘은 Figure 2와 같다. TS>50% 및 SF 증가된 경우에 철과잉증을 의심하게 된다. 이차성 철과잉을 배제하게 되면 2가지 HFE 유전자 돌연변이에 대한 검사를 시행한다. HFE 유전자의 C282Y 돌연변이의 동형접합(homozygosity) 또는 C282Y/H63D 이형접합(heterozygotes)이 몇몇 예외를 제외하고 유전성 혈색소증과 연관되어 있다[53-56].
자기공명영상(magnetic resonance imaging, MRI)은 간과 심장의 철 침착을 장기간 관찰하는 데 사용된다. 심장 T2* MRI는 심장의 위험도를 예측하는 데 유용하다[57]. 심장 T2*<10 ms인 경우에 심부전의 위험이 증가한다. 심장 T2*<6 ms인 경우에는 12개월 이내에 심부전이 발생할 위험성이 50%를 초과하게 된다[36]. 심장 T2*의 cut off 수치는 다음과 같다. T2*>20 ms 심근 철과잉 없음, T2*<20 ms >8 ms 경도 및 중등도 심근 철과잉, T2*<8 ms 중증 심근 철과잉. 대부분의 지침에서는 심장 및 간 MRI를 매년 실시하는 것을 권장한다.
만약 간 철 농도(liver iron concentration, LIC)가 건체중(dry weight)의 0.15 mg/g 이상이거나 심장 기능 저하가 확인되면 MRI를 6개월마다 실시하는 것이 좋다. 만약 LIC가 정상이라면 MRI 실시 주기를 매 2년 정도로 늦춰볼 수 있다. MRI를 실시할 수 없는 경우에는 간생검을 시행할 수 있으나 부작용 및 출혈의 위험이 있음을 유의해야 한다.
철 킬레이크화 치료의 일차 목표는 수혈로부터 발생하는 철 축적과 철 킬레이트화 치료에 의한 배출을 맞추어 체내 철이 유해한 수준에 도달하지 않도록 예방하는 것이다[58]. NTBI와 간내 축적은 어느 정도 킬레이트화가 되지만, 심장과 같이 다른 장기에 축적된 철은 쉽게 제거되지 않아서 장기적인 수혈을 받은 환자들의 주된 사망 원인으로 심부전이 발생하곤 한다[59]. 철 킬레이트화 치료를 언제 시작할 지는 수혈량, 간과 심장의 철 침착 정도, 장기의 기능 장애 정도, 수혈의 종류, 수혈 의존성 기간 및 기저 질환의 중증도 등에 따라 달라진다[60]. 치료의 성공 여부는 환자의 치료 순응도에 달려있다. 따라서 치료방법을 결정함에 있어 환자 순응도를 높일 수 있는 방향으로 조정해야 한다. 예방적 철 킬레이트화 치료는 임상적으로 심각한 철과잉이 발생하기 전에 시작해야 한다. 대부분의 환자가 빈혈 상태에 있으므로 동정맥절개(phlebotomy)를 치료법으로 고려하지는 않는다. 철 킬레이트화 치료의 시작은 장기 철과잉의 증거가 있는 경우, 즉 100 mL/kg (약 20 단위) 정도의 적혈구 수혈 및 지속적으로 SF>1,000 mcg/L인 경우 이다. DFO, deferiprone과 deferasirox(DFX)가 일반적으로 사용되는 약제이다.
DFO는 수혈성 철과잉증에 1970년대부터 사용된 약제로서 철과잉의 진행 및 조기 사망을 예방할 수 있는 약제이다[61]. DFO는 반감기가 짧으며 경구 복용으로 활성화되지 않으므로 정맥 또는 피하주사를 통하여 지속 주입을 해야 하므로 치료 순응도에 문제가 있다[62]. 인체 내 순환 또는 조직의 철과 복합체를 이룬 후 ferrioxamine의 형태로 주로 소변을 통하여, 3분의 1 정도는 담즙으로 배출하게 된다. 일반적인 용량은 40 mg/kg이지만 체내 철 축적이 많은 경우에는 60 mg/kg까지도 사용한다[63]. 더 높은 용량은 폐 및 신경 독성을 유발할 수 있으므로 피해야 한다. 소아에서는 부작용을 최소화하기 위해 DFO 용량이 25-30 mg/kg를 초과하지 않도록 한다. DFO를 조기에 사용할 경우 체내 철분을 줄이고 당뇨, 심장 질환 및 조기 사망을 줄이는 데 도움이 된다[64]. 또한 DFO는 철과잉증으로 인한 간 섬유화가 간경화로 진행하는 것을 멈추게 해 준다[65]. DFO의 주된 제한점은 짧은 순환 시간으로 인하여 더 자주 주입해야 할 필요성이 있고 뇌, 신장, 근육, 폐와 같은 장기에는 약 침투가 어렵다는 것이다[66].
Deferiprone 1,2 dimethyl-3-hydroxypyridine-4-one은 복용 후 빠르게 흡수되어 45분 후 최대 혈중 농도에 도달하고 간에서 85% 변환되어 빠르게 혈중에서 제거된다[63]. 반감기는 약 2시간이며 불활성 대사 물질은 주로 소변으로 배출된다. 일반적인 시작 용량은 일일 75 mg/kg이지만, 순응도가 좋을 경우에는 일일 100 mg/kg까지 증량 가능하다[67,68]. 복약 순응도 및 심장 철 축적을 줄이는 효과가 DFO에 비해 좋다[69,70].
DFX는 경구용 철 킬레이트화 약제이다. 간세포 및 다른 조직에 흡수되어 2:1의 비율로 철과 결합한다. DFX는 조직내 철을 킬레이트화하여 주로 담즙으로 배출시킨다[71]. DFS의 용량은 일일 20 mg/kg이며, 3-6개월 간격으로 철 저장량에 따라 5-10 mg 증량한다. 철 킬레이트화 약제의 용량은 SF 및 간, 심장 영상검사에 기초하여 적정 수준으로 변경한다. 목표는 SF 1,000 ng/mL 미만, 심장T2* <20 ms, LIC <3 mg/g dry weight 이다[52,72,73]. 임신 및 수유 중인 환자는 철 킬레이트화 치료를 피해야 한다[74]. DFX 단일 요법으로 심장 및 간 철과잉증에 효과가 있다는 것이 확인되었다[75,76]. 일주일에 5회 이상 평균적으로 51 mg/kg 용량의 DFX를 사용할 경우 LIC를 6.4 mg/g dry weight 정도 낮춘다[77]. DFX 일일 평균 용량 30 mg/kg은 LIC를 3.1에서 7.8 mg/g dry weight 정도 낮춘다[78]. 국내에서 혈액질환자 중 수혈성 철과잉증 치료에 DFX를 사용하는 임상연구를 진행하여 SF가 치료 후에 의미 있는 수준으로 감소함을 확인하였다[79].
2013년에 대한혈액학회에서 수혈성 철과잉증의 철 킬레이트화 치료에 대한 한국 진료 지침을 발표하였다[80]. 국내 진료 지침의 중요한 사항은 Table 3에 요약되어 있다[80]. 수혈 의존성 환자들(MDS, 재생불량빈혈, 순수적혈구 무형성증, 골수섬유화증 등)은 철 킬레이트화 치료가 필요하다. 적혈구 수혈을 8단위 이상 받았으며, 최소 2번 연속 검사에서 SF>1,000 ng/mL인 경우를 철 킬레이트화 치료가 필요한 수혈 의존성이라고 규정한다. 한국 진료 지침 발표 후 개정된 보험 규정에는 농축 적혈구 약 20단위(100 mL/kg과 동등) 수혈 이후 또는 임상모니터링 결과 만성 철분 축적의 임상증거가 있을 때(혈청 ferritin >1,000 μg/L 또는 간내철분농도 >2 mg Fe/g dry weight) 시작하는 것으로 변경되었다. 철 킬레이션 치료 대상 환자의 예상 여명이 1년 이상이어야 한다. 철과잉증인 한국 환자들에게는 경구 DFX을 권장한다. 권장 초기 용량은 DFX 20 (필름 코팅정의 경우에는 14) mg/kg body weight로 음식 섭취 최소 30분 전 공복 상태에서 물, 오렌지쥬스 또는 사과쥬스에 확산하여(필름 코팅정의 경우에는 물과 함께 통째로 삼켜야 하며 정제를 삼키기 어려운 환자는 이 약을 부수어 요거트나 사과 퓨레 같은 부드러운 음식에 뿌려 전체를) 복용한다. 철 킬레이트화 치료를 시작한 후에 첫 3개월에는 매달, 그 이후로는 최소 3개월 간격으로 SF와 심장, 간 및 신장 기능을 포함한 장기 기능을 확인한다. SF는 1,000 ng/mL 미만으로 유지할 것을 권장하며 철 킬레이트화 치료를 시작한 후에 SF가 지속적으로 상승하면 DFX 용량을 30(필름 코팅정의 경우에는 21) mg/kg/day으로 증량한다. 2번 연속 검사에서 SF<500 ng/mL 인 경우에는 철 킬레이트화 치료를 중단하고 SF>1,000 ng/mL으로 다시 증가하는 경우에는 DFX를 동일한 용량으로 다시 시작한다.
Acknowledgement
This study was supported by the Shinpoong Pharmaceutical Company for a clinical trial for iron chelation treatment in chronic anemia patients with transfusional iron overload.
Figure 1.
Schematic representation of the different causes leading to high transferrin saturation and/or serum ferritin values increase in iron overload disorders. Adapted from Piperno A. Haematologica 1998; 83:447-455, according to the Creative Commons license [33]. RE, reticuloendothelial.
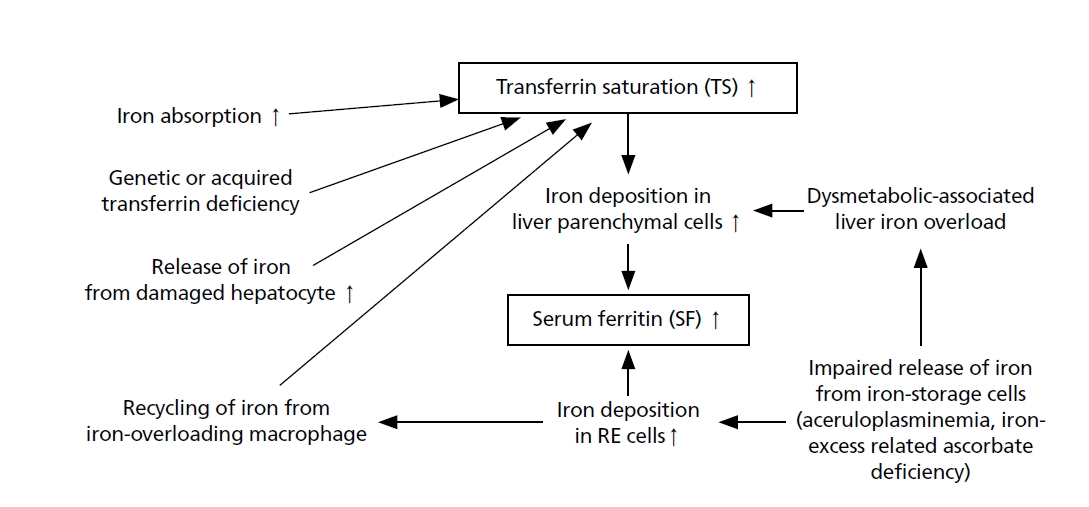
Figure 2.
Algorithm for the diagnosis of iron overload. TS, transferrin saturation; SF, serum ferritin; LIC, liver iron concentration. Illlustrated by the author.
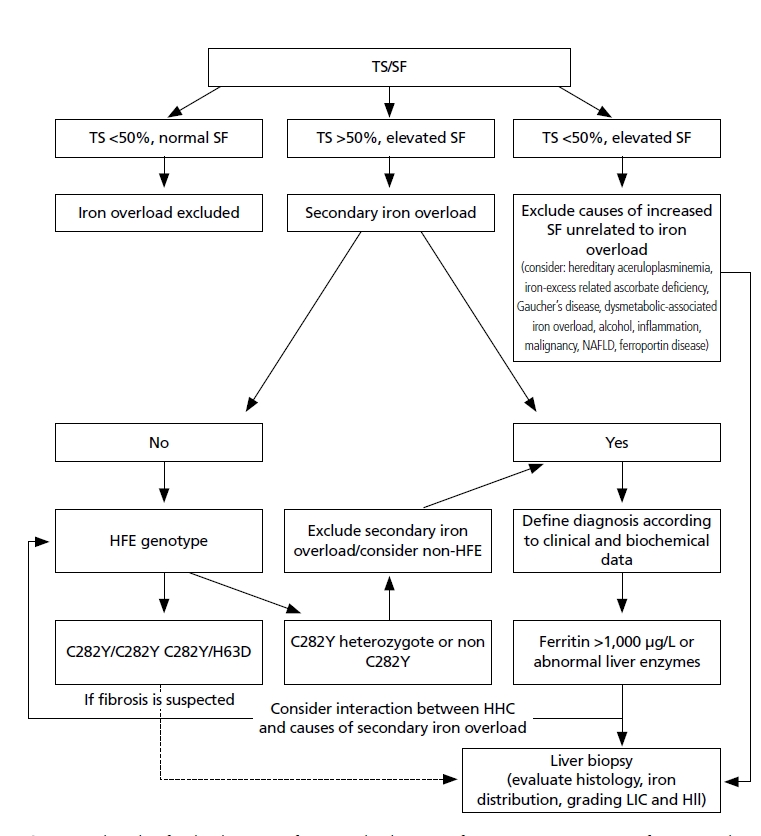
Table 1.
Classification of iron overload
Table 2.
Baseline investigations, toxicity monitoring and efficacy monitoring
Table 3.
Korean guideline for iron overload.
Adapted from Jang JH et al. J Korean Med Sci 2013;28:1563-1572, according to the Creative Commons license [80].
MDS, myelodysplastic syndrome.
References
1. Yiannikourides A, Latunde-Dada GO. A short review of iron metabolism and pathophysiology of iron disorders. Medicines (Basel) 2019;6:85.



2. Cook JD, Flowers CH, Skikne BS. The quantitative assessment of body iron. Blood 2003;101:3359-3364.



3. Camaschella C, Nai A, Silvestri L. Iron metabolism and iron disorders revisited in the hepcidin era. Haematologica 2020;105:260-272.



4. Siddique A, Kowdley KV. Review article: the iron overload syndromes. Aliment Pharmacol Ther 2012;35:876-893.


6. McNamara L, Gordeuk VR, MacPhail AP. Ferroportin (Q248H) mutations in African families with dietary iron overload. J Gastroenterol Hepatol 2005;20:1855-1858.


8. Abbasi U, Abbina S, Gill A, Takuechi LE, Kizhakkedathu JN. Role of iron in the molecular pathogenesis of diseases and therapeutic opportunities. ACS Chem Biol 2021;16:945-972.


9. Coates TD. Physiology and pathophysiology of iron in hemoglobin-associated diseases. Free Radic Biol Med 2014;72:23-40.



10. Gordan R, Wongjaikam S, Gwathmey JK, Chattipakorn N, Chattipakorn SC, Xie LH. Involvement of cytosolic and mitochondrial iron in iron overload cardiomyopathy: an update. Heart Fail Rev 2018;23:801-816.




11. Marques VB, Nascimento TB, Ribeiro RF Jr, Broseghini-Filho GB, Rossi EM, Graceli JB, dos Santos L. Chronic iron overload in rats increases vascular reactivity by increasing oxidative stress and reducing nitric oxide bioavailability. Life Sci 2015;143:89-97.


12. Olivieri NF, Nathan DG, MacMillan JH, Wayne AS, Liu PP, McGee A, Martin M, Koren G, Cohen AR. Survival in medically treated patients with homozygous beta-thalassemia. N Engl J Med 1994;331:574-578.


13. Suarez WA, Snyder SA, Berman BB, Brittenham GM, Patel CR. Preclinical cardiac dysfunction in transfusion-dependent children and young adults detected with low-dose dobutamine stress echocardiography. J Am Soc Echocardiogr 1998;11:948-956.


14. Wolfe L, Olivieri N, Sallan D, Colan S, Rose V, Propper R, Freedman MH, Nathan DG. Prevention of cardiac disease by subcutaneous deferoxamine in patients with thalassemia major. N Engl J Med 1985;312:1600-1603.


15. Cantinieaux B, Janssens A, Boelaert JR, Lejeune M, Vermylen C, Kerrels V, Cornu G, Winand J, Fondu P. Ferritin-associated iron induces neutrophil dysfunction in hemosiderosis. J Lab Clin Med 1999;133:353-361.


16. Stoyanova E, Cloutier G, Felfly H, Lemsaddek W, Ah-Son N, Trudel M. Evidence for a novel mechanism independent of myocardial iron in β-thalassemia cardiac pathogenesis. PLoS One 2012;7:e52128.



17. El-Beshlawy A, Youssry I, El-Saidi S, El Accaoui R, Mansi Y, Makhlouf A, Taher A. Pulmonary hypertension in beta-thalassemia major and the role of L-carnitine therapy. Pediatr Hematol Oncol 2008;25:734-743.

18. Tam DH, Farber HW. Pulmonary hypertension and beta-thalassemia major: report of a case, its treatment, and a review of the literature. Am J Hematol 2006;81:443-447.


19. Voskaridou E, Tsetsos G, Tsoutsias A, Spyropoulou E, Christoulas D, Terpos E. Pulmonary hypertension in patients with sickle cell/beta thalassemia: incidence and correlation with serum N-terminal pro-brain natriuretic peptide concentrations. Haematologica 2007;92:738-743.


20. Piatti G, Allegra L, Fasano V, Gambardella C, Bisaccia M, Cappellini MD. Lung function in beta-thalassemia patients: a longitudinal study. Acta Haematol 2006;116:25-29.



21. Jean G, Terzoli S, Mauri R, Borghetti L, Di Palma A, Piga A, Magliano M, Melevendi M, Cattaneo M. Cirrhosis associated with multiple transfusions in thalassaemia. Arch Dis Child 1984;59:67-70.



22. Liuzzi JP, Aydemir F, Nam H, Knutson MD, Cousins RJ. Zip14 (Slc39a14) mediates non-transferrin-bound iron uptake into cells. Proc Natl Acad Sci U S A 2006;103:13612-13617.



23. Mawuli G, Dzudzor B, Tachi K, Kuma AAB, Odame-Aboagye J, Obeng BM, Boateng AT, Edu-Quansah EP, Attiku KO, Agbosu E, Arjarquah A, Bonney JHK. Hepatitis C virus (HCV) infection among patients with sickle cell disease at the Korle-Bu teaching hospital. Virol J 2022;19:73.




24. Hassan M, Hasan S, Giday S, Alamgir L, Banks A, Frederick W, Smoot D, Castro O. Hepatitis C virus in sickle cell disease. J Natl Med Assoc 2003;95:939-942.


25. Moayeri H, Oloomi Z. Prevalence of growth and puberty failure with respect to growth hormone and gonadotropins secretion in beta-thalassemia major. Arch Iran Med 2006;9:329-334.

26. He LN, Chen W, Yang Y, Xie YJ, Xiong ZY, Chen DY, Lu D, Liu NQ, Yang YH, Sun XF. Elevated prevalence of abnormal glucose metabolism and other endocrine disorders in patients with β-thalassemia major: a meta-analysis. Biomed Res Int 2019;2019:6573497.


27. De Sanctis V, Roos M, Gasser T, Fortini M, Raiola G, Galati MC; Italian Working Group on Endocrine Complications in Non-Endocrine Diseases. Impact of long-term iron chelation therapy on growth and endocrine functions in thalassaemia. J Pediatr Endocrinol Metab 2006;19:471-480.


28. Gao C, Li L, Chen B, Song H, Cheng J, Zhang X, Sun Y. Clinical outcomes of transfusion-associated iron overload in patients with refractory chronic anemia. Patient Prefer Adherence 2014;8:513-517.


29. Chirio R, Collignon A, Sabbah L, Lestradet H, Torlotin JC. Yersinia enterocolitica infections and thalassemia major in children. Ann Pediatr (Paris) 1989;36:308-4.

30. Bergmann TK, Vinding K, Hey H. Multiple hepatic abscesses due to Yersinia enterocolitica infection secondary to primary haemochromatosis. Scand J Gastroenterol 2001;36:891-895.


31. Chiu HY, Flynn DM, Hoffbrand AV, Politis D. Infection with Yersinia enterocolitica in patients with iron overload. Br Med J (Clin Res Ed) 1986;292:97.

32. Karimi M, Jamalian N, Rasekhi A, Kashef S. Magnetic resonance imaging (MRI) findings of joints in young beta-thalassemia major patients: fluid surrounding the scaphoid bone: a novel finding, as the possible effect of secondary hemochromatosis. J Pediatr Hematol Oncol 2007;29:393-398.

35. Tsung SH, Rosenthal WA, Milewski KA. Immunological measurement of transferrin compared with chemical measurement of total iron-binding capacity. Clin Chem 1975;21:1063-1066.



37. Deugnier Y, Turlin B, le Quilleuc D, Moirand R, Loreal O, Messner M, Meunier B, Brissot P, Launois B. A reappraisal of hepatic siderosis in patients with end-stage cirrhosis: practical implications for the diagnosis of hemochromatosis. Am J Surg Pathol 1997;21:669-675.


38. Bonkovsky HL, Banner BF, Lambrecht RW, Rubin RB. Iron in liver diseases other than hemochromatosis. Semin Liver Dis 1996;16:65-82.


39. Kaplan J, Craven C, Alexander J, Kushner J, Lamb J, Bernstein S. Regulation of the distribution of tissue iron: lessons learned from the hypotransferrinemic mouse. Ann N Y Acad Sci 1988;526:124-135.

40. Yoshida K, Furihata K, Takeda S, Nakamura A, Yamamoto K, Morita H, Hiyamuta S, Ikeda S, Shimizu N, Yanagisawa N. A mutation in the ceruloplasmin gene is associated with systemic hemosiderosis in humans. Nat Genet 1995;9:267-272.



41. Moirand R, Mortaji AM, Loreal O, Paillard F, Brissot P, Deugnier Y. A new syndrome of liver iron overload with normal transferrin saturation. Lancet 1997;349:95-97.


42. Lee RE, Balcerzak SP, Westerman MP. Gaucher’s disease: a morphologic study and measurements of iron metabolism. Am J Med 1967;42:891-898.

43. Wood JC. Diagnosis and management of transfusion iron overload: the role of imaging. Am J Hematol 2007;82((12 Suppl):1132-1135.



44. Taher A, El Rassi F, Isma'eel H, Koussa S, Inati A, Cappellini MD. Correlation of liver iron concentration determined by R2 magnetic resonance imaging with serum ferritin in patients with thalassemia intermedia. Haematologica 2008;93:1584-1586.


45. Origa R, Galanello R, Ganz T, Giagu N, Maccioni L, Faa G, Nemeth E. Liver iron concentrations and urinary hepcidin in beta-thalassemia. Haematologica 2007;92:583-588.


46. Cullis JO, Fitzsimons EJ, Griffiths WJ, Tsochatzis E, Thomas DW; British Society for Haematology. Investigation and management of a raised serum ferritin. Br J Haematol 2018;181:331-340.



47. Taher AT, Saliba AN. Iron overload in thalassemia: different organs at different rates. Hematology Am Soc Hematol Educ Program 2017;2017:265-271.




48. Telfer PT, Prestcott E, Holden S, Walker M, Hoffbrand AV, Wonke B. Hepatic iron concentration combined with long-term monitoring of serum ferritin to predict complications of iron overload in thalassaemia major. Br J Haematol 2000;110:971-977.



49. Chapman RW, Hussain MA, Gorman A, Laulicht M, Politis D, Flynn DM, Sherlock S, Hoffbrand AV. Effect of ascorbic acid deficiency on serum ferritin concentration in patients with beta-thalassaemia major and iron overload. J Clin Pathol 1982;35:487-491.



50. Malcovati L, Porta MG, Pascutto C, Invernizzi R, Boni M, Travaglino E, Passamonti F, Arcaini L, Maffioli M, Bernasconi P, Lazzarino M, Cazzola M. Prognostic factors and life expectancy in myelodysplastic syndromes classified according to WHO criteria: a basis for clinical decision making. J Clin Oncol 2005;23:7594-7603.


51. Deugnier YM, Loréal O, Turlin B, Guyader D, Jouanolle H, Moirand R, Jacquelinet C, Brissot P. Liver pathology in genetic hemochromatosis: a review of 135 homozygous cases and their bioclinical correlations. Gastroenterology 1992;102:2050-2059.


52. Olivieri NF, Brittenham GM. Iron-chelating therapy and the treatment of thalassemia. Blood 1997;89:739-761.



53. Feder JN, Gnirke A, Thomas W, Tsuchihashi Z, Ruddy DA, Basava A, Dormishian F, Domingo R Jr, Ellis MC, Fullan A, Hinton LM, Jones NL, Kimmel BE, Kronmal GS, Lauer P, Lee VK, Loeb DB, Mapa FA, McClelland E, Meyer NC, Mintier GA, Moeller N, Moore T, Morikang E, Prass CE, Quintana L, Starnes SM, Schatzman RC, Brunke KJ, Drayna DT, Risch NJ, Bacon BR, Wolff RK. A novel MHC class I-like gene is mutated in patients with hereditary haemochromatosis. Nat Genet 1996;13:399-408.



54. Beutler E. The significance of the 187G (H63D) mutation in hemochromatosis. Am J Hum Genet 1997;61:762-764.



55. Carella M, D'Ambrosio L, Totaro A, Grifa A, Valentino MA, Piperno A, Girelli D, Roetto A, Franco B, Gasparini P, Camaschella C. Mutation analysis of the HLA-H gene in Italian hemochromatosis patients. Am J Hum Genet 1997;60:828-832.


56. Jouanolle AM, Gandon G, Jezequel P, Blayau M, Campion ML, Yaouanq J, Mosser J, Fergelot P, Chauvel B, Bouric P, Carn G, Andrieux N, Gicquel I, Le Gall JY, David V. Haemochromatosis and HLA-H. Nat Genet 1996;14:251-252.



57. Anderson LJ, Holden S, Davis B, Prescott E, Charrier CC, Bunce NH, Firmin DN, Wonke B, Porter J, Walker JM, Pennell DJ. Cardiovascular T2-star (T2*) magnetic resonance for the early diagnosis of myocardial iron overload. Eur Heart J 2001;22:2171-2179.


58. Porter JB. Concepts and goals in the management of transfusional iron overload. Am J Hematol 2007;82((12 Suppl):1136-1139.


59. Borgna-Pignatti C, Rugolotto S, De Stefano P, Zhao H, Cappellini MD, Del Vecchio GC, Romeo MA, Forni GL, Gamberini MR, Ghilardi R, Piga A, Cnaan A. Survival and complications in patients with thalassemia major treated with transfusion and deferoxamine. Haematologica 2004;89:1187-1193.

60. Porter JB, Shah FT. Iron overload in thalassemia and related conditions: therapeutic goals and assessment of response to chelation therapies. Hematol Oncol Clin North Am 2010;24:1109-1130.


61. Pippard MJ, Callender ST, Weatherall DJ. Intensive iron-chelation therapy with desferrioxamine in iron-loading anaemias. Clin Sci Mol Med 1978;54:99-106.



62. Cappellini MD, Bejaoui M, Agaoglu L, Porter J, Coates T, Jeng M, Lai ME, Mangiagli A, Strauss G, Girot R, Watman N, Ferster A, Loggetto S, Abish S, Cario H, Zoumbos N, Vichinsky E, Opitz H, Ressayre-Djaffer C, Abetz L, Rofail D, Baladi JF. Prospective evaluation of patient-reported outcomes during treatment with deferasirox or deferoxamine for iron overload in patients with beta-thalassemia. Clin Ther 2007;29:909-917.

63. Hoffbrand AV, Taher A, Cappellini MD. How I treat transfusional iron overload. Blood 2012;120:3657-3669.



64. Brittenham GM, Griffith PM, Nienhuis AW, McLaren CE, Young NS, Tucker EE, Allen CJ, Farrell DE, Harris JW. Efficacy of deferoxamine in preventing complications of iron overload in patients with thalassemia major. N Engl J Med 1994;331:567-573.


65. Kushner JP, Porter JP, Olivieri NF. Secondary iron overload. Hematology Am Soc Hematol Educ Program 2001;2001:47-61.


66. Kang H, Han M, Xue J, Baek Y, Chang J, Hu S, Nam H, Jo MJ, El Fakhri G, Hutchens MP, Choi HS, Kim J. Renal clearable nanochelators for iron overload therapy. Nat Commun 2019;10:5134.




67. Wonke B, Wright C, Hoffbrand AV. Combined therapy with deferiprone and desferrioxamine. Br J Haematol 1998;103:361-364.



68. Taher A, Sheikh-Taha M, Sharara A, Inati A, Koussa S, Ellis G, Dhillon AP, Hoffbrand AV. Safety and effectiveness of 100 mg/kg/vday deferiprone in patients with thalassemia major: a two-year study. Acta Haematol 2005;114:146-149.



69. Hoffbrand AV, Cohen A, Hershko C. Role of deferiprone in chelation therapy for transfusional iron overload. Blood 2003;102:17-24.



70. Anderson LJ, Wonke B, Prescott E, Holden S, Walker JM, Pennell DJ. Comparison of effects of oral deferiprone and subcutaneous desferrioxamine on myocardial iron concentrations and ventricular function in beta-thalassaemia. Lancet 2002;360:516-520.


71. Waldmeier F, Bruin GJ, Glaenzel U, Hazell K, Sechaud R, Warrington S, Porter JB. Pharmacokinetics, metabolism, and disposition of deferasirox in beta-thalassemic patients with transfusion-dependent iron overload who are at pharmacokinetic steady state. Drug Metab Dispos 2010;38:808-816.


72. Aydinok Y, Kattamis A, Viprakasit V. Current approach to iron chelation in children. Br J Haematol 2014;165:745-755.


74. Brittenham GM. Iron-chelating therapy for transfusional iron overload. N Engl J Med 2011;364:146-156.



75. Pennell DJ, Porter JB, Cappellini MD, El-Beshlawy A, Chan LL, Aydinok Y, Elalfy MS, Sutcharitchan P, Li CK, Ibrahim H, Viprakasit V, Kattamis A, Smith G, Habr D, Domokos G, Roubert B, Taher A. Efficacy of deferasirox in reducing and preventing cardiac iron overload in beta-thalassemia. Blood 2010;115:2364-2371.

76. Aydinok Y, Ulger Z, Nart D, Terzi A, Cetiner N, Ellis G, Zimmermann A, Manz C. A randomized controlled 1-year study of daily deferiprone plus twice weekly desferrioxamine compared with daily deferiprone monotherapy in patients with thalassemia major. Haematologica 2007;92:1599-1606.


77. Cappellini MD, Cohen A, Piga A, Bejaoui M, Perrotta S, Agaoglu L, Aydinok Y, Kattamis A, Kilinc Y, Porter J, Capra M, Galanello R, Fattoum S, Drelichman G, Magnano C, Verissimo M, Athanassiou-Metaxa M, Giardina P, KourakliSymeonidis A, Janka-Schaub G, Coates T, Vermylen C, Olivieri N, Thuret I, Opitz H, Ressayre-Djaffer C, Marks P, Alberti D. A phase 3 study of deferasirox (ICL670), a once-daily oral iron chelator, in patients with beta-thalassemia. Blood 2006;107:3455-3462.


78. Cappellini MD, Bejaoui M, Agaoglu L, Canatan D, Capra M, Cohen A, Drelichman G, Economou M, Fattoum S, Kattamis A, Kilinc Y, Perrotta S, Piga A, Porter JB, Griffel L, Dong V, Clark J, Aydinok Y. Iron chelation with deferasirox in adult and pediatric patients with thalassemia major: efficacy and safety during 5 years’ follow-up. Blood 2011;118:884-893.



79. Kim IH, Moon JH, Lim SN, Sohn SK, Kim HG, Lee GW, Kim YS, Lee HS, Kwon KY, Kim SH, Park KT, Chung JS, Lee WS, Lee SM, Hyun MS, Kim H, Ryoo HM, Bae SH, Joo YD. Efficacy and safety of deferasirox estimated by serum ferritin and labile plasma iron levels in patients with aplastic anemia, myelodysplastic syndrome, or acute myeloid leukemia with transfusional iron overload. Transfusion 2015;55:1613-1620.


Peer Reviewers’ Commentary
이 논문은 고령화와 의학의 발전으로 만성적으로 수혈이 필요한 골수부전증후군 환자들이 증가하면서 수혈의 장기적 합병증인 수혈성 철과잉증의 기전과 임상 양상, 진단과 치료법에 대한 최신 문헌을 정리하여 상세히 설명해 주고 있다. 과도한 철의 축적은 non-transferrin bound iron, labile plasma iron, 반응산소종 증가로 이어지고, 이는 심근, 간, 내분비계 등의 손상과 기능장애의 원인이 된다. 지중해빈혈, 골수형성이상증후군을 비롯한 혈액 질환 환자의 경우 비효율적인 적혈구 형성으로 인해 그 자체로 철과잉이 발생할 수도 있고, 빈혈을 교정하기 위한 적혈구 수혈도 철과잉을 야기하므로 주된 철분 과잉 치료의 대상이 된다. 수혈성 철과잉증의 철킬레이트화 치료에 대한 대한혈액학회의 진료지침을 자세히 설명하고 있다. 이 논문은 임상 현장에서 철분 과잉의 원인, 치료의 필요성, 철분 과잉 치료의 실제를 이해하는 데 많은 도움을 줄 것으로 판단된다.
[정리: 편집위원회]
-
METRICS

-
Related articles in
J Korean Med Assoc -
Diagnosis and management of sarcopenia2024 July;67(7)
Diagnosis and management of frailty2024 July;67(7)
Diagnosis and treatment of dyslipidemia in children and adolescents2024 May;67(5)
Diagnosis and treatment of dysphagia2023 October;66(10)
Diagnosis and treatment of adult spinal deformity2023 August;66(8)






