|
 |
- Search
| J Korean Med Assoc > Volume 66(5); 2023 > Article |
|
Abstract
Background: Targeted temperature management is a treatment strategy to lower core body temperature to achieve neuroprotection or reduce elevated intracranial pressure. Therefore, it has been increasingly used in the neurointensive care unit to manage various types of acute neurologic injuries.
Current Concepts: Targeted temperature management can be divided into three distinct phases, including induction, maintenance, and rewarming, and each phase has risks and predictable complications. In patients with acute neurocritical illnesses, including traumatic brain injury, subarachnoid hemorrhage, intracranial hemorrhage, and ischemic stroke, brain edema is a potentially life-threatening complication as it raises the intracranial pressure, leading to brain herniation and permanent neurological damage. In this sense, targeted temperature management can be considered the final strategy for medical treatment for controlling an intracranial pressure crisis in patients with severe brain injury.
Discussion and Conclusion: In the neurointensive care unit, applying targeted temperature management to patients with severe brain injuries may be challenging. Targeted temperature management in critically ill neurological patients is associated with an increased risk of systemic complications, as hypothermia is prolonged, requiring a comprehensive patient-by-patient assessment of the advantages and disadvantages of treatment. Except for cerebral pressure management, analyses of targeted temperature management in patients with traumatic brain injury and subarachnoid hemorrhage remain controversial regarding its effect on prognosis. Targeted temperature management should be reserved for selective patients, and further studies are needed to improve the efficacy of hypothermia for individual conditions, including intracerebral hemorrhage and ischemic stroke.
Current Concepts: Targeted temperature management can be divided into three distinct phases, including induction, maintenance, and rewarming, and each phase has risks and predictable complications. In patients with acute neurocritical illnesses, including traumatic brain injury, subarachnoid hemorrhage, intracranial hemorrhage, and ischemic stroke, brain edema is a potentially life-threatening complication as it raises the intracranial pressure, leading to brain herniation and permanent neurological damage. In this sense, targeted temperature management can be considered the final strategy for medical treatment for controlling an intracranial pressure crisis in patients with severe brain injury.
Discussion and Conclusion: In the neurointensive care unit, applying targeted temperature management to patients with severe brain injuries may be challenging. Targeted temperature management in critically ill neurological patients is associated with an increased risk of systemic complications, as hypothermia is prolonged, requiring a comprehensive patient-by-patient assessment of the advantages and disadvantages of treatment. Except for cerebral pressure management, analyses of targeted temperature management in patients with traumatic brain injury and subarachnoid hemorrhage remain controversial regarding its effect on prognosis. Targeted temperature management should be reserved for selective patients, and further studies are needed to improve the efficacy of hypothermia for individual conditions, including intracerebral hemorrhage and ischemic stroke.
목표체온유지치료(targeted temperature management)는 보통 유도저체온요법(induced hypothermia therapy)이라고 하며, 환자의 심부 체온을 특정 온도로 조절하는 치료를 통칭한다. 두개내압(intracranial pressure)이 상승하였을 때에는 정상 체온보다 낮은 32-35℃로 체온을 유지하여 뇌와 전신의 신진대사 및 산소 소비량을 감소시켜 뇌세포를 보호하는 치료 전략이다[1]. 이러한 목표체온유지치료는 성인 심정지 환자의 뇌손상을 최소화하여 생존율을 높이고 신경학적 예후를 개선하며[2,3], 신생아 저산소 허혈뇌손상에서도 뇌신경 보호효과를 입증하였다[4,5].
최근 목표체온유지치료는 신경계중환자실 영역에서 허혈성 및 출혈성 뇌졸중을 비롯해 외상성뇌손상(traumatic brain injury), 뇌전증 지속 환자들의 치료에도 적용이 확대되고 있다[6,7]. 신경계 중환자 치료에서 중요한 점은 뇌졸중이나 외상 등 일차 뇌손상을 최소화하고, 동반된 뇌부종(brain edema) 및 두개내압 상승에 의한 이차 뇌손상을 예방하는 것인데, 이러한 측면에서 목표체온유지치료는 뇌신경 보호효과를 포함한 뇌부종 및 두개내압 상승을 억제하는 데에도 효과적이기 때문이다[8].
다만 목표체온유지치료는 체온이 낮아질수록 신체 전반의 다양한 생리적인 변화들과 함께 감염 위험 증가, 전해질 불균형, 인슐린 저항성 증가, 응고 병증, 오한(shivering) 등의 합병증 발생의 위험이 증가하여 주의가 필요하다[9]. 특히 심정지 소생후 치료(post cardiac arrest care)를 시행할 때에는 목표체온유지치료의 총 기간이 48시간 내외로 비교적 짧지만, 신경계 중환자에서 뇌부종 및 뇌압 관리를 위해 목표체온유지치료를 시행할 경우 약 1-2주 이상의 치료기간이 필요한 경우들이 많기 때문에[10], 부작용을 최소화하면서도 효과를 극대화할 수 있는 전략들을 개발하는 연구들이 현재 활발하게 진행되고 있다.
이러한 관점에서 이 논문에서는 신경계 중환자실에서 시행되는 목표체온유지치료의 방법, 부작용 및 신경계 중환자들에 대한 적응증에 대한 내용을 소개하고자 한다.
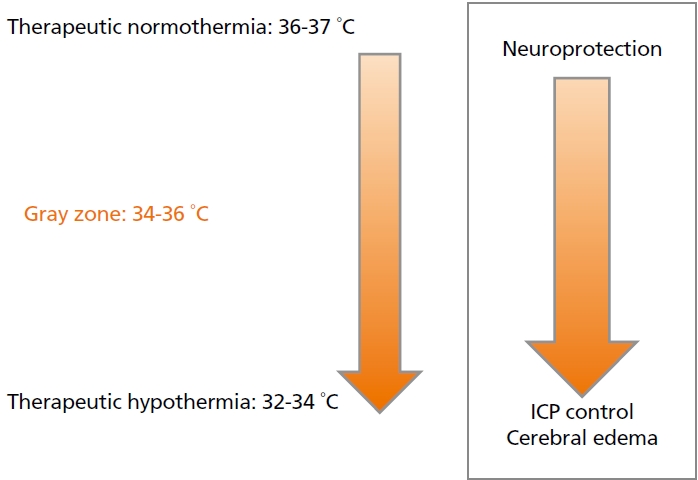
목표체온유지치료로 체온을 낮추면 뇌대사 감소, 신경보호효과, 혈액뇌장벽보호 등에서 효과가 있으며[11], 특히 체온이 1°C 낮아질 때마다 뇌대사는 약 6% 정도 감소되고, 뇌대사의 감소는 대사-뇌혈류의 커플링(coupling) 작용을 통해 뇌혈류를 감소시켜 두개내압을 낮추게 된다[12]. 하지만 통상적으로 심부 체온이 30-32℃ 이하가 되면 저칼륨혈증, 부정맥(심방세동, 심실세동, 심실빈맥), 심박출계수의 저하, 신기능의 변화, 감염의 증가, 혈액 응고장애, 젖산산혈증, 고혈당증, 췌장염, 혈소판감소 등의 부작용이 발생하기 때문에[8], 현재 통용되고 있는 치료적인 저체온의 허용범위는 32-34°C로 제안하고 있다. 다만 신경계 중환자실에서 두개내압 상승으로 인해 시행하는 저체온 치료는 치료 유지지간이 통상적인 치료에 비해 매우 길어질 수 있기에, 유지기간에 비례하여 증가되는 전신 합병증의 위험도를 감안하여, 기본적인 뇌보호효과와 함께 뇌압상승 및 뇌부종에 대한 효과도 가지면서 부작용은 최소화하여 장기간 유지가 가능한 적정 목표 온도를 일종의 gray zone을 포함한 범위에서 찾기 위한 노력들이 지속되고 있다(Figure 1).
목표체온유지치료로 체온을 낮추는 과정은 저체온 유도(induction), 유지(maintenance), 및 재가온(rewarming)의 세 단계로 구분할 수 있고, 각 시기별로 저체온 유지에 따른 전신적인 합병증이 발생할 수 있다(Figure 2) [13].
먼저 유도기는 체온을 목표 체온(대개 32-34℃)까지 낮추는 단계이며, 이 시기에서는 최대한 신속히 목표 체온에 도달하도록 한다. 이를 위해, 체온 조절장치의 냉각 속도를 최대치로 설정하면서, 약 4°C 정도로 냉장 보관된 생리식염수를 20-30 mL/kg 정도 신속히 정맥주사하면 체온을 빠르게 낮추는 데 도움이 된다. 하지만 과다 투여시 폐부종을 유발할 수 있으므로 주의가 필요하다. 저체온을 유도하는 과정에서 오한이 발생하면 체온 감소에 방해가 되고, 전신 대사량을 상승시켜 환자의 예후를 불량하게 만들 수 있기 때문에, 오한을 적절히 예방하고 조절하는 치료전략이 필요하다[14].
유지 단계는 목표에 도달한 체온을 치료기간 동안 일정하게 유지하는 것이며, 이를 위해 심부 체온의 변동이 최소화되도록 한다. 유지 단계의 적정 기간은 질환에 따라 다른데, 뇌부종이나 뇌압상승의 치료를 목표로 하는 경우, 원인질환의 부종이 감소되는 기간까지 치료가 필요하므로 대략 1주일 이상 유지하는 경우도 많다[15].
재가온 단계는 목표체온을 유지하던 단계에서 정상 체온으로 되돌리는 단계이며, 심정지 환자의 치료에서는 일반적으로 시간당 0.25-0.5℃의 속도로 체온이 서서히 상승하도록 설정하지만[16], 뇌부종과 뇌압상승의 우려가 높은 신경계 중환자 치료에서는 시간당 0.05-0.1°C 의 속도로 천천히 재가온 하도록 권고한다[17]. 재가온 시기에는 그동안 수축되어 있던 뇌혈관 및 전신 혈관이 확장되면서, 뇌혈류가 증가되어 뇌압이 다시 상승할 수 있고, 전신 혈관의 확장으로 인해 저혈압이 발생하면서 뇌관류압 저하로 인해 허혈뇌손상이 악화될 위험성이 높기 때문이다[18].
체온요법을 조절하는 방법은 표면 냉각(surface cooling)과 혈관 내 냉각(endovascular cooling)으로 구분할 수 있다[19]. 표면 냉각법은 냉각된 물이나 공기가 내부적으로 순환되는 냉각 담요나 패드를 환자 피부에 밀착시켜 열전도(conduction)에 의해 체온을 낮추는 방법이고, 혈관 내 냉각법은 쇄골하정맥이나 하대정맥 등 중심정맥에 냉각 도관을 삽입하여 혈액을 직접 냉각하여 온도를 조절하는 방법이다.
표면 냉각법은 비침습적이고 사용이 편한 장점이 있지만, 체온 강하속도가 다소 느리기 때문에 목표체온에 도달하는 시간이 혈관내 냉각에 비해 조금 더 오래걸리며, 유지 단계에서는 목표체온의 상하로 체온변동 폭이 약간 더 큰 경향이 있다.
혈관 내 냉각법은 목표체온을 안정적으로 유지할 수 있고, 표면 냉각법에 비해 오한을 덜 유발하는 장점은 있지만, 냉각치료를 시행하기 위해 중심정맥에 체온 조절용 특수 카테터를 삽입해야 하므로 추가적 합병증의 위험이 있다. 혈관 내 냉각법을 시작한 뒤 체온 하강 속도는 빠르지만, 중심정맥관을 삽입하는 데 시간이 걸리기 때문에 표면 냉각법에 비해 저체온 치료 시작 시간은 늦어지는 경향이 있다[20].
저체온요법은 신체 전반의 생리적인 변화를 유발하면서 다양한 부작용이 발생할 수 있기 때문에, 치료에 앞서 각종 부작용의 조기 발견과 대처법을 숙지해야 한다.
오한은 가장 흔히 동반되는 부작용으로, 환자에게 불편감을 유발하는 것은 물론이고 오한에 의해 대사량이 증가하고 열이 발생하면 저체온 유도에 이르는 시간을 느리게 하고, 저체온 유지기에는 체온의 변동을 크게 만든다. 또한 대사량이 증가하면서 뇌압을 올리고, 뇌세포의 손상을 초래할 수 있다[21]. 따라서 오한을 오한평가지표(bedside shivering assessment scale)를 이용해 조기에 발견하고, 오한이 있다면 적절히 조절하는 것이 매우 중요하다. 오한을 예방하기 위해, 보온공기담요 등을 이용하여 피부를 따뜻하게 해주거나(skin counterwarming), 아세트아미노펜 등의 해열제나 magnesium sulfate 등을 투여하거나, 부스피론등의 세로토닌 작용제(serotonine agonist), 아편유사제(meperidine, fentanyl), 진정제(dexmedetomidine, propofol) 등의 정맥주사를 고려해 볼 수 있으며, 그럼에도 불구하고 조절되지 않을 경우에는 근이완제까지도 투여해 볼 수도 있다[22].
심혈관계 합병증으로는 서맥과 심근 수축력 저하로 인해 혈압이 감소하고 심박출량이 저하될 수 있으나[23], 심근경색이 동반된 경우, 오히려 심장 보호효과에 의해 심근 기능 회복에 도움이 될 수도 있다[24].
호흡기계 합병증으로는 폐부종 발생의 위험도가 상승한다. 저체온 치료기간 동안 진정제를 많이 사용하기 때문에 기계호흡을 사용하게 되는 경우가 많은데, 치료기간이 길어지면 저체온으로 인한 면역기능 저하로 폐렴의 발생 위험도가 상승한다[25].
소화기계 합병증으로는 위장운동저하, 무력성 장폐색증, 위궤양 등이 발생할 수 있다[26].
내분비계 합병증으로는 저체온 유도기에 인슐린 저항성으로 인한 고혈당이 초래될 수 있다[27].
신기능 및 전해질 이상으로 저체온 유도기에는 소변량 증가하여 순환 혈액량이 감소할 수 있으며, 혈액 내 칼륨, 마그네슘, 인산, 칼슘 수치가 낮아지는 경우가 많다[28]. 반대로 재가온 시에는 전해질 수치들과 인슐린에 대한 민감도 상승에 따라 혈당이 상승할 수 있다.
면역기능 이상으로는 백혈구의 기능이 저하되며 감염 위험이 높아지고, 감염이 발생하더라도 체온 조절중에는 발열을 확인할 수 없어 진단이 늦어질 수 있기에, 혈액검사 등의 면밀한 감시가 필요하다[29].
또한 저체온 유도기에는 소변량 증가에 따른 순환혈액량의 감소로 혈전이 발생할 수 있으며, 저체온 유지기간이 길어지면 혈소판의 기능과 혈액응고인자의 활성도가 저하되면서 출혈 경향이 높아질 수 있다. 그 외 저체온 상태에서는 약물대사(pharmacokinetics and pharmacodynamics)와 배설이 감소되므로 진정제, 진통제, 근이완제 등의 약물 농도가 높아질 수 있어[30], 약제의 진정효과가 평소보다 오래 지속될 수 있음을 반드시 알고 있어야 한다.
목표체온유지요법은 심정지 환자의 치료를 넘어 다양한 신경계 손상 환자들에서 적용이 확대되고 있고, 국내에서도 2019년 7월부로 급여가 적용되면서, 신경계 중환자실에서의 사용이 증가하고 있다. 특히 신경계 중환자들에서는 뇌부종에 동반된 뇌압상승을 효과적으로 조절하기 위해 목표체온유지요법을 사용하고 있다. 다만 신경계 중환자들에서는 뇌압 및 뇌부종을 낮추기 위한 목적의 저체온 치료는 유지지간이 길어질 수 있기에 전신 합병증의 위험도를 감안하여, ‘꼭 필요한 환자들에게 선택적으로 시행하는 치료’ 방법으로 접근해야 하며, 이를 위해 의료진은 내원시 뇌손상 정도 및 추가 뇌손상 위험 등을 종합적으로 판단하여 저체온 치료의 필요성을 결정하여야 한다. 뇌손상의 원인에 따른 목표체온유지치료의 현재까지의 근거는 다음과 같다.
의식 수준이 글라스고혼수척도(Glasgow Coma Scale) 12점 이하인 중증 외상성뇌손상 환자들에서 적절한 약물 치료에도 불구하고 뇌압상승이 잘 조절되지 않을 때 고려해 볼 수 있다[31]. 이는 일련의 연구들을 분석한 2017년 메타분석에서도 전체 무작위대조연구들을 종합하면 특히 외상성뇌손상을 받은 성인 환자들에서 저체온요법은 18%의 유의한 사망률 감소(risk ratio [RR], 0.82; 95% confidence interval [CI], 0.70-0.96; P=0.01)와 35%의 유의한 기능적 회복(RR, 1.35; 95% CI, 1.18-1.54; P<0.00001)이 확인되었다[32].
거미막밑출혈(subarachnoid hemorrhage)은 뇌동맥류 파열에 의해 발생하는 질환으로, 2018년 출혈성 뇌졸중 환자들을 대상으로 moderate quality 이상으로 확인된 9개의 저체온 연구들을 종합한 메타분석에서는, 전체 환자들에 대해서 저체온요법은 22%의 사망률 감소(RR, 0.78; 95% CI, 0.58-1.06; P=0.11) 경향성을 보였지만 통계적으로 유의하지는 않았다. 또한 그 중 무작위환자/대조군연구로 진행된 8개 연구만을 분석한 하위그룹 분석에서는 저체온 치료는 통계적으로도 유의한 60%의 불량한 예후 감소(RR, 0.40; 95% CI 0.22-0.74; P=0.003) 효과가 확인되었으며, 특히 거미막밑출혈 환자들에서 중요한 합병증 중의 하나인 지연성 뇌경색에 대해서는 통계적으로도 유의한 39% 예방효과(RR, 0.61; 95% CI, 0.40-0.93; P=0.02)가 확인되어[33], 추후 거미막밑출혈 환자들에 대한 저체온요법에 대한 연구결과들이 기대된다.
목표체온유지요법 또는 유도저체온요법은 급성 뇌손상 환자들의 심부 체온을 낮추어 신경 보호와 뇌부종 감소를 유도하는 치료법으로, 다양한 뇌손상이 동반된 신경계 중환자들에서 잘 조절이 되지 않는 뇌부종과 뇌압상승을 치료하기 위한 목적으로 사용하고 있다. 하지만 신경계 중환자들에서 사용하는 목표체온유지요법은 저체온 유지기간이 길어짐에 따라 전신 합병증의 위험도가 상승하게 되므로, 치료의 장단점을 고려하여 환자별로 종합적인 판단이 필요하다. 뇌압관리를 제외하고, 외상성뇌손상 및 거미막밑출혈 환자들을 대상으로 진행된 저체온요법에 대한 분석은 질환의 예후에 대한 치료효과의 관점에서 여전히 논쟁점들이 있어, 현재까지는 선택적인 환자들에 한하여 시행하며, 추후 뇌내출혈 및 허혈뇌졸중을 포함한 개별 질환의 치료효과를 개선하기 위해서는 추가적인 연구가 필요하다.
Acknowledgement
This study was supported by a 2023 research grant from Pusan National University Yangsan Hospital.
References
1. Nunnally ME, Jaeschke R, Bellingan GJ, et al. Targeted temperature management in critical care: a report and recommendations from five professional societies. Crit Care Med 2011;39:1113-1125.


2. Hypothermia after Cardiac Arrest Study Group. Mild therapeutic hypothermia to improve the neurologic outcome after cardiac arrest. N Engl J Med 2002;346:549-556.


3. Bernard SA, Gray TW, Buist MD, et al. Treatment of comatose survivors of out-of-hospital cardiac arrest with induced hypothermia. N Engl J Med 2002;346:557-563.


4. Shankaran S, Laptook AR, Ehrenkranz RA, et al. Whole-body hypothermia for neonates with hypoxic-ischemic encephalopathy. N Engl J Med 2005;353:1574-1584.


5. Azzopardi DV, Strohm B, Edwards AD, et al. Moderate hypothermia to treat perinatal asphyxial encephalopathy. N Engl J Med 2009;361:1349-1358.


7. Han MK. Therapeutic hypothermia. J Neurocrit Care 2009;2 Suppl 2:S62-S67.
8. Polderman KH. Mechanisms of action, physiological effects, and complications of hypothermia. Crit Care Med 2009;37((7 Suppl):S186-S202.


9. Hwang SO. Therapeutic hypothermia after cardiac arrest. Int J Arrhythm 2010;11:31-34.
10. Madden LK, Hill M, May TL, et al. The implementation of targeted temperature management: an evidence-based guideline from the Neurocritical Care Society. Neurocrit Care 2017;27:468-487.



11. Badjatia N. Fever control in the neuro-ICU: why, who, and when? Curr Opin Crit Care 2009;15:79-82.


12. Erecinska M, Thoresen M, Silver IA. Effects of hypothermia on energy metabolism in Mammalian central nervous system. J Cereb Blood Flow Metab 2003;23:513-530.



13. Polderman KH, Herold I. Therapeutic hypothermia and controlled normothermia in the intensive care unit: practical considerations, side effects, and cooling methods. Crit Care Med 2009;37:1101-1120.


14. Armahizer MJ, Strein M, Pajoumand M. Control of shivering during targeted temperature management. Crit Care Nurs Q 2020;43:251-266.


15. Choi HA, Badjatia N, Mayer SA. Hypothermia for acute brain injury: mechanisms and practical aspects. Nat Rev Neurol 2012;8:214-222.



16. Arrich J; European Resuscitation Council Hypothermia After Cardiac Arrest Registry Study Group. Clinical application of mild therapeutic hypothermia after cardiac arrest. Crit Care Med 2007;35:1041-1047.


17. Rincon F. Targeted temperature management in brain injured patients. Neurol Clin 2017;35:665-694.


18. Diephuis JC, Balt J, van Dijk D, Moons KG, Knape JT. Effect of rewarming speed during hypothermic cardiopulmonary bypass on cerebral pressure-flow relation. Acta Anaesthesiol Scand 2002;46:283-288.



19. Hoedemaekers CW, Ezzahti M, Gerritsen A, van der Hoeven JG. Comparison of cooling methods to induce and maintain normo- and hypothermia in intensive care unit patients: a prospective intervention study. Crit Care 2007;11:R91.



20. Diringer MN; Neurocritical Care Fever Reduction Trial Group. Treatment of fever in the neurologic intensive care unit with a catheter-based heat exchange system. Crit Care Med 2004;32:559-564.


21. Badjatia N, Strongilis E, Gordon E, et al. Metabolic impact of shivering during therapeutic temperature modulation: the Bedside Shivering Assessment Scale. Stroke 2008;39:3242-3247.


22. Choi HA, Ko SB, Presciutti M, et al. Prevention of shivering during therapeutic temperature modulation: the Columbia anti-shivering protocol. Neurocrit Care 2011;14:389-394.



23. Bro-Jeppesen J, Kjaergaard J, Søholm H, et al. Hemodynamics and vasopressor support in therapeutic hypothermia after cardiac arrest: prognostic implications. Resuscitation 2014;85:664-670.


24. Fordyce CB, Chen AY, Wang TY, et al. Patterns of use of targeted temperature management for acute myocardial infarction patients following out-of-hospital cardiac arrest: insights from the National Cardiovascular Data Registry. Am Heart J 2018;206:131-133.


25. Dankiewicz J, Nielsen N, Linder A, et al. Infectious complications after out-of-hospital cardiac arrest: a comparison between two target temperatures. Resuscitation 2017;113:70-76.


26. Martin M, Reignier J, Le Thuaut A, et al. Nutrition during targeted temperature management after cardiac arrest: Observational Study of Neurological Outcomes and Nutrition Tolerance. JPEN J Parenter Enteral Nutr 2020;44:138-145.



27. Xie C, Basken R, Finger J, Erstad B. Targeted temperature management: quantifying the extent of serum electrolyte and blood glucose shifts in postcardiac arrest patients. Ther Hypothermia Temp Manag 2020;10:76-81.


28. Barlow B, Landolf K, LaPlante R, et al. Electrolyte considerations in targeted temperature management. Am J Health Syst Pharm 2023;80:102-110.



29. Polderman KH. Application of therapeutic hypothermia in the intensive care unit: opportunities and pitfalls of a promising treatment modality--Part 2: Practical aspects and side effects. Intensive Care Med 2004;30:757-769.



30. Beaufort AM, Wierda JM, Belopavlovic M, Nederveen PJ, Kleef UW, Agoston S. The influence of hypothermia (surface cooling) on the time-course of action and on the pharmacokinetics of rocuronium in humans. Eur J Anaesthesiol Suppl 1995;11:95-106.

31. Robinson CP. Moderate and severe traumatic brain injury. Continuum (Minneap Minn) 2021;27:1278-1300.


Peer Reviewers’ Commentary
이 논문은 뇌부종과 두개내압 상승에 대한 여러 치료 방법 중에서 목표체온 유지치료의 작용 원리, 적응증, 적용 방법, 부작용 등에 대한 최신 문헌을 정리하여 설명해 주고 있다. 중증 뇌손상 환자에서 뇌부종 발생 및 두개내압 상승으로 인한 이차적 뇌손상을 억제하기 위한 치료전략은 중증 신경계 환자치료에서 매우 주요하다. 목표체온 유지치료는 뇌와 전신의 신진대사와 산소 소비량을 감소시켜 뇌를 보호할 수 있게 해준다. 하지만, 체온의 변화 시마다 다양한 합병증이 발생할 수 있어, 각각의 목표체온 유지치료의 과정마다 생기는 생리적 현상을 잘 이해하는 것은 중요하다. 이 논문은 목표체온 유지치료 과정에 발생할 수 있는 전신 합병증을 설명하고, 심한 뇌손상 환자들에서 적용한 목표체온 유지치료의 최근 연구 결과들을 잘 제시하고 있어 신경계 중환자를 진료하는 임상 현장에 많은 도움이 될 것으로 판단된다.
[정리: 편집위원회]
-
METRICS

-
- 0 Crossref
- Scopus
- 1,914 View
- 173 Download
-
Related articles in
J Korean Med Assoc -
Recent trends in the management of anterior knee pain2023 August;66(8)
Current status of pharmaceutical safety management in Korea2012 September;55(9)
Preoperative management of chronic disease2014 October;57(10)
Targeted therapy and immunotherapy in ovarian cancer2016 March;59(3)