 |
 |
- Search
| J Korean Med Assoc > Volume 64(2); 2021 > Article |
|
Abstract
Ankylosing spondylitis (AS) is a chronic inflammatory disease predominantly affecting the axial skeleton. AS treatment aims to reduce pain and inflammation and maintain functional capacity. Nonsteroidal anti-inflammatory drugs are the first-line treatment for those with active AS. While for peripheral arthritis, sulfasalazine or local glucocorticoid injection can be used, these are not recommended for axial symptoms. Twenty years ago, biological products that target the tumor necrosis factor (TNF) were developed. These have been approved for use in rheumatoid arthritis and AS. Since the introduction of these TNF inhibitors, the control of disease activity in AS has improved markedly. TNF inhibitors, including both anti-TNF-alpha monoclonal antibodies and recombinant TNF soluble receptors, can be considered for patients with persistently active disease despite nonsteroidal anti-inflammatory drug treatment. Recently, interleukin-17 inhibitors have also been approved for use in AS patients with insufficient responses to TNF inhibitors. Ongoing clinical trials are exploring the effect of Janus kinase inhibitors against AS. This review summarizes the current pharmaceutical treatment for AS, focusing on the biological products. Recommendations for AS management are also discussed in this review.
척추관절염(spondyloarthritis)은 임상 증상, HLA-B27 등의 유전적 관련성 및 발병 기전이 유사한 만성 염증성 질환을 포괄하는 질환군으로 주 침범 부위에 따라 축형척추관절염(axial spondyloarthritis)과 말초척추관절염(peripheral spondyloarthritis)으로 분류된다. 강직척추염(ankylosing spondylitis)은 축형척추관절염의 대표적인 질환으로 천장관절염(sacroiliits)과 척추염(spondylitis), 부착부염(enthesitis), 소수관절염(oligoarthritis) 같은 근골격 증상 및 포도막염, 건선 또는 염증장질환과 같은 근골격 외 임상증상을 보인다[1].
척추관절염의 치료목표는 통증 및 염증이 없는 관해 상태를 유지시키는 것으로 운동 및 금연 같은 교육과 약물치료가 적절히 병행되어야 한다. 약물치료로는 비스테로이드소염제의 사용이 근간이 되며 설파살라진(sulfalalazine)과 같은 질환조절항류마티스약제(disease modifying anti-rheumatic drugs)도 말초관절염 증상에 효과가 있는 것으로 알려져 있다. 2000년대 초 척추관절염의 치료에 생물학적제제인 항종양괴사인자제제가 도입된 이후 척추관절염 치료는 획기적으로 발전하였다. 2017년 인터루킨-17(interleukin-17) 억제제가 국내 식품의약품안전청 승인을 획득하였으나 이차 생물학적제제로 항종양괴사인자제제 사용에도 충분한 효과를 얻지 못한 경우 제한적으로 허가되었다. 이에 본 종설을 통해 주요 류마티스학회에서 권고하고 있는 강직척추염 및 축형척추관절염 치료 권고사항과 가이드라인을 소개하고 국내 생물학적제제 현황에 대해 정리하여 의료진 간 소통에 도움을 주고자 한다.
강직척추염을 포함한 척추관절염 치료는 2016년 유럽류마티스학회(European League Against Rheumatism) 지침과(Figure 1) [2] 2019년 미국류마티스학회(American College of Rheumatology)의 치료지침 [3]을 따른다. 환자 치료의 첫 번째 목표는 증상과 염증의 조절, 진행 중인 구조적 손상의 예방, 사회 구성원으로서의 기능 보존 또는 정상화를 통하여 장기간 건강과 관련된 삶의 질을 최대화하는 것이다. 척추관절염 환자의 치료는 주 침범 부위(척추, 말초 손발 관절, 골근 부착부, 관절 외 증상) 및 전반적인 임상적 상태(동반 질환, 심리 사회적 요인)에 따라 달라진다. 일상생활에서 가장 중요한 치료는 규칙적인 운동이며 반드시 금연해야 한다. 통증 및 강직이 있는 환자는 비스테로이드소염제를 먼저 사용하며 충분한 양을 사용해야한다. 파라세타몰(paracetamol), 마약진통제 등은 일반적인 치료에 효과가 없는 경우 단기간 고려한다. 한두 부위의 말초 관절염이 있는 경우 관절 내 글루코코티코이드 주사를 사용할 수 있으며 척추 증상만 있는 경우 장기간 전신 글루코코티코이드 사용은 피해야 한다. 척추 증상이 있는 경우 질환조절항류마티스약제는 효과가 없으나 말초 관절염의 경우 설파살라진을 고려할 수 있다. 생물학적제제는 위의 일반적인 치료에도 불구하고 질환 활성도가 높은 경우 고려되며 항종양괴사인자제제가 먼저 추천된다. 한가지 항종양괴사인자제제에 효과가 없는 경우 다른 종류의 항종양괴사인자제제로 변경하거나 인터루킨-17 억제제를 사용해볼 수 있다. 또한 강직척추염 환자를 대상으로 국내에서는 아직 허가되지 않은 토파시티닙(tofacitinib)을 항종양괴사인자제제에 효과가 없는 경우 이차 약제로 조건부 사용이 권고되기도 한다 [3]. 유럽류마티스학회에서는 환자의 상태가 6개월 이상 관해를 유지하면 생물학제제 감량을 고려할 수 있다고 하였으나, 미국류마티스학회 치료지침에서는 생물학적제제로 강직척추염이 안정적으로 유지되더라도 생물학적제제의 중단이나 감량은 주의하도록 권고하였다.
비스테로이드소염제는 활동성 강직척추염 환자의 일차 치료제이다. 활동성 강직척추염의 판단은 적혈구침강속도, C반응단백질을 포함하는 혈액학적 검사와 임상증상 및 영상(자기공명영상촬영) 결과를 참고한다[4]. 활동성 강직척추염의 증상개선을 위한 비스테로이드소염제 효능은 여러 연구에서 입증되었다[5]. 과거 비스테로이드소염제를 간헐적 복용하는 경우보다 꾸준히 복용하는 경우에서 경추와 요추 융합이 더디게 진행된다는 연구들이 학계에서도 인정되고 있었으나 최근 연구결과에서는 비스테로이드소염제의 간헐적 복용에 비해 꾸준한 복용이 척추 융합속도를 느리게 한다는 증거는 일관성이 없는 것으로 보고되기도 하였다[6,7]. 하지만 이러한 불확실성에도 불구하고 질병의 활동을 제어하기 위해 활동성 강직척추염 환자에서 비스테로이드소염제의 지속적인 사용이 최근 치료지침에서도 추천되고 있다[3]. 특정 종류의 비스테로이드소염제가 더 효과가 좋다고 알려져 있지는 않으며 활동성 강직척추염에서는 각 약제의 최대 허용 용량(항염증용량)의 사용을 권장한다[3,8]. 비스테로이드소염제를 2-3주 이상 사용 후 효과여부를 판단하여 만약 효과가 없으면 다른 계열의 비스테로이드소염제로 변경하는 것이 추천되며 여러 비스테로이드소염제를 중복해서 사용하는 것은 피해야 한다. 비스테로이드소염제 사용 시 위장관, 심혈관 및 신장 부작용이 발생할 수 있음을 인지하고 고령, 위궤양 병력 등의 위장관 부작용 발생 고위험 환자군에서는 선택적 COX-2 저해제 사용을 고려할 수 있다.
질환조절항류마티스약제가 류마티스관절염에서 염증을 낮추고 관절변형 예방효과가 있다는 점에 착안해서 강직척추염에서도 사용되어 왔다. 설파살라진이 말초 관절염이 동반된 경우에는 일부 효과가 보고되고 있지만 염증성 요통 및 척추강직 증상에는 만족할 만한 효과는 관찰되지 않았다[9]. 류마티스관절염의 가장 중요한 약제인 메토트렉세이트(methotrexate)는 척추관절염에는 효과가 없다는 의견이 대다수이다[9]. 글루코코티코이드는 비스테로이드소염제 사용에도 말초 관절염, 부착부염 또는 천장관절염이 심한 경우 국소 주사치료로 사용할 수 있다. 다만 아킬레스건, 슬개골, 대퇴사두근건(quadriceps tendons) 주위의 글루코코티코이드 주사는 피해야 한다[3]. 또한 전신적인 글루코코티코이드 사용은 추천되지 않는다.
생물학적제제는 생물체 유래된 물질이나 생물체를 이용하여 만들어진 물질을 함유한 의약품을 총칭하는 말로 유전자 재조합 기술을 이용하여 표적단백질을 만들어내고 이를 세포주를 통해 대량 생산함으로써 실용화한 치료제이다. 생물학적제제는 강직척추염의 발병 및 염증에 관여할 것으로 생각되는 세포의 기능 및 사이토카인을 차단하는 역할을 함으로써 치료에 이용된다. 현재 국내에서 강직척추염에 보험 급여로 사용 가능한 생물학제제는 두 종류로 항종양괴사인자제제와 인터루킨-17 억제제가 있다. 항종양괴사인자제제는 두 가지 종류 이상의 비스테로이드소염제 혹은 항류마티스약제로 3개월 이상 치료를 하였으나 치료효과가 미흡하거나 상기 약제들의 부작용으로 치료를 중단한 중증의 활동성 강직척추염 환자에서 보험 급여로 투여할 수 있다. 중증 활동성 강직척추염의 판단은 질병의 활성도를 측정하는 지표인 Bath Ankylosing Spondylitis Disease Activity Index (BASDAI) 점수 4점 이상을 기준으로 한다. 인터루킨-17 억제제는 1종 이상의 항종양괴사인자제제에 반응이 불충분하거나 약제부작용 등으로 치료를 중단한 중증의 활동성 강직척추염 환자에서 투여할 수 있다. 국내 건강보험심사평가원 급여 인정기준에 따르면 생물학적제제를 환자에게 투여한 지 3개월째에 BASDAI가 50% 또는 2 (스케일 0-10) 이상 감소한 경우 추가 6개월의 투여를 인정하며, 이후에는 6개월마다 평가하여 첫 3개월째의 평가결과가 유지되면 지속적인 투여를 인정한다. 국내 강직척추염의 치료제로 승인되어 사용 중인 생물학제제들의 표적물질과 사용법을 Table 1에 정리하였다.
종양괴사인자(tumor necrosis factor, TNF)는 주로 단핵구, 대식세포와 활성화된 T세포에 의해 생성되는 전 염증성 사이토카인으로 인터루킨-1, 인터루킨-6와 같은 다른 사이토카인 및 림프구를 활성화하고 파골세포 형성에 관여하는 메탈로프로테이나제(metalloproteinases)와 프로스타글란딘(prostaglandin)의 방출을 유도하여 체내 염증반응에 중요한 역할을 한다[10]. 항종양괴사인자제제는 TNF의 작용을 차단하여 인터루킨-1, 인터루킨-6, TNF 등 염증성 사이토카인의 생산, 림프구의 활성화 및 관절 내 이동을 억제한다. 항종양괴사인자제제는 생물학적제제 중 가장 먼저 개발되어 사용되고 있는 약제로 내에서 국내에서는 에터너셉트(etanercept), 아달리무맵(adalimumab), 골리무맙(golimumab)과 인플릭시매브(infliximab)가 사용 가능하다. 에터너셉트는 사람 면역글로불린 G1의 Fc 부위와 TNF수용체의 세포 바깥 부위 인 p75단백질 두 개를 융합한 수용성 수용체이고 아달리무맵, 골리무맙과 인플릭시매브는 면역글로불린 G1의 단클론항체이다. 항종양괴사인자제제 중 특정 약제를 추천하지는 않고 있으나, 만약 반복적인 비감염성 포도막염, 홍채염이나 염증장질환이 동반된 환자의 경우에는 항종양괴사인자제제 중 아달리무맵, 인플릭시매브 등의 단클론항체제제 사용을 권고한다[3]. 에터너셉트는 주 1회 50 mg을 피하주사, 아달리무맵은 2주에 한번 40 mg 피하주사, 골리무맙은 4주마다 50 mg 피하주사를 하고, 인플릭시매브는 체중 kg당 5 mg 용량을 정맥주사, 그 후에 2주, 6주째 주사하며, 이후에는 8주 간격으로 반복 투여한다. 또한 인플릭시매브 및 에터너셉트는 특허기간 만료로 동등생물의약품이 다양한 제약회사에서 개발되었으며 가격 경쟁력을 통해 국내외에서 사용이 늘어나고 있다. 이러한 동등생물의약품도 기존 제제와 비교하여 강직척추염의 치료에 유사한 효과와 안전성을 보이는 것으로 보고되고 있다[11,12]. 다만 오리지널 항종양괴사인자제제로 질병이 안정적으로 유지되는 경우에는 동등생물의약품으로 변경하지 않고 기존약제를 유지하는 것을 추천하고 있다[3]. 여러 대규모 임상시험에서 상기 네 가지 약제 모두 국제척추관절염평가학회(Assessment of SpondyloArthritis international Society)에서 정한 20%, 40% 반응기준에 효과적인 것으로 판정되었고 치료 2-4주부터 질병의 활성도를 측정하는 지표인 BASDAI 점수와 조조 강직, 엉치엉덩관절 부위 통증 등의 임상적 소견과 적혈구침 강속도, C반응단백질을 포함하는 혈액학적 염증지표도 유의하게 호전시켰다[13-16]. 자기공명영상촬영 검사에서 척추 및 천장관절의 염증소견이 항종양괴사인자제제 치료 후 염증이 감소하는 결과를 보였다[17,18]. 유병기간이 짧고, 40세 이하의 젊은 연령, 골부착염이 없는 경우, HLA-B27 양성, 좋은 기능상태 및 높은 C반응단백질 수치를 보이는 환자에서 항종양괴사인자제제의 치료반응이 좋았다[19]. 강직 예방에 대한 효과에 대해서는 아직 논란이 많으나 최근 국내 연구진에 의하여 장기간 항종양괴사인자제제를 사용한 강직척추염 환자가 사용하지 않은 환자에 비하여 방사선적 질병 진행이 느리다는 결과가 발표되었다[20].
항종양괴사인자제제 이후 척추관절염에서 인터루킨-17 경로가 유망한 치료표적으로 연구되어왔다. 인터루킨-17은 TNF 등의 염증성 사이토카인을 증가시켜 염증을 일으킨다. 실제로 강직척추염 환자의 혈액 및 조직에서 인터루킨-17 생성 세포의 수가 증가하는 것으로 알려져 있다[21,22]. T 도움 17세포(T helper 17 cell, Th17세포)에서 분비되는 염증성 사이토카인인 인터루킨-17은 척추관절염뿐만 아니라 건선 등 다양한 염증성 질환 매개물로 알려져 있다. 인터루킨-23은 Th17세포의 인터루킨-23 수용체를 통하여 Th17세포의 분화와 인터루킨-17 분비에 관여한다[23]. 인터루킨-17 억제제로 현재 국내에서 강직척추염에 허가된 약제는 세쿠키누맙(secukinumab)과 익세키주맙(ixekizumab)이 있다. 이들 약제는 인터루킨-17의 다양한 이소형 중 A에 대한 단클론항체로 인터루킨-17A에 결합하여 혈중 인터루킨-17이 수용체에 결합하는 것을 막아 기능을 억제한다. 국내 허가된 제형은 피하주사제로 세쿠키누맙은 1회 150 mg을 0, 1, 2, 3, 4주에 투여하고 이후에는 4주마다 투여하며, 익세키주맙은 첫 투약 시 160 mg 이후 4주마다 80 mg 투여한다.
항종양괴사인자제제 및 인터루킨-17 억제제 외의 생물학적제제에 대한 연구도 많이 진행되었으나 아직 강직척추염에서 국내 적응증을 받은 약제는 없다. 류마티스관절염에서 허가를 받아 현재 사용중인 세포 내 염증전달물질인 야누스인산화효소(Janus kinase, JAK)를 표적으로 하는 소분자억제제인 토파시티닙(tofacitinib)과 유파다시티닙(upadacitinib)을 강직척추염의 치료에 사용한 연구가 있다. 토파시티닙은 경구 JAK 억제제로 JAK2보다 상대적으로 JAK3, JAK1을 같이 억제한다. 토파시티닙의 2상 임상연구에서 위약 대비 12주 후 국제척추관절염평가학회에서 정한 20% 반응 달성률 및 영상 결과 모두에서 유의한 효과를 보였다[24]. 아직 토파시티닙의 강직척추염에서의 3상 임상시험 결과는 없으나 2019년도 발표된 미국류마티스학회 강직척추염 치료지침 [3]에서는 감염을 제외한 항종양괴사인자제제의 금기로 사용할 수 없는 경우 토파시티닙을 잠재적인 이차 약제로 고려할 수 있다고 권고하였다. JAK1 선택억제제인 유파다시티닙도 위약에 비하여 임상증상 호전을 보이는 성공적인 2/3 임상시험 결과를 발표하였다[25]. 인터루킨-12/23 p40 억제제인 우스테키누맙(ustekinumab)은 건선, 건선관절염에 효과적이나 축형척추관절염의 임상시험에서 일차목표치 도달에 실패하여 강직척추염 치료에는 사용하지 않는다[26].
생물학적제제 사용 시 피부 이상반응 및 감염위험 증가에 대한 우려가 있다. 자가 피하주사의 경우 주사 부위에 국한된 국소 염증, 부종은 비교적 흔하게 발생하고 이로 인해 약제를 중단하는 경우는 드물다. 하지만 전신 피부 이상 및 심한 가려움증이 동반되어 투약을 지속할 수 없는 경우도 드물게 발생할 수 있다. 인플릭시매브 정맥 투여 시 두통, 오심, 두드러기, 가려움, 열, 호흡곤란과 같은 과민반응이 나타날 수 있으며 아세트아미노펜, 항히스타민, 글루코코티코이드로 치료한다. 또한 생물학적제제 사용 시 감염의 빈도가 증가한다. 특히 항종양괴사인자제제에 의해 육아종 형성이 억제되므로 잠복결핵 활성화 위험이 증가한다. 따라서, 항종양괴사인자제제 치료예정자는 반드시 투약 전 활동성 결핵 및 잠복결핵에 대한 검사를 시행하여야 한다. 흉부X선검사 및 결핵반응검사(투베르쿨린 피부반응 검사 또는 인터페론 감마반응 검사[27])를 시행하게 된다. 잠복결핵으로 판정되면 최소 3-4주간 결핵 예방치료 후 항종양괴사인자제제 투약을 시작할 수 있다. 결핵 예방 치료는 아이소니아지드(isoniazid) 9개월, 리팜핀(rifampin) 4개월 또는 아이소니아지드와 리팜핀 동시 투약 시 3개월 요법이 권고되어 있다. 그 외 항종양괴사인자제제 사용 시 범혈구감소증과 같은 혈액학적 이상, 탈수초화 질환, 심부전증의 악화, 전신홍반루푸스와 관련한 자가항체 및 임상양상의 발생과 건선 등 자가면역질환의 발생 및 심각한 간질환 등이 발생할 수 있다. 인터루킨-17A 억제제의 경우 곰팡이 감염이나 염증 대장염을 악화시킬 수 있다는 보고가 있어 염증성 장질환이 동반된 경우 주의가 필요하다[28].
2000년대 초 생물학적제제가 국내 도입된 이후 강직척추염 치료는 획기적으로 발전하였다. 현재 국내에서 강직척추염에 사용 가능한 생물학적제제는 항종양괴사인자제제와 인터루킨-17A 억제제가 있다. 항종양괴사인자제제는 두 가지 종류 이상의 비스테로이드소염제 혹은 항류마티스약제로 3개월 이상 치료를 하였으나 치료효과가 미흡하거나 상기 약제들의 부작용으로 치료를 중단한 중증의 활동성 강직척추염 환자에서 국민건강보험 급여로 투여할 수 있고 인터루킨-17A 억제제는 한 가지 이상의 항종양괴사인자제제에 불충분한 반응을 보이는 활동성 강직척추염 환자에게 투약할 수 있다. 또한, 아직 승인되지는 않았으나 JAK 억제제도 강직척추염 치료제로 임상연구 중으로 기대되고 있다. 생물학적제제는 비스테로이드소염제에 반응이 불충분한 활동성 강직척추염 환자의 치료에 탁월한 효과를 보이나 결핵 등의 감염 위험성 증가 등 부작용에 대해서 적절한 사전조치와 모니터링이 필요하다.
Figure 1.
Algorithm based on the Assessment of SpondyloArthritis international Society (ASAS)-European League Against Rheumatism (EULAR) recommendations for the management of axial spondyloarthritis. SpA, spondyloarthritis; ASDAS, Ankylosing Spondylitis Disease Activity Score; BASDAI, Bath Ankylosing Spondylitis Disease Activity Index; bDMARD, biological disease-modifying antirheumatic drug; TNFi, tumor necrosis factor inhibitor; IL17, interleukin-17. a)Either BASDAI or ASDAS, but the same outcome per patient. Adapted from van der Heijde D et al. Ann Rheum Dis 2017;76:978-991, with permission from BMJ Publishing Group [2].
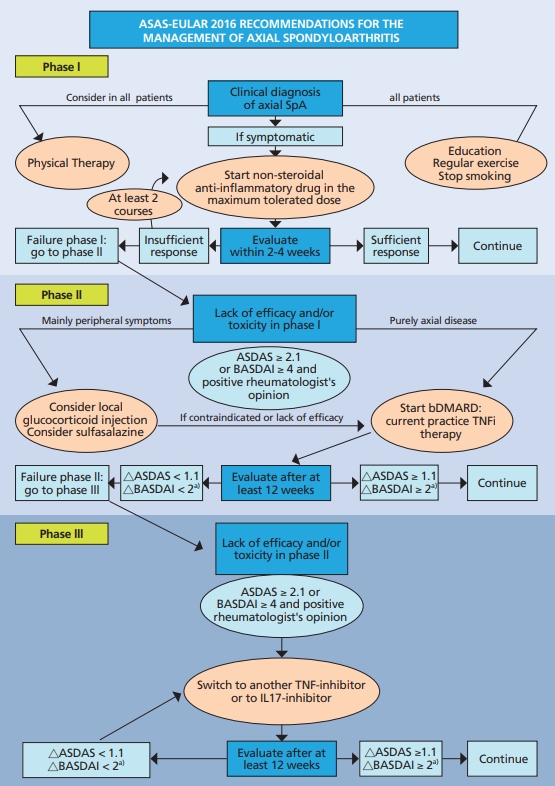
Table 1.
Biological products for ankylosing spondylitis approved by the Korea Food and Drug Administration
References
1. Sieper J, Rudwaleit M, Baraliakos X, Brandt J, Braun J, Burgos-Vargas R, Dougados M, Hermann KG, Landewe R, Maksymowych W, van der Heijde D. The Assessment of SpondyloArthritis international Society (ASAS) handbook: a guide to assess spondyloarthritis. Ann Rheum Dis 2009;68 Suppl 2:ii1-ii44.


2. van der Heijde D, Ramiro S, Landewe R, Baraliakos X, Van den Bosch F, Sepriano A, Regel A, Ciurea A, Dagfinrud H, Dougados M, van Gaalen F, Geher P, van der Horst-Bruinsma I, Inman RD, Jongkees M, Kiltz U, Kvien TK, Machado PM, Marzo-Ortega H, Molto A, Navarro-Compan V, Ozgocmen S, Pimentel-Santos FM, Reveille J, Rudwaleit M, Sieper J, Sampaio-Barros P, Wiek D, Braun J. 2016 update of the ASAS-EULAR management recommendations for axial spondyloarthritis. Ann Rheum Dis 2017;76:978-991.


3. Ward MM, Deodhar A, Gensler LS, Dubreuil M, Yu D, Khan MA, Haroon N, Borenstein D, Wang R, Biehl A, Fang MA, Louie G, Majithia V, Ng B, Bigham R, Pianin M, Shah AA, Sullivan N, Turgunbaev M, Oristaglio J, Turner A, Maksymowych WP, Caplan L. 2019 Update of the American College of Rheumatology/Spondylitis Association of America/Spondyloarthritis Research and Treatment Network recommendations for the treatment of ankylosing spondylitis and nonradiographic axial spondyloarthritis. Arthritis Rheumatol 2019;71:1599-1613.



4. Machado PM, Landewe R, Heijde DV; Assessment of SpondyloArthritis international Society (ASAS). Ankylosing Spondylitis Disease Activity Score (ASDAS): 2018 update of the nomenclature for disease activity states. Ann Rheum Dis 2018;77:1539-1540.


5. Wang R, Dasgupta A, Ward MM. Comparative efficacy of non-steroidal anti-inflammatory drugs in ankylosing spondylitis: a Bayesian network meta-analysis of clinical trials. Ann Rheum Dis 2016;75:1152-1160.


6. Sieper J, Listing J, Poddubnyy D, Song IH, Hermann KG, Callhoff J, Syrbe U, Braun J, Rudwaleit M. Effect of continuous versus on-demand treatment of ankylosing spondylitis with diclofenac over 2 years on radiographic progression of the spine: results from a randomised multicentre trial (ENRADAS). Ann Rheum Dis 2016;75:1438-1443.


7. Wanders A, Heijde Dv, Landewe R, Behier JM, Calin A, Olivieri I, Zeidler H, Dougados M. Nonsteroidal antiinflammatory drugs reduce radiographic progression in patients with ankylosing spondylitis: a randomized clinical trial. Arthritis Rheum 2005;52:1756-1765.


8. Ward MM, Deodhar A, Akl EA, Lui A, Ermann J, Gensler LS, Smith JA, Borenstein D, Hiratzka J, Weiss PF, Inman RD, Majithia V, Haroon N, Maksymowych WP, Joyce J, Clark BM, Colbert RA, Figgie MP, Hallegua DS, Prete PE, Rosenbaum JT, Stebulis JA, van den Bosch F, Yu DT, Miller AS, Reveille JD, Caplan L. American College of Rheumatology/Spondylitis Association of America/Spondyloarthritis Research and Treatment Network 2015 recommendations for the treatment of ankylosing spondylitis and nonradiographic axial spondyloarthritis. Arthritis Rheumatol 2016;68:282-298.


9. Chen J, Liu C. Sulfasalazine for ankylosing spondylitis. Cochrane Database Syst Rev 2005;(2):CD004800.

10. Davis JC Jr. Understanding the role of tumor necrosis factor inhibition in ankylosing spondylitis. Semin Arthritis Rheum 2005;34:668-677.


11. Kim HA, Lee E, Lee SK, Park YB, Shin K. Retention rate and efficacy of the biosimilar CT-P13 versus reference infliximab in patients with ankylosing spondylitis: a propensity score-matched analysis from the Korean College of Rheumatology Biologics registry. BioDrugs 2020;34:529-539.



12. Baji P, Pentek M, Szanto S, Geher P, Gulacsi L, Balogh O, Brodszky V. Comparative efficacy and safety of biosimilar infliximab and other biological treatments in ankylosing spondylitis: systematic literature review and meta-analysis. Eur J Health Econ 2014;15 Suppl 1((Suppl 1):S45-S52.


13. Davis JC Jr, Van Der Heijde D, Braun J, Dougados M, Cush J, Clegg DO, Kivitz A, Fleischmann R, Inman R, Tsuji W; Enbrel Ankylosing Spondylitis Study Group. Recombinant human tumor necrosis factor receptor (etanercept) for treating ankylosing spondylitis: a randomized, controlled trial. Arthritis Rheum 2003;48:3230-3236.


14. van der Heijde D, Dijkmans B, Geusens P, Sieper J, DeWoody K, Williamson P, Braun J; Ankylosing Spondylitis Study for the Evaluation of Recombinant Infliximab Therapy Study Group. Efficacy and safety of infliximab in patients with ankylosing spondylitis: results of a randomized, placebocontrolled trial (ASSERT). Arthritis Rheum 2005;52:582-591.


15. van der Heijde D, Kivitz A, Schiff MH, Sieper J, Dijkmans BA, Braun J, Dougados M, Reveille JD, Wong RL, Kupper H, Davis JC Jr; ATLAS Study Group. Efficacy and safety of adalimumab in patients with ankylosing spondylitis: results of a multicenter, randomized, double-blind, placebo-controlled trial. Arthritis Rheum 2006;54:2136-2146.


16. Inman RD, Davis JC Jr, Heijde Dv, Diekman L, Sieper J, Kim SI, Mack M, Han J, Visvanathan S, Xu Z, Hsu B, Beutler A, Braun J. Efficacy and safety of golimumab in patients with ankylosing spondylitis: results of a randomized, double-blind, placebo-controlled, phase III trial. Arthritis Rheum 2008;58:3402-3412.


17. Braun J, Baraliakos X, Hermann KG, van der Heijde D, Inman RD, Deodhar AA, Baratelle A, Xu S, Xu W, Hsu B. Golimumab reduces spinal inflammation in ankylosing spondylitis: MRI results of the randomised, placebo-controlled GO-RAISE study. Ann Rheum Dis 2012;71:878-884.


18. Ritchlin C, Maksymowych W. MRI outcomes in AS patients after two years of etanercept therapy. Curr Rheumatol Rep 2006;8:253-254.

19. Deodhar A, Yu D. Switching tumor necrosis factor inhibitors in the treatment of axial spondyloarthritis. Semin Arthritis Rheum 2017;47:343-350.


20. Koo BS, Oh JS, Park SY, Shin JH, Ahn GY, Lee S, Joo KB, Kim TH. Tumour necrosis factor inhibitors slow radiographic progression in patients with ankylosing spondylitis: 18-year real-world evidence. Ann Rheum Dis 2020;79:1327-1332.


21. Shen H, Goodall JC, Hill Gaston JS. Frequency and phenotype of peripheral blood Th17 cells in ankylosing spondylitis and rheumatoid arthritis. Arthritis Rheum 2009;60:1647-1656.


22. Noordenbos T, Yeremenko N, Gofita I, van de Sande M, Tak PP, Caňete JD, Baeten D. Interleukin-17-positive mast cells contribute to synovial inflammation in spondylarthritis. Arthritis Rheum 2012;64:99-109.


24. van der Heijde D, Deodhar A, Wei JC, Drescher E, Fleishaker D, Hendrikx T, Li D, Menon S, Kanik KS. Tofacitinib in patients with ankylosing spondylitis: a phase II, 16-week, randomised, placebo-controlled, dose-ranging study. Ann Rheum Dis 2017;76:1340-1347.



25. van der Heijde D, Song IH, Pangan AL, Deodhar A, van den Bosch F, Maksymowych WP, Kim TH, Kishimoto M, Everding A, Sui Y, Wang X, Chu AD, Sieper J. Efficacy and safety of upadacitinib in patients with active ankylosing spondylitis (SELECT-AXIS 1): a multicentre, randomised, double-blind, placebo-controlled, phase 2/3 trial. Lancet 2019;394:2108-2117.


26. Deodhar A, Gensler LS, Sieper J, Clark M, Calderon C, Wang Y, Zhou Y, Leu JH, Campbell K, Sweet K, Harrison DD, Hsia EC, van der Heijde D. Three multicenter, randomized, doubleblind, placebo-controlled studies evaluating the efficacy and safety of ustekinumab in axial spondyloarthritis. Arthritis Rheumatol 2019;71:258-270.



Peer Reviewers’ Commentary
강직척추염은 하부요통과 척추강직 외에도 다양한 임상 양상과 합병증이 동반될 수 있고, 그 양상에 따라 치료제의 선택이 복잡한 질환이다. 이 논문은 강직척추염에 대한 최근의 치료 권고안을 제시하고, 기존 치료약제와 더불어 최근 관심이 높아지고 있는 생물학적제제들의 치료 효과에 대한 최신 지식을 정리하여 제시하고 있다. 특히, 최근 널리 사용되고 있는 항종양괴사인자제제와 인터루킨-17 억제제들의 작용기전과 효능효과, 약제별 사용 방법 및 주의해야 할 부작용에 대한 자세한 정보를 제공하며 치료 권고안의 근거가 되는 대표적인 임상연구 결과들을 잘 설명해 주고 있다. 이 논문은 강직척추염을 치료하는 데 있어서 안전성과 효능의 균형을 유지하면서 최적의 치료제를 선택하는데 좋은 지침을 제공할 것으로 판단된다.
[정리: 편집위원회]
-
METRICS

-
Related articles in
J Korean Med Assoc -
Changing the strategic paradigm for the treatment of adult acute myeloid leukemia2023 April;66(4)
Pharmacologic treatment of tinnitus2022 December;65(12)
Surgical treatment of senile spinal diseases2021 March;64(3)
Biologic therapies for the treatment of psoriatic arthritis2021 February;64(2)
Biologic therapies for the treatment of systemic lupus erythematosus2021 February;64(2)






