 |
 |
- Search
| J Korean Med Assoc > Volume 64(6); 2021 > Article |
|
Abstract
Background:: As global life expectancy increases, an interest in maintaining health and beauty in old age has increased. As a barrier organ, the skin is an ideal model for studying both genetically-programmed (intrinsic) and environmentally-induced (extrinsic) aging.
Current Concepts:: Among the extrinsic aging factors, solar ultraviolet radiation is the most important, accounting for 80% of facial skin aging. Other nongenetic factors include air pollution, cigarette smoke, nutrition, temperature, sleep, and stress. Through complex interplay, genome, exposome and microbiome all contribute to skin aging. Intrinsic aging causes thinning of the skin and fine wrinkles, while extrinsic aging leads to thick rubbery skin texture, deep wrinkles and dyspigmentation in exposed areas. Fibroblast senescence is a fundamental mechanism of skin aging, with these cells persisting and exhibiting a senescence-associated secretory phenotype which secrets proinflammatory cytokines. Chronic low-level inflammation associated with aging, termed inflamm-aging, is exacerbated by oxidative damage caused by extrinsic factors.
Discussion and Conclusion:: Understanding the pathogenesis of skin aging may help in developing anti-aging strategies in general. In addition to applying sunscreen every morning and retinoic acid every night, taking antioxidant-rich foods and maintaining a healthy lifestyle are all important for preventing skin aging.
Current Concepts:: Among the extrinsic aging factors, solar ultraviolet radiation is the most important, accounting for 80% of facial skin aging. Other nongenetic factors include air pollution, cigarette smoke, nutrition, temperature, sleep, and stress. Through complex interplay, genome, exposome and microbiome all contribute to skin aging. Intrinsic aging causes thinning of the skin and fine wrinkles, while extrinsic aging leads to thick rubbery skin texture, deep wrinkles and dyspigmentation in exposed areas. Fibroblast senescence is a fundamental mechanism of skin aging, with these cells persisting and exhibiting a senescence-associated secretory phenotype which secrets proinflammatory cytokines. Chronic low-level inflammation associated with aging, termed inflamm-aging, is exacerbated by oxidative damage caused by extrinsic factors.
Discussion and Conclusion:: Understanding the pathogenesis of skin aging may help in developing anti-aging strategies in general. In addition to applying sunscreen every morning and retinoic acid every night, taking antioxidant-rich foods and maintaining a healthy lifestyle are all important for preventing skin aging.
피부노화의 대표적인 현상은 주름이다. 주름 외에 얼룩덜룩한 색소침착, 건조함 등의 현상도 동반되는데 이런 현상들은 개인의 유전적 요인, 생활방식과 환경적 요인에 따라 그리고 한 개인에서도 노출부와 비노출부에서 매우 다르게 나타난다. 피부는 우리 몸의 제일 표면에 있는 장기이므로 인체 다른 장기의 노화와 달리 생물학적 내인성 노화 현상 외에 다양한 외부 요인에 의한 외인성 노화도 함께 진행되기 때문이다. 피부건강에 영향을 미치는 요소 중 내인성 요인은 유전체(genome) 요인으로 개인의 유전, 연령과 성별에 따른 요인을 의미하며 노화 요인의 20% 이하를 차지한다. 80%를 차지하는 요인은 exposome, 즉 유전체 외의 모든 환경적 요인의 평생 노출의 합을 일컫는 것으로[1], 자외선, 공해, 기후 외에 수면, 운동, 영양 등 생활방식도 포함된다. 여기에 추가로 피부의 미생물군 유전체(microbiome)도 관여하여 이 세 가지 요인이 복잡한 상호작용을 통해 피부노화를 일으킨다.
피부는 가장 바깥쪽부터 표피, 진피, 피하지방으로 구성되어 있다. 표피를 구성하는 각질형성세포는 기저층에서부터 여러 층의 가시층을 거쳐 과립층, 각질층으로 올라가며 분화하여 탈락된다. 각질층은 피부장벽을 형성하는데 각질 세포간 지질의 50%는 세라마이드, 25%는 콜레스테롤, 15%는 자유지방산으로 구성되어 보습기능과 외부 유해환경으로부터 인체를 보호하는 역할을 하며, 항균 펩타이드도 분비하여 면역장벽기능도 수행한다. 노화와 함께 특히 콜레스테롤이 많이 감소한다. 기저층에서는 멜라닌세포가 멜라닌색소를 합성하여 주변 각질형성세포에 멜라닌을 나눠 줌으로써 자외선으로부터 세포의 DNA 손상을 막아준다. 표피에는 항원전달세포인 랑게르한스세포도 있어 피부의 면역기능에 중요한 역할을 한다. 진피는 피부의 대부분을 차지하는 결체조직으로, 섬유모세포가 만드는 콜라젠, 탄력소, 세포외기질단백이 피부를 지지하고 신경, 혈관도 포함한다. 노화와 더불어 제일 먼저 보이는 피부의 구조적 변화는 표피가 얇아지고 표피 망능선이 사라지는 것이다(Figure 1). 그 결과 피부가 건조해지고 피부장벽 회복이 느려지고 감염에 취약해지며 표피-진피 경계부의 결합이 약해져서 전단력에 의해 피부가 표피와 진피 사이에서 쉽게 분리된다. 랑게르한스세포가 감소하여 면역감시기능이 감소한다. 진피에서는 콜라젠 다발이 성글어지고 진피와 피하지방의 두께가 모두 감소하고, 그 결과 주름과 처짐이 발생하나, 노출부보다는 그 정도가 경미하다. 섬유모세포는 면역기능도 갖고 있어 감염 자극에 대해 반응성 지방생성을 하는데 노화피부에서는 지방생성이 저하되어 지방세포에서 분비하는 항균 펩타이드가 감소한다[2]. 최종당화산물(advanced glycation end products)은 콜라젠과 탄력소가 당류와 공유결합을 하여 발생하는 물질인데, 노화에 따라 그 양이 진피에서 증가하여 피부탄력이 감소하고 피부회복과 세포순환을 억제한다[3]. 얼굴처럼 자외선에 노출되는 부위는 표피의 색소가 불규칙하게 증가하고 상부진피에 일광탄력섬유증이 생기는데 이는 변성된 탄력섬유다. 광노화는 임상적으로 고무처럼 두꺼워진 피부, 깊은 주름, 탄력 소실, 혈관확장, 일광흑자, 검버섯 및 발암위험 증가로 나타난다. 노화 피부에서는 Foxp3+ 조절T세포의 비율이 증가하여 항원특이 면역반응을 저해할 수 있다. 피부에 자외선B를 조사하면 이 세포가 증가하여 인터루킨(interleukin, IL)-10 합성을 통해 다른 면역세포를 억제한다[4].
대표적인 요인은 인종 및 개인 간의 유전적 차이다. 피부노화 양상은 인종에 따라 차이가 있는데, 백인은 다른 인종보다 피부주름이 더 일찍 생기는 반면 동양인은 주로 색소성 반점이 많이 생기고 주름은 백인보다 10년 늦게 생긴다[5]. 표피 기저층에 존재하는 멜라닌색소는 백인보다 유색인종에 그 양이 더 많아 자외선에 대해 보호작용을 하여 광노화와 암발생을 억제하지만 대신 광노화의 한 현상으로 불규칙한 색소침착이 더 흔히, 더 일찍 나타난다. 인종 간 피부색의 다양성에 관여하는 또 하나의 인자는 자가포식 현상으로, 유색인종보다 백인에서 자가포식 활성이 더 높고 백인은 노화와 더불어 피부톤이 더 붉어지는 반면, 동양인은 더 노랗게 된다[6]. 노화 유전자의 존재도 밝혀졌는데 MC1R 유전자 돌연변이가 있다. MC1R 위험 홑배수체형의 동형접합체를 가진 사람은 안 가진 사람에 비해 평균 2년 늙어 보인다[7]. 후성유전학 연구에서는 DNA 메틸화 정도와 피부노화의 연관성이 보고되었다.
연령과 성별 차이도 있다. 남자는 여자보다 진피가 더 두껍고 피하지방은 더 얇은데, 이는 성호르몬의 영향을 의미한다[8]. 여자는 폐경 후 콜라젠 양이 매년 2.1%씩 꾸준히 감소하여 피부 두께가 매년 1.1%씩 감소하는데, 이는 에스트로겐의 감소에 기인한다[9]. 실제로 한 일본인 연구에서는 폐경 후 여성에서 해마다 감소하던 피부탄력이 경구호르몬대체요법 1년 시행 후 5.2% 회복되었다[10].
프로그램설에 의하면 동물 각 종마다 노화과정과 수명이 유전적으로 정해져 있으며 유전 프로그램에 의해 일정한 속도와 과정을 거치면서 늙어간다. 그 증거로 특정 세포가 배양 시 일정 횟수 이상 분열하지 못하고 늙어버리는 현상, 즉 세포노쇠가 있다. 세포노쇠의 기전은 염색체 끝분절(telomere) 단축으로 일부 설명할 수 있다. 노화 억제기능을 갖는 끝분절은 세포가 분열할 때마다 그 길이가 짧아지는데, 끝분절 길이와 노쇠세포의 기능 감소에 밀접한 연관성이 밝혀져 있다.
가장 주된 요인은 자외선으로, 얼굴 노화의 약 80%를 유발한다[11]. 광노화를 일으키는 자외선은 파장에 따라 자외선A (320-400 nm), 자외선B (290-320 nm), 자외선C (100-290 nm)로 구분하는데, 파장이 짧을수록 에너지는 높지만 피부 투과력은 약하다. 자외선C는 오존층에 막혀서 지표면에 도달을 못하고 자외선B는 표피까지 도달하는 반면, 자외선A는 하부 진피까지 도달하여 광노화를 일으키는 주범이다. 자외선B는 지표면에 도달하는 자외선의 5% 미만을 차지하고 자외선A는 자외선B보다 100배 더 많이 도달한다[12]. 자외선A는 진피의 섬유모세포와 혈관에 주로 산화손상을 일으켜 섬유모세포에서 콜라젠을 분해하는 효소인 바탕질금속단백질분해효소(matrix metalloproteinases, MMP) 합성을 증가시키고 진피에 염증세포 침윤을 일으킬 뿐 아니라 특히 동양인에서 색소침착을 유발한다. 자외선B는 표피 세포에 직접 흡수되어 DNA 손상을 일으키고 표피 각질형성 세포의 신호전달체계를 통해 진피에서 MMP 발현을 증가시킨다[13]. 자외선에 의한 만성적인 약한 염증은 노화 현상의 주된 부분을 차지하기 때문에 염증노화(inflamm-aging)라는 말까지 생겼다. 가시광선(390-700 nm)은 태양광의 50% 이상을 차지하는데, 자외선보다는 훨씬 약하나 태양광 노출 후 적외선과 가시광선만으로도 MMP 발현이 증가하여 콜라젠 합성이 감소함이 밝혀져 있다[14]. 태양의 가시광선 중 청색 빛(400-440 nm)은 피부에 색소침착을 유발할 수 있으나[1], 태블릿 PC나 휴대폰 같은 기기에서 방출되는 청색 빛은 상대적인 조사량이 너무 적어 색소침착을 일으키지 않는다[15].
공해 또한 피부노화를 일으키는데, 흔한 공해물질로는 미세먼지, 휘발성 유기화합물, 오존, 질소, 이산화황이 있다. 도시의 공해에 만성적으로 노출되면 산화손상에 의해 얼굴의 노화가 가속화되는데 특히 기미 같은 색소침착 질환이 증가한다[16]. 생활방식에 따른 공해물질인 담배연기는 3,800여 종의 화학물질을 함유하는데 피부에서 MMP 발현 증가, 모세혈관 수축, 얼굴 산소량 감소를 유발하여[17], 특히 입 주위와 눈가 주름을 증가시키며, 특히 여자에서 피부의 기저세포암과 편평세포암 위험을 증가시킨다[18]. 종합하면 얼굴주름 발생에는 자외선이 공해물질보다 훨씬 중요하고, 얼굴 일광흑자 발생에는 두 요인이 비슷하게 중요하다[19].
기후요인을 보면 대개 색소와 주름은 여름보다 겨울에 감소하는 반면 피부장벽과 피부 수분은 겨울에 악화된다. 습도가 낮으면 표피의 염증성 매개물질 합성이 증가하여 잔주름이 증가한다. 피지 분비는 기온이 올라갈수록 증가한다. 적외선이나 고열 환경에 노출되어 피부온도가 상승하면 열에 의해 피부노화가 촉진된다.
생활방식도 노화의 중요한 요인인데, 만성적으로 5시간 이하의 수면을 취하면 피부장벽기능이 감소하고 얼굴피부노화가 증가한다는 연구결과가 있다[20]. 자는 동안 분비되는 멜라토닌은 24시간 주기리듬에 중요한 호르몬인데, 강력한 항염증작용 및 항산화작용, 미토콘드리아 보호작용, 광보호 작용을 갖는 물질로, 수면의 질이 떨어지면 멜라토닌 분비가 감소하기 때문이다[21]. 운동을 하면 피를 통한 산소와 영양분의 전신 공급, 땀을 통한 노폐물 배출, 적정 혈중 코티솔 농도 유지 외에도 콜라젠 합성 촉진, 미토콘드리아 기능 향상, 피부를 지지하는 하부 근육 강화 등에 의해 피부가 건강해진다. 영양 섭취 또한 중요하다. 심리적 스트레스는 스트레스호르몬 분비를 통해 염증성 사이토카인 합성을 증가시켜 정상인에서 표피의 장벽기능 자체를 떨어뜨리고 장벽 회복도 늦춘다[22]. 또 스트레스는 장 내 미생물군을 변화시켜 장 투과성 증가 및 전신 염증을 유발한다. 특정 유산균을 복용한 후 피부 습도와 생체역학적 성질이 호전되고[23], 섬유모세포에서 MMP-1 발현이 억제되었다는 보고가 있다[23]. 지속적인 심리적 스트레스는 피부의 미생물군 조성도 변화시킨다. 피부 미생물군유전체는 항염증 환경을 조성함으로써 자외선에 대한 피부 세포반응과 면역기능에 영향을 준다. 특정 Lactobacillus 균주는 IL-6, IL-8 같은 염증성 사이토카인을 억제하여 자외선B 손상으로부터 피부를 보호하였다[24].
진피 섬유모세포의 노쇠는 비가역적 증식 정지와 노쇠관련분비표현형(senescence-associated secretory phenotype, SASP) 증가를 일으켜 피부노화에 핵심적인 작용을 하는 것으로 생각된다. SASP는 다양한 케모카인(CXCL-1/3, CXCR2)과 염증물질(IL-1, IL-6, IL-8, IL-18 등) 분비를 통해 만성 염증을 일으키고 필수 성장인자(hepatocyte growth factor, insulin-like growth factor-1 [IGF-1], transforming growth factor- β [TGF-β] 등) 분비 감소로 인해 증식이 감소하며 MMP 같은 단백분해효소 활성화로 결체조직의 분해를 촉진한다[25]. 세포노쇠 표지자로는 p16INK4a, p21, p53 발현, senescence-associated β-galactosidase 활성 증가가 있다[26]. 전신의 섬유모세포 노쇠는 세포가 죽지 않고 노쇠가 영구적으로 지속되는 상태로, 결국 비가역적 피부노화, 인체 노화뿐만 아니라 치유되지 않는 상처, 편평세포암 등 노화 관련 질환을 유발한다[27]. 비증식성 섬유모세포에서 영구적 노쇠는 세포 자체적 혹은 외부 스트레스 요인에 의해 유발되는데, 여기엔 염색체 끝분절 단축, 미토콘드리아 기능 이상, DNA 손상, 종양 발생 돌연변이가 포함된다. 스트레스로 인한 섬유모세포 노쇠에는 p38-mitogen-activated protein kinase 경로가 중요하게 작용한다[28]. 이후 DNA 손상반응 신호 체계 활성화를 통해 세포주기 정지가 일어난다. 섬유모세포 미토콘드리아의 기능 이상은 세포의 DNA 손상을 촉진하거나 반응산소종 농도를 높여서 전사인자 activator protein-1 (AP-1)과 nuclear factor κB (NF-κB) 의존 신호전달체계를 증가시켜 내·외인성 피부노화의 주된 역할을 한다[29]. 특히 광 노화된 피부에서는 미토콘드리아 DNA의 4,977 염기쌍 결손이 비노출부 노화피부보다 10배 높았다[30]. 진피 섬유모세포 내 자외선 관련 미토콘드리아 DNA 돌연변이 축적은 피하지방 감소도 일으킨다[31]. AP-1은 TGF-β 신호전달을 감소시켜 제1형 및 제3형 콜라젠 합성을 억제하고, AP-1과 NF-κB 모두 MMP-1, 3, 9 유전자 전사를 증가시켜 기존 콜라젠 분해를 증가시켜 결국 광노화된 피부에서 콜라젠 총량이 감소한다. 콜라젠 합성에는 섬유모세포와 온전한 콜라젠의 물리적인 상호작용이 중요한데, 분해된 콜라젠의 고분자 파편들이 진피 기질에 축적되면 이 상호작용을 방해하여 제1형 콜라젠 합성은 더욱 감소한다[32]. 노쇠는 stromal cell-derived factor 1 억제를 통해 노화 관련 색소침착에도 관여한다[33]. 섬유모세포 노쇠는 주변 비노쇠 세포로 확산되어 노쇠가 증폭됨이 확인되었다[34].
표피 각질형성세포에도 노쇠가 일어난다. 자외선에 의해 발생한 반응산소종은 mitogen-activated protein kinase와 extracellular signal-regulated kinase, p38, c-Jun N-terminal kinase를 활성화시켜 AP-1의 c-Jun, c-Fos를 활성화시키고, 그 결과 MMP 발현이 증가하며 종양괴사인자 알파(tumor necrosis factor-α), IL-1α, IL-1β, IL-6 같은 염증성 사이토카인이 증가하는데 이들은 모두 SASP 인자이다. 다만 각질형성세포는 섬유모세포보다 회전율이 높고 주기적으로 탈락되기 때문에 표피에서는 SASP의 영향이 제한적이다[35]. 각질형성세포는 IGF-1은 분비하지 않고 그 수용체만 갖고 있는데 자외선B에 노출되면 섬유모세포에서 IGF-1을 분비하여 이 수용체에 결합함으로써 각질 형성세포의 세포자멸사를 막아준다. 노쇠 섬유모세포에서는 IGF-1 발현이 감소하여 각질형성세포가 자멸사하고 생존한 세포는 DNA 손상이 수복되지 않은 상태로 증식을 계속하여 피부암의 위험이 증가한다[36]. 따라서 노쇠세포의 효과적인 제거는 조직의 항상성 유지와 질환 발생 예방에 중요하다.
노화에 따라 적응면역이 감소하는데 이를 면역노쇠라 한다. 면역노쇠에 따른 비효율적인 적응면역으로 인해 만성의 경미한 염증상태가 지속되는데 이를 염증노화라 하며, IL-6, IL-8, 종양괴사인자 알파 같은 혈중 염증성 사이토카인이 증가되어 있다[37]. 이 사이토카인들은 선천면역을 증강시키고 그 결과 가지돌기세포, 중성구, 대식세포, 섬유모 세포 같은 세포의 기능장애가 발생한다[38]. 노쇠세포의 축적은 만성염증과 대사장애를 유발하여 노화를 악화시킨다.
노화 피부에서는 피부 두께 감소 등의 구조적인 변화로 인해 선천면역세포인 대식세포 등이 세균에 더 많이 노출되어 만성적으로 활성화되고 염증성 사이토카인을 분비하여 낮은 수준의 만성 염증이 지속되어 노화가 촉진된다[39]. 자외선에 의한 손상도 염증노화를 일으키는데, 자외선B에 반복적으로 노출되면 피부에 대식세포가 축적되어 반응산소종과 MMP 증가, 세포외기질 손상으로 이어진다. 또 하나의 인자는 노쇠세포의 축적이다. SASP가 증가된 노쇠세포에서 염증매개물질을 분비하여 약한 염증상태가 된다[40]. 노쇠 섬유모세포는 HLA-E 발현을 증가시킴으로써 자연살해세포와 CD8+ T세포에 의해 인지되지 않아 제거되지 않고 피부에 계속 존재한다[41]. 또한 면역세포가 노화된 조직의 세포외기질에 갇히게 되어 면역반응의 효율이 더욱 감소하게 되며, 축적된 세포독성세포가 분비하는 MMP, serine proteases, cathepsins 같은 효소에 세포외기질이 더 많이 노출되어 탄력섬유 저하가 심화된다.
광노화 예방에 가장 중요한 전략은 자외선 차단이다. 자외선이 제일 강한 오전 10시부터 오후 4시 사이에는 가급적 야외 활동을 삼가고, 매일 자외선차단제를 바르고 외출할 때는 긴소매 옷을 입고 챙이 넓은 모자와 선글라스를 쓰도록 한다. 자외선차단제는 1차적 광보호를 위해 제일 중요한 화장품으로, 보통 자외선A와 B를 차단하는 다양한 유기 성분(과거 화학적 차단제)과 무기 성분(과거 물리적 차단제)을 혼합하여 제조한다. Sun protection factor (SPF)는 주로 자외선B 차단지수로 1-50까지 표기하며, protection against ultraviolet A (PA)는 자외선A 차단등급으로 SPF와 구분을 위해 +에서 ++++까지 4등급으로 표기한다. 적어도 SPF30 이상의 제품을 사용해야 자외선A까지 막아주는 광범위 차단 효과를 볼 수 있다. 외출 20분 전에 500원짜리 동전 크기(2 mg/cm2)의 양을 얼굴 전체, 귀, 목, 손, 팔 등 햇빛 노출 부위에 균일하게 꼼꼼히 발라서 흡착시켜야 제품에 표기된 수치만큼의 효과를 볼 수 있다. 칼슘 대사와 뼈 건강에 중요한 비타민D의 90%는 자외선B에 의해 피부에서 만들어지는데, 최근 비타민D의 중요성이 부각되면서 자외선을 너무 차단하면 건강에 좋지 않을 것이라는 우려가 있다. 그러나 사람들이 실제 바르는 차단제의 양은 SPF를 측정할 때 기준이 되는 도포 용량의 1/3에서 1/4 정도이므로 자외선을 충분히 차단하지 못한다. 또한 주 2회 낮 동안 5-30분간 산책을 통해 팔과 다리를 노출시키는 것만으로도 비타민D 요구량은 충분히 만들어지며, 노인, 비만한 사람, 주로 집에 있는 사람 등 비타민D 결핍에 취약한 사람들은 하루 1,000 IU의 비타민D를 복용한다.
세포의 성장, 분화와 주기를 조절하는 물질들은 콜라젠 대사에 직접 작용하여 콜라젠과 탄력섬유 합성을 촉진한다. 이 중 제일 뛰어난 효능을 지닌 물질은 레티노이드라 부르는 비타민A 유도체들이다. 비타민A (retinol), retinal (retinaldehyde), retinoic acid (tretinoin) 등이 있는데, tretinoin은 광노화 예방에 승인된 전문의약품이고 그 전구체인 retinol, retinal 등은 항노화화장품 원료로 가장 흔히 사용된다. Tretinoin은 원래 여드름치료제로 개발되었는데, 연고를 바른 부위의 피부결과 톤이 좋아짐이 발견되어 이후 많은 연구를 통해 진피에서 콜라젠 분해를 억제하고 콜라젠 합성을 증가시킴이 입증된 물질이다. 또한 표피 각질형성세포 분화를 정상화시켜 피부암을 예방하고 멜라닌 배출을 원활히 하여 잡티를 감소시키기도 하는 만능 항노화물질이다. 도포 초기에 피부가 붉어지고 각질이 생기는 레티노이드피부염이 생길 수 있으나 계속 바르면 없어진다. 적어도 4개월 이상 발라야 진피 효과를 볼 수 있다. 모든 레티노이드는 강도 차이는 있으나 모두 핵 내 retinoic acid 수용체를 통해 유전자를 조절하여 전사인자 NF-κB와 AP-1의 비활성화를 통해 MMP 발현을 감소시켜 콜라젠의 양을 유지 및 증가시킨다. 레티노이드는 자외선에 의해 분해되므로 밤에만 바르도록 한다.
그 외 콜라젠이나 탄력소 같은 피부단백의 펩타이드 서열을 본뜬 펩타이드 서열을 만들어서 도포 시 콜라젠 합성이나 진피 대사 촉진을 기대하는 펩타이드 성분, 근육에서 신경전달물질의 방출을 억제하여 근 수축을 막음으로써 표정근 수축에 의한 주름 형성을 감소시키는 신경독 유사 작용 펩타이드가 있다. 또한 상처회복 과정에 피부에서 TGF-β, 혈소판 유래성장인자, 혈관내피성장인자, 성장호르몬, 신경성장인자, IGF, 섬유모세포성장인자-2 등의 성장인자와 사이토카인이 분비되어 진피 리모델링을 돕는데 착안하여 동물 혹은 식물세포를 배양한 배양액에 분비된 성장인자, 사이토카인, 기질단백을 혼합한 제품도 있는데, 표피세포에 작용하여 신호전달 사이토카인을 분비시켜 간접적으로 진피 세포에 영향을 미친다.
우리 몸의 산화손상을 막아주는 항산화제는 수소 공여체로 작용하여 자유라디칼을 반응성이 떨어지는 hydroxyl 형태로 환원시키고 그 과정에서 자신은 수동 라디칼로 변환된다. 수동 라디칼은 비교적 안정적이며 두 번째 자유라디칼을 중화시킬 수 있다. 이런 반응을 반복하다 보면 항산화제는 결국 고갈된다. 항산화제는 피부조직에서 자유라디칼 농도를 감소시켜 콜라젠 분해를 억제한다. 우리 몸에는 superoxide dismutase, catalase 같은 항산화 효소들과 glutathione, 비타민C, 비타민E 같은 항산화 화합물이 있는데 후자는 영양분 섭취를 통해서만 얻을 수 있으므로 비타민A(카로테노이드), B, C와 E 등의 영양소를 고루 섭취하도록 한다. 화장품 원료로 사용되는 항산화제는 매우 다양한데, 고전적 물질로는 비타민과 다양한 식물에서 유래한 폴리페놀이 있다(Table 1). Niacinamide(비타민B3)는 색소침착, 홍반, 일광흑자, 피부의 황색변화 같은 노화 징후를 감소시키고 피부탄력과 잔주름을 호전시킨다. 비타민C는 진피에서 콜라젠 합성을 증가시키고 표피 피부장벽기능을 정상화시키지만, 열에 약한 수용성 물질이라 쉽게 산화, 분해되므로 안정된 제형을 사용해야 효과가 있다. 비타민E는 비타민C의 항산화효과를 상승시키고 항염효과를 나타낸다. 그 외 α-lipoic acid, coenzyme Q10도 항염작용으로 콜라젠 합성 증가를 돕는다. 폴리페놀은 벤질 환에 두 개의 hydroxyl기가 나란히 붙어있는 분자로, 구조적 특징으로 인해 항산화작용을 한다. 포도주, 홍차/녹차, 과일, 채소 등 수 많은 식물성 식품에 들어있다. 대표적인 물질로는 자몽, 견과류, 적포도주에 들어있는 resveratrol, 녹차의 주된 폴리페놀인 epigallocatechin-3-gallate, 콩의 isoflavone, 블루베리, 포도에 많이 함유된 anthocyanidin이 있다[44]. 식물의 색이 진할수록 항산화능이 강하므로[45], 녹색 채소와 베리류 과일의 항산화제 함량이 제일 높다.
노쇠세포를 제거하면 장기의 기능이 현저히 호전되어 건강 상태 유지 및 수명 증가를 기대할 수 있기에 피부노화 치료의 새로운 전략으로 대두되고 있다. Heat shock protein 90 억제제, Bcl-2 단백군 억제제 및 자연화합물(quercetin, fisetin 등)이 있다. 세포자멸사 억제단백인 Bcl-2, BclXL, Bcl-W를 억제하는 navitoclax, tyrosinase 억제제인 dasatinib, 항산화제 flavonoid인 quercetin을 이용한 임상시험이 진행 중이며 미역취 같은 식물 추출물의 노쇠분해능에 대한 연구도 활발히 이뤄지고 있다[46]. 영양분 인지단백 kinase인 mTOR는 세포성장과 대사를 조절하는데 rapamycin은 이 효소를 억제하여 노쇠세포 형성을 감소시킨다[47]. 메트포민은 mTOR 경로 억제, adenosine monophosphate kinase 활성화, 용해소체 경로 및 미토콘드리아 스트레스 조절, 미생물군유전체 변화 기전으로 수명을 증가시킬 수 있어[48], 도포제로도 개발되고 있다.
피부는 쉽게 조직을 채취할 수 있어 피부노화에서 나타나는 생화학적 변화를 통해 전신노화 기전을 파악할 수 있다. 다른 장기와 마찬가지로 피부노화에도 산화손상과 DNA 손상이 관여하며 여기엔 자외선을 비롯한 다양한 요인과 세포노쇠 현상, 염증이 맞물려 작용한다. 피부의 광노화 예방에 제일 중요한 것은 매일 아침 자외선차단제를 바르는 것이다. 나이가 들수록 피부장벽의 지질이 감소하고 pH가 상승하기 때문에 생리적 노화를 늦추려면 때를 밀지 말고 콜레스테롤이 주가 되는 생리적 지질 복합물이 함유된 보습제와 pH 4.0 이하의 산성 보습제를 바른다. 일상생활에서 스트레스를 최소화하고 항산화제 성분이 풍부하게 함유된 건강한 식단을 꾸리면서 금연과 소식을 통해 반응산소종 발생을 최소화하고 알코올 섭취를 줄이는 게 좋다. 혈당이 높으면 콜라젠과 탄력소가 당과 결합하는 당화반응을 통해 최종당화산물을 형성하여 피부가 뻣뻣해지고 피부노화가 심화되므로[49], 혈당지수가 낮은 음식을 먹는다. 운동은 혈액순환을 돕고 면역 및 미토콘드리아 기능을 증강시키므로 1주에 적어도 4시간 이상 운동한다. 하루 8시간 정도 숙면을 취하면 피부 겉모습뿐만 아니라 장벽기능도 좋아진다. 이러한 피부노화 예방을 위한 노력은 전신노화의 예방도 가능하게 해주므로 어렸을 때부터 평생 지속하는 것이 바람직하다.
Figure 1.
Pathologic findings of (A) face of a 15-year-old female, with preserved epidermal rete ridges (arrow) and normal dermal components, (B) face of an 84-year-old female, with flat, atrophic epidermis and solar elastosis (asterisk) replacing the upper dermis, (C) back of a 24-year-old male, and (D) back of an 84-year-old male with mildly atrophic epidermis and relatively preserved dermis (hematoxylin and eosin, x100).
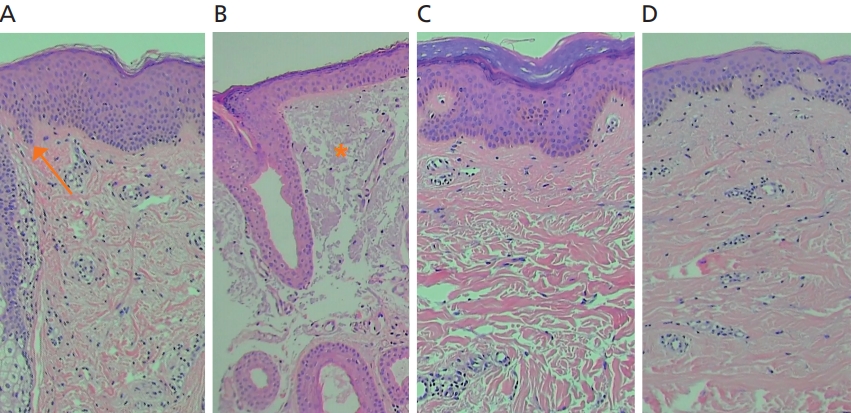
Table 1.
Topical anti-aging agents
References
1. Krutmann J, Bouloc A, Sore G, Bernard BA, Passeron T. The skin aging exposome. J Dermatol Sci 2017;85:152-161.


2. Zhang LJ, Chen SX, Guerrero-Juarez CF, Li F, Tong Y, Liang Y, Liggins M, Chen X, Chen H, Li M, Hata T, Zheng Y, Plikus MV, Gallo RL. Age-related loss of innate immune antimicrobial function of dermal fat is mediated by transforming growth factor beta. Immunity 2019;50:121-136. e5.


3. Couturaud V, Coutable J, Khaiat A. Skin biomechanical properties: in vivo evaluation of influence of age and body site by a non-invasive method. Skin Res Technol 1995;1:68-73.


4. Yamazaki S, Nishioka A, Kasuya S, Ohkura N, Hemmi H, Kaisho T, Taguchi O, Sakaguchi S, Morita A. Homeostasis of thymus-derived Foxp3+ regulatory T cells is controlled by ultraviolet B exposure in the skin. J Immunol 2014;193:5488-5497.


5. Nouveau-Richard S, Yang Z, Mac-Mary S, Li L, Bastien P, Tardy I, Bouillon C, Humbert P, de Lacharriere O. Skin ageing: a comparison between Chinese and European populations. A pilot study. J Dermatol Sci 2005;40:187-193.

6. Murase D, Hachiya A, Takano K, Hicks R, Visscher MO, Kitahara T, Hase T, Takema Y, Yoshimori T. Autophagy has a significant role in determining skin color by regulating melanosome degradation in keratinocytes. J Invest Dermatol 2013;133:2416-2424.


7. Liu F, Hamer MA, Deelen J, Lall JS, Jacobs L, van Heemst D, Murray PG, Wollstein A, de Craen AJ, Uh HW, Zeng C, Hofman A, Uitterlinden AG, Houwing-Duistermaat JJ, Pardo LM, Beekman M, Slagboom PE, Nijsten T, Kayser M, Gunn DA. The MC1R gene and youthful looks. Curr Biol 2016;26:1213-1220.


8. Makrantonaki E, Brink TC, Zampeli V, Elewa RM, Mlody B, Hossini AM, Hermes B, Krause U, Knolle J, Abdallah M, Adjaye J, Zouboulis CC. Identification of biomarkers of human skin ageing in both genders. Wnt signalling - a label of skin ageing? PLoS One 2012;7:e50393.



9. Brincat M, Kabalan S, Studd JW, Moniz CF, de Trafford J, Montgomery J. A study of the decrease of skin collagen content, skin thickness, and bone mass in the postmenopausal woman. Obstet Gynecol 1987;70:840-845.

10. Sumino H, Ichikawa S, Abe M, Endo Y, Ishikawa O, Kurabayashi M. Effects of aging, menopause, and hormone replacement therapy on forearm skin elasticity in women. J Am Geriatr Soc 2004;52:945-949.


11. Friedman O. Changes associated with the aging face. Facial Plast Surg Clin North Am 2005;13:371-380.


12. Cortat B, Garcia CC, Quinet A, Schuch AP, de Lima-Bessa KM, Menck CF. The relative roles of DNA damage induced by UVA irradiation in human cells. Photochem Photobiol Sci 2013;12:1483-1495.


13. Wlaschek M, Bolsen K, Herrmann G, Schwarz A, Wilmroth F, Heinrich PC, Goerz G, Scharffetter-Kochanek K. UVAinduced autocrine stimulation of fibroblast-derived-collagenase by IL-6: a possible mechanism in dermal photodamage? J Invest Dermatol 1993;101:164-168.


14. Cho S, Lee MJ, Kim MS, Lee S, Kim YK, Lee DH, Lee CW, Cho KH, Chung JH. Infrared plus visible light and heat from natural sunlight participate in the expression of MMPs and type I procollagen as well as infiltration of inflammatory cell in human skin in vivo. J Dermatol Sci 2008;50:123-133.


15. Passeron T. The key question of irradiance when it comes to the effects of visible light in the skin. J Dermatol Sci 2019;93:69-70.


16. Roberts WE. Pollution as a risk factor for the development of melasma and other skin disorders of facial hyperpigmentation: is there a case to be made? J Drugs Dermatol 2015;14:337-341.

17. Ono Y, Torii K, Fritsche E, Shintani Y, Nishida E, Nakamura M, Shirakata Y, Haarmann-Stemmann T, Abel J, Krutmann J, Morita A. Role of the aryl hydrocarbon receptor in toba-cco smoke extract-induced matrix metalloproteinase-1 expression. Exp Dermatol 2013;22:349-353.


18. Rollison DE, Iannacone MR, Messina JL, Glass LF, Giuliano AR, Roetzheim RG, Cherpelis BS, Fenske NA, Jonathan KA, Sondak VK. Case-control study of smoking and nonmelanoma skin cancer. Cancer Causes Control 2012;23:245-254.


19. Krutmann J, Schikowski T, Morita A, Berneburg M. Environmentally-induced (extrinsic) skin aging: exposomal factors and underlying mechanisms. J Invest Dermatol 2021;141((4 Suppl):1096-1103.


20. Oyetakin-White P, Suggs A, Koo B, Matsui MS, Yarosh D, Cooper KD, Baron ED. Does poor sleep quality affect skin ageing? Clin Exp Dermatol 2015;40:17-22.


21. Rusanova I, Martínez-Ruiz L, Florido J, Rodriguez-Santana C, Guerra-Librero A, Acuna-Castroviejo D, Escames G. Protective effects of melatonin on the skin: future perspectives. Int J Mol Sci 2019;20:4948.



22. Fukuda S, Baba S, Akasaka T. Psychological stress has the potential to cause a decline in the epidermal permeability barrier function of the horny layer. Int J Cosmet Sci 2015;37:63-69.


23. Lee DE, Huh CS, Ra J, Choi ID, Jeong JW, Kim SH, Ryu JH, Seo YK, Koh JS, Lee JH, Sim JH, Ahn YT. Clinical evidence of effects of lactobacillus plantarum hy7714 on skin aging: a randomized, double blind, placebo-controlled study. J Microbiol Biotechnol 2015;25:2160-2168.


24. Khmaladze I, Butler E, Fabre S, Gillbro JM. Lactobacillus reuteri DSM 17938-A comparative study on the effect of probiotics and lysates on human skin. Exp Dermatol 2019;28:822-828.


25. Coppe JP, Desprez PY, Krtolica A, Campisi J. The senescence-associated secretory phenotype: the dark side of tumor suppression. Annu Rev Pathol 2010;5:99-118.



27. Campisi J. Senescent cells, tumor suppression, and organismal aging: good citizens, bad neighbors. Cell 2005;120:513-522.


28. Alimbetov D, Davis T, Brook AJ, Cox LS, Faragher RG, Nurgozhin T, Zhumadilov Z, Kipling D. Suppression of the senescence-associated secretory phenotype (SASP) in human fibroblasts using small molecule inhibitors of p38 MAP kinase and MK2. Biogerontology 2016;17:305-315.


29. Krutmann J, Schroeder P. Role of mitochondria in photoaging of human skin: the defective powerhouse model. J Investig Dermatol Symp Proc 2009;14:44-49.


30. Berneburg M, Gattermann N, Stege H, Grewe M, Vogelsang K, Ruzicka T, Krutmann J. Chronically ultraviolet-exposed human skin shows a higher mutation frequency of mitochondrial DNA as compared to unexposed skin and the hematopoietic system. Photochem Photobiol 1997;66:271-275.


31. Kamenisch Y, Fousteri M, Knoch J, von Thaler AK, Fehrenbacher B, Kato H, Becker T, Dolle ME, Kuiper R, Majora M, Schaller M, van der Horst GT, van Steeg H, Rocken M, Rapaport D, Krutmann J, Mullenders LH, Berneburg M. Proteins of nucleotide and base excision repair pathways interact in mitochondria to protect from loss of subcutaneous fat, a hallmark of aging. J Exp Med 2010;207:379-390.



32. Varani J, Schuger L, Dame MK, Leonard C, Fligiel SE, Kang S, Fisher GJ, Voorhees JJ. Reduced fibroblast interaction with intact collagen as a mechanism for depressed collagen synthesis in photodamaged skin. J Invest Dermatol 2004;122:1471-1479.


33. Yoon JE, Kim Y, Kwon S, Kim M, Kim YH, Kim JH, Park TJ, Kang HY. Senescent fibroblasts drive ageing pigmentation: a potential therapeutic target for senile lentigo. Theranostics 2018;8:4620-4632.



34. Nelson G, Wordsworth J, Wang C, Jurk D, Lawless C, MartinRuiz C, von Zglinicki T. A senescent cell bystander effect: senescence-induced senescence. Aging Cell 2012;11:345-349.


35. Pilkington SM, Bulfone-Paus S, Griffiths CEM, Watson REB. Inflammaging and the Skin. J Invest Dermatol 2021;141((4S):1087-1095. PubMed 2021;141(4 Suppl):1087-1095.


36. Loesch MM, Collier AE, Southern DH, Ward RE, Tholpady SS, Lewis DA, Travers JB, Spandau DF. Insulin-like growth factor-1 receptor regulates repair of ultraviolet B-induced DNA damage in human keratinocytes in vivo. Mol Oncol 2016;10:1245-1254.



37. Freund A, Orjalo AV, Desprez PY, Campisi J. Inflammatory networks during cellular senescence: causes and consequences. Trends Mol Med 2010;16:238-246.



38. Hearps AC, Martin GE, Angelovich TA, Cheng WJ, Maisa A, Landay AL, Jaworowski A, Crowe SM. Aging is associated with chronic innate immune activation and dysregulation of monocyte phenotype and function. Aging Cell 2012;11:867-875.


39. Thevaranjan N, Puchta A, Schulz C, Naidoo A, Szamosi JC, Verschoor CP, Loukov D, Schenck LP, Jury J, Foley KP, Schertzer JD, Larche MJ, Davidson DJ, Verdu EF, Surette MG, Bowdish DME. Age-associated microbial dysbiosis promotes intestinal permeability, systemic inflammation, and macrophage dysfunction. Cell Host Microbe 2017;21:455-466. e4.



41. Pereira BI, Devine OP, Vukmanovic-Stejic M, Chambers ES, Subramanian P, Patel N, Virasami A, Sebire NJ, Kinsler V, Valdovinos A, LeSaux CJ, Passos JF, Antoniou A, Rustin MHA, Campisi J, Akbar AN. Senescent cells evade immune clearance via HLA-E-mediated NK and CD8+ T cell inhibition. Nat Commun 2019;10:2387.



42. de Miranda RB, Weimer P, Rossi RC. Effects of hydrolyzed collagen supplementation on skin aging: a systematic review and meta-analysis. Int J Dermatol 2021 Mar 20 [Epub]. https://doi.org/10.1111/ijd.15518

43. Ohara H, Ichikawa S, Matsumoto H, Akiyama M, Fujimoto N, Kobayashi T, Tajima S. Collagen-derived dipeptide, prolinehydroxyproline, stimulates cell proliferation and hyaluronic acid synthesis in cultured human dermal fibroblasts. J Dermatol 2010;37:330-338.


44. Działo M, Mierziak J, Korzun U, Preisner M, Szopa J, Kulma A. The potential of plant phenolics in prevention and therapy of skin disorders. Int J Mol Sci 2016;17:160.



45. Hernandez-Marin E, Galano A, Martinez A. Cis carotenoids: colorful molecules and free radical quenchers. J Phys Chem B 2013;117:4050-4061.


46. Wlaschek M, Maity P, Makrantonaki E, Scharffetter-Kochanek K. Connective tissue and fibroblast senescence in skin aging. J Invest Dermatol 2021;141((4 Suppl):985-992.


47. Blagosklonny MV. Rapamycin, proliferation and geroconversion to senescence. Cell Cycle 2018;17:2655-2665.



Peer Reviewers’ Commentary
이 논문은 피부노화의 기전, 발생 요인, 임상 양상, 조직학적 변화, 예방법 등에 대해 최신 논문을 정리하여 체계적으로 기술하고 설명해 주고 있다. 피부노화의 주요한 요인으로 진피 섬유모 세포와 표피 각질형성세포의 노쇠와 면역 노쇠로 인한 만성적인 경미한 염증 상태가 지속되는 염증 노화가 중요한 역할을 한다는점을 잘 설명하고 있다. 이에 따른 피부노화 예방으로는 전통적인 방법인 자외선차단제의 올바른 사용, 세포 조절제인 레티노이드의 장기 도포, 폴리페놀 등 황산화제 사용 이외에 콜라젠이나 유산균 복용 등 최근 연구 경향을 소개하고, 노쇠 세포 제거물질의 개발 등 앞으로의 연구 방향도 제시해주고 있다. 이 논문은 피부노화를 늦출 수 있는 생활방식 및 예방 방법까지 잘 제시해 주고 있어 피부노화 및 예방에 대해 궁금해하는 환자들을 진료하는 데 좋은 정보를 제공해 줄 것으로 판단된다.
[정리: 편집위원회]
-
METRICS

-
Related articles in
J Korean Med Assoc -
Pathogenesis and epidemiology of chronic subdural hematoma2024 June;67(6)
Diagnosis and treatment of dysphagia2023 October;66(10)
Diagnosis and treatment of adult spinal deformity2023 August;66(8)
Diagnosis and treatment of glossopharyngeal neuralgia2023 January;66(1)
Diagnosis and treatment of trigeminal neuralgia2023 January;66(1)






